- § 21. Способы изображения органических соединений
- 1. Какую информацию можно получить из молекулярной формулы органического соединения?
- 2. Приведены названия и формулы различных веществ: а) оксид углерода(IV) $\mathrm;$ б) дихлорметан $\mathrm;$ в) метан $\mathrm;$ г) карбонат натрия $\mathrm.$ Какие из них относятся к органическим веществам? К органическим веществам относят: б) дихлорметан $\mathrm;$ в) метан $\mathrm;$ к неорганическим — а) оксид углерода(IV) $\mathrm;$ г) карбонат натрия $\mathrm.$ 3. Назовите различия между шаростержневыми и масштабными моделями органических соединений. В шаростержневых моделях атомы изображают в виде трубок из пластмассы и отражают взаимное расположение атомов в пространстве. В масштабных моделях атомы изображают в виде сферы с размерами, пропорциональными их радиусу. 4. Раскройте сущность понятия «химическое строение вещества». Химическое строение — последовательность соединения атомов в молекулах органических соединений; в молекуле этана, например: атомы углерода соединены друг с другом, а атомы водорода связаны с атомами углерода. 5. Химическую связь между какими атомами указывает черточка в сокращенной структурной формуле этана $\mathrm<СН_3 - СН_3>?$ В сокращённой структурной формуле этана чёрточка показывает связь между атомами углерода. 6. Укажите общее число атомов в молекуле метана: а) 2; б) 3; в) 4; г) 5. Общее число атомов в молекуле метана $\mathrm$ равно 5 (г). 7. Попытайтесь написать структурную формулу органического соединения c молекулярной формулой $\mathrm,$ являющегося производным углеводорода этана. Структурная формула соединения $\mathrm$ 8. Изобразите соединение, показанное на рисунке 88, в виде структурной формулы. Структурная формула отображает порядок (последовательность) соединения атомов в молекулах. 9. На основании пространственного изображения молекулы этана на рисунке 86 попытайтесь изобразить пространственное строение молекулы с молекулярной формулой $\mathrm.$ Пространственное строение молекулы $\mathrm:$ Источник Способы изображения органических молекул. Органическая химия. 2.1.Тема: «Теория строения органических соединений» 2.1.1. Основные положения теории строения органических соединений и классификация органических соединений. 1. Природные и синтетические органические вещества. Немного из истории органической химии. Общие свойства органических веществ (состав, тип химической связи, кристаллическое строение, растворимость, отношение к нагреванию в присутствии кислорода и без него). 2. Теория строения органических соединений А.М.Бутлерова. Развитие теории и ее значение. 3. Классификация органических веществ. Свое название органические вещества получили потому, что первые из изученных веществ этой группы входили в состав живых организмов. Большинство известных сейчас органических веществ не встречаются в живых организмах, они получены (синтезированы) в лаборатории. Поэтому различают природные (натуральные) органические вещества (хотя большинство из них может быть сейчас получено в лаборатории), а органические вещества, не существующие в природе – синтетические органические веществами. Т.е. название «органические вещества» историческое и особого смысла не имеет. Все органические соединения являются соединениями углерода. К органическим веществам относятся соединения углерода, кроме изучаемых в курсе неорганической химии простых веществ, образованных Карбоном, его оксидов, угольной кислоты и ее солей. Другими словами: органическая химия – это химия соединений углерода. Краткая история развития орг.химии: Берцелиус, 1827, первый учебник органической химии. Виталисты. Учение о «жизненной силе». Первые органические синтезы. Велер, 1824, синтез щавелевой кислоты и мочевины. Кольбе,1845, уксусная кислота. Бертло,1845, жир. Бутлеров,1861, сахаристое вещество. Но как наука органическая химия началась с создания теории строения органических соединений. Существенный вклад в нее внесли немецкий ученый Ф.А.Кекуле и шотландец А.С.Купер. Но решающий вклад несомненно принадлежит русскому химику А.М.Бутлерову. Среди всех элементов углерод выделяется своей способностью образовывать устойчивые соединения, в которых его атомы связаны друг с другом в длинные цепи различной конфигурации (линейные, разветвленные, замкнутые). Причина этой способности: примерно одинаковая энергия связи С-С и С-О (для других элементов энергия второй – намного больше). Кроме того, атом углерода может находиться в одном из трех видов гибридизации, образуя соответственно одинарные, двойные или тройные связи, причем не только между собой, но и с атомами кислорода или азота. Правда, гораздо чаще (практически всегда) атомы углерода соединены с атомами водорода. Если в состав органического соединения входит только углерод и водород, то соединения называются углеводородами. Все остальные соединения можно рассматривать как производные углеводородов, в которых некоторые атомы водорода замещены на другие атомы или группы атомов. Поэтому более точное определение: Органические соединения – это углеводороды и их производные. Органических соединений очень много — более 10 млн. (неорганических около 500 тыс.). Состав, строение и свойства всех органических веществ имеют много общего. Органические вещества имеют ограниченный качественный состав. Обязательно С и Н, часто О или N, реже галогены, фосфор, сера. Другие элементы входят в состав очень редко. А вот число атомов в молекуле может достигать млн, и молекулярная масса может быть очень большая. Строение органических соединений. Т.к. состав – неметаллы. => Химическая связь: ковалентная. Неполярная и полярная. Ионная очень редко. => Кристаллическая решетка чаще всего молекулярная. Общие физические свойства: невысокая температура кипения и плавления. Среди органических веществ есть газы, жидкости и легкоплавкие твердые вещества. Часто летучи, могут иметь запах. Обычно бесцветные. Большинство органических веществ нерастворимо в воде. Общие химические свойства: 1) при нагревании без доступа воздуха все органические вещества «обугливаются», т.е. при этом образуется уголь (точнее сажа) и некоторые другие неорганические вещества. Происходит разрыв ковалентных связей, сначала полярных, потом и неполярных. 2) При нагревании в присутствии кислорода все органические вещества легко окисляются, и при этом конечными продуктами окисления являются углекислый газ и вода. Особенности протекания органических реакций. В органических реакциях участвуют молекулы, в процессе реакции должны разорваться одни ковалентные связи и образуются другие. Поэтому химические реакции с участием органических соединений идут обычно очень медленно, для их проведения необходимо применять повышенную температуру, давление и катализаторы.В неорганических реакциях обычно участвуют ионы, реакции протекают очень быстро, иногда мгновенно, при нормальной температуре. Органические реакции редко приводят к высокому выходу продукции (обычно менее 50%). Они часто являются обратимыми, кроме того, может протекать не одна, а несколько реакций, конкурирующих между собой, а значит продуктами реакции будет смесь различных соединений. Поэтому и форма записи органических реакций тоже несколько другая. Т.е. используют не химические уравнения, а схемы химических реакций, в которых нет коэффициентов, но зато подробно указаны условия реакции. Принято также под уравнением записывать названия орг. веществ и тип реакции. Но в целом органические вещества и реакции подчиняются общим законам химии, а органические вещества превращаются в неорганические или могут образовываться из неорганических. Что еще раз подчеркивает единство окружающего нас мира. Основные принципы теории химического строения, изложенные молодым А.М.Бутлеровым на международном съезде естествоиспытателей в 1861 г. 1). Атомы в молекулах соединены между собой в определенном порядке, в соответствии с их валентностью. Последовательность соединения атомов называют химическим строением. Валентность — это способность атомов образовывать определенное количество связей (ковалентных). Валентность зависит от числа неспаренных электронов в атоме элемента, потому что ковалентные связи образуются за счет общих электронных пар при спаривании электронов. Углерод во всех органических веществах четырехвалентен. Водород — 1, Кислород -П, азот – Ш, сера – П, хлор – 1. Способы изображения органических молекул. Молекулярная формула – условное изображение состава вещества. Н2СО3 — угольная кислота, С12Н22О11 – сахароза. Такие формулы удобны для расчетов. Но они не дают информацию о строении и свойствах вещества. Поэтому даже молекулярные формулы в органике пишут особым образом: СН3ОН. Но гораздо чаще пользуются структурными формулами. Структурная формула отражает порядок соединения атомов в молекуле (т.е. химическое строение).И в основе любой органической молекулы лежит углеродный скелет – это цепочка связанных между собой ковалентными связями атомы углерода. Электронные формулы молекул – связи между атомами показаны парами электронов. Полная структурная формула показаны все связи черточками. Химическая связь, образованная одной парой электронов, называется одинарной и в структурной формуле изображается одной черточкой. Двойная связь ( =) образована двумя парами электронов. Тройная (≡ ) образована тремя парами электронов. И общее количество этих связей должно соответствовать валентности элемента. В сжатой структурной формуле опускаются черточки одинарных связей, а атомы, связанные с тем или иным атомом углерода, пишутся сразу после него (иногда в скобках). Еще более сокращенными являются скелетные формулы. Но они используются реже. Например: Структурные формулы отражают только порядок соединения атомов. Но молекулы органических соединений редко имеют плоское строение. Объемный образ молекулы важен для понимания многих химических реакций. Образ молекулы описывают с помощью таких понятий как длина связи и валентный угол. Кроме того, возможно свободное вращение вокруг одинарных связей. Наглядное представление дают молекулярные модели. Источник Химические формулы для «чайников» Структурные формулы — это просто! Я думаю, что знакомство с формулами лучше всего начать со структурных формул органических веществ. Считается, что они сложны для понимания, поэтому в школе их изучают в выпускных классах. Но я уверен, что через 10 минут вы разберетесь, как легко составлять структурные формулы. Перед нами структурная формула метана — самого простого органического вещества. Что мы видим? В центре латинская буква C, а от неё четыре палочки, на концах которых четыре латинских буквы H. C означает углерод, а H — водород. Это два самых важных элемента, которые входят в состав любых органических веществ. А что означают палочки? Это химические связи. В них кроется практически весь секрет органической химии. Фокус в том, что валентность углерода равна 4. Поэтому у каждой буквы C должно быть 4 палочки. А валентность водорода равна 1, поэтому у него палочка должна быть только одна. По-моему, палочки отлично демонстрируют такие «страшные» понятия, как химические связи и валентность. Структурные формулы могут слегка менять свой внешний вид. В них главное — количество элементов и наличие нужных связей. Например, формула метана может иметь и такой вид: В общем, структурные формулы не являются какими-то жесткими конструкциями. Если вдруг Вам захотелось бы сделать модель молекулы из подручных материалов, то для этого лучше всего подошли бы шарики, соединённые пружинками или резинками. Под шариками я конечно подразумеваю атомы, а резинки — химические связи. Но в химии приняты не только структурные формулы. И здесь мы познакомимся с некоторыми из них. Достаточно распространены так называемые истинные формулы. Для метана истинная формула записывается так: Стоит упомянуть, что метан — это природный газ, который знаком всем, у кого есть газовая плита. Но не будем на нём долго задерживаться. Пора посмотреть, какие ещё бывают варианты органических структур. Углеводороды Прежде, чем мы начнём знакомство с многочисленными органическими соединениями, хочу напомнить — мы здесь изучаем химические формулы. А все упоминаемые вещества служат для иллюстрации. Вещество Развёрнутая структурная формула Упрощенная структурная формула Брутто-формула Этан H-C-C-H; H|#2|H; H|#3|H CH3-CH3 Пропан H-C-C-C-H; H|#2|H; H|#3|H; H|#4|H CH3-CH2-CH3 Бутан H-C-C-C-C-H; H|#2|H; H|#3|H; H|#4|H; H|#5|H CH3-CH2-CH2-CH3 Пентан H-C-C-C-C-C-H;H|#2|H;H|#3|H;H|#4|H;H|#5|H;H|#6|H CH3-CH2-CH2-CH2-CH3 Гексан H-C-C-C-C-C-C-H;H|#2|H;H|#3|H;H|#4|H;H|#5|H;H|#6|H;H|#7|H Здесь представлены органические вещества, называемые углеводородами. Название означает, что они состоят только из углерода и водорода. Эти вещества в различной мере входят в состав нефти. И это далеко не полный список. Но сначала смотрим ту колонку, которая называется Развёрнутая структурная формула. Мы видим уже знакомые буквы C и H, соединённые химическими связями — палочками. Главное правило по-прежнему в силе: у каждой буквы C четыре палочки, а у каждой H — одна. Что здесь нового? Появились химические связи между атомами углерода. И в результате оказалось, что молекулы органических веществ могут строиться при помощи таких цепочек, где звеньями являются атомы углерода с прилипшими к ними водородами. Теперь посмотрим на колонку, где представлены упрощённые структурные формулы. Несложно догадаться, что они призваны экономить время людей, которые постоянно пишут формулы. Особенно, если эти формулы достаточно большие. Правила здесь довольно простые — убираем палочки между углеродом и водородом и пишем число атомов водорода в виде числа. Таким образом, звенья цепочки становятся видны гораздо более отчётливо. По-научному они называются функциональные группы. Можно даже довольно быстро понять некоторые более хитрые закономерности. Например, группа на конце цепочки записывается CH3 , а в середине цепочки — CH2 . А для ещё большей экономии повторяющиеся группы можно объединить в скобочках, подписав количество повторов. Это показано в последней строке таблицы для формулы гексана: CH3-(CH2)4-CH3 . Некоторые функциональные группы получают собственные названия и даже специальные обозначения. Например, группа CH3 называется метильная группа (от названия метана) и имеет собственное обозначение: Me. Если Вам попадётся, к примеру, такая формула: -CH2- , то ничего страшного тут нет. Это то же самое, что CH3-CH2-CH3 , то есть — пропан. Двойные и тройные связи Итак, за короткое время мы уже разобрались, что такое структурные формулы и выяснили, что они бывают развёрнутые и упрощённые. Но пока что мы познакомились только с одинарными химическими связями. Но на самом деле существуют двойные и даже тройные связи. Посмотрим на следующую таблицу. Вещество Развёрнутая формула Упрощённая формула Брутто-фломула Этен (Этилен) $slope(55)H\C _(x1,N2)C /H CH2=CH2 Пропен (Пропилен) $slope(45)H\C-C/C/H; H\#-3\H;H/#2-#3\H CH2=CH-CH3 Бутен (Бутилен) H\C =C -C -C-H; H|#-3|H CH2=CH-CH2-CH3 Этин (Ацетилен) H-C%C-H CH%CH Пропин (Метилацетилен) H-C%C-C-H; H|#-3|H CH%C-CH3 Бутин (Этилацетилен) H-C%C-C -C-H; H|#-3|H CH%C-CH2-CH3 Представленные здесь вещества тоже относятся к углеводородам. Если хорошенько присмотреться, то можно увидеть определённое сходство с веществами из первой таблицы. Названия формируются заменой буквы в конце названия: этан — этен — этин или пропан — пропен — пропин. Сходство не ограничивается названиями. Главное — одинаковое количество атомов углерода. А значит — одинаковое количество звеньев в цепи. Различие кроется в наличии двойных и тройных связей. Углеводороды в первой таблице называются предельными. Это означает, что к ним больше ничего нельзя добавить. А во второй таблице представлены непредельные углеводороды. То есть, при определённых условиях к ним можно добавить по парочке атомов водорода. Кроме того, появились дополнительные названия. Тут тоже нет ничего страшного. Верхние названия, которые без скобок — это научные названия. А в скобках даны традиционные названия, которые тоже довольно часто употребляются как в научной литературе, так и в быту. Циклические углеводороды Продолжим знакомство с формулами углеводородов. Они ещё не раскрыли нам всех своих секретов. Оказывается, что цепочки могут быть замкнутыми. То есть, атомы углерода соединяются друг с другом циклически. Вещество Развёрнутая формула Упрощённая формула Брутто-формула Циклопропан $slope(60)H`/C`/C:a`/H; H\#C\C:b\H; H-#a-#b-H H2C_(x1.4)CH2_q3CH2_q3 Циклобутан H|C|C|H; H|C|C|H; H-#2-#6-H; H-#3-#7-H H2C-CH2`|CH2`-H2C_#1 Циклопентан C_(x1.1)C@:H2() @()_qC@H2()_qC@H2()_qC@H2()_q@H2() H2C_(x1.4)CH2_qCH2_qCH2_qH2C_q Циклогексан C\C@:H2() @()|C@H2()`/C@H2()`\C@H2()`|C@H2()/@H2() $L(1.3)CH2\CH2|CH2`/CH2`\H2C`|H2C/ Изомеры До сих пор мы не особенно обращали внимания на последнюю колонку, где выведены брутто-формулы. Но может возникнуть вполне законный вопрос: зачем вообще нужны структурные формулы? Ведь брутто-формулы гораздо проще записывать. Может быть, достаточно было бы пользоваться только ими? Но оказывается, что без структурных формул обойтись не получится. Например, если сравнить брутто-формулы из двух предыдущих таблиц, то мы увидим, что циклопропан имеет абсолютно тот же состав, что и пропен ( C3H6 ). А брутто-формула циклобутана совпадает с бутеном ( C4H8 ). Но это разные вещества! И разница заключается в структуре. То есть, имеет большое значение, в каком порядке элементы соединены друг с другом. А значит, именно структурные формулы позволяют точно описать нужное вещество. В химии существует такое понятие как изомеры. Так называют разные вещества, которые имеют одинаковый состав. Это не редкость. И в этом нет ничего странного. Ведь бывают же совершенно разные слова, состоящие из одинаковых букв. Классическими изомерами среди углеводородов можно назвать бутан и изобутан. Посмотрим на их формулы: Вещество Развёрнутая структурная формула Упрощенная структурная формула Брутто-формула Бутан H-C-C-C-C-H; H|#2|H; H|#3|H; H|#4|H; H|#5|H CH3-CH2-CH2-CH3 Метилпропан (Изобутан) H\C\C/C/H; H|#2`/H; H|#4\H; H|#3|C|H; H/#-3\H CH3-CH -CH3 Изобутан является изомером бутана. Обратите внимание, что брутто-формулы одинаковы. Но хотя они близки по свойствам, это разные вещества. Как видно, разнообразие углеводородов не перестаёт удивлять. Оказывается, они могут состоять не только из линейных цепочек, но могут образовывать разветвлённые структуры. И чем длиннее исходная цепочка, тем больше вариантов. Если у бутана возможны только два изомера, то у пентана их уже три: Вещество Упрощённая формула Брутто-формула Пентан CH3-CH2-CH2-CH2-CH3 2-метилбутан (Изопентан) CH3-CH -CH2-CH3 2,2-диметилпропан (Неопентан) CH3-C -CH3 А у вещества декан, имеющего формулу C10H22 , существует 75 изомеров. Но мы не будем их здесь рассматривать. Обратите внимание, что научное название зависит от числа звеньев в прямой цепочке, а традиционное название просто учитывает количество атомов углерода в молекуле. Так получилось из-за того, что химики, которые только начинали исследовать углеводороды, первым делом научились определять состав веществ. То есть, сначала люди смогли получить лишь брутто-формулы. А из них невозможно понять, какова длина самой длинной цепочки. Поэтому названия учитывали общее число атомов углерода. Затем наука дошла до того, что люди смогли исследовать структуру молекул, придумали структурные формулы и переименовали уже известные вещества в соответствии с новыми знаниями. Но старые названия уже успели прижиться и существуют до сих пор. Бензол и скелетные формулы Думаю, что пора познакомиться ещё с одним весьма примечательным представителем углеводородов. Это вещество называется бензол. Вот его формулы: Развёрнутая формула Упрощённая формула Скелетная формула Брутто-формула H|C\C|C `//C `\C `||C /\/H H_(y.5)C\CH|CH`//C `\HC`||HC/ \|`//`\`||/ Чем же этот бензол так примечателен? Дело в том, что это шестиугольное колечко входит в состав огромного числа органических веществ. И вот на примере бензола предлагаю ознакомиться с ещё одним очень важным способом записи структурных формул — скелетными формулами. Как видно из таблицы, скелетная формула бензола представляет собой правильный шестиугольник без каких-либо букв, зато изображения химических связей выглядят одинаково. В общем, правила составления скелетных формул отличаются от уже знакомых нам развёрнутых всего двумя особенностями: Буквы C не пишутся. Предполагается, что каждый угол изображаемой геометрической фигуры содержит атом углерода. Буквы H тоже не пишутся. Если в углу сходятся меньше четырёх линий, то это означает, что все оставшиеся заняты водородом. Конечно, скелетные формулы не так просты, как развёрнутые, но зато их гораздо легче записывать. Поэтому в органической химии это самый популярный вид формул. И мне кажется, Вам тоже будет несложно к ним привыкнуть. Давайте посмотрим, как выглядят формулы других веществ, производных от бензола. Вещество Развёрнутая формула Скелетная формула Смешанный вариант Брутто-формула Нафталин C/C \C |C `//C `\C`|`\C `/C ||C \C/`/|H /\|`//`\`|`\`/||\// C10H8 Толуол H|C|C\C|C `//C `\C `||C /\/H; H-#2-H |\|`//`\`||/ CH3|\|`//`\`||/ Кумол H\C\C/C/H; H|#2|H; H|#4|H; H|#3|C\C|C `//C `\C `||C /\/H \ |\|`//`\`||/ H3C\ |\|`//`\`||/ Как видите, появился ещё и смешанный вариант. Опять какой-то новый вид формул? На этот раз уже нет. Просто иногда внутри одной формулы удобно сочетать различные способы. А вот скелетная формула углеводорода, который называется коронен. Причём, другие варианты здесь уже использовать нет смысла. Скелетные формулы существуют не только для циклических молекул. Понятно, что метан и этан имеют слишком мало узлов, поэтому для них не стоит пытаться использовать скелетные формулы. А вот какая-нибудь длинная молекула изображается довольно легко. Только не в виде прямой цепочки, а при помощи ломаной линии, ведь атомы углерода изображаются углами. Бутан Бутен Изобутан Гексан /\/ //\/ \|`|0/ /\/\/ Трехмерные изображения Иногда плоского изображения становится недостаточно. Поэтому для изображения трехмерных структурных формул используют особое изображение для химических связей: Формулы с окружностью Само собой, все они означают одно и то же. Но первые три отличаются только поворотом вокруг собственного центра. Тут нет ничего необычного, ведь молекулы не стоят на одном месте. А вот дальше мы видим кружок вместо трёх двойных связей. Причём, я намеренно изобразил все атомы водорода в последней формуле. Чтобы было хорошо видно, что каждый угол фактически лишился одной чёрточки. Их заменил кружок. Он как бы означает, что все двойные связи равномерно распределены внутри кольца. Формулы бензола, где используется чередование одинарных и двойных связей называются формулами Кекуле в честь немецкого учёного, который внёс значительный вклад в исследование структуры бензола. На самом деле, среди химиков нет единого мнения по поводу того, насколько правильно использование формул с кружком. Некоторые авторы категорически против. Но есть масса публикаций, где такая запись широко употребляется. Моя задача состоит в том, чтобы Вы узнали о существовании подобных формул и не удивлялись, увидев их. Вот пара примеров записи уже для уже знакомых нам веществ: Нафталин: /\|`/`\`|_o`\`/|\/_o Толуол: `/`-`\/-\_o-CH3 Знакомство с кислородом. Спирты До сих пор мы знакомились со структурными формулами углеводородов, которые состоят только из углерода и водорода. Думаю, пора познакомиться с новым элементом — кислородом. Он обозначается латинской буквой O. Его валентнсть равна 2. То есть, каждая буква O в структурных формулах должна снабжаться двумя палочками. Кислород — очень распространённый элемент на нашей планете. Он входит в состав большого количества органических и неорганических веществ. Но мы начнём знакомство с группы веществ, называемых спиртами: Вещество Развёрнутая структурная формула Упрощенная структурная формула Скелетная формула Брутто-формула Метанол (метиловый спирт) H-C-O-H; H|#C|H CH3-OH \OH Этанол (этиловый спирт) H-C-C-O-H; H|#2|H; H|#3|H CH3-CH2-OH /\OH 1-Пропанол (пропиловый спирт) H-C-C-C-O-H; H|#2|H; H|#3|H; H|#4|H CH3-CH2-CH2-OH /\/OH 2-Пропанол (изопропиловый спирт) H-C-C-C-H; H|#2|H; H|#3|O|H; H|#4|H CH3-CH -CH3 \ / Не правда ли, что в этом есть что-то знакомое? Метан — метанол, этан — этанол, пропан — пропанол. Да, можно сказать, что спирт получается из углеводорода, если заменить один атом -H на группу -O-H (или -OH в упрощенных структурных формулах). Химики называют её: гидроксильная группа, по латинским названиям водорода и кислорода. А иногда она даже называется спиртовой группой. Все спирты можно описать в виде обобщённой формулы -OH , где OH — гидроксильная группа, а R — остальная часть молекулы органического вещества. Конечно же стоит упомянуть, что этанол — это тот самый спирт, который входит в состав алкогольных напитков. Другие представленные здесь спирты по запаху, цвету и даже вкусу довольно похожи на этиловый спирт. Но они очень вредны для здоровья человка. Например, один глоток метанола может оставить человека слепым на всю жизнь. А если выпить больше, то это можеть оказаться фатальным для жизни. Ещё здесь из четырёх спиртов есть два изомера: 1-пропанол и 2-пропанол. У них одинаковые брутто-формулы, хотя вещества это разные. Их молекулы отличаются номером углеродного атома, к которому крепится группа OH. Возможно, Вы спросите, почему у 1-пропанола гидроксильная группа присоединена к третьему, а не к первому атому углерода? Тут следует вспомнить, что молекулы не находятся в одном положении. Они постоянно крутятся. И вполне могут развернуться как угодно: Все спирты, с которыми мы уже успели познакомиться, имеют в своём составе одну гидроксильную группу. Химики называют их одноатомные спирты. Но существуют вещества с различным количеством гидроксильных групп. Они соответственно называются двухатомные спирты, трёхатомные спирты и так далее. В качестве примера трёхатомного спирта можно привести достаточно известное вещество — глицерин: Развёрнутая формула Упрощённая формула Скелетная формула Брутто-формула H-C-C-C-H; $slope(45)H`/O|#2|H; H`/O|#3|H; H`/O|#4|H OH|CH2-CH -CH2`|OH HO\/ \/OH Ну и чтобы завершить знакомство со спиртами, приведу ещё формулу другого известного вещества — холестерина. Далеко не все знают, что он является одноатомным спиртом! Карбоновые кислоты Любой винодел знает, что вино должно храниться без доступа воздуха. Иначе оно скиснет. Но химики знают причину — если к спирту присоединить ещё один атом кислорода, то получится кислота. Посмотрим на формулы кислот, которые получаются из уже знакомых нам спиртов: Вещество Развёрнутая структурная формула Упрощенная структурная формула Скелетная формула Брутто-формула Метановая кислота (муравьиная кислота) H/C`|O|\OH HCOOH O//\OH Этановая кислота (уксусная кислота) H-C-C \O-H; H|#C|H CH3-COOH /`|O|\OH Пропановая кислота (метилуксусная кислота) H-C-C-C \O-H; H|#2|H; H|#3|H CH3-CH2-COOH \/`|O|\OH Бутановая кислота (масляная кислота) H-C-C-C-C \O-H; H|#2|H; H|#3|H; H|#4|H CH3-CH2-CH2-COOH /\/`|O|\OH Обобщённая формула -C \O-H -COOH или -CO2H /`|O|\OH Отличительной особенностью органических кислот является наличие карбоксильной группы (COOH), которая и придаёт таким веществам кислотные свойства. Все, кто пробовал уксус, знают что он весьма кислый. Причиной этого является наличие в нём уксусной кислоты. Обычно столовый уксус содержит от 3 до 15% уксусной кислоты, а остальное (по большей части) — вода. Употребление в пищу уксусной кислоты в неразбавленном виде представляет опасность для жизни. Карбоновые кислоты могут иметь несколько карбоксильных групп. В этом случае они называются: двухосновная, трёхосновная и т.д. В пищевых продуктах содержится немало других органических кислот. Вот только некоторые из них: Щавелевая кислота Молочная кислота Яблочная кислота Лимонная кислота HOOC-COOH H3C\ /COOH HOOC\/ \COOH HOOC\/ \/COOH двухосновная карбоновая кислота оксикарбоновая кислота Двухосновная оксикарбоновая кислота Трёхосновная оксикарбоновая кислота Название этих кислот соответствует тем пищевым продуктам, в которых они содержатся. Кстати, обратите внимание, что здесь встречаются кислоты, имеющие и гидроксильную группу, характерную для спиртов. Такие вещества называются оксикарбоновыми кислотами (или оксикислотами). Внизу под каждой из кислот подписано, уточняющее название той группы органических веществ, к которой она относится. Радикалы Радикалы — это ещё одно понятие, которое оказало влияние на химические формулы. Само слово наверняка всем известно, но в химии радикалы не имеют ничего общего с политиками, бунтовщиками и прочими гражданами с активной позицией. Здесь это всего лишь фрагменты молекул. И сейчас мы разберёмся, в чём их особенность и познакомимся с новым способом записи химических формул. Выше по тексту уже несколько раз упоминались обобщённые формулы: спирты — -OH и карбоновые кислоты — -COOH . Напомню, что -OH и -COOH — это функциональные группы. А вот R — это и есть радикал. Не зря он изображается в виде буквы R. Если выражаться более определённо, то одновалентным радикалом называется часть молекулы, лишённая одного атома водорода. Ну а если отнять два атома водорода, то получится двухвалентный радикал. Радикалы в химии получили собственные названия. Некоторые из них получили даже латинские обозначения, похожие на обозначения элементов. И кроме того, иногда в формулах радикалы могут быть указаны в сокращённом виде, больше напоминающем брутто-формулы. Всё это демонстрируется в следующей таблице. Название Структурная формула Обозначение Краткая формула Пример спирта Метил CH3-<> Me CH3 -OH CH3OH Этил CH3-CH2-<> Et C2H5 -OH C2H5OH Пропил CH3-CH2-CH2-<> Pr C3H7 -OH C3H7OH Изопропил H3C\CH(*`/H3C*)-<> i-Pr C3H7 -OH (CH3)2CHOH Фенил `/`=`\//-\-<> Ph C6H5 -OH C6H5OH Думаю, что здесь всё понятно. Хочу только обратить внимание на колонку, где приводятся примеры спиртов. Некоторые радикалы записываются в виде, напоминающем брутто-формулу, но функциональная группа записывается отдельно. Например, CH3-CH2-OH превращается в C2H5OH . А для разветвлённых цепочек вроде изопропила применяются конструкции со скобочками. Существует ещё такое явление, как свободные радикалы. Это радикалы, которые по каким-то причинам отделились от функциональных групп. При этом нарушается одно из тех правил, с которых мы начали изучение формул: число химических связей уже не соответствует валентности одного из атомов. Ну или можно сказать, что одна из связей становится незакрытой с одного конца. Обычно свободные радикалы живут короткое время, ведь молекулы стремятся вернуться в стабильное состояние. Знакомство с азотом. Амины Предлагаю познакомиться с ещё одним элементом, который входит в состав многих органических соединений. Это азот. Он обозначается латинской буквой N и имеет валентность, равную трём. Посмотрим, какие вещества получаются, если к знакомым нам углеводородам присоединить азот: Вещество Развёрнутая структурная формула Упрощенная структурная формула Скелетная формула Брутто-формула Аминометан (метиламин) H-C-N \H;H|#C|H CH3-NH2 \NH2 Аминоэтан (этиламин) H-C-C-N \H;H|#C|H;H|#3|H CH3-CH2-NH2 /\NH2 Диметиламин H-C-N -C-H; H|#-3|H; H|#2|H $L(1.3)H/N \dCH3 /N \ Аминобензол (Анилин) H\N |C\C |C `//C `\C `||C / NH2|C\CH|CH`//C `\HC`||HC/ NH2|\|`/`\`|/_o Триэтиламин $slope(45)H-C-C/N\C-C-H;H|#2|H; H|#3|H; H|#5|H;H|#6|H; #N`|C `|C `|H CH3-CH2-N -CH2-CH3 \/N \| Как Вы уже наверное догадались из названий, все эти вещества объединяются под общим названием амины. Функциональная группа <>-NH2 называется аминогруппой. Вот несколько обобщающих формул аминов: По числу замещённых атомов водорода По числу аминогрупп в молекуле Первичный амин -NH2 Моноамин -NH2 Вторичный амин -NH- Диамин H2N--NH2 Третичный амин -N — Триамин H2N-(*`|NH2*)-NH2 В общем, никаких особых новшеств здесь нет. Если эти формулы Вам понятны, то можете смело заниматься дальнейшим изучением органической химии, используя какой-нибудь учебник или интернет. Но мне бы хотелось ещё рассказать о формулах в неорганической химии. Вы убедитесь, как их легко будет понять после изучения строения органических молекул. Рациональные формулы Не следует делать вывод о том, что неорганическая химия проще, чем органическая. Конечно, неорганические молекулы обычно выглядят гораздо проще, потому что они не склонны к образованию таких сложных структур, как углеводороды. Но зато приходится изучать более сотни элементов, входящих в состав таблицы Менделеева. А элементы эти имеют склонность объединяться по химическим свойствам, но с многочисленными исключениями. Так вот, ничего этого я рассказывать не буду. Тема моей статьи — химические формулы. А с ними как раз всё относительно просто. Наиболее часто в неорганической химии употребляются рациональные формулы. И мы сейчас разберёмся, чем же они отличаются от уже знакомых нам. Для начала, познакомимся с ещё одним элементом — кальцием. Это тоже весьма распространённый элемент. Обозначается он Ca и имеет валентность, равную двум. Посмотрим, какие соединения он образует с известными нам углеродом, кислородом и водородом. Вещество Структурная формула Рациональная формула Брутто-формула Оксид кальция Ca=O CaO Гидроксид кальция H-O-Ca-O-H Ca(OH)2 Карбонат кальция $slope(45)Ca`/O\C|O`|/O`\#1 CaCO3 Гидрокарбонат кальция HO/`|O|\O/Ca\O/`|O|\OH Ca(HCO3)2 Угольная кислота H|O\C|O`|/O`|H H2CO3 При первом взгляде можно заметить, что рациональная формула является чем то средним между структурной и брутто-формулой. Но пока что не очень понятно, как они получаются. Чтобы понять смысл этих формул, нужно рассмотреть химические реакции, в которых участвуют вещества. Кальций в чистом виде — это мягкий белый металл. В природе он не встречается. Но его вполне возможно купить в магазине химреактивов. Он обычно хранится в специальных баночках без доступа воздуха. Потому что на воздухе он вступает в реакцию с кислородом. Собственно, поэтому он и не встречается в природе. Итак, реакция кальция с кислородом: Но и гидроксид кальция не встречается в природе из-за наличия в воздухе углекислого газа. Думаю, что все слыхали про этот газ. Он образуется при дыхании людей и животных, сгорании угля и нефтепродуктов, при пожарах и извержениях вулканов. Поэтому он всегда присутствует в воздухе. Но ещё он довольно хорошо растворяется в воде, образуя угольную кислоту: Таким образом, гидроксид кальция, растворённый в воде, вступает в реакцию с угольной кислотой и превращается в малорастворимый карбонат кальция: Из карбоната кальция в значительной степени состоят мел, известняк, мрамор, туф и многие другие минералы. Так же он входит в состав кораллов, раковин моллюсков, костей животных и т.д. Но если карбонат кальция раскалить на очень сильном огне, то он превратится в оксид кальция и углекислый газ. Этот небольшой рассказ о круговороте кальция в природе должен пояснить, для чего нужны рациональные формулы. Так вот, рациональные формулы записываются так, чтобы были видны функциональные группы. В нашем случае это: OH Гидроксильная группа CO3 Карбонат — соль угольной кислоты HCO3 Гидрокарбонат — кислая соль угольной кислоты Кроме того, отдельные элементы — Ca, H, O(в оксидах) — тоже являются самостоятельными группами. Думаю, что пора знакомиться с ионами. Это слово наверняка всем знакомо. А после изучения функциональных групп, нам ничего не стоит разобраться, что же представляют собой эти ионы. В общем, природа химических связей обычно заключается в том, что одни элементы отдают электроны, а другие их получают. Электроны — это частицы с отрицательным зарядом. Элемент с полным набором электронов имеет нулевой заряд. Если он отдал электрон, то его заряд становится положительным, а если принял — то отрицатеньным. Например, водород имеет всего один электрон, который он достаточно легко отдаёт, превращаясь в положительный ион. Для этого существует специальная запись в химических формулах: Отрицательно заряженные ионы называются анионы. Обычно к ним относятся кислотные остатки. Положительно заряженные ионы — катионы. Чаще всего это водород и металлы. И вот здесь наверное можно полностью понять смысл рациональных формул. В них сначала записывается катион, а за ним — анион. Даже если формула не содержит никаких зарядов. Вы наверное уже догадываетесь, что ионы можно описывать не только рациональными формулами. Вот скелетная формула гидрокарбонат-аниона: Система Хилла Итак, можно считать, что мы уже изучили структурные и рациональные формулы. Но есть ещё один вопрос, который стоит рассмотреть подробнее. Чем же всё-таки отличаются брутто-формулы от рациональных? Мы знаем почему рациональная формула угольной кислоты записывается H2CO3 , а не как-то иначе. (Сначала идут два катиона водорода, а за ними карбонат-анион). Но почему брутто-формула записывается CH2O3 ? В принципе, рациональная формула угольной кислоты вполне может считаться истинной формулой, ведь в ней нет повторяющихся элементов. В отличие от NH4OH или Ca(OH)2 . Но к брутто-формулам очень часто применяется дополнительное правило, определяющее порядок следования элементов. Правило довольно простое: сначала ставится углерод, затем водород, а дальше остальные элементы в алфавитном порядке. Вот и выходит CH2O3 — углерод, водород, кислород. Это называется системой Хилла. Она используется практически во всех химических справочниках. И в этой статье тоже. Немного о системе easyChem Вместо заключения мне хотелось бы рассказать о системе easyChem. Она разработана для того, чтобы все те формулы, которые мы тут обсуждали, можно было легко вставить в текст. Собственно, все формулы в этой статье нарисованы при помощи easyChem. Зачем вообще нужна какая-то система для вывода формул? Всё дело в том, что стандартный способ отображения информации в интернет-браузерах — это язык гипертекстовой разметки (HTML). Он ориентирован на обработку текстовой информации. Рациональные и брутто-формулы вполне можно изобразить при помощи текста. Даже некоторые упрощённые структурные формулы тоже могут быть записаны текстом, например спирт CH3-CH2-OH . Хотя для этого пришлось бы в HTML использовать такую запись: CH3-CH2-OH . Это конечно создаёт некоторые трудности, но с ними можно смириться. Но как изобразить структурную формулу? В принципе, можно использовать моноширинный шрифт: Выглядит конечно не очень красиво, но тоже осуществимо. Настоящая проблема возникает при попытке изобразить бензольные кольца и при использовании скелетных формул. Здесь не остаётся иного пути, кроме подключения растрового изображения. Растры хранятся в отдельных файлах. Браузеры могут подключать изображения в формате gif, png или jpeg. Для создания таких файлов требуется графический редактор. Например, Фотошоп. Но я более 10 лет знаком с Фотошопом и могу сказать точно, что он очень плохо подходит для изображения химических формул. Гораздо лучше с этой задачей справляются молекулярные редакторы. Но при большом количестве формул, каждая из которых хранится в отдельном файле, довольно легко в них запутаться. Например, число формул в этой статье равно . Из них выведены виде графических изображений (остальные при помощи средств HTML). Система easyChem позволяет хранить все формулы прямо в HTML-документе в текстовом виде. По-моему, это очень удобно. Кроме того, брутто-формулы в этой статье вычисляются автоматически. Потому что easyChem работает в два этапа: сначала текстовое описание преобразуется в информационную структуру (граф), а затем с этой структурой можно выполнять различные действия. Среди них можно отметить следующие функции: вычисление молекулярной массы, преобразование в брутто-формулу, проверка на возможность вывода в виде текста, графическая и текстовая отрисовка. Таким образом, для подготовки этой статьи я пользовался только текстовым редактором. Причём, мне не пришлось думать, какая из формул будет графической, а какая — текстовой. Вот несколько примеров, раскрывающих секрет подготовки текста статьи: Текстовое описание easyChem Выводимый результат Сгенерированная брутто-формула (NH4)2CO3 (NH4)2CO3 H-C-C-O-H; H|#2|H; H|#3|H H-C-C-O-H; H|#2|H; H|#3|H CH3|\|`//`\`||/ CH3|\|`//`\`||/ Описания из левого столбца автоматически превращаются в формулы во втором столбце. В первой строчке описание рациональной формулы очень похоже на отображаемый результат. Разница только в том, что числовые коэффициенты выводятся подстрочником. Во второй строке развёрнутая формула задана в виде трёх отдельных цепочек, разделённых символом ; Я думаю, нетрудно заметить, что текстовое описание во многом напоминает те действия, которые потребовались бы для изображения формулы карандашом на бумаге. В третьей строке демонстрируется использование наклонных линий при помощи символов \ и /. Значок ` (обратный апостроф) означает, что линия проводится справа налево (или снизу вверх). Здесь есть гораздо более подробная документация по использованию системы easyChem. На этом разрешите закончить статью и пожелать удачи в изучении химии. Источник
- 3. Назовите различия между шаростержневыми и масштабными моделями органических соединений.
- 4. Раскройте сущность понятия «химическое строение вещества».
- 5. Химическую связь между какими атомами указывает черточка в сокращенной структурной формуле этана $\mathrm<СН_3 - СН_3>?$
- 6. Укажите общее число атомов в молекуле метана: а) 2; б) 3; в) 4; г) 5.
- 7. Попытайтесь написать структурную формулу органического соединения c молекулярной формулой $\mathrm,$ являющегося производным углеводорода этана.
- 8. Изобразите соединение, показанное на рисунке 88, в виде структурной формулы.
- 9. На основании пространственного изображения молекулы этана на рисунке 86 попытайтесь изобразить пространственное строение молекулы с молекулярной формулой $\mathrm.$
- Способы изображения органических молекул.
- Химические формулы для «чайников»
- Структурные формулы — это просто!
- Углеводороды
- Двойные и тройные связи
- Циклические углеводороды
- Изомеры
- Бензол и скелетные формулы
- Трехмерные изображения
- Формулы с окружностью
- Знакомство с кислородом. Спирты
- Карбоновые кислоты
- Радикалы
- Знакомство с азотом. Амины
- Рациональные формулы
- Система Хилла
- Немного о системе easyChem
§ 21. Способы изображения органических соединений
1. Какую информацию можно получить из молекулярной формулы органического соединения?
Молекулярная формула органического соединения показывает, какие атомы и каком количестве присутствуют в данном органическом соединении.
2. Приведены названия и формулы различных веществ: а) оксид углерода(IV) $\mathrm;$ б) дихлорметан $\mathrm;$ в) метан $\mathrm;$ г) карбонат натрия $\mathrm.$ Какие из них относятся к органическим веществам?
К органическим веществам относят: б) дихлорметан $\mathrm
3. Назовите различия между шаростержневыми и масштабными моделями органических соединений.
В шаростержневых моделях атомы изображают в виде трубок из пластмассы и отражают взаимное расположение атомов в пространстве. В масштабных моделях атомы изображают в виде сферы с размерами, пропорциональными их радиусу.
4. Раскройте сущность понятия «химическое строение вещества».
Химическое строение — последовательность соединения атомов в молекулах органических соединений; в молекуле этана, например:
атомы углерода соединены друг с другом, а атомы водорода связаны с атомами углерода.
5. Химическую связь между какими атомами указывает черточка в сокращенной структурной формуле этана $\mathrm<СН_3 - СН_3>?$
В сокращённой структурной формуле этана чёрточка показывает связь между атомами углерода.
6. Укажите общее число атомов в молекуле метана: а) 2; б) 3; в) 4; г) 5.
Общее число атомов в молекуле метана $\mathrm
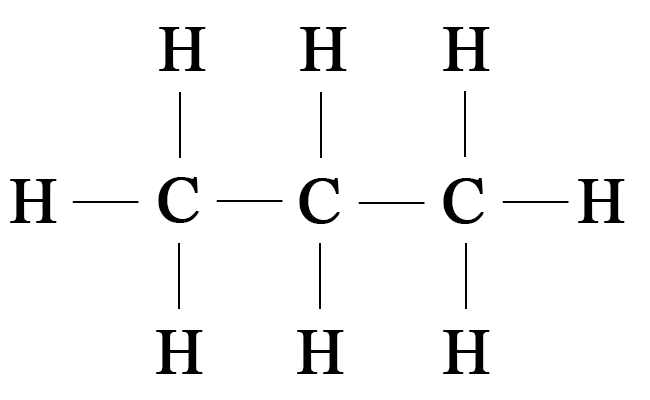
7. Попытайтесь написать структурную формулу органического соединения c молекулярной формулой $\mathrm,$ являющегося производным углеводорода этана.
Структурная формула соединения $\mathrm
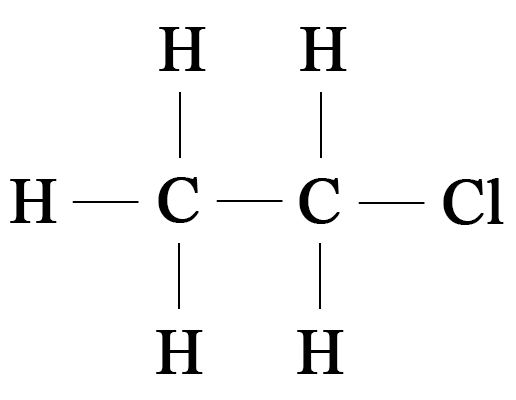
8. Изобразите соединение, показанное на рисунке 88, в виде структурной формулы.
Структурная формула отображает порядок (последовательность) соединения атомов в молекулах.
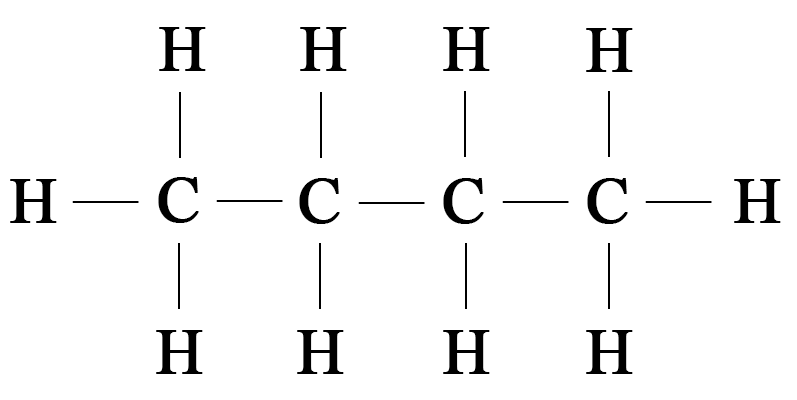
9. На основании пространственного изображения молекулы этана на рисунке 86 попытайтесь изобразить пространственное строение молекулы с молекулярной формулой $\mathrm.$
Пространственное строение молекулы $\mathrm
Источник
Способы изображения органических молекул.
Органическая химия.
2.1.Тема: «Теория строения органических соединений»
2.1.1. Основные положения теории строения органических соединений и классификация органических соединений.
1. Природные и синтетические органические вещества. Немного из истории органической химии. Общие свойства органических веществ (состав, тип химической связи, кристаллическое строение, растворимость, отношение к нагреванию в присутствии кислорода и без него).
2. Теория строения органических соединений А.М.Бутлерова. Развитие теории и ее значение.
3. Классификация органических веществ.
Свое название органические вещества получили потому, что первые из изученных веществ этой группы входили в состав живых организмов. Большинство известных сейчас органических веществ не встречаются в живых организмах, они получены (синтезированы) в лаборатории. Поэтому различают природные (натуральные) органические вещества (хотя большинство из них может быть сейчас получено в лаборатории), а органические вещества, не существующие в природе – синтетические органические веществами. Т.е. название «органические вещества» историческое и особого смысла не имеет. Все органические соединения являются соединениями углерода. К органическим веществам относятся соединения углерода, кроме изучаемых в курсе неорганической химии простых веществ, образованных Карбоном, его оксидов, угольной кислоты и ее солей. Другими словами: органическая химия – это химия соединений углерода.
Краткая история развития орг.химии:
Берцелиус, 1827, первый учебник органической химии. Виталисты. Учение о «жизненной силе».
Первые органические синтезы. Велер, 1824, синтез щавелевой кислоты и мочевины. Кольбе,1845, уксусная кислота. Бертло,1845, жир. Бутлеров,1861, сахаристое вещество.
Но как наука органическая химия началась с создания теории строения органических соединений. Существенный вклад в нее внесли немецкий ученый Ф.А.Кекуле и шотландец А.С.Купер. Но решающий вклад несомненно принадлежит русскому химику А.М.Бутлерову.
Среди всех элементов углерод выделяется своей способностью образовывать устойчивые соединения, в которых его атомы связаны друг с другом в длинные цепи различной конфигурации (линейные, разветвленные, замкнутые). Причина этой способности: примерно одинаковая энергия связи С-С и С-О (для других элементов энергия второй – намного больше). Кроме того, атом углерода может находиться в одном из трех видов гибридизации, образуя соответственно одинарные, двойные или тройные связи, причем не только между собой, но и с атомами кислорода или азота. Правда, гораздо чаще (практически всегда) атомы углерода соединены с атомами водорода. Если в состав органического соединения входит только углерод и водород, то соединения называются углеводородами. Все остальные соединения можно рассматривать как производные углеводородов, в которых некоторые атомы водорода замещены на другие атомы или группы атомов. Поэтому более точное определение: Органические соединения – это углеводороды и их производные.
Органических соединений очень много — более 10 млн. (неорганических около 500 тыс.). Состав, строение и свойства всех органических веществ имеют много общего.
Органические вещества имеют ограниченный качественный состав. Обязательно С и Н, часто О или N, реже галогены, фосфор, сера. Другие элементы входят в состав очень редко. А вот число атомов в молекуле может достигать млн, и молекулярная масса может быть очень большая.
Строение органических соединений. Т.к. состав – неметаллы. => Химическая связь: ковалентная. Неполярная и полярная. Ионная очень редко. => Кристаллическая решетка чаще всего молекулярная.
Общие физические свойства: невысокая температура кипения и плавления. Среди органических веществ есть газы, жидкости и легкоплавкие твердые вещества. Часто летучи, могут иметь запах. Обычно бесцветные. Большинство органических веществ нерастворимо в воде.
Общие химические свойства:
1) при нагревании без доступа воздуха все органические вещества «обугливаются», т.е. при этом образуется уголь (точнее сажа) и некоторые другие неорганические вещества. Происходит разрыв ковалентных связей, сначала полярных, потом и неполярных.
2) При нагревании в присутствии кислорода все органические вещества легко окисляются, и при этом конечными продуктами окисления являются углекислый газ и вода.
Особенности протекания органических реакций. В органических реакциях участвуют молекулы, в процессе реакции должны разорваться одни ковалентные связи и образуются другие. Поэтому химические реакции с участием органических соединений идут обычно очень медленно, для их проведения необходимо применять повышенную температуру, давление и катализаторы.В неорганических реакциях обычно участвуют ионы, реакции протекают очень быстро, иногда мгновенно, при нормальной температуре. Органические реакции редко приводят к высокому выходу продукции (обычно менее 50%). Они часто являются обратимыми, кроме того, может протекать не одна, а несколько реакций, конкурирующих между собой, а значит продуктами реакции будет смесь различных соединений. Поэтому и форма записи органических реакций тоже несколько другая. Т.е. используют не химические уравнения, а схемы химических реакций, в которых нет коэффициентов, но зато подробно указаны условия реакции. Принято также под уравнением записывать названия орг. веществ и тип реакции.
Но в целом органические вещества и реакции подчиняются общим законам химии, а органические вещества превращаются в неорганические или могут образовываться из неорганических. Что еще раз подчеркивает единство окружающего нас мира.
Основные принципы теории химического строения, изложенные молодым А.М.Бутлеровым на международном съезде естествоиспытателей в 1861 г.
1). Атомы в молекулах соединены между собой в определенном порядке, в соответствии с их валентностью. Последовательность соединения атомов называют химическим строением.
Валентность — это способность атомов образовывать определенное количество связей (ковалентных). Валентность зависит от числа неспаренных электронов в атоме элемента, потому что ковалентные связи образуются за счет общих электронных пар при спаривании электронов. Углерод во всех органических веществах четырехвалентен. Водород — 1, Кислород -П, азот – Ш, сера – П, хлор – 1.
Способы изображения органических молекул.
Молекулярная формула – условное изображение состава вещества. Н2СО3 — угольная кислота, С12Н22О11 – сахароза. Такие формулы удобны для расчетов. Но они не дают информацию о строении и свойствах вещества. Поэтому даже молекулярные формулы в органике пишут особым образом: СН3ОН. Но гораздо чаще пользуются структурными формулами. Структурная формула отражает порядок соединения атомов в молекуле (т.е. химическое строение).И в основе любой органической молекулы лежит углеродный скелет – это цепочка связанных между собой ковалентными связями атомы углерода.
Электронные формулы молекул – связи между атомами показаны парами электронов.



Структурные формулы отражают только порядок соединения атомов. Но молекулы органических соединений редко имеют плоское строение. Объемный образ молекулы важен для понимания многих химических реакций. Образ молекулы описывают с помощью таких понятий как длина связи и валентный угол. Кроме того, возможно свободное вращение вокруг одинарных связей. Наглядное представление дают молекулярные модели.
Источник
Химические формулы для «чайников»
Структурные формулы — это просто!
Я думаю, что знакомство с формулами лучше всего начать со структурных формул органических веществ. Считается, что они сложны для понимания, поэтому в школе их изучают в выпускных классах. Но я уверен, что через 10 минут вы разберетесь, как легко составлять структурные формулы.
Перед нами структурная формула метана — самого простого органического вещества.
Что мы видим? В центре латинская буква C, а от неё четыре палочки, на концах которых четыре латинских буквы H. C означает углерод, а H — водород. Это два самых важных элемента, которые входят в состав любых органических веществ. А что означают палочки? Это химические связи. В них кроется практически весь секрет органической химии.
Фокус в том, что валентность углерода равна 4. Поэтому у каждой буквы C должно быть 4 палочки. А валентность водорода равна 1, поэтому у него палочка должна быть только одна.
По-моему, палочки отлично демонстрируют такие «страшные» понятия, как химические связи и валентность.
Структурные формулы могут слегка менять свой внешний вид. В них главное — количество элементов и наличие нужных связей. Например, формула метана может иметь и такой вид:
В общем, структурные формулы не являются какими-то жесткими конструкциями. Если вдруг Вам захотелось бы сделать модель молекулы из подручных материалов, то для этого лучше всего подошли бы шарики, соединённые пружинками или резинками. Под шариками я конечно подразумеваю атомы, а резинки — химические связи.
Но в химии приняты не только структурные формулы. И здесь мы познакомимся с некоторыми из них. Достаточно распространены так называемые истинные формулы. Для метана истинная формула записывается так:
Стоит упомянуть, что метан — это природный газ, который знаком всем, у кого есть газовая плита. Но не будем на нём долго задерживаться. Пора посмотреть, какие ещё бывают варианты органических структур.
Углеводороды
Прежде, чем мы начнём знакомство с многочисленными органическими соединениями, хочу напомнить — мы здесь изучаем химические формулы. А все упоминаемые вещества служат для иллюстрации.
| Вещество | Развёрнутая структурная формула | Упрощенная структурная формула | Брутто-формула | |||
|---|---|---|---|---|---|---|
| Этан | H-C-C-H; H|#2|H; H|#3|H | CH3-CH3 | Пропан | H-C-C-C-H; H|#2|H; H|#3|H; H|#4|H | CH3-CH2-CH3 | Бутан | H-C-C-C-C-H; H|#2|H; H|#3|H; H|#4|H; H|#5|H | CH3-CH2-CH2-CH3 | Пентан | H-C-C-C-C-C-H;H|#2|H;H|#3|H;H|#4|H;H|#5|H;H|#6|H | CH3-CH2-CH2-CH2-CH3 | Гексан | H-C-C-C-C-C-C-H;H|#2|H;H|#3|H;H|#4|H;H|#5|H;H|#6|H;H|#7|H |
| Вещество | Развёрнутая формула | Упрощённая формула | Брутто-фломула |
|---|---|---|---|
| Этен (Этилен) | $slope(55)H\C _(x1,N2)C /H | CH2=CH2 | |
| Пропен (Пропилен) | $slope(45)H\C-C/C/H; H\#-3\H;H/#2-#3\H | CH2=CH-CH3 | |
| Бутен (Бутилен) | H\C =C -C -C-H; H|#-3|H | CH2=CH-CH2-CH3 | |
| Этин (Ацетилен) | H-C%C-H | CH%CH | |
| Пропин (Метилацетилен) | H-C%C-C-H; H|#-3|H | CH%C-CH3 | |
| Бутин (Этилацетилен) | H-C%C-C -C-H; H|#-3|H | CH%C-CH2-CH3 |
Представленные здесь вещества тоже относятся к углеводородам. Если хорошенько присмотреться, то можно увидеть определённое сходство с веществами из первой таблицы. Названия формируются заменой буквы в конце названия: этан — этен — этин или пропан — пропен — пропин. Сходство не ограничивается названиями. Главное — одинаковое количество атомов углерода. А значит — одинаковое количество звеньев в цепи.
Различие кроется в наличии двойных и тройных связей. Углеводороды в первой таблице называются предельными. Это означает, что к ним больше ничего нельзя добавить. А во второй таблице представлены непредельные углеводороды. То есть, при определённых условиях к ним можно добавить по парочке атомов водорода.
Кроме того, появились дополнительные названия. Тут тоже нет ничего страшного. Верхние названия, которые без скобок — это научные названия. А в скобках даны традиционные названия, которые тоже довольно часто употребляются как в научной литературе, так и в быту.
Циклические углеводороды
Продолжим знакомство с формулами углеводородов. Они ещё не раскрыли нам всех своих секретов. Оказывается, что цепочки могут быть замкнутыми. То есть, атомы углерода соединяются друг с другом циклически.
| Вещество | Развёрнутая формула | Упрощённая формула | Брутто-формула |
|---|---|---|---|
| Циклопропан | $slope(60)H`/C`/C:a`/H; H\#C\C:b\H; H-#a-#b-H | H2C_(x1.4)CH2_q3CH2_q3 | |
| Циклобутан | H|C|C|H; H|C|C|H; H-#2-#6-H; H-#3-#7-H | H2C-CH2`|CH2`-H2C_#1 | |
| Циклопентан | C_(x1.1)C@:H2() @()_qC@H2()_qC@H2()_qC@H2()_q@H2() | H2C_(x1.4)CH2_qCH2_qCH2_qH2C_q | |
| Циклогексан | C\C@:H2() @()|C@H2()`/C@H2()`\C@H2()`|C@H2()/@H2() | $L(1.3)CH2\CH2|CH2`/CH2`\H2C`|H2C/ |
Изомеры
До сих пор мы не особенно обращали внимания на последнюю колонку, где выведены брутто-формулы. Но может возникнуть вполне законный вопрос: зачем вообще нужны структурные формулы? Ведь брутто-формулы гораздо проще записывать. Может быть, достаточно было бы пользоваться только ими?
Но оказывается, что без структурных формул обойтись не получится. Например, если сравнить брутто-формулы из двух предыдущих таблиц, то мы увидим, что циклопропан имеет абсолютно тот же состав, что и пропен ( C3H6 ). А брутто-формула циклобутана совпадает с бутеном ( C4H8 ). Но это разные вещества! И разница заключается в структуре. То есть, имеет большое значение, в каком порядке элементы соединены друг с другом. А значит, именно структурные формулы позволяют точно описать нужное вещество.
В химии существует такое понятие как изомеры. Так называют разные вещества, которые имеют одинаковый состав. Это не редкость. И в этом нет ничего странного. Ведь бывают же совершенно разные слова, состоящие из одинаковых букв.
Классическими изомерами среди углеводородов можно назвать бутан и изобутан. Посмотрим на их формулы:
| Вещество | Развёрнутая структурная формула | Упрощенная структурная формула | Брутто-формула | Бутан | H-C-C-C-C-H; H|#2|H; H|#3|H; H|#4|H; H|#5|H | CH3-CH2-CH2-CH3 | Метилпропан (Изобутан) | H\C\C/C/H; H|#2`/H; H|#4\H; H|#3|C|H; H/#-3\H | CH3-CH -CH3 |
|---|---|---|---|---|---|---|
| Вещество | Упрощённая формула | Брутто-формула |
|---|---|---|
| Пентан | CH3-CH2-CH2-CH2-CH3 | |
| 2-метилбутан (Изопентан) | CH3-CH -CH2-CH3 | |
| 2,2-диметилпропан (Неопентан) | CH3-C -CH3 |
А у вещества декан, имеющего формулу C10H22 , существует 75 изомеров. Но мы не будем их здесь рассматривать.
Обратите внимание, что научное название зависит от числа звеньев в прямой цепочке, а традиционное название просто учитывает количество атомов углерода в молекуле. Так получилось из-за того, что химики, которые только начинали исследовать углеводороды, первым делом научились определять состав веществ. То есть, сначала люди смогли получить лишь брутто-формулы. А из них невозможно понять, какова длина самой длинной цепочки. Поэтому названия учитывали общее число атомов углерода.
Затем наука дошла до того, что люди смогли исследовать структуру молекул, придумали структурные формулы и переименовали уже известные вещества в соответствии с новыми знаниями. Но старые названия уже успели прижиться и существуют до сих пор.
Бензол и скелетные формулы
Думаю, что пора познакомиться ещё с одним весьма примечательным представителем углеводородов. Это вещество называется бензол. Вот его формулы:
| Развёрнутая формула | Упрощённая формула | Скелетная формула | Брутто-формула |
|---|---|---|---|
| H|C\C|C `//C `\C `||C /\/H | H_(y.5)C\\CH|CH`//C `\HC`||HC/ | \\|`//`\`||/ |
Чем же этот бензол так примечателен? Дело в том, что это шестиугольное колечко входит в состав огромного числа органических веществ.
И вот на примере бензола предлагаю ознакомиться с ещё одним очень важным способом записи структурных формул — скелетными формулами.
Как видно из таблицы, скелетная формула бензола представляет собой правильный шестиугольник без каких-либо букв, зато изображения химических связей выглядят одинаково.
В общем, правила составления скелетных формул отличаются от уже знакомых нам развёрнутых всего двумя особенностями:
- Буквы C не пишутся. Предполагается, что каждый угол изображаемой геометрической фигуры содержит атом углерода.
- Буквы H тоже не пишутся. Если в углу сходятся меньше четырёх линий, то это означает, что все оставшиеся заняты водородом.
Конечно, скелетные формулы не так просты, как развёрнутые, но зато их гораздо легче записывать. Поэтому в органической химии это самый популярный вид формул. И мне кажется, Вам тоже будет несложно к ним привыкнуть.
Давайте посмотрим, как выглядят формулы других веществ, производных от бензола.
| Вещество | Развёрнутая формула | Скелетная формула | Смешанный вариант | Брутто-формула |
|---|---|---|---|---|
| Нафталин | C/C \\C |C `//C `\C`|`\\C `/C ||C \C/`/|H | /\\|`//`\`|`\\`/||\// | C10H8 | |
| Толуол | H|C|C\C|C `//C `\C `||C /\/H; H-#2-H | |\\|`//`\`||/ | CH3|\\|`//`\`||/ | |
| Кумол | H\C\C/C/H; H|#2|H; H|#4|H; H|#3|C\C|C `//C `\C `||C /\/H | \ |\\|`//`\`||/ | H3C\ |\\|`//`\`||/ |
Как видите, появился ещё и смешанный вариант. Опять какой-то новый вид формул? На этот раз уже нет. Просто иногда внутри одной формулы удобно сочетать различные способы.
А вот скелетная формула углеводорода, который называется коронен. Причём, другие варианты здесь уже использовать нет смысла.
Скелетные формулы существуют не только для циклических молекул. Понятно, что метан и этан имеют слишком мало узлов, поэтому для них не стоит пытаться использовать скелетные формулы. А вот какая-нибудь длинная молекула изображается довольно легко. Только не в виде прямой цепочки, а при помощи ломаной линии, ведь атомы углерода изображаются углами.
| Бутан | Бутен | Изобутан | Гексан |
| /\/ | //\/ | \|`|0/ | /\/\/ |
Трехмерные изображения
Иногда плоского изображения становится недостаточно. Поэтому для изображения трехмерных структурных формул используют особое изображение для химических связей:
Формулы с окружностью
Само собой, все они означают одно и то же. Но первые три отличаются только поворотом вокруг собственного центра. Тут нет ничего необычного, ведь молекулы не стоят на одном месте. А вот дальше мы видим кружок вместо трёх двойных связей. Причём, я намеренно изобразил все атомы водорода в последней формуле. Чтобы было хорошо видно, что каждый угол фактически лишился одной чёрточки. Их заменил кружок. Он как бы означает, что все двойные связи равномерно распределены внутри кольца.
Формулы бензола, где используется чередование одинарных и двойных связей называются формулами Кекуле в честь немецкого учёного, который внёс значительный вклад в исследование структуры бензола.
На самом деле, среди химиков нет единого мнения по поводу того, насколько правильно использование формул с кружком. Некоторые авторы категорически против. Но есть масса публикаций, где такая запись широко употребляется. Моя задача состоит в том, чтобы Вы узнали о существовании подобных формул и не удивлялись, увидев их.
Вот пара примеров записи уже для уже знакомых нам веществ:
| Нафталин: | /\|`/`\`|_o`\`/|\/_o | Толуол: | `/`-`\/-\_o-CH3 |
Знакомство с кислородом. Спирты
До сих пор мы знакомились со структурными формулами углеводородов, которые состоят только из углерода и водорода. Думаю, пора познакомиться с новым элементом — кислородом. Он обозначается латинской буквой O. Его валентнсть равна 2. То есть, каждая буква O в структурных формулах должна снабжаться двумя палочками.
Кислород — очень распространённый элемент на нашей планете. Он входит в состав большого количества органических и неорганических веществ. Но мы начнём знакомство с группы веществ, называемых спиртами:
| Вещество | Развёрнутая структурная формула | Упрощенная структурная формула | Скелетная формула | Брутто-формула |
|---|---|---|---|---|
| Метанол (метиловый спирт) | H-C-O-H; H|#C|H | CH3-OH | \OH | |
| Этанол (этиловый спирт) | H-C-C-O-H; H|#2|H; H|#3|H | CH3-CH2-OH | /\OH | |
| 1-Пропанол (пропиловый спирт) | H-C-C-C-O-H; H|#2|H; H|#3|H; H|#4|H | CH3-CH2-CH2-OH | /\/OH | |
| 2-Пропанол (изопропиловый спирт) | H-C-C-C-H; H|#2|H; H|#3|O|H; H|#4|H | CH3-CH -CH3 | \ / |
Не правда ли, что в этом есть что-то знакомое? Метан — метанол, этан — этанол, пропан — пропанол.
Да, можно сказать, что спирт получается из углеводорода, если заменить один атом -H на группу -O-H (или -OH в упрощенных структурных формулах). Химики называют её: гидроксильная группа, по латинским названиям водорода и кислорода. А иногда она даже называется спиртовой группой.
Все спирты можно описать в виде обобщённой формулы
Конечно же стоит упомянуть, что этанол — это тот самый спирт, который входит в состав алкогольных напитков. Другие представленные здесь спирты по запаху, цвету и даже вкусу довольно похожи на этиловый спирт. Но они очень вредны для здоровья человка. Например, один глоток метанола может оставить человека слепым на всю жизнь. А если выпить больше, то это можеть оказаться фатальным для жизни.
Ещё здесь из четырёх спиртов есть два изомера: 1-пропанол и 2-пропанол. У них одинаковые брутто-формулы, хотя вещества это разные. Их молекулы отличаются номером углеродного атома, к которому крепится группа OH. Возможно, Вы спросите, почему у 1-пропанола гидроксильная группа присоединена к третьему, а не к первому атому углерода? Тут следует вспомнить, что молекулы не находятся в одном положении. Они постоянно крутятся. И вполне могут развернуться как угодно:
Все спирты, с которыми мы уже успели познакомиться, имеют в своём составе одну гидроксильную группу. Химики называют их одноатомные спирты. Но существуют вещества с различным количеством гидроксильных групп. Они соответственно называются двухатомные спирты, трёхатомные спирты и так далее.
В качестве примера трёхатомного спирта можно привести достаточно известное вещество — глицерин:
| Развёрнутая формула | Упрощённая формула | Скелетная формула | Брутто-формула |
|---|---|---|---|
| H-C-C-C-H; $slope(45)H`/O|#2|H; H`/O|#3|H; H`/O|#4|H | OH|CH2-CH -CH2`|OH | HO\/ \/OH |
Ну и чтобы завершить знакомство со спиртами, приведу ещё формулу другого известного вещества — холестерина. Далеко не все знают, что он является одноатомным спиртом!
Карбоновые кислоты
Любой винодел знает, что вино должно храниться без доступа воздуха. Иначе оно скиснет. Но химики знают причину — если к спирту присоединить ещё один атом кислорода, то получится кислота.
Посмотрим на формулы кислот, которые получаются из уже знакомых нам спиртов:
| Вещество | Развёрнутая структурная формула | Упрощенная структурная формула | Скелетная формула | Брутто-формула |
|---|---|---|---|---|
| Метановая кислота (муравьиная кислота) | H/C`|O|\OH | HCOOH | O//\OH | |
| Этановая кислота (уксусная кислота) | H-C-C \O-H; H|#C|H | CH3-COOH | /`|O|\OH | |
| Пропановая кислота (метилуксусная кислота) | H-C-C-C \O-H; H|#2|H; H|#3|H | CH3-CH2-COOH | \/`|O|\OH | |
| Бутановая кислота (масляная кислота) | H-C-C-C-C \O-H; H|#2|H; H|#3|H; H|#4|H | CH3-CH2-CH2-COOH | /\/`|O|\OH | |
| Обобщённая формула |
Отличительной особенностью органических кислот является наличие карбоксильной группы (COOH), которая и придаёт таким веществам кислотные свойства.
Все, кто пробовал уксус, знают что он весьма кислый. Причиной этого является наличие в нём уксусной кислоты. Обычно столовый уксус содержит от 3 до 15% уксусной кислоты, а остальное (по большей части) — вода. Употребление в пищу уксусной кислоты в неразбавленном виде представляет опасность для жизни.
Карбоновые кислоты могут иметь несколько карбоксильных групп. В этом случае они называются: двухосновная, трёхосновная и т.д.
В пищевых продуктах содержится немало других органических кислот. Вот только некоторые из них:
| Щавелевая кислота | Молочная кислота | Яблочная кислота | Лимонная кислота |
| HOOC-COOH | H3C\ /COOH | HOOC\/ \COOH | HOOC\/ \/COOH |
| двухосновная карбоновая кислота | оксикарбоновая кислота | Двухосновная оксикарбоновая кислота | Трёхосновная оксикарбоновая кислота |
Название этих кислот соответствует тем пищевым продуктам, в которых они содержатся. Кстати, обратите внимание, что здесь встречаются кислоты, имеющие и гидроксильную группу, характерную для спиртов. Такие вещества называются оксикарбоновыми кислотами (или оксикислотами).
Внизу под каждой из кислот подписано, уточняющее название той группы органических веществ, к которой она относится.
Радикалы
Радикалы — это ещё одно понятие, которое оказало влияние на химические формулы. Само слово наверняка всем известно, но в химии радикалы не имеют ничего общего с политиками, бунтовщиками и прочими гражданами с активной позицией.
Здесь это всего лишь фрагменты молекул. И сейчас мы разберёмся, в чём их особенность и познакомимся с новым способом записи химических формул.
Выше по тексту уже несколько раз упоминались обобщённые формулы: спирты —
Если выражаться более определённо, то одновалентным радикалом называется часть молекулы, лишённая одного атома водорода. Ну а если отнять два атома водорода, то получится двухвалентный радикал.
Радикалы в химии получили собственные названия. Некоторые из них получили даже латинские обозначения, похожие на обозначения элементов. И кроме того, иногда в формулах радикалы могут быть указаны в сокращённом виде, больше напоминающем брутто-формулы.
Всё это демонстрируется в следующей таблице.
| Название | Структурная формула | Обозначение | Краткая формула | Пример спирта | ||
|---|---|---|---|---|---|---|
| Метил | CH3-<> | Me | CH3 | CH3OH | ||
| Этил | CH3-CH2-<> | Et | C2H5 | C2H5OH | ||
| Пропил | CH3-CH2-CH2-<> | Pr | C3H7 | C3H7OH | ||
| Изопропил | H3C\CH(*`/H3C*)-<> | i-Pr | C3H7 | (CH3)2CHOH | ||
| Фенил | `/`=`\//-\\-<> | Ph | C6H5 | C6H5OH | ||
Думаю, что здесь всё понятно. Хочу только обратить внимание на колонку, где приводятся примеры спиртов. Некоторые радикалы записываются в виде, напоминающем брутто-формулу, но функциональная группа записывается отдельно. Например, CH3-CH2-OH превращается в C2H5OH .
А для разветвлённых цепочек вроде изопропила применяются конструкции со скобочками.
Существует ещё такое явление, как свободные радикалы. Это радикалы, которые по каким-то причинам отделились от функциональных групп. При этом нарушается одно из тех правил, с которых мы начали изучение формул: число химических связей уже не соответствует валентности одного из атомов. Ну или можно сказать, что одна из связей становится незакрытой с одного конца. Обычно свободные радикалы живут короткое время, ведь молекулы стремятся вернуться в стабильное состояние.
Знакомство с азотом. Амины
Предлагаю познакомиться с ещё одним элементом, который входит в состав многих органических соединений. Это азот.
Он обозначается латинской буквой N и имеет валентность, равную трём.
Посмотрим, какие вещества получаются, если к знакомым нам углеводородам присоединить азот:
| Вещество | Развёрнутая структурная формула | Упрощенная структурная формула | Скелетная формула | Брутто-формула |
|---|---|---|---|---|
| Аминометан (метиламин) | H-C-N \H;H|#C|H | CH3-NH2 | \NH2 | |
| Аминоэтан (этиламин) | H-C-C-N \H;H|#C|H;H|#3|H | CH3-CH2-NH2 | /\NH2 | |
| Диметиламин | H-C-N -C-H; H|#-3|H; H|#2|H | $L(1.3)H/N \dCH3 | /N \ | |
| Аминобензол (Анилин) | H\N |C\\C |C `//C `\C `||C / | NH2|C\\CH|CH`//C `\HC`||HC/ | NH2|\|`/`\`|/_o | |
| Триэтиламин | $slope(45)H-C-C/N\C-C-H;H|#2|H; H|#3|H; H|#5|H;H|#6|H; #N`|C `|C `|H | CH3-CH2-N -CH2-CH3 | \/N \| |
Как Вы уже наверное догадались из названий, все эти вещества объединяются под общим названием амины. Функциональная группа <>-NH2 называется аминогруппой. Вот несколько обобщающих формул аминов:
| По числу замещённых атомов водорода | По числу аминогрупп в молекуле |
|---|---|
| Первичный амин | Моноамин |
Вторичный амин | Диамин H2N- | |
Третичный амин | Триамин H2N- | |
В общем, никаких особых новшеств здесь нет. Если эти формулы Вам понятны, то можете смело заниматься дальнейшим изучением органической химии, используя какой-нибудь учебник или интернет.
Но мне бы хотелось ещё рассказать о формулах в неорганической химии. Вы убедитесь, как их легко будет понять после изучения строения органических молекул.
Рациональные формулы
Не следует делать вывод о том, что неорганическая химия проще, чем органическая. Конечно, неорганические молекулы обычно выглядят гораздо проще, потому что они не склонны к образованию таких сложных структур, как углеводороды. Но зато приходится изучать более сотни элементов, входящих в состав таблицы Менделеева. А элементы эти имеют склонность объединяться по химическим свойствам, но с многочисленными исключениями.
Так вот, ничего этого я рассказывать не буду. Тема моей статьи — химические формулы. А с ними как раз всё относительно просто.
Наиболее часто в неорганической химии употребляются рациональные формулы. И мы сейчас разберёмся, чем же они отличаются от уже знакомых нам.
Для начала, познакомимся с ещё одним элементом — кальцием. Это тоже весьма распространённый элемент.
Обозначается он Ca и имеет валентность, равную двум. Посмотрим, какие соединения он образует с известными нам углеродом, кислородом и водородом.
| Вещество | Структурная формула | Рациональная формула | Брутто-формула |
|---|---|---|---|
| Оксид кальция | Ca=O | CaO | |
| Гидроксид кальция | H-O-Ca-O-H | Ca(OH)2 | |
| Карбонат кальция | $slope(45)Ca`/O\C|O`|/O`\#1 | CaCO3 | |
| Гидрокарбонат кальция | HO/`|O|\O/Ca\O/`|O|\OH | Ca(HCO3)2 | |
| Угольная кислота | H|O\C|O`|/O`|H | H2CO3 |
При первом взгляде можно заметить, что рациональная формула является чем то средним между структурной и брутто-формулой. Но пока что не очень понятно, как они получаются. Чтобы понять смысл этих формул, нужно рассмотреть химические реакции, в которых участвуют вещества.
Кальций в чистом виде — это мягкий белый металл. В природе он не встречается. Но его вполне возможно купить в магазине химреактивов. Он обычно хранится в специальных баночках без доступа воздуха. Потому что на воздухе он вступает в реакцию с кислородом. Собственно, поэтому он и не встречается в природе.
Итак, реакция кальция с кислородом:
Но и гидроксид кальция не встречается в природе из-за наличия в воздухе углекислого газа. Думаю, что все слыхали про этот газ. Он образуется при дыхании людей и животных, сгорании угля и нефтепродуктов, при пожарах и извержениях вулканов. Поэтому он всегда присутствует в воздухе. Но ещё он довольно хорошо растворяется в воде, образуя угольную кислоту:
Таким образом, гидроксид кальция, растворённый в воде, вступает в реакцию с угольной кислотой и превращается в малорастворимый карбонат кальция:
Из карбоната кальция в значительной степени состоят мел, известняк, мрамор, туф и многие другие минералы. Так же он входит в состав кораллов, раковин моллюсков, костей животных и т.д.
Но если карбонат кальция раскалить на очень сильном огне, то он превратится в оксид кальция и углекислый газ.
Этот небольшой рассказ о круговороте кальция в природе должен пояснить, для чего нужны рациональные формулы. Так вот, рациональные формулы записываются так, чтобы были видны функциональные группы. В нашем случае это:
| OH | Гидроксильная группа |
| CO3 | Карбонат — соль угольной кислоты |
| HCO3 | Гидрокарбонат — кислая соль угольной кислоты |
Кроме того, отдельные элементы — Ca, H, O(в оксидах) — тоже являются самостоятельными группами.
Думаю, что пора знакомиться с ионами. Это слово наверняка всем знакомо. А после изучения функциональных групп, нам ничего не стоит разобраться, что же представляют собой эти ионы.
В общем, природа химических связей обычно заключается в том, что одни элементы отдают электроны, а другие их получают. Электроны — это частицы с отрицательным зарядом. Элемент с полным набором электронов имеет нулевой заряд. Если он отдал электрон, то его заряд становится положительным, а если принял — то отрицатеньным. Например, водород имеет всего один электрон, который он достаточно легко отдаёт, превращаясь в положительный ион. Для этого существует специальная запись в химических формулах:
Отрицательно заряженные ионы называются анионы. Обычно к ним относятся кислотные остатки.
Положительно заряженные ионы — катионы. Чаще всего это водород и металлы.
И вот здесь наверное можно полностью понять смысл рациональных формул. В них сначала записывается катион, а за ним — анион. Даже если формула не содержит никаких зарядов.
Вы наверное уже догадываетесь, что ионы можно описывать не только рациональными формулами. Вот скелетная формула гидрокарбонат-аниона:
Система Хилла
Итак, можно считать, что мы уже изучили структурные и рациональные формулы. Но есть ещё один вопрос, который стоит рассмотреть подробнее. Чем же всё-таки отличаются брутто-формулы от рациональных?
Мы знаем почему рациональная формула угольной кислоты записывается H2CO3 , а не как-то иначе. (Сначала идут два катиона водорода, а за ними карбонат-анион). Но почему брутто-формула записывается CH2O3 ?
В принципе, рациональная формула угольной кислоты вполне может считаться истинной формулой, ведь в ней нет повторяющихся элементов. В отличие от NH4OH или Ca(OH)2 .
Но к брутто-формулам очень часто применяется дополнительное правило, определяющее порядок следования элементов. Правило довольно простое: сначала ставится углерод, затем водород, а дальше остальные элементы в алфавитном порядке.
Вот и выходит CH2O3 — углерод, водород, кислород. Это называется системой Хилла. Она используется практически во всех химических справочниках. И в этой статье тоже.
Немного о системе easyChem
Вместо заключения мне хотелось бы рассказать о системе easyChem. Она разработана для того, чтобы все те формулы, которые мы тут обсуждали, можно было легко вставить в текст. Собственно, все формулы в этой статье нарисованы при помощи easyChem.
Зачем вообще нужна какая-то система для вывода формул? Всё дело в том, что стандартный способ отображения информации в интернет-браузерах — это язык гипертекстовой разметки (HTML). Он ориентирован на обработку текстовой информации.
Рациональные и брутто-формулы вполне можно изобразить при помощи текста. Даже некоторые упрощённые структурные формулы тоже могут быть записаны текстом, например спирт CH3-CH2-OH . Хотя для этого пришлось бы в HTML использовать такую запись: CH3-CH2-OH .
Это конечно создаёт некоторые трудности, но с ними можно смириться. Но как изобразить структурную формулу? В принципе, можно использовать моноширинный шрифт:
Выглядит конечно не очень красиво, но тоже осуществимо.
Настоящая проблема возникает при попытке изобразить бензольные кольца и при использовании скелетных формул. Здесь не остаётся иного пути, кроме подключения растрового изображения. Растры хранятся в отдельных файлах. Браузеры могут подключать изображения в формате gif, png или jpeg.
Для создания таких файлов требуется графический редактор. Например, Фотошоп. Но я более 10 лет знаком с Фотошопом и могу сказать точно, что он очень плохо подходит для изображения химических формул.
Гораздо лучше с этой задачей справляются молекулярные редакторы. Но при большом количестве формул, каждая из которых хранится в отдельном файле, довольно легко в них запутаться.
Например, число формул в этой статье равно . Из них выведены виде графических изображений (остальные при помощи средств HTML).
Система easyChem позволяет хранить все формулы прямо в HTML-документе в текстовом виде. По-моему, это очень удобно.
Кроме того, брутто-формулы в этой статье вычисляются автоматически. Потому что easyChem работает в два этапа: сначала текстовое описание преобразуется в информационную структуру (граф), а затем с этой структурой можно выполнять различные действия. Среди них можно отметить следующие функции: вычисление молекулярной массы, преобразование в брутто-формулу, проверка на возможность вывода в виде текста, графическая и текстовая отрисовка.
Таким образом, для подготовки этой статьи я пользовался только текстовым редактором. Причём, мне не пришлось думать, какая из формул будет графической, а какая — текстовой.
Вот несколько примеров, раскрывающих секрет подготовки текста статьи:
| Текстовое описание easyChem | Выводимый результат | Сгенерированная брутто-формула |
|---|---|---|
| (NH4)2CO3 | (NH4)2CO3 | |
| H-C-C-O-H; H|#2|H; H|#3|H | H-C-C-O-H; H|#2|H; H|#3|H | |
| CH3|\\|`//`\`||/ | CH3|\\|`//`\`||/ |
Описания из левого столбца автоматически превращаются в формулы во втором столбце.
В первой строчке описание рациональной формулы очень похоже на отображаемый результат. Разница только в том, что числовые коэффициенты выводятся подстрочником.
Во второй строке развёрнутая формула задана в виде трёх отдельных цепочек, разделённых символом ; Я думаю, нетрудно заметить, что текстовое описание во многом напоминает те действия, которые потребовались бы для изображения формулы карандашом на бумаге.
В третьей строке демонстрируется использование наклонных линий при помощи символов \ и /. Значок ` (обратный апостроф) означает, что линия проводится справа налево (или снизу вверх).
Здесь есть гораздо более подробная документация по использованию системы easyChem.
На этом разрешите закончить статью и пожелать удачи в изучении химии.
Источник