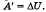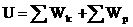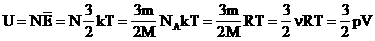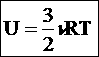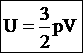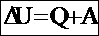Работа в термодинамике. Внутренняя энергия. Первый закон термодинамики. Адиабатный процесс
В термодинамике рассматривается перемещение частиц макроскопического тела относительно друг друга. При совершении работы меняется объем тела. Скорость самого тела остается равной нулю, но скорости
молекул тела меняются! Поэтому меняется и температура тела. Причина в том, что при столкновении с движущимся поршнем (сжатие газа) кинетическая энергия молекул изменяется — поршень отдает часть своей механической энергии. При столкновении с удаляющимся поршнем (расширение) скорости молекул уменьшаются, газ охлаждается. При совершении работы в термодинамике меняется состояние макроскопических тел: их объем и температура.
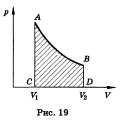
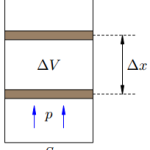
Газ, находящийся в сосуде под поршнем, действует на поршень с силой F’ = pS, где p — давление газа, S — площадь поршня. Если при этом поршень перемещается, то газ совершает работу. Предположим, что газ расширяется при постоянном давлении p. Тогда сила F’, с которой газ действует на поршень, также постоянна. Пусть поршень переместился на расстояние ∆x (рис.1). Работа газа равна: A’ = F’ ∆x = pS∆x = p∆V. – работа газа при изобарном расширении. Если V1 и V2 — начальный и конечный объём газа, то для работы газа имеем: A’ = p(V2 − V1). При расширении работа газа положительна. При сжатии — отрицательна. Таким образом: A’ = pΔV — работа газа. A= — pΔV — работа внешних сил.
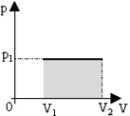
В изобарном процессе площадь под графиком в координатах p,V численно равна работе (рис. 2). Внешняя работа над системой равна работе системы, но с противоположным знаком А = — А’.
В изохорном процессе объем не меняется, следовательно, в изохорном процессе работа не совершается! A=0
Любое тело (газ, жидкость или твердое) обладает энергией, даже если тело не имеет скорости и находится на Земле. Эта энергия называется внутренней , обусловлена она хаотическим (тепловым) движением и взаимодействием частиц, из которых состоит тело. Внутренняя энергия состоит из кинетической и потенциальной энергии частиц поступательного и колебательного движений микрочастиц системы. Внутренняя энергия одноатомного идеального газа определяется по формуле: 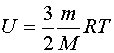
Теплопередача — это изменение внутренней энергии без совершения работы: энергия передается от более нагретых тел к менее нагретым телам. Теплопередача бывает трех видов: теплопроводность (непосредственный обмен энергией между хаотически движущимися частицами взаимодействующих тел или частей одного и того же тела); конвекция (перенос энергии потоками жидкости или газа) и излучение (перенос энергии электромагнитными волнами). Мерой переданной энергии при теплопередаче является количество теплоты (Q).
Эти способы количественно объединены в закон сохранения энергии, который для тепловых процессов читается так: изменение внутренней энергии замкнутой системы равно сумме количества теплоты, переданной системе, и работы внешних сил, совершенной над системой. 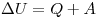
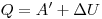
Рассмотрим применение первого закона термодинамики к изопроцессам, происходящим с идеальным газом.
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение I закона термодинамики примет вид: Q = А’, т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
В изобарном процессе газ расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы: Q = ΔU +А’
При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е. А = 0. Уравнение I закона имеет вид Q = ΔU (переданное количество теплоты идет на увеличение внутренней энергии газа).
Адиабатным называют процесс , протекающий без теплообмена с окружающими телами. Пример теплоизолированного сосуда — термос. При адиабатном процессе Q = 0, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается, А’= — ΔU. Если заставить газ совершить достаточно большую работу, то охладить его можно очень сильно. Именно на этом основаны методы сжижения газов. И наоборот, в процессе адиабатного сжатия будет А > 0, поэтому ∆U > 0: газ нагревается. Адиабатное нагревание воздуха используется в дизельных двигателях для воспламенения топлива
Практически все реальные процессы происходят с теплообменом: адиабатические процессы — это редкое исключение.
Наглядные примеры адиабатных процессов:
- В закрытом пробкой с продетым шлангом насоса сосуде находится капельки воды. После нагнетания в сосуд определенно количества воздуха, пробка быстро вылетает и в сосуде наблюдается туман (рис.).
- В закрытом подвижным поршнем цилиндре находится небольшое количество топлива. После быстрого нажатия на поршень топливо воспламеняется.
Источник
Внутренняя энергия. Первый закон термодинамики
Основы термодинамики
Термодинамика изучает процессы и явления, происходящие в природе и технике, с точки зрения преобразования энергии, в том числе внутренней энергии тел.
Термодинамическая система – это совокупность тел, способных обмениваться энергией между собой и с другими системами. Замкнутая термодинамическая система не обменивается энергией с другими системами.
Каждое тело имеет вполне определенную структуру, оно состоит из частиц, которые хаотически движутся и взаимодействуют друг с другом, поэтому любое тело обладает внутренней энергией.
Внутренняя энергия — это величина, характеризующая собственное состояние тела, т. е. энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т. д.) и энергия взаимодействия этих частиц.
Внутренняя энергия идеального газа складывается только из энергии движения молекул, так как взаимодействием молекул можно пренебречь. Внутренняя энергия одноатомного идеального газа определяется по формуле U = 3/2 • m/М • RT. Внутренняя энергия одного моля одноатомного идеального газа:
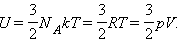 |
Внутреннюю энергию можно изменить двумя способами: путем теплопередачи и путем совершения механической работы
Теплопередача — это изменение внутренней энергии без совершения работы: энергия передается от более нагретых тел к менее нагретым. Теплопередача бывает трех видов: теплопроводность (непосредственный обмен энергией между хаотически движущимися частицами взаимодействующих тел или частей одного и того же тела); конвекция (перенос энергии потоками жидкости или газа) и излучение (перенос энергии электромагнитными волнами). Мерой переданной энергии при теплопередаче является количество теплоты (Q). Принято считать, что Q > 0, если тело получает энергию, и Q 0) за счет внутренней энергии газа. Если внешние силы больше силы давления газа, то газ сжимается и работа газа будет отрицательной (A
При изобарном нагреваниигаз совершает работу над внешними силами 
Первый закон термодинамики :
изменение внутренней энергии замкнутой системы равно сумме количества теплоты, переданной системе, и работы внешних сил, совершенной над системой. 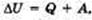
где 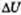
Применение первого закона термодинамики к изопроцессам
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение первого закона термодинамики примет вид: 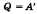
В изобарном процессегаз расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы: 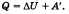
При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е. А = 0, и уравнение первого закона имеет вид 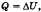
Адиабатным называют процесс, протекающий без теплообмена с окружающей средой. Q = 0, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается,
Второе начало термодинамики гласит, что невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Внутренняя энергия. 1-й закон термодинамики.
Внутренняя энергия
1-й закон термодинамики.
Сумма кинетических энергий хаотического движения всех частиц тела относительно центра масс тела (молекул, атомов) и потенциальных энергий их взаимодействия друг с другом называется внутренней энергией.
- Энергия упорядоченного движения частиц тела представляет собой механическую кинетическую энергию тела.
Вообще говоря, во внутреннюю энергию входят энергии внутриатомных частиц, но при не очень больших температурах эта энергия остается неизменной.
Кинетическая энергия частиц определяется скоростью, а значит — температурой тела.
Потенциальная — расстоянием между частицами, а значит — объемом.
Следовательно: U=U(T,V) — внутренняя энергия зависит от объема и температуры.
Для идеального газа: U=U(T), т.к. взаимодействием на расстоянии пренебрегаем.
— внутренняя энергия идеального одноатомного газа.
Внутренняя энергия — однозначная функция состояния (с точностью до произвольной постоянной) и в замкнутой системе сохраняется. Обратное неверно(!) — одной и той же энергии могут соответствовать разные состояния.
Идеальный газ:
Опыты Джоуля доказали эквивалентность работы и количества теплоты, т.е. и та и другая величины являются мерой изменения энергии, их можно измерять в одинаковых единицах: 1 кал = 4,1868 Дж ≈ 4,2 Дж. Эта величина наз. механическим эквивалентом теплоты.
Р.Майер, Д.Джоуль, Г.Гельмгольц — закон сохранения энергии для тепловых процессов — 1-й закон термодинамики.
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
Изменений внутренней энергии не зависит от способа, которым осуществляется этот переход. Т.о. существует два способа изменения внутренней энергии: совершение механической работы и теплопередача (теплообмен). Работа и количество теплоты характеризуют процесс изменения внутренней энергии, но не саму внутреннюю энергию.
Если А — работа внешних сил, а А’ — работа газа, то А = — А’ (в соответствии с 3-м законом Ньютона). Тогда:
— другая форма записи первого закона термодинамики.Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Невозможность создания вечного двигателя 1-го рода.
Вечный двигатель первого рода — устройство, которое могло бы совершать неограниченное количество работы без затраты энергии.
Тогда Q=0. Следовательно: A’= — ΔU. Т.е. такой двигатель должен совершать работу за счет убыли внутренней энергии. Но ее запасы конечны. После того, как запас энергии будет исчерпан, двигатель остановится.
Источник