Молекулярная физика. Температура и ее измерение.
Температура — физическая величина, характеризующая тепловое состояние тел.
В окружающем нас мире происходят различные явления, связанные с нагреванием и охлаждением тел. Их называют тепловыми явлениями. Так, при нагревании холодная вода сначала становится теплой, а затем горячей; вынутая из пламени металлическая деталь постепенно охлаждается и т. д. Степень нагретости тела, или его тепловое состояние, мы обозначаем словами «теплый», «холодный», «горячий», Для количественной оценки этого состояния и служит температура.
Температура — один из макроскопических параметров системы. В физике, тела, состоящие из очень большого числа атомов или молекул, называют макроскопическими. Размеры макроскопических тел во много раз превышают размеры атомов. Все окружающие тела — от стола или газа в воздушном шарике до песчинки — макроскопические тела.
Величины, характеризующие состояние макроскопических тел без учета их молекулярного строения, называют макроскопическими параметрами. К ним относятся объем, давление, температура, концентрация частиц, масса, плотность, намагниченность и т. д. Температура — один из важнейших макроскопических параметров системы (газа, в частности).
Температура — характеристика теплового равновесия системы.
Известно, что для определения температуры среды следует поместить в эту среду термометр и подождать до тех нор, пока температура термометра не перестанет изменяться, приняв значение, равное температуре окружающей среды. Другими словами, необходимо некоторое время для установления между средой и термометром теплового равновесия.
Тепловым, или термодинамическим, равновесием называют такое состояние, при котором все макроскопические параметры сколь угодно долго остаются неизменными. Это означает, что не меняются объем и давление в системе, не происходят фазовые превращения, не меняется температура.
Однако микроскопические процессы при тепловом равновесии не прекращаются: скорости молекул меняются, они перемещаются, сталкиваются.
Любое макроскопическое тело или группа макроскопических тел — термодинамическая система — может находиться в различных состояниях теплового равновесия. В каждом из этих состояний температура имеет свое вполне определенное значение. Другие величины могут иметь разные (но постоянные) значения. Например, давление сжатого газа в баллоне будет отличаться от давления в помещении и при температурном равновесии всей системы тел в этом помещении.
Температура характеризует состояние теплового равновесия макроскопической системы: во всех частях системы, находящихся в состоянии теплового равновесия, температура имеет одно и то же значение (это единственный макроскопический параметр, обладающий таким свойством).
Если два тела имеют одинаковую температуру, между ними не происходит теплообмен, если разную — теплообмен происходит, причем тепло передается от более нагретого тела к менее нагретому до полного выравнивания температур.
Измерение температуры основано на зависимости какой-либо физической величины (например, объема) от температуры. Эта зависимость и используется в температурной шкале термометра — прибора, служащего для измерения температуры.
Действие термометра основано на тепловом расширении вещества. При нагревании столбик используемого в термометре вещества (например, ртути или спирта) увеличивается, при охлаждении — уменьшается. Использующиеся в быту термометры позволяют выразить температуру вещества в градусах Цельсия (°С).
А. Цельсий (1701-1744) — шведский ученый, предложивший использовать стоградусную шкалу температур. В температурной шкале Цельсия за нуль (с середины XVIII в.) принимается температура тающего льда, а за 100 градусом — температура кипения воды при нормальном атмосферном давлении.
Поскольку различные жидкости расширяются с повышением температуры по-разному, то температурные шкалы в термометрах с разными жидкостями различны.
Поэтому в физике используют идеальную газовую шкалу температур, основанную на зависимости объема (при постоянном давлении) или давления (при постоянном объеме) газа от температуры.
Источник
Способы изменения температуры физика
Тепловые явления – это явления, связанные с нагреванием или охлаждением тел, а также с изменением их агрегатного состояния.
Все тепловые явления связаны с температурой.
Все тела характеризуются состоянием своего теплового равновесия. Главной характеристикой теплового равновесия является температура.
Температура – это мера «нагретости» тела.
Поскольку температура является физической величиной, то её можно и нужно измерить. Для измерения температуры используется прибор, который называется термометр (от греч. термо – тепло, метрео – измеряю).
Первый термометр (а, точнее, его аналог) изобрёл Галилео Галилей. Изобретение Галилея, которое он представил своим студентам на лекциях в университете в конце XVI века (1597 г.), было названо термоскопом.
Любой термометр основан на следующем принципе: изменение физических свойств веществ в зависимости от температуры.
Опыт Галилея
Рис. 1. Опыт Галилея
Опыт Галилея (см. Рис. 1) состоял в следующем: он взял колбу с длинной ножкой и наполнил её водой. Затем взял стакан с водой и перевернул колбу ножкой вниз, поставив в стакан. Часть воды, естественно, вылилась, однако, в результате, в ножке остался определённый уровень воды. Если теперь нагревать колбу (в которой находится воздух), то уровень воды будет опускаться, а если охлаждать, то, наоборот, повышаться. Это связано с тем, что при нагревании вещества (в частности, воздух) имеют свойство расширяться, а при охлаждении – наоборот, сужаться (именно поэтому рельсы делают несплошными, а провода между столбами иногда немного провисают).
Эта идея и легла в основу первого термоскопа, который позволял оценивать изменение температуры (точно измерить температуру таким термоскопом нельзя, так как его показания будут сильно зависеть от атмосферного давления).
В это же время была введена так называемая градусная шкала. Само слово «градус» в переводе с латинского означает «ступень».
На сегодняшний день сохранились три основные шкалы.
1. Шкала Цельсия
Наибольшее распространение получение шкала, которая с детства известна каждому – шкала Цельсия.
Андерс Цельсий – шведский астроном, который предложил следующую шкалу температур: 0 о С – температура кипения воды; 100 о С – температура замерзания воды. В настоящее время все мы привыкли к перевёрнутой шкале Цельсия.
Примечание: сам Цельсий говорил, что такой выбор шкалы вызван простым фактом: зато зимой не будет отрицательной температуры.
2. Шкала Фаренгейта
В Англии, США, Франции, Латинской Америке и некоторых других странах популярностью пользуется шкала Фаренгейта.
Габриель Фаренгейт – немецкий исследователь – инженер, который впервые применил свою собственную шкалу для изготовления стекла. Шкала Фаренгейта более тонкая: по размерности градус шкалы Фаренгейта меньше градуса шкалы по Цельсию.
3. Шкала Реомюра
Техническая шкала придумана французским исследователем Р. А. Реомюром. По этой шкале 0 соответствует температуре замерзания воды, а вот в качестве температуры кипения воды Реомюром была выбрана температура в 80 градусов.
В физике, в основном, используется так называемая абсолютная шкала – шкала Кельвина. 1 градус по Цельсию равен 1 градусу по Кельвину, однако температура в 0 о С соответствует приблизительно 273 К .
Кем и
когда
введена.
А. Цельсия
шведский
астроном, физик
1742 г.
Фаренгейт
стеклодув из Голландии
1724 г.
Реомюр французский физик
1726 г.
Томсон
(лорд Кельвин)
английский физик
1848 г.
Наличие положительных и отрицательных температур
0 о C
– температура таяния льда,
100 о C
– температура кипения воды.
32F
– температура таяния льда,
212F
– температура кипения воды.
0R
– температура таяния
льда,
80R
– температура кипения воды.
0K – абсолютный нуль,
273К
– температура таяния льда
Т = t + 273
Самая высокая температура.
Она получена в центре взрыва термоядерной бомбы – около 300. 400 млн °C. Максимальная температура, достигнутая в ходе управляемой термоядерной реакции на испытательной термоядерной установке ТОКАМАК в Принстонской лаборатории физики плазмы, США, в июне 1986г., составляет 200 млн °C.
Самая низкая температура.
Абсолютный нуль по шкале Кельвина (0 K) соответствует –273,15°С или –459,67° F . Самая низкая температура, 2·10 –9 K выше абсолютного нуля, была достигнута в двухступенчатом криостате ядерного размагничивания в Лаборатории низких температур Хельсинкского технологического университета, Финляндия, группой учёных под руководством профессора Олли Лоунасмаа (род. в 1930 г.), о чём было объявлено в октябре 1989 г.
Напомним, что при изменении температуры тела изменяются его линейные размеры (при нагревании – расширяются, при охлаждении – сужаются). Это связано с поведением молекул. При нагревании увеличивается скорость движения частиц, соответственно, они начинают чаще взаимодействовать, и объём увеличивается.
Из этого можно сделать вывод, что температура связана с движением частиц, из которых состоят тела (это относится и к твёрдым, и к жидким, и к газообразным телам).
Движение частиц в газах является беспорядочным (так как молекулы и атомы в газах практически не взаимодействуют).
Движение частиц в жидкостях является «скачкообразным», то есть: молекулы ведут «осёдлый образ жизни», но способны «перепрыгивать» с одного места на другое. Этим определяется текучесть жидкостей.
Движение частиц в твёрдых телах называется колебательным.
Таким образом, все частицы находятся в непрерывном движении. Это движение частиц называется тепловым движением (беспорядочное, хаотическое движение).
Это движение никогда не останавливается (до тех пор, пока у тела есть температура).
Подтвердил наличие теплового движения в 1827 году английский ботаник Роберт Броун, по имени которого данное движение называют броуновским движением.
На сегодняшний день известно, что самая низкая температура, которая может быть достигнута, составляет приблизительно -273 о С . Именно при такой температуре замирает движение частиц (однако не замирает движение внутри самих частиц).
Рассмотрим в заключении ещё один опыт – опыт французского учёного Гильома Амонтона, который в 1702 году изобрёл так называемый газовый термометр. С небольшими изменениями этот термометр дошёл и до наших дней.
Опыт Амонтона
Рис. 2. Опыт Амонтона
Возьмём колбу с водой и заткнём её пробкой с тонкой трубкой (см. Рис. 2). Если теперь нагревать воду, то за счёт расширения воды, её уровень в трубке будет повышаться. По уровню поднятия воды в трубке можно сделать вывод об изменении температуры. Преимущество термометра Амонтона состоит в том, что он не зависит от атмосферного давления.
На этом уроке мы рассмотрели такую важную физическую величину, как температура. Изучили способы её измерения, характеристики и свойства. На дальнейших уроках мы изучим такое понятие, как внутренняя энергия.
Источник
Температура в физике — основные понятия, формулы и определение с примерами
Содержание:
Температура:
Перед тем как, например, пойти на пляж, многие интересуются прогнозом погоды. И если ожидается температура воздуха 10 °С, то, скорее всего, планы будут изменены. А стоит ли отказываться от прогулки, если прогнозируется температура 300 К (кельвинов)? И что на самом деле вкладывают физики в понятие «температура»?
Что такое температура
Эксперименты показывают, что макроскопическая система может переходить из одного состояния в другое. Например, если в морозный день занести в комнату шарик, наполненный гелием, то гелий в шарике будет нагреваться и при этом будут изменяться давление, объем и некоторые другие параметры газа. После того как шарик пробудет в комнате некоторое время, изменения прекратятся. Один из постулатов молекулярной физики и термодинамики — его еще называют нулевое начало термодинамики — гласит: любое макроскопическое тело или система тел при неизменных внешних условиях самопроизвольно переходит в термодинамическое равновесное состояние (состояние теплового равновесия), после достижения которого все части системы имеют одинаковую температуру. Нулевое начало термодинамики фактически вводит и определяет понятие температуры.
Температура — физическая величина, характеризующая состояние теплового равновесия макроскопической системы.
Состояние теплового равновесия — это такое состояние макроскопической системы, при котором все макроскопические параметры системы остаются неизменными сколь угодно долго.
В состоянии теплового равновесия все части системы имеют одинаковую температуру; другие макроскопические параметры неизменны, но могут быть разными. Вспомните пример с шариком: после того как установится тепловое равновесие, температура окружающего воздуха и температура гелия в шарике будут одинаковыми, а давление, плотность и объем — разными.
Как работают термометры
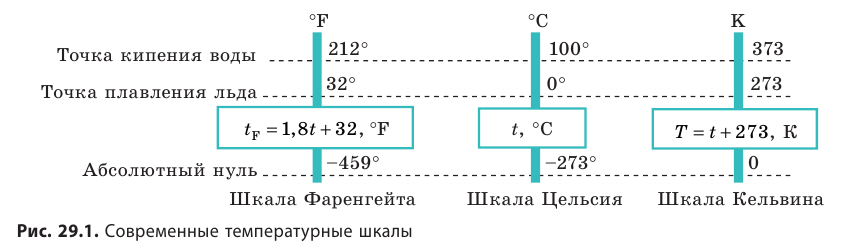
Температура — это физическая величина, и ее можно измерять. Для этого нужно установить шкалу температур. Самые распространенные температурные шкалы — шкалы Цельсия, Кельвина, Фаренгейта (рис. 29.1).
Построение шкалы температур начинается с выбора реперных (опорных) точек, которые должны быть однозначно связаны с какими-либо физическими процессами, которые легко воспроизвести. Например, за нулевую точку температурной шкалы Цельсия принята температура таяния льда при нормальном атмосферном давлении ( t = 0 °С). Температуре кипения воды при нормальном атмосферном давлении приписывают значение t =100 °С. Единица температуры по шкале Цельсия — градус Цельсия: 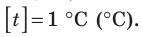
Рис. 29.2. различные виды термометров: а — жидкостный (принцип действия: изменение объема жидкости при изменении температуры); б — термометр сопротивления (изменение электрического сопротивления проводника при изменении температуры); в — биметаллический деформационный (изменение длин двух разных металлических пластин при изменении температуры)
Приборы для измерения температуры — термометры (рис. 29.2). Основные части любого термометра — термометрическое тело (ртуть или спирт в жидкостном термометре, биметаллическая пластина в металлическом деформационном термометре и т. д.) и шкала. Если термометрическое тело привести в контакт с телом, температуру которого нужно измерить, система придет в неравновесное состояние. При переходе в равновесное состояние будут изменяться некоторые параметры термометрического тела (объем, сопротивление и т. п.). Зная, как эти параметры зависят от температуры, определяют температуру тела.
- Термометр фиксирует собственную температуру, равную температуре тела, с которым термометр находится в термодинамическом равновесии.
- Термометрическое тело не должно быть массивным, иначе оно существенно изменит температуру тела, с которым контактирует.
Температура и средняя кинетическая энергия молекул
То, что температура тела должна быть связана с кинетической энергией его молекул, следует из простых соображений. Например, с увеличением температуры увеличивается скорость движения броуновских частиц, ускоряется диффузия, повышается давление газа, а это значит, что молекулы движутся быстрее и их кинетическая энергия становится больше. Можно предположить: если газы находятся в состоянии теплового равновесия, средние кинетические энергии молекул этих газов одинаковы. Но как это доказать, ведь непосредственно измерить эти энергии невозможно?
Обратимся к основному уравнению МКТ идеального газа: 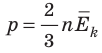
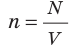
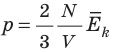
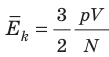
Таким образом, чтобы экспериментально убедиться в равенстве средних кинетических энергий молекул различных газов при одинаковой температуре, нужно измерить объемы (V), давления (p) и массы (m) газов и, зная их молярную массу (M), найти число молекул каждого газа (N) по формуле 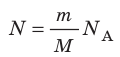
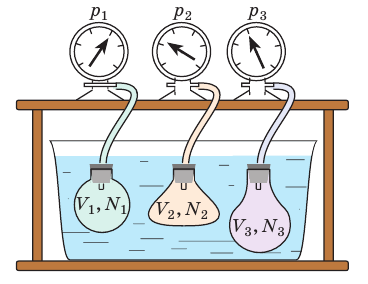
Чтобы обеспечить одинаковую температуру, можно, например, погрузить баллоны с различными газами в сосуд с водой и дождаться состояния теплового равновесия (рис. 29.3).
Рис. 29.3. опыт, позволяющий установить связь между температурой и средней кинетической энергией поступательного движения молекул газа. Газы в сосудах находятся в состоянии теплового равновесия со средой, а следовательно, и друг с другом
Эксперименты показывают, что для всех газов в состоянии теплового равновесия отношение 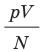
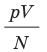
Например, при температуре 0 °С (сосуды с газами погрузили в тающий лед) 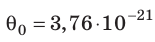
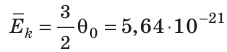
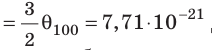
Абсолютная шкала температур
Понятно, что в джоулях представлять температуру неудобно (прежде всего потому, что значения θ очень малы), к тому же неудобно полностью отказываться от шкалы Цельсия. В 1848 г. английский физик Уильям Томсон (лорд Кельвин) (1824–1907) предложил абсолютную шкалу температур (сейчас ее называют шкалой Кельвина).
Температуру Т, измеренную по шкале кельвина, называют абсолютной температурой.
Единица абсолютной температуры — кельвин — основная единица СИ: [T] = 1 К (К).
Шкала Кельвина построена следующим образом:
- изменение температуры по шкале Кельвина равно изменению температуры по шкале Цельсия: ∆ = T t ∆ , то есть цена деления шкалы Кельвина равна цене деления шкалы Цельсия: 1 °С = 1 К; температуры, измеренные по шкалам Кельвина и Цельсия, связаны соотношениями:
- температура по шкале Кельвина связана с величиной
соотношением θ = kT, где k — постоянная Больцмана — коэффициент пропорциональности, не зависящий ни от температуры, ни от состава и количества газа:
- абсолютная температура имеет глубокий физический смысл: средняя кинетическая энергия поступательного движения молекул идеального газа прямо пропорциональна абсолютной температуре:
(1) То есть, если газ охладить до температуры T= 0 К, движение его молекул должно прекратиться (
). Таким образом, нулевая точка шкалы Кельвина — это самая низкая теоретически возможная температура. На самом деле движение молекул не прекращается никогда, поэтому достичь температуры 0 К (–273 °С) невозможно.
Абсолютный нижний предел температуры, при котором движение молекул и атомов должно прекратиться, называют абсолютным нулем температуры. Давление p газа полностью определяется его абсолютной температурой T и концентрацией n молекул газа: p=nkT (2).
- Физическая величина, характеризующая состояние теплового равновесия макроскопической системы, называется температурой. Абсолютный нижний предел температуры, при котором движение молекул и атомов должно прекратиться, называют абсолютным нулем температуры. Шкала, за нулевую точку которой взят абсолютный нуль температуры, называется абсолютной шкалой температур (шкалой Кельвина). Единица абсолютной температуры — кельвин (К) — основная единица СИ. Температуры по шкале Кельвина и Цельсия связаны соотношением: T=t + 273; t=T – 273.
- Средняя кинетическая энергия поступательного движения молекул идеального газа прямо пропорциональна абсолютной температуре, а давление газа определяется абсолютной температурой и концентрацией молекул газа:
— постоянная Больцмана.
| Рекомендую подробно изучить предметы: |
|
| Ещё лекции с примерами решения и объяснением: |
- Парообразование и конденсация
- Тепловое равновесие в физике
- Изопроцессы в физике
- Твердые тела и их свойства в физике
- Механизмы, работающие на основе правила моментов
- Идеальный газ в физике
- Уравнение МКТ идеального газа
- Уравнение состояния идеального газа
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.
Источник





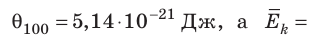
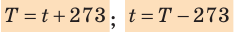
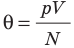 соотношением θ = kT, где k — постоянная Больцмана — коэффициент пропорциональности, не зависящий ни от температуры, ни от состава и количества газа:
соотношением θ = kT, где k — постоянная Больцмана — коэффициент пропорциональности, не зависящий ни от температуры, ни от состава и количества газа: 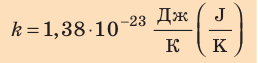
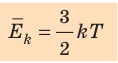 (1) То есть, если газ охладить до температуры T= 0 К, движение его молекул должно прекратиться (
(1) То есть, если газ охладить до температуры T= 0 К, движение его молекул должно прекратиться (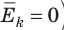 ). Таким образом, нулевая точка шкалы Кельвина — это самая низкая теоретически возможная температура. На самом деле движение молекул не прекращается никогда, поэтому достичь температуры 0 К (–273 °С) невозможно.
). Таким образом, нулевая точка шкалы Кельвина — это самая низкая теоретически возможная температура. На самом деле движение молекул не прекращается никогда, поэтому достичь температуры 0 К (–273 °С) невозможно.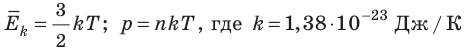 — постоянная Больцмана.
— постоянная Больцмана.


