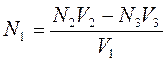Титрование по заместителю
Этот метод считается косвенным, его применяют тогда, когда по какой либо причине трудно определить точку эквивалентности, например, при работе с неустойчивыми веществами, либо определяемый ион не взаимодействует непосредственно с рабочим (титрантом) раствором, либо реагирует с ним в нестехиометрических соотношениях и т.п.
В этом методе используют исследуемое вещество, титрант и нестандартный раствор вспомогательного вещества.
К определяемому веществу добавляют вспомогательное вещество (в избытке), вступающего с ним в реакцию, один из выделившихся продуктов реакции (заместитель) в количестве, эквивалентном исследуемому, оттитровывают рабочим раствором
Например, при йодометрическом определении меди к анализируемому раствору добавляют заведомый избыток КI (вспомогательное вещество). Происходит реакция:
2Cu 2+ + 4I — = 2CuI + I2
Выделившийся иод (заместитель) оттитровывают тиосульфатом натрия.
Расчеты в заместительном титровании ведутся как при прямом титровании.
Обратное титрование (титрование по остатку)
Применяют в тех случаях, когда основная реакция протекает не очень быстро и процесс обратимый или нет подходящего индикатора. В этом случае используются два титранта:
основной и вспомогательный.
К исследуемому раствору добавляют заведомо в избытке определенный объем основного рабочего раствора, реагирующего с исследуемым веществом в эквивалентном количестве.
Остаток основного титранта, не всупивщего в реакцию с исследуемым веществом, оттитровывают вспомогательным титрантом.
Например, широко применяют обратное титрование хлорид ионов в кислых растворах при тиоцианатометрическом осадительном титровании.
К анализируемому раствору хлорида сначала добавляют заведомый избыток основного рабочего раствора нитрата серебра.
При этом происходит реакция образования малорастворимого хлорида серебра:
Не вступившее в реакцию избыточное (остаток) количество вещества AgNO3 оттитровывают раствором тиоцианата аммония или калия (вспомогательного рабочего раствора):
Содержание хлорида легко рассчитать, так как известно общее количество вещества серебра, введенное в раствор, и количество вещества AgNO3, не вступившее в реакцию с хлоридом
Для расчётов используют закон эквивалентов, исходя из которого:
С1(fэкв) V1 = С2(fэкв) V2 , где
С1(fэкв)-молярная концентрация эквивалента рабочего ра-ра;
V1-объём рабочего ра-ра;
С2(fэкв)- молярная концентрация эквивалента исследуемого ра-ра;
V2-объём исследуемого ра-ра
Применение титриметрических методов анализа в медико-биологических исследованиях:
· Данный метод может быть использован для:
· определения рН биологических жидкостей;
· определения концентрации катионов и анионов в биологических средах;
· количественного определения свободного хлора в воде;
· определения примесей органических веществ в воде и др.
36.
Нейтрализации метод — это объемный (титриметрический) метод определения концентрации кислот (ацидиметрия) и щелочей (алкалиметрия) в растворах.
При определении концентрации кислоты к точно отмеренному пипеткой объему исследуемого раствора постепенно приливают из бюретки рабочий раствор щелочи (обычно NaOH) известной концентрации, пока не изменится окраска индикатора, предварительно добавленного к титруемому раствору. Объем рабочего раствора, пошедший на взаимодействие с кислотой, отсчитывают по шкале бюретки. Определение концентрации щелочи производят аналогичным путем, только в качестве рабочего раствора в этом случае используют раствор кислоты (обычно HCl).
При титровании слабой кислоты сильной щелочью в качестве индикатора применяют обычно фенолфталеин, а при титровании слабой щелочи сильной кислотой — метиловый оранжевый. При титровании сильной кислоты сильной щелочью можно применять любой из названных индикаторов. При
выборе индикатора руководствуются правилом: значение рН в точке эквивалентности (рНэ) должно попадать в зону перехода цвета индикатора (т.е. рНэ ∋рТ±1)
37.
Индикаторы, применяемые в методах оксидиметрии, различны. Часто это органические вещества, которые сами являются окислителями или восстановителями. Иногда это специфические реактивы, например, крахмал в иодометрии. Перманганатометрические определения производят без индикатора.
Перманганатометрией называется такой вид оксидиметрии, в котором в качестве рабочего раствора применяют перманганат калия KMnO4. Он является сильным окислителем, особенно в кислой среде. В зависимости от кислотности среды при восстановлении KMnO4 получаются различные конечные продукты
38.
39.
Поддержанию на постоянном уровне концентрации ионов водорода способствуют буферные растворы – растворы, рН которых не меняется при добавлении к ним небольших количеств сильных кислот, щелочей, а также при разведении.
Простейший буферный раствор- это смесь слабой кислоты и соли, имеющей с этой кислотой общий анион, либо смесь слабого основания и соли с общим катионом.
1 тип буферных растворов:
¢ Ацетатный — СН3СООН и СН3СООNa
¢ Белковый – РtCOOH и PtCOONa
¢ Гемоглобиновый – HHb и KHb
¢ Оксигемоглобиновый -HHbO2 и KHbO2.
2 тип буферных растворов:
По более современной классификации БР делят на следующие группы :
1. БР, состоящие из слабой кислоты и её аниона — НА/A — (CH3COOH / CH3COO — )
2. БР, состоящие из слабого основания и его катиона – В/BH + ( NH4OH / NH4 + )
3. БР, состоящие из аниона кислой и средней соли, или из анионов двух кислых солей, например, фосфатная буферная система – Н2РО4 — /HPO4 2-
4. БР, состоящие из ионов и молекул амфолитов. К ним относятся белковые БС, гемоглобиновая и оксигемоглобиновая БС.
Так как любой БР содержит слабый электролит, к процессу его диссоциации можно применить закон действующих масс, например, для ацетатного БР:
Так как концентрация ионов СН3СОО — велика из-за диссоциации соли, процесс диссоциации СН3СООН по принципу Ле -Шателье сдвинут влево, поэтому концентрация недиссоциированных молекул СН3СООН практически равна общей концентрации кислоты в БР, а концентрация ионов СН3СОО — равна концентрации соли в БР, поэтому:
40.
Если к буферному раствору добавить сильную кислоту, то ионы водорода будут соединяться с анионами с образованием слабого электролита и реакция среды при этом не меняется:
СН3СООNa + HCl = CH3COOH + NaCl
СН3СОО- + H+ = CH3COOH
Если к буферному раствору прибавить сильное основание, то ионы ОН- будут взаимодействовать с ионами Н+, которые содержатся в небольшом количестве, вследствие небольшой диссоциации кислоты. В результате образуется Н2О. Способность буферного раствора сохранять рН при добавлении сильных кислот или щелочей не беспредельна и ограничена величиной, называемой буферной ёмкостью.
В(к.) = ( рН0 –рН1) V(б.р.)
Буферная ёмкость зависит от:
· природы и общих концентраций компонентов буферного раствора, а также от соотношения их концентраций:
· чем больше концентрация компонентов и
· чем ближе отношение кислота/ соль к 1, тем больше буферная ёмкость.
Буферные системы в живых организмах поддерживают постоянство рН в крови и тканях. Исследования показали, что в процессе обмена веществ в организме образуется большое количество кислых продуктов. Так, в организме человека за сутки образуется такое количество различных кислот, которое эквивалентно 20-30 л I н. сильной кислоты. Сохранение постоянства рН среды в организме обеспечивается наличием в нем мощных буферных систем.
Большую роль при этом играют белковый, бикарбонатный и фосфатный буферы. Буферной системой крови являются бикарбонатный и фосфатный буферы: Н2С03 + NaHCO3; NaH2P04 + Na2НРО4 соответственно.
Однако наиболее мощной буферной системой крови является гемоглобиновый буфер (75% всей буферной ёмкости крови), который удаляет из организма большое количество углекислоты
41.
Водородкарбонатная(гидрокарбонатная): СО2 + Н2О = Н2СО3 Фосфатная буферная система: состоит из слабой кислоты Н2РО4- и сопряжённого основания НРО42-. В основе её действия лежит равновесие:
Н2РО4- = НРО42- + Н+
Белковые буферные системы— состоят из остатков аминокислот, которые содержат -NH2 группы, имеющие слабый основный характер, и –СООН группы, со слабыми кислотными свойствами.
Гемоглобиновая/оксигемоглобиновая БС, на долю которой приходится 75% буферной ёмкости крови.
Гемоглобиновый буфер является разновидностью белковой БС и состоит из 2х форм гемоглобина:
Нарушение в любой буферной системе сказывается на концентрациях составляющих гидрокарбонатной БС, поэтому изменение её параметров может достаточно точно характеризовать состояние дыхательных или метаболических нарушений, т.е. кислотно-основного состояния. Таким образом, благодаря буферному действию буферных систем происходит лишь небольшое снижение рН крови, т.е. сохраняется кислотно-основное состояние, несмотря на поступление в кровь значительных количеств кислот, т.к. в процессе усвоения пищи в организме генерируются значительное количество диоксида углерода (550- 775 г/cут), при взаимодействии которого с с влагой образуется угольная кислота в количестве, эквивалентном поступлению в кровь от 25 до 35 ммоль/ сут ионов Н+.
Кислотно- основное состояние организма – неотъемлемая часть гомеостаза внутренней среды организма
Смещение кислотно- основного равновесия крови в сторону повышения концентрации ионов Н+ (снижения рН) и уменьшения резервной щёлочности называется ацидозом, смещение его в сторону снижения концентрации ионов водорода ( повышение рН) и увеличение резервной щёлочности- алкалозом.
· -метаболический ацидоз и алкалоз.
Метаболический ацидоз характеризуется нарушением метаболизма и может наступить в результате следующих причин:
— избыточное введение или образование в организме стойких кислот (поступление кетокислот при голодании и диабете, повышенное образование молочной кислоты при шоке; поступление кислот с пищей, питьём, медикаментами, в результате вдыхания загрязнённого воздуха и т.д.);
— неполное удаление кислот( при почечной недостаточности);
— избыточные потери НСО3- иона ( в результате поноса, колита, язвы кишечника)
Метаболический алкалоз наступает вследствие:
потери ионов Н+ (рвоте, кишечной непроходимости и др.);
Увеличения концентрации НСО3- иона (при потере воды, введение солей органических кислот- молочной, уксусной ,лимонной, катаболизирующихся с поглощением ионов Н+ ).
Источник
Способы титрования



Реакция должна быть практически необратимой, т.е. заканчиваться полным расходованием исходных веществ и иметь большое значение константы равновесия.
При этом не должно образовываться никаких побочных продуктов как вследствие взаимодействия исходных веществ с окружающей средой (например, с кислородом или углекислым газом, содержащимися в воздухе), так и в результате протекания между ними нескольких параллельных реакций.
В реакциях должна точно и быстро фиксироваться точка эквивалентности.
2. Реакция между веществами рабочего и исследуемого растворов должна протекать в строгом стехиометрическом соотношении, соответствующем её химическому уравнению.
4. Реакция должна протекать с достаточной скоростью, т.е. за малый отрезок времени. Наиболее оптимальным в этом случае является время, необходимое для перемешивания одной добавленной капли титранта с объёмом титруемого раствора, т.е. 1-3 секунды.
Если реакция осуществляется медленно, то сложно точно определить наступление точки эквивалентности. При этом также теряется основное достоинство титриметрии – быстрота выполнения анализа и получения результата.
Если химическая реакция не удовлетворяет хотя бы одному из вышеперечисленных требований, она не может быть использована в титриметрическом анализе. Но если ей невозможно найти замену, то такую реакцию пытаются «приспособить» для применения в титриметрии. Например, многие окислительно-восстановительные реакции при обычных условиях протекают медленно, являются обратимыми и многонаправленными, т.е. исходные вещества в них расходуются одновременно по нескольким направлениям. Для устранения данных недостатков изменяют условия проведения реакции. Например, осуществляют её при нагревании или в присутствии катализаторов (это позволяет существенно увеличить скорость реакции), а также в определённой среде: кислой, нейтральной или щелочной (это позволяет устранить обратимость и многонаправленность).
Следует, однако, подчеркнуть, что такое «приспособление» приводит к усложнению метода. Применение его целесообразно идти лишь тогда, когда неизвестна более удобная химическая реакция.
Различают три основных способа титрования: прямое, обратное, косвенное или заместительное.
При прямом титровании используют исследуемый и один рабочий растворы. В процессе определения к определённому точно измеренному объёму одного из них по каплям добавляют второй раствор до наступления точки эквивалентности.
Закон эквивалентов в этом случае может быть математически записан следующим образом:
где V1 и V2 – объёмы израсходованных исследуемого и рабочего растворов, соответственно; N1 и N2— молярные концентрации химических эквивалентов веществ исследуемого и рабочего растворов, соответственно.
Молярную концентрацию химического эквивалента вещества в исследуемом растворе рассчитывают по формуле:
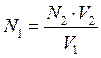
При обратном титровании используют исследуемый и два рабочих раствора, один их которых является вспомогательным, а второй применяют для титрования.
В процессе анализа к определённому точно измеренному объёму исследуемого раствора одномоментно добавляют взятый в избытке фиксированный объём вспомогательного рабочего раствора. В результате протекания химической реакции вещество, присутствующее в исследуемом растворе, расходуется полностью. Не прореагировавший избыток вещества вспомогательного раствора титруется затем вторым рабочим раствором до наступления точки эквивалентности, например:
раствор рабочий раствор
Таким образом, вещество, присутствующее во вспомогательном рабочем растворе, реагирует как с веществом исследуемого раствора, так и с веществом второго рабочего раствора. Закон эквивалентов в этом случае математически может быть записан следующим образом:
где V1, V2, V3 – израсходованные объёмы исследуемого, вспомогательного и второго рабочих растворов, соответственно; N1, N2, N3 – молярные концентрации химических эквивалентов веществ в исследуемом, вспомогательном и во втором рабочих растворах, соответственно.

Молярную концентрацию химического эквивалента рассчитывают по формуле:
Обратное титрование в аналитической практике может называться иначе титрованием по остатку или с двумя титрантами.
Оно используется, если определяемое вещество не реагирует или реагируют медленно с веществом второго рабочего раствора, либо в реакции между ними невозможно определить точку эквивалентности.
При косвенном, или заместительном, титровании также используют исследуемый раствор и два рабочих раствора. В ходе анализа к точно измеренному объёму исследуемого раствора одномоментно добавляют нефиксированный заведомый избыток первого рабочего раствора. В результате протекающей реакции вещество исследуемого раствора полностью расходуется с образованием эквивалентного количества соответствующего продукта реакции, который затем титруется вторым рабочим раствором до наступления точки эквивалентности, например:
исследуемый первый рабочий эквивалентное
раствор раствор кол-во продукта реакции
второй рабочий раствор
Таким образом, мы как бы замещаем определяемое вещество на другое, которое впоследствии и подвергаем анализу.
Так как количество вещества эквивалента образовавшегося продукта и количество вещества эквивалента в исследуемом растворе равны между собой, то молярную концентрацию химического эквивалента вещества в исследуемом растворе рассчитываем по такой же формуле, как и при прямом титровании.
Заместительное титрование применяют, когда непосредственное определение вещества в исследуемом растворе невозможно: отсутствует подходящий титрант, нельзя установить точку эквивалентности и т.п.
Источник