Способ задания состава смеси газов
Репетитор по химии и биологии
Богунова В.Г.
100 баллов ЕГЭ по химии!
Первый МГМУ им. И.М. Сеченова
выпускница репетитора В.Богуновой
РГМУ по химии 2010
Диплом II степени
РНИМУ им. Н.И. Пирогова
выпускница репетитора В.Богуновой
Первый МГМУ им. И.М. Сеченова
выпускница репетитора В.Богуновой
МГМСУ, лечебный факультет
выпускник репетитора В.Богуновой
МГМСУ, лечебный факультет
выпускница репетитора В. Богуновой
Первый МГМУ им. И.М. Сеченова
выпускница репетитора В.Богуновой
МГМСУ им. А.И. Евдокимова
выпускница репетитора В.Богуновой
РНИМУ им. Н.И. Пирогова
выпускник репетитора В.Богуновой
Первый МГМУ им. И.М. Сеченова
выпускница репетитора В.Богуновой
МГМСУ им. А.И. Евдокимова
выпускница репетитора В. Богуновой
РНИМУ им. Н.И. Пирогова
выпускник репетитора В.Богуновой
МГМСУ им. А.И. Евдокимова
выпускник репетитора В.Богуновой
Секретная шпаргалка по химии
4.2 Состав смеси газов
Вы хотите познавать химию и профессионально, и с удовольствием? Тогда вам сюда! Автор методики системно-аналитического изучения химии Богунова В.Г. раскрывает тайны решения задач, делится секретами мастерства при подготовке к ОГЭ, ЕГЭ, ДВИ и олимпиадам
Команда «Газы!» была объявлена еще две недели назад. И что?! Легкие задачи решили и расслабились?! Или вы думаете, что задачи на газы касаются только 28-х заданий ЕГЭ?! Как бы не так! Если газов пока еще не было в 34-х заданиях, это ничего не значит! Задач на электролиз тоже не было в ЕГЭ до 2018 года. А потом как врезали, мама не горюй! Обязательно прочитайте мою статью «Тайны задач по химии? Тяжело в учении — легко в бою!» . В этой статье очень подробно рассказывается о новых фишках на электролиз. Статья вызвала шквал самых разных эмоций у преподавателей химии. До сих пор мне и пишут, и звонят, и благодарят, и бьются в конвульсиях. Просто цирк с конями, в котором я — зритель в первом ряду.
Однако, вернемся к нашим баранам, вернее, Газам. Я прошла через огонь и воду вступительных экзаменов и знаю точно — хочешь завалить абитуриента, дай ему задачу на Газы. Почитайте на досуге сборник задач И.Ю. Белавина. Я процитирую одну такую «мозгобойню», чтобы вам жизнь медом не казалась. Попробуйте решить.
И.Ю. Белавин, 2005, задача 229
Два из трех газов (сероводород, водород и кислород) смешали и получили газовую смесь, плотность которой оказалась равной плотности оставшегося газа. Полученную газовую смесь вместе с равным ей объемом третьего газа под давлением поместили в замкнутый сосуд емкостью 4 л, содержавший азот при н.у. и нагревали при 600 С до окончания химических реакций, затем постепенно охладили. Определите массы веществ, содержавшихся в сосуде после охлаждения, если плотность газовой смеси в сосуде перед нагреванием равнялась 9,25г/л. (Ответ: m(S) = 7,5 г, m(SO2) = 15 г, m(Н2О) = 9 г)
Ну как, решили? Нет?! А ваши репетиторы?! Извините, это был риторический вопрос. Кстати, мои ученики, абитуриенты 2003-2008 гг. такие задачи щелкали, как семечки, на экзаменах во 2-й медицинский (теперь РНИМУ им. Н.И. Пирогова). Надеюсь, вам понятно, что 34-м задачам ЕГЭ еще есть куда усложняться, perfectio interminatus est (нет предела совершенству), с газами нужно работать, работать и работать. Поэтому команду «Газы!» отменять рано. Итак, поехали!
Сегодня мы поговорим о газовых смесях, затронем понятие плотности газа (абсолютной и относительной), средней молярной массы, решим задачи: определение средней молярной массы и плотности газа по компонентам смеси и наоборот.
• Газовая смесь — смесь отдельных газов НЕ вступающих между собой в химические реакции. К смесям газов относятся: воздух (состоит из азота, кислорода, углекислого газа, водяного пара и др.), природный газ (смесь предельных и непредельных углеводородов, оксида углерода, водорода, сероводорода, азота, кислорода, углекислого газа и др.), дымовые газы (содержат азот, углекислый газ, пары воды, сернистый газ и др.) и др.
• Объемная доля — отношение объема данного газа к общему объему смеси, показывает, какую часть общего объема смеси занимает данный газ, измеряется в долях единицы или в процентах.
• Мольная доля — отношение количества вещества данного газа к общему количеству вещества смеси газов, измеряется в долях единицы или в процентах.
• Плотность газа (абсолютная) — определяется как отношение массы газа к его объему, единица измерения (г/л). Физический смысл абсолютной плотности газа — масса 1 л, поэтому молярный объем газа (22,4 л при н.у. t° = 0°C, P = 1 атм) имеет массу, численно равную молярной массе.
• Относительная плотность газа (плотность одного газа по другому) — это отношение молярной массы данного газа к молярной массе того газа, по которому она находится
• Средняя молярная масса газа — рассчитывается на основе молярных масс составляющих эту смесь газов и их объемных долей
Настоятельно рекомендую запомнить: средняя молярная масса воздуха Мср(в) = 29 г/моль , в заданиях ЕГЭ часто встречается.
Обязательно посетите страницу моего сайта «Изучаем Х-ОбХ-04. Закон Авогадро. Следствия из закона Авогадро. Нормальные условия. Молярный объем газа. Абсолютная и относительная плотность газа. Закон объемных отношений » и сделайте конспекты по теории. Затем возьмите бумагу и ручку и решайте задачи вместе со мной. Чует мое сердце, что ЕГЭ по химии устроит нам газовую атаку, а противогазы не выдаст!
Определить плотность по азоту газовой смеси, состоящей из 30% кислорода, 20% азота и 50% углекислого газа.
Вычислите плотность по водороду газовой смеси, содержащей 0,4 моль СО2, 0,2 моль азота и 1,4 моль кислорода.
5 л смеси азота и водорода имеют относительную плотность по водороду 12. Определить объем каждого газа в смеси.
Плотность по водороду пропан-бутановой смеси равна 23,5. Определите объемные доли пропана и бутана
Газообразный алкан объемом 8 л (н.у.) имеет массу 14,28 г. Чему равна его плотность по воздуху
Плотность паров альдегида по метану равна 2,75. Определите альдегид
Ну как? Пошло дело? Если туго, вернитесь к задачам и решайте их самостоятельно до тех пор, пока не щелкнет! А для стимуляции — десерт в виде еще одной задачи И.Ю. Белавина на газы. Наслаждайтесь ее решением самостоятельно!
И.Ю. Белавин, 2005, задача 202
Сосуд емкостью 5,6 л при н.у. заполнили метаном, затем нагрели до высокой температуры, в результате чего про-изошло частичное разложение метана. Определите массу образовавшейся сажи, если известно, что после приведения к нормальным условиям объем полученной газовой смеси оказался в 1,6 раза больше объема исходного метана, эта газовая смесь обесцвечивает бромную воду и имеет плотность по воздуху 0,2931. (Ответ: m(C) = 0,6 г)
Задачи И.Ю. Белавина — это крутой драйв! Попробуйте решить, и вы откажетесь от просмотра любых ужастиков, поскольку запасетесь адреналином надолго! Но нам нужно спуститься на землю к ЕГЭ, простому и надежному, как первый советский трактор. Кстати, у меня в коллекции припасено немало сюрпризов с газовыми фишками, собранными за все годы работы и бережно хранимыми. Думаю, пришло время сказать им: «И снова здравствуйте!», поскольку ЕГЭ с каждым годом становится «все чудесатее и чудесатее». Но это уже совсем другая история. Читайте мои статьи — и вы подстелите соломку под свою ЕГЭшную попу.
Вы готовитесь к ЕГЭ и хотите поступить в медицинский? Обязательно посетите мой сайт Репетитор по химии и биологии. Здесь вы найдете огромное количество задач, заданий и теоретического материала, познакомитесь с моими учениками, многие из которых уже давно работают врачами.
Полный каталог статей репетитора Богуновой В.Г. вы найдете на странице сайта Статьи репетитора
Подписывайтесь на видео-канал Репетитор по химии и биологии. Ежедневно появляются новые вебинары, видео-уроки, видео-консультации, видео-решения заданий ЕГЭ.
Источник
ЛЕКЦИЯ 3. Способы задания состава смеси
Способы задания состава смеси. Соотношения между ними
Смеси идеальных газов. Закон Дальтона
В ТТД чистым веществом наз. вещество, все молекулы которого одинаковы. Смесь, состоящая из нескольких чистых веществ наз. раствором. Чистыми веществами явл., например, вода, этиловый спирт, азот, аммиак и т.п. Чистые вещества, составляющие смесь, наз. компонентами.
При рассмотрении смесей газов исходят из того, что смесь идеальных газов, не вступающих в химическое взаимодействие друг с другом, так же явл. идеальным газом и подчиняется таким же законам. При этом каждый газ, входящий в состав газовой смеси, ведет себя так, как будто он один при данной температуре Т занимает весь объём смеси, т.е. равномерно распространяется по всему объёму смеси и оказывает на стенки сосуда своё давление, наз. парциальным.
В 1801г. английский учёный Дальтон экспериментально установил связь между парци- альными давлениями отдельных газов и давлением смеси. При постоянной температуре полное давление смеси нескольких газов равно сумме их парциальных давлений:

где pі— парциальное давление i-го газа; n-количество газов, составляющих газовую смесь.
Газовая смесь может быть задана массовыми, объёмными и мольными долями.
Газовая смесь, заданная массовым составом, характеризуется массовыми долями. Массовой долей компонента gi наз. отношение массы отдельного компонента mi, входящего в смесь, к массе всей смеси Мсм, т.е.
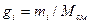
Очевидно, что масса газовой смеси равна сумме масс всех входящих в неё газов:

Определим сумму массовых долей отдельных газов:
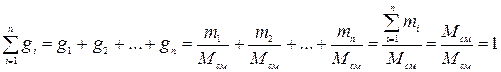
Массовые доли часто задаются в процентах (%).
Газовая смесь, заданная объёмным составом, характеризуется объемными долями (ri). Объёмная доля каждого газа выражается отношением приведенного объёма газа Vi к полному объёму смеси Vсм.
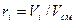
Приведенным Vi наз. объём, который занимал бы компонент газа, если бы его давление рi и температура Тi равнялись давлению рсм и температуре Тсм.
Парциальный объём каждого газа определяется по закону Бойля-Мариотта. При T=const.=Tсм

Из уравнений (2.26) имеем: 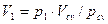
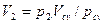
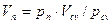
Сложив отдельно левые и правые части уравнений (2.27), получим:

По закону Дальтона 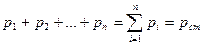
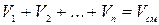
составляющих смесь, равна объёму смеси газов (закон Амала).
Сумма объёмных долей газов, составляющих смесь, равна единице
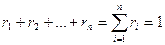
Объёмные доли часто задаются в процентах (%).
Газовая смесь, заданная мольным составом, характеризуется мольными долями. Мольной долей 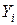
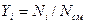
Вполне очевидно, что сумма молей всех газов, составляющих смесь, равна общему числу молей газовой смеси, т.е. 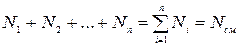
Сумма мольных долей смеси газов равна единице: 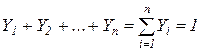
Если известен массовый состав смеси, то по нему можно найти её мольный состав. Массы отдельных газов mi и полную массу смеси Мсм можно выразить через число молей следующем образом: 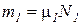
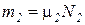
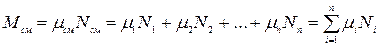
2.8. Теплоёмкость. Массовая, объёмная и молярная теплоемкости.
Теплоемкости при постоянных объёме и давлении
Теплоёмкостью наз. количество теплоты, необходимое для повышения температуры тела на один градус. Теплоёмкость не является постоянной величиной и в общем случае изменяется с изменением температуры и давления. Теплоёмкость единицы количества вещества наз. удельной теплоёмкостью. Удельная теплоёмкость тела зависит от химического состава, параметров состояния рабочего тела, а также от вида процесса, в котором телу сообщается
теплота, поскольку теплота есть функция процесса. Размерность удельной теплоёмкости:
Дж/(кг(м 3 , (моль))) К).
В ТТД различают удельные массовую с, (Дж/(кг К)), объемную с’ , (Дж/(м 3 К)) и мольную сµ (Дж/(моль К)) теплоёмкости.
Зависимости между удельными теплоёмкостями устанавливаются из следующих выражений:
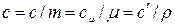
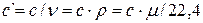
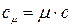
Различают истинную и среднюю теплоёмкости.
Истинной теплоёмкостьюназ. производная от количества теплоты, подведённой к телу, по температуре этого тела и определяется выражением:
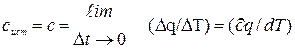
То есть истинная теплоёмкость тела – это его теплоёмкость при данной температуре.
Средней теплоёмкостью наз. теплоёмкость в интервале температур Т2 – Т1, она обозначается Сm. При уменьшении разности температур средняя теплоёмкость приближается к истинной.
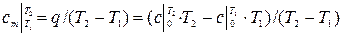
Удельной изохорной теплоемкостью 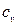
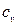
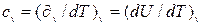
Удельной изобарной теплоемкостью 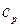
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник






m.jpg)
m.jpg)
m.jpg)

m.jpg)
m.jpg)
m(2).jpg)
_m.jpg)


m.jpg)
_m.jpg)


_01.jpg)
_02.jpg)
_03.jpg)
_04.jpg)
_1.jpg)
_2.jpg)
_3.jpg)
_4.jpg)
_5.jpg)
_6.jpg)