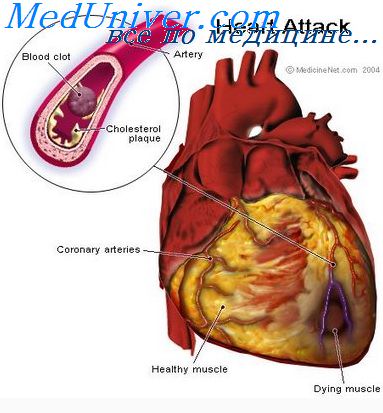
Способ введения обезболивающих препаратов при инфаркте миокарда
Адекватное и быстрое обезболивание при инфаркте миокарда (первоочередная проблема) должно проводиться еще на догоспитальном этапе. Оно помогает разорвать порочный круг (ишемия миокарда -> боль -> ишемия миокарда), снизить активность симпатической нервной системы (уменьшить работу миокарда), ослабить рефлекторные влияния из очага поражения на тонус периферических сосудов и сердечный выброс (предотвратить формирование рефлекторного КШ).
Подход к купированию боли состоит из двух этапов: уменьшения ишемии миокарда и непосредственного влияния на боль. Антиишемическая терапия включает реинфузию, назначение р-АБ, нитратов, ингаляции кислорода.
Больному нельзя давать половинные дозы анальгетиков, он не должен терпеть боль — это угроза его жизни. Важный аспект обезболивания — снижение ПО2 миокардом (на фоне строгого постельного режима, нормализации ЧСС и АД). Оптимальный путь обезболивания — устранение причины боли, т.е. восстановление коронарного кровотока (тромболизис).
Для купирования боли в отсутствие гипотонии сразу используют не более 3 раз сублингвальный прием нитроглицерина (в домашних условиях, если нет возможности ввести парентерально обезболивающие), потом его назначают внутривенно капельно. Если боль не купируется, то обычно вводят внутривенно наркотические ЛС (но не внутримышечно или подкожно, ибо в этом случае анальгезирующий эффект слаб и наступает поздно). При болевом синдроме на фоне возбуждения и повышения АД наркотические ЛС назначают сразу. Они уменьшают ишемию миокарда, страх и тахикардию. Наркотики купируют боль не только прямо, но и опосредованно за счет снижения тонуса САС, что уменьшает П02 миокардом. В качестве дополнительных мер (когда внутривенное введение опиатов оказалось недостаточно эффективным) назначают внутривенно АБ и нитраты.
Купирование боли при инфаркте миокарда включает следующее.
• Прием таблетки нитроглицерина под язык, если нет гипотонии (ибо даже малая его доза может вызвать гипотонию, что опасно для больного, особенно на фоне брадикардии), повторить через 5—10 мин (если больной находится дома). Сублингвальный прием нитроглицерина очень редко «открывает» окклюзивную коронарную артерию. Следует узнать у больного, не принимал ли он последнее время силденафил (виагру), так как прием нитроглицерина на этом фоне в последние 24 ч может вызвать опасное падение АД. Если он неэффективен, то в больнице вводят наркотические ЛС. У части больных ИМ анальгетики только временно устраняют болевой синдром. В этих случаях внутривенно капельно вводят 100 мл 1% раствора нитроглицерина с начальной скоростью 5-10 мкг/мин и постепенным увеличением скорости до 20 мкг/мин и более (на 5— 10 мкг/мин каждые 5-10 мин) под контролем АД (лучше проводить непрерывную инфузию в течение 48-72 ч) и ЯСС (может повышаться более чем на 10 уд/мин, но не должно превышать 110 уд/мин).
САД должно не снижаться менее 100 мм рт. ст. или уменьшаться на 15% от исходного у больных с нормальным АД (на 30% у гипертоников). Нитроглицерин полезен в лечении ИМ, осложненного ОСН в случае сохранения симптоматики или повышения АД. Вместо нитроглицерина можно использовать изокет (внутривенно капельно 50 мг в 100 мл изотонического раствора со скоростью вливания 8—10 капель в минуту под контролем АД). Нитраты не назначают больным с САД менее 90 мм рт. ст., ЧСС менее 50 уд/мин или более 110 уд/мин и подозрением на ИМ ПЖ. После внутривенного введения нитратов больным с СН или сохраняющейся ишемией назначают их орально с большими временными интервалами, чтобы избежать тахифилаксии. Нитраты нормализуют коронарный кровоток, особенно в ишемизированной зоне, и уменьшают боль (за счет снижения ПО2 миокардом вследствие возникновения периферической вазодилатаиии), зону некроза, напряжение и объем желудочков, ремоделирование миокарда в пораженной зоне и частоту механических осложнений. Но надо иметь в виду, что нитраты купируют ангинозную боль, тогда как при ИМ превалирует боль от околонекрозных участков, поэтому здесь лучше использовать наркотические ЛС.
• Назначение оксигенотерапии (100% увлажненный кислород) позволяет повысить диффузию кислорода в ишемизированный миокард. Она должна проводиться каждому больному через носовой катетер в первые 6 ч, а при появлении признаков застоя в легких, ОЛ или КШ — через маску или интубационную трубку.
• АБ показаны всем больным (при отсутствии противопоказаний) в первые 4—12 ч инфаркта миокарда независимо от проведения тромболизиса при гипердинамических состояниях (тахиаритмиях, повышении АД), повторно возникающих ангинозных приступах, не «отпускающих» после введения наркотических ЛС, прогрессирующем росте кардиоспецифических ферментов (что указывает на расширение зоны ИМ). Р-АБ снижают симпатическое влияние на миокард, ЧСС и ПО2 миокардом (этим сохраняют его жизнеспособность), вероятность повторной ишемии (и нового ИМ), зону некроза миокарда (при раннем назначении), боль, потребность в анальгетиках и появление опасных аритмий. Для быстрого эффекта Р-АБ назначают сначала в малой дозе внутривенно болюсом метопролол по 5 мг через каждые 5—10 мин, 3 болюса — под контролем ЭКГ и АД (ориентиры — целевая ЧСС 50—60 уд/мин, САД 100 мм рт. ст. и более) и потом внутрь (обычно при сохранении стабильной гемодинамики после 3-й дозы) по 50 мг через каждые 6 ч в течение 2 дней, а позднее — по 100 мг 2 раза в сутки; альтернатива — внутрь пропранолол (по 50 мг через каждые 6 ч; поддерживающая доза — 50—200 мг/сут) или атенолол (внутривенно 2 болюса по 5 мг с интервалом в 5 мин, потом поддерживающая доза — 100 мг/сут).
У больных с пограничными параметрами гемодинамики лечение начинают с небольших доз АБ (метопролол 12,5—25 мг 2 раза в сутки). Орально АБ должны использоваться в лечении ИМ как можно раньше, независимо от параллельного проведения ПЧКА или тромболизиса. Р-АБ должны назначаться в период клинических проявлений ИМ до тех пор, пока не появятся «специфические» осложнения (слабость ЛЖ, брадикардия). Эти ЛС уменьшают ударный объем сердца, который при ИМ уже заметно снижен. Они противопоказаны при ОСН (влажные хрипы выше 10 см над диафрагмой); тяжелой ХСН с малой ФВЛЖ; гипотонии (САД менее 90 мм рт. ст.); брадикардии (ЧСС менее 60 уд/мин); прогрессирующей АВ-блокаде II степени (или PQ более 0,24 с); бронхоспастическом синдроме (даже в анамнезе); выраженной патологии периферических артерий, инсулинзависимом СД. Следует избегать назначения АБ у больных с неясной тахикардией, так как это может вызвать декомпенсацию имеющейся СН у больных с компенсаторной тахикардией.
Источник
Боль и обезболивание в неотложной кардиологии
Проблема боли в неотложной кардиологии изучается на протяжении многих лет. Тем не менее, не разработаны обоснованные принципы обезболивания даже при таком заболевании, как инфаркт миокарда. Пятидесятилетний опыт изучения инфаркта миокарда свидетельствует, что начальные проявления этого заболевания у лиц от 18 до 75 лет характеризуется остро возникающими и быстро нарастающими давящими, жгучими , распирающими и др. болями за грудиной, в области сердца, нередко иррадиирующими вплоть до кончика уха и левой половины языка. Боли не купируются приемом таблеток нитроглицерина. Возникает status anginosus. Больной находится в состоянии стресса. Он мечется от боли и психоэмоционального возбуждения. Требуется экстренная помощь, чтобы освободиться от них.
Обезболивание является первым важным мероприятием в комплексе экстренной помощи, призванной снять боль и ослабить нарушения метаболизма. Ведь ухудшение метаболизма при болевом стрессе сопровождается снижением силы и скорости сокращения миокарда, гипоксией других органов.
Несмотря на полувековой период изучения болевого синдрома при остром инфаркте миокарда клиницистами, физиологами, биохимиками до настоящего времени не удалось синтезировать препарат, который полностью удовлетворял бы современным требованиям эффективного обезболивания при остром инфаркте миокарда при минимальных побочных явлениях.
На обезболивание возлагается задача разомкнуть звенья складывающегося порочного круга и оказать регулирующее, но не подавляющее действие (прежде всего, на системы кровообращения и дыхания), поскольку излишнее уменьшение (угнетение) вентиляции ослабляет компенсаторную роль внешнего дыхания по отношению к потребностям тканевого дыхания. Это выдвигает необходимость тщательного контроля за больным в процессе обезболивания. Следует учесть необходимость наряду с обезболиванием провести нейролепсию.
Рекомендуемые для обезболивания наркотические препараты (морфин, промедол, омнопон) полностью не удовлетворяют запросам практики: обладают умеренным обезболивающим действием, у лиц пожилого возраста довольно часто угнетают функцию внешнего дыхания, а при наличии сопутствующих заболеваний в стадии ремиссии обостряют их течение и тем самым усугубляют клиническое течение инфаркта миокарда.
Среди методов купирования интенсивных болей в острой фазе инфаркта миокарда, применяемых в последние 20 лет, считаем наиболее эффективным нейролептаналгезию (НЛА) фентанилом в сочетании с дроперидолом. В наших клинико-экспериментальных исследованиях проводилась сравнительная оценка обезболивающего действия при отром инфаркте миокарда наркотиков (морфин) и фентанила в сочетании с дроперидолом. Дозы фентнила и дроперидола подбирались индивидуально.
Если в распоряжении врачей есть нейролептанальгетические препараты, начинать обезболивание надо сразу же с НЛА. Для усиления обезболивающего эффекта НЛА желательно в начале ввести внутривенно ( при отсутствии противопоказаний) 10 000 ед.гепарина. Начинать обезболивание с морфина и его аналогов и только в случае недостаточного их эффекта переходить к НЛА как к крайнему средству – ошибочная тактика: действие морфина и фентанила на дыхание суммируется, значительно возрастает опасность дыхательных расстройств. При НЛА фентанилом и дроперидолом анальгетический эффект начинается во время внутривенного введения препратов и резко усиливается через 3-7 минут, на высоте действия фентанила. Затем развивается действием дроперидола и за счет его потенцирующего влияния анальгезия усиливается еще в течение примерно 10 мин. Таким образом, основной анальгетический эффект отмечается в первые минуты, окончательно же судить о степени обезболивания можно через 10 мин.
Обычно обезболивание сопровождается наступлением легкого сна, но больные остаются доступными для словесного контакта. Это нужно использовать для волевой стимуляции дыхания в случае его угнетения, что проявляется нарушением ритма дыхательных движений (может наступить дыхание типа Чейна-Стокса), значительным урежением дыхания и одновременно нарастанием цианоза. Поскольку больной находится в состоянии относительного покоя, безразличия, но сознание сохранено, он достаточно адекватно осуществляет акт произвольного дыхания по команде: «Вдох-выдох». Депрессия дыхания существенно уменьшается через 15 мин, поэтому такая стимуляция дыхания требуется лишь в течение этого короткого периода времени и отпадает необходимость в дыхательных аналептиках.
В некоторых ситуациях есть показания для сочетания НЛА со средствами, корригирующими исходные неблагоприятные гемодинамические сдвиги. Следует отметить, что сама НЛА обладает регулирующим свойством в отношении гемодинамики. Поэтому специальные корригирующие средства следует применять во вторую очередь – после НЛА. При брадикардии без гипотензии нет необходимости вводить атропин. При рефлекторной гипотензии с брадикардией следует вводить 0,5 мл или 1,0 мл 0,1 % раствора атропина внутривенно струйно или капельно. При исходной гипотензии без брадикардии НЛА часто способствует выведению больного из рефлекторного шока. Если этого не происходит и артериальное давление не повышается или даже есколько снижается, начинают капельное введение 200 мл полиглюкина и 1 мл 1% раствора мезатона. В отличие от фенотиазиновых нейролептиков, входящих в состав «литических коктейлей», дроперидол не блокирует чувствительность сосудов к действию вазоактивных веществ, а смягчает ее.
К сожалению, не всегда удается даже с помощью НЛА достичь желаемого обезболивающего эффекта. В таких случаях дополнительно применяют закись азота. В настоящее время во многих лабораториях проводятся исследования по усилению обезболивающего действия морфина.
После купирования острого болевого статуса в течение первых суток развития острого крупноочагового инфаркта миокарда с учетом особенностей клинической кратины проводится пролонгированная НЛА дроперидолом, трамалом с добавлением, при необходимости, фентанила. Дозировки препаратов уточняются в зависимости от реакции, выясненной во время контролированной НЛА. Общее правило – стремиться к минимальным эффективным дозам наркотических анальгетиков путем усиления НЛА за счет ненаркотических компонентов. При госпитализации больного в первые часы заболевания с выраженным болевым синдромом следует проводить струйно тромболитическую терапию с одновременным внутривенным введением нитроглицерина под контролем электрокардиограммы и АД.
В заключении считаем полезным обсудить некоторые организационно-методические вопросы. Практическое проведение обезболивания о остром периоде инфаркта миокарда с использованием современных лекарственных средств требует определенных знаний и навыков, целенаправленной постановки клинического мышления.
Каждый случай обезболивания представляет собой по существу логическую оптимизационную задачу. Анализ показывает, что врачи догоспитального этапа и стационаров часто выбирают ошибочную тактику обезболивания, не владеют современными методами контроля за больным. Отсюда вытекает необходимость систематического обучения врачей догоспитального и стационарного этапов оказанию помощи больным инфарктов миокарда на базе специализированных научно-практических центров.
Источник
Диагностика и лечение инфаркта миокарда на догоспитальном этапе
Как проводится купирование болевого приступа? В каких случаях показана тромболитическая терапия, а в каких — антикоагулянтная? Как проводится тромболитическая терапия? Что важно уточнить перед проведением тромболитической терапии? Инфаркт миокарда —
Как проводится купирование болевого приступа?
В каких случаях показана тромболитическая терапия, а в каких — антикоагулянтная?
Как проводится тромболитическая терапия? Что важно уточнить перед проведением тромболитической терапии?
Инфаркт миокарда — неотложное клиническое состояние, обусловленное некрозом участка сердечной мышцы, развившимся в результате нарушения ее кровоснабжения. Поскольку в первые часы (а иногда и сутки) от начала заболевания бывает сложно дифференцировать острый инфаркт миокарда и нестабильную стенокардию, для обозначения периода обострения ишемической болезни сердца (ИБС) в последнее время пользуются термином «острый коронарный синдром», под которым понимают любую группу клинических признаков, позволяющих заподозрить инфаркт миокарда или нестабильную стенокардию. Острый коронарный синдром может рассматриваться как первичный диагноз; он диагностируется на основании болевого синдрома (затяжной ангинозный приступ, впервые возникшая, прогрессирующая стенокардия) и изменений ЭКГ. Различают острый коронарный синдром с подъемом сегмента ST или остро возникшей полной блокадой левой ножки пучка Гиса (состояние, требующее проведения тромболизиса, а при наличии технических возможностей — ангиопластики) и без подъема сегмента ST — с его депрессией сегмента ST, инверсией, сглаженностью псевдонормализацией зубца Т, или вообще без изменений на ЭКГ (тромболитическая терапия не показана). Таким образом, диагноз «острый коронарный синдром» позволяет оперативно оценить объем необходимой неотложной помощи и выбрать адекватную тактику ведения пациентов.
С точки зрения определения объема необходимой лекарственной терапии и оценки прогноза представляют интерес три классификации. По глубине поражения (на основе данных электрокардиографического исследования) различают трансмуральный и крупноочаговый («Q-инфаркт» с подъемом сегмента ST в первые часы заболевания и формированием зубца Q в последующем) и мелкоочаговый («не Q-инфаркт», не сопровождающийся формированием зубца Q, а проявляющийся отрицательными зубцами Т); по клиническому течению — неосложненный и осложненный инфаркт миокарда; по локализации — инфаркт левого желудочка (передний, задний или нижний, перегородочный) и инфаркт правого желудочка.
Диагностика инфаркта миокарда на догоспитальном этапе
Наиболее типичным проявлением инфаркта миокарда является приступ боли в грудной клетке. Диагностически значимы такие параметры, как интенсивность болевого синдрома (если аналогичные боли возникали ранее, то при инфаркте они бывают необычно интенсивными), его продолжительность (необычно длительный приступ, продолжающийся более 15-20 мин), неэффективность сублингвального приема нитратов. При анализе клинической картины необходимо получить ответы на следующие вопросы:
- Когда начался приступ (желательно определить как можно точнее)?
- Сколько времени он длится (менее 15-20 мин или более)?
- Были ли попытки купировать приступ нитроглицерином (нитрокором) (удалось ли добиться хотя бы кратковременного эффекта)?
- Зависит ли боль от позы, положения тела, движений и дыхания (при коронарогенном приступе такая зависимость отсутствует)?
- Наблюдались ли аналогичные приступы в прошлом (аналогичные приступы, не завершившиеся инфарктом, требуют проведения дифференциальной диагностики с нестабильной стенокардией и с некардиальными причинами)?
- Возникали ли приступы боли или удушья при физической нагрузке (ходьбе), вынужден ли был пациент при этом останавливаться, какова была их продолжительность (в минутах), как пациент реагировал на нитроглицерин (нитрокор) (диагноз стенокардии напряжения делает весьма вероятным предположение об остром инфаркте миокарда)?
- Напоминает ли настоящий приступ по локализации или характеру болей ощущения, возникавшие при физической нагрузке (по интенсивности и сопутствующим симптомам приступ при инфаркте миокарда обычно более тяжелый, чем при стенокардии напряжения)?
По симптоматике острейшей фазы инфаркта миокарда, помимо болевого, выделяют и другие клинические варианты инфаркта миокарда (см. таблицу).
Данные физикального обследования (гипергидроз, резкая общая слабость, бледность кожных покровов, признаки острой сердечной недостаточности) при любом клиническом варианте инфаркта миокарда имеют только вспомогательное диагностическое значение.
Электрокардиографическими критериями инфаркта миокарда являются изменения, служащие признаками:
- повреждения — дугообразный подъем сегмента ST выпуклостью вверх, сливающийся с положительным зубцом T или переходящий в отрицательный зубец T (возможна дугообразная депрессия сегмента ST выпуклостью вниз);
- крупноочагового или трансмурального инфаркта — появление патологического зубца Q и уменьшение амплитуды зубца R или исчезновение зубца R и формирование QS;
- мелкоочагового инфаркта — появление отрицательного симметричного зубца T.
При инфаркте передней стенки подобные изменения выявляются в I и II стандартных отведениях, усиленном отведении от левой руки (aVL) и соответствующих грудных отведениях (V1, 2, 3, 4, 5, 6). При высоком боковом инфаркте миокарда изменения могут регистрироваться только в отведении aVL, и для подтверждения диагноза необходимо снять высокие грудные отведения. При инфаркте задней стенки (нижнем, диафрагмальном) эти изменения обнаруживаются во II, III стандартном и усиленном отведении от правой ноги (aVF). При инфаркте миокарда высоких отделов задней стенки левого желудочка (заднебазальном) изменения в стандартных отведениях не регистрируются, диагноз ставится на основании реципрокных изменений — высоких зубцов R и Т в отведениях V1-V2.
Кроме того, косвенным признаком инфаркта миокарда, не позволяющим определить фазу и глубину процесса, является остро возникшая блокада ножек пучка Гиса (при наличии соответствующей клиники).
Наибольшей достоверностью обладают электрокардиографические данные в динамике, поэтому электрокардиограммы по возможности должны сравниваться с предыдущими.
Таким образом, на догоспитальном этапе оказания медицинской помощи диагноз острого инфаркта миокарда ставится на основании клинической картины и изменений электрокардиограммы. В дальнейшем диагноз уточняется в стационаре после определения уровня маркеров некроза миокарда в крови и на основании динамики ЭКГ. В большинстве случаев острого коронарного синдрома с подъемом сегмента ST формируется инфаркт миокарда с зубцом Q; при остром коронарном синдроме без подъема сегмента ST при повышении уровня маркеров некроза диагностируется инфаркт миокарда без зубца Q, а при нормальном их уровне — нестабильная стенокардия.
Ведение больных на догоспитальном этапе
- Купирование болевого приступа при остром инфаркте миокарда представляет собой одну из важнейших задач, поскольку боль через активацию симпатоадреналовой системы вызывает повышение сосудистого сопротивления, частоты и силы сердечных сокращений, то есть увеличивает гемодинамическую нагрузку на сердце, повышает потребность миокарда в кислороде и усугубляет ишемию.
Если предварительный сублингвальный прием нитроглицерина (нитрокора, нитроспрея) (повторно по 0,5 мг в таблетках или 0,4 мг в аэрозоле) оказался неэффективым, рекомендуется начать терапию наркотическими анальгетиками, обладающими анальгетическим и седативным действием и влияющими на гемодинамику: вследствие вазодилатирующих свойств они обеспечивают гемодинамическую разгрузку миокарда, уменьшая в первую очередь преднагрузку. На догоспитальном этапе препаратом выбора для купирования болевого синдрома при инфаркте миокарда является морфин, не только обеспечивающий необходимый эффект, но и обладающий достаточной для транспортировки длительностью действия. Препарат вводится в/в дробно: 1 мл 1%-ного раствора разводят изотоническим раствором натрия хлорида до 20 мл (1 мл полученного раствора содержит 0,5 мг активного вещества) и вводят 2-5 мг каждые 5-15 мин до полного устранения болевого синдрома либо до появления побочных эффектов (гипотензии, угнетения дыхания, рвоты). На догоспитальном этапе не допускается превышение общей дозы 20 мг.
Для купирования тошноты и рвоты рекомендуют в/в введение 10-20 мг метоклопрамида (церукала, реглана). При выраженной брадикардии показано использование атропина в дозе 0,5 мг (0,5 мл 0,1%-ного раствора) в/в; терапия артериальной гипотензии проводится по общим принципам коррекции гипотензии при инфаркте миокарда.
Недостаточная эффективность обезболивания наркотическими анальгетиками служит показанием к в/в инфузии нитратов (см. ниже). При низкой эффективности нитратов в сочетании с тахикардией дополнительный обезболивающий эффект может быть получен благодаря введению бета-адреноблокаторов (см. ниже). Боль может быть купирована в результате эффективного тромболизиса (см. ниже).
Продолжающиеся интенсивные ангинозные боли служат показанием к применению масочного наркоза закисью азота (обладающей седативным и анальгезирующим действием) в смеси с кислородом. Начинают с ингаляции кислорода в течение 1-3 мин, затем используют закись азота (20 %) с кислородом (80 %) с постепенным повышением концентрации закиси азота до 80 %; после засыпания больного переходят на поддерживающую концентрацию газов — 50:50. Закись азота не снижает выброса левого желудочка. Возникновение побочных эффектов (тошноты, рвоты, возбуждения или спутанности сознания) является показанием для уменьшения концентрации закиси азота или отмены ингаляции. При выходе из наркоза ингалируют чистый кислород в течение 10 мин для предупреждения артериальной гипоксемии.
- Восстановление коронарного кровотока в острейшей фазе инфаркта миокарда при отсутствии противопоказаний осуществляется путем тромболизиса.
А. Показаниями к проведению тромболизиса служит подъем сегмента ST более чем на 0,1 мВ по крайней мере в двух стандартных отведениях ЭКГ и более чем на 0,2 мВ в двух смежных грудных отведениях или остро возникшая полная блокада левой ножки пучка Гиса в период от 30 мин до 12 ч от начала заболевания. Применение тромболитических средств возможно и позднее, если сохраняется подъем ST на ЭКГ, продолжается болевой приступ и/или наблюдается нестабильная гемодинамика.
В отличие от внутрикоронарного системный тромболизис (осуществляется внутривенным введением тромболитических средств) не требует каких-либо сложных манипуляций и специального оборудования. При этом он достаточно эффективен, если проводится в первые часы развития инфаркта миокарда (оптимально — на догоспитальном этапе), поскольку сокращение летальности напрямую зависит от сроков достижения реперфузии.
При отсутствии противопоказаний решение вопроса о проведении тромболизиса принимается на основании анализа фактора времени: при транспортировке более 30 мин или при отсрочке внутрибольничного проведения тромболизиса более чем на 60 мин введение тромболитических средств должно осуществляться на догоспитальном этапе. Во всех остальных случаях оно должно быть отложено до стационара.
Наиболее часто для проведения тромболизиса используется стрептокиназа внутривенно только через периферические вены, попытки катетеризации центральных вен недопустимы; перед инфузией возможно внутривенное введение 5-6 мл 25%-ного магния сульфата либо 10 мл кормагнезина-200 в/в струйно, медленно (за 5 мин); «нагрузочная» доза аспирина (250-300 мг разжевать) дается всегда, за исключением случаев, когда аспирин противопоказан (аллергические и псевдоаллергические реакции); 1 500 000 Ед стрептокиназы разводятся в 100 мл изотонического раствора хлорида натрия и вводятся внутривенно за 30 мин.
Одновременного назначения гепарина при использовании стрептокиназы не требуется — предполагают, что стрептокиназа сама обладает антикоагуляционными и антиагрегационными свойствами. Показано, что внутривенное введение гепарина не снижает летальности и частоты рецидивов инфаркта миокарда, а эффективность подкожного введения препарата сомнительна. Если гепарин по каким-либо причинам был введен ранее, это не является препятствием к проведению тромболизиса. Рекомендуется назначение гепарина через 12 ч после прекращения инфузии стрептокиназы. Практиковавшееся ранее использование гидрокортизона для профилактики анафилаксии признано не только малоэффективным, но и небезопасным в острейшей стадии инфаркта миокарда (глюкокортикоиды увеличивают риск разрыва миокарда).
Основные осложнения тромболизиса:
- Кровотечения (в том числе наиболее грозные — внутричерепные). Развиваются вследствие угнетения процессов свертывания крови и лизиса кровяных сгустков. Риск развития инсульта при системном тромболизисе составляет 0,5-1,5%, обычно инсульт развивается в первые сутки после проведения тромболизиса. Для остановки незначительного кровотечения (из места пункции, изо рта, носа) достаточно прижать кровоточащий участок. При более значимых кровотечениях (желудочно-кишечном, внутричерепном) необходима внутривенная инфузия аминокапроновой кислоты — 100 мл 5%-ного раствора вводят в течение 30 мин и далее 1 г/ч до остановки кровотечения — или транексамовой кислоты по 1-1,5 г 3-4 раза в сутки внутривенно капельно; кроме того, эффективно переливание свежезамороженной плазмы. Следует, однако, помнить о том, что при использовании антифибринолитических средств возрастает риск реокклюзии коронарной артерии и реинфаркта, поэтому использовать их можно лишь при угрожающих жизни кровотечениях.
- Аритмии, возникающие после восстановления коронарного кровообращения (реперфузионные). Не требуют интенсивной терапии медленный узловой или желудочковый ритм (при частоте сердечных сокращений менее 120 в мин и стабильной гемодинамике), наджелудочковая и желудочковая экстрасистолия (в том числе аллоритмированная), атриовентрикулярная блокада I и II (типа Мобитц I) степени. Неотложной терапии требуют фибрилляция желудочков (необходимы дефибрилляция, комплекс стандартных реанимационных мероприятий); двунаправленная веретенообразная желудочковая тахикардия типа «пируэт» (показаны дефибрилляция, введение сульфата магния внутривенно струйно); иные разновидности желудочковой тахикардии (используют введение лидокаина либо проводят кардиоверсию); стойкая суправентрикулярная тахикардия (купируется внутривенным струйным введением верапамила или новокаинамида); атриовентрикулярная блокада II (типа Мобитц II) и III степени, синоатриальная блокада (внутривенно струйно вводят атропин в дозе до 2,5 мг, при необходимости проводят экстренную электрокардиостимуляцию).
- Аллергические реакции. Сыпь, зуд, периорбитальный отек встречаются в 4,4% случаев, тяжелые реакции (отек Квинке, анафилактический шок) — в 1,7% случаев. При подозрении на развитие анафилактоидной реакции необходимо немедленно остановить инфузию стрептокиназы и ввести внутривенно болюсом 150 мг преднизолона. При выраженном угнетении гемодинамики и появлении признаков анафилактического шока внутривенно вводят 1 мл 1%-ного раствора адреналина, продолжая введение стероидных гормонов внутривенно капельно. При лихорадке назначают аспирин или парацетамол.
- Рецидивирование болевого синдрома после проведения тромболизиса купируется внутривенным дробным введением наркотических анальгетиков. При нарастании ишемических изменений на ЭКГ показано внутривенное капельное введение нитроглицерина или, если инфузия уже налажена, увеличение скорости его введения.
- При артериальной гипотонии в большинстве случаев бывает достаточно временно прекратить инфузию тромболитика и поднять ноги пациента; при необходимости уровень АД корректируется введением жидкости, вазопрессоров (допамина или норадреналина внутривенно капельно до стабилизации систолического АД на уровне 90-100 мм рт. ст.).
Клинические признаки восстановления коронарного кровотока: прекращение ангинозных приступов через 30-60 мин после введения тромболитика, стабилизация гемодинамики, исчезновение признаков левожелудочковой недостаточности, быстрая (в течение 2-3 ч) динамика ЭКГ с приближением сегмента ST к изолинии на 50% от исходного уровня подъема и ранним формированием патологического зубца Q и/или отрицательного зубца Т, появление реперфузионных аритмий (ускоренного идиовентрикулярного ритма, желудочковой экстрасистолии и др.), быстрая динамика МВ-КФК.
Для решения вопроса о возможности использования тромболитических средств следует уточнить ряд моментов:
- убедиться в отсутствии в течение предшествовавших 14 дней острых внутренних кровотечений — желудочно-кишечного, легочного, маточного (за исключением менструального), гематурии и других (обратить внимание на их наличие в анамнезе) или оперативных вмешательств и травм с повреждением внутренних органов;
- исключить наличие в течение предшествовавшего года острого нарушения мозгового кровообращения, операции или травмы головного или спинного мозга (обратить внимание на их наличие в анамнезе);
- убедиться в отсутствии признаков острого панкреатита, расслаивающей аневризмы аорты, а также аневризмы церебральных артерий, опухоли головного мозга или метастазирующих злокачественных опухолей;
- убедиться в отсутствии физикальных признаков или анамнестических указаний на патологию свертывающей системы крови — геморрагического диатеза, тромбоцитопении (обратить внимание на геморрагическую диабетическую ретинопатию);
- убедиться в том, что больной не получает непрямые антикоагулянты;
- уточнить, не было ли аллергических реакций на соответствующие тромболитические препараты, не вводилась ли стрептокиназа ранее, а именно в сроки от 5 дней до 2 лет (в этот период в связи с высоким титром антител 1 повторное введение стрептокиназы недопустимо);
- в случае успешно проведенных реанимационных мероприятий следует убедиться, что они не были травматичными и длительными (не более 10 мин при отсутствии признаков постреанимационных травм — переломов ребер и повреждений внутренних органов);
- при повышении АД следует снизить его и стабилизировать на уровне менее 180/100 мм рт. ст.
Следует также обратить внимание на другие состояния, чреватые развитием геморрагических осложнений и служащие относительными противопоказаниями к проведению системного тромболизиса: тяжелые заболевания печени и почек; подозрение на хроническую аневризму сердца, перикардит, инфекционный миокардит, тромб в сердечных полостях; тромбофлебит и флеботромбоз; варикозное расширение вен пищевода; язвенная болезнь в стадии обострения; беременность.
В сомнительных случаях проведение тромболитической терапии должно быть отложено до поступления больного в стационар (при атипичном развитии заболевания, неспецифических изменениях ЭКГ, давно существующей блокаде ножки пучка Гиса или ЭКГ-признаках несомненного предшествующего инфаркта миокарда, маскирующих типичные изменения).
Б. При отсутствии показаний к тромболитической терапии (поздние сроки, так называемый мелкоочаговый или «не-Q-инфаркт») проводится антикоагулянтная терапия. Ее цель заключается в предупреждении или ограничении тромбоза венечных артерий, а также в профилактике тромбоэмболических осложнений (особенно часто развивающихся у больных передним инфарктом миокарда, при низком сердечном выбросе, мерцательной аритмии). Для этого на догоспитальном этапе внутривенно болюсно вводится гепарин в дозе до 5000 МЕ. Если в условиях стационара не проводится тромболитическая терапия, то начинается длительная внутривенная инфузия гепарина со скоростью 800-1000 МЕ/ч под контролем активированного частичного тромбопластинового времени. Альтернативой может, по-видимому, служить подкожное введение низкомолекулярного гепарина в «лечебной» дозе. Введение гепарина на догоспитальном этапе не препятствует проведению тромболизиса в стационаре.
В. С первых минут от начала развития инфаркта миокарда всем больным при отсутствии противопоказаний следует назначать малые дозы ацетилсалициловой кислоты (аспирина). Антитромбоцитарный эффект препарата максимально проявляется уже через 30 мин, а своевременное начало применения аспирина позволяет существенно снизить летальность. Назначение ацетилсалициловой кислоты перед проведением тромболизиса дает наибольший клинический эффект. Доза для первого приема на догоспитальном этапе составляет 160-325 мг (разжевать). На стационарном этапе препарат назначается 1 раз в сутки по 100-125 мг.
- Уменьшение работы сердца и потребности миокарда в кислороде кроме полноценного обезболивания обеспечивается применением нитратов, бета-адреноблокаторов и магния сульфата.
А. Внутривенное введение нитратов при остром инфаркте миокарда способствует купированию болевого синдрома, гемодинамической разгрузке левого желудочка, снижает АД. Растворы нитратов для внутривенного введения готовят ex tempore: каждые 10 мг нитроглицерина (например, 10 мл 0,1%-ного раствора в виде препарата перлинганит) или изосорбида динитрата (например, 10 мл 0,1%-ного раствора в виде препарата изокет) разводят в 100 мл физиологического раствора (20 мг препарата — в 200 мл физиологического раствора и т. д.); таким образом, 1 мл приготовленного раствора содержит 100 мкг препарата. Нитраты вводят капельно под постоянным контролем АД и ЧСС с начальной скоростью 5-10 мкг/мин и последующим увеличением скорости на 20 мкг/мин каждые 5 мин до достижения желаемого эффекта или максимальной скорости введения — 400 мкг/мин. Обычно эффект достигается при скорости инфузии 50-100 мкг/мин. При отсутствии дозатора приготовленный раствор, содержащий в 1 мл 100 мкг нитрата, вводят при тщательном контроле (см. выше) с начальной скоростью 2-4 капли в минуту, при условии стабильной гемодинамики и сохранения болевого синдрома скорость может постепенно увеличиваться вплоть до максимальной — 30 капель в минуту. Введение нитратов начинают как линейные, так и специализированные бригады СиНМП и продолжают в стационаре. Продолжительность внутривенного введения нитратов — 24 ч и более; за 2-3 ч до окончания инфузии назначается первая доза нитратов внутрь. Передозировка нитратов, вызывающая падение сердечного выброса и снижение САД ниже 80 мм рт. ст., может привести к ухудшению коронарной перфузии и к увеличению размеров инфаркта миокарда.
Б. Внутривенное введение бета-адреноблокаторов, так же как и применение нитратов, способствует купированию болевого синдрома. Ослабляя симпатические влияния на сердце (усиливающиеся в первые 48 ч от начала развития инфаркта миокарда как вследствие самого заболевания, так и в качестве реакции на боль) и снижая потребность миокарда в кислороде, они способствуют уменьшению размеров инфаркта миокарда, подавляют желудочковые аритмии, уменьшают риск разрыва миокарда и повышают таким образом выживаемость пациентов. Очень важно, что, согласно экспериментальным данным, бета-адреноблокаторы позволяют отсрочить гибель ишемизированных кардиомиоцитов (они увеличивают время, в течение которого эффективна реперфузионная терапия).
При отсутствии противопоказаний бета-адреноблокаторы назначаются всем больным острым инфарктом миокарда. На догоспитальном этапе показаниями к их внутривенному введению для линейной бригады служат соответствующие нарушения ритма, а для специализированной — упорный болевой синдром, тахикардия, артериальная гипертензия. В первые часы заболевания показано дробное внутривенное введение пропранолола (обзидана) по 1 мг в минуту каждые 3-5 мин под контролем АД и ЭКГ до достижения ЧСС 55-60 в минуту или до достижения общей дозы 0,1 мг на кг массы тела пациента. При брадикардии, признаках сердечной недостаточности, AV-блокаде и снижении САД менее 100 мм рт. ст. пропранолол не назначается, а при развитии указанных изменений на фоне его применения введение препарата прекращается.
Отсутствие осложнений терапии бета-адреноблокаторами на догоспитальном этапе служит показанием для обязательного ее продолжения в условиях стационара с переходом на прием пропранолола внутрь в суточной дозе 40-320 мг в 4 приема (первый прием — спустя 1 ч после внутривенного введения).
В. Внутривенная инфузия магния сульфата проводится у больных с доказанной или вероятной гипомагнезиемией или при синдроме удлиненного QT, а также в случае осложнения инфаркта миокарда некоторыми вариантами аритмий. При отсутствии противопоказаний магния сульфат может служить определенной альтернативой применению нитратов и бета-адреноблокаторов, если их введение по какой-то причине невозможно (из-за противопоказаний или отсутствия препаратов). Согласно результатам ряда исследований, он снижает летальность при остром инфаркте миокарда, а также предотвращает развитие аритмий (в том числе реперфузионных при проведении системного тромболизиса) и постинфарктной сердечной недостаточности.
- Ограничение размеров инфаркта миокарда достигается адекватным обезболиванием, восстановлением коронарного кровотока и уменьшением работы сердца и потребности миокарда в кислороде (см. выше).
Этой же цели служит оксигенотерапия, показанная при остром инфаркте миокарда всем больным в связи с частым развитием гипоксемии даже при неосложненном течении заболевания. Ингаляция увлажненным кислородом проводится (если это не причиняет чрезмерных неудобств) с помощью маски или через носовой катетер со скоростью 3-5 л/мин и целесообразна в течение первых 24-48 ч от начала заболевания (начинается на догоспитальном этапе и продолжается в стационаре).
- Лечение и профилактика осложнений инфаркта миокарда. Все перечисленные мероприятия наряду с обеспечением физического и психического покоя и проведением госпитализации на носилках служат профилактикой осложнений острого инфаркта миокарда. Лечение же в случае их развития проводится дифференцированно, в зависимости от вида осложнений: отек легких, кардиогенный шок, нарушения сердечного ритма и проводимости, а также затянувшийся или рецидивирующий болевой приступ.
Тактика ведения больного с различными вариантами инфаркта миокарда на догоспитальном этапе представлена на рис. 1 и рис. 2.
Острый инфаркт миокарда является прямым показанием к госпитализации в отделение (блок) интенсивной терапии или кардиореанимации. Транспортировка больного осуществляется на носилках.
А. Л. Верткин, доктор медицинских наук, профессор
В. В. Городецкий, кандидат медицинских наук
О. Б. Талибов, кандидат медицинских наук
Источник