Способ проникновения липофильных неполярных молекул лекарственных веществ через клеточные мембраны
Способность проникать сквозь двойные липидные слои является условием для всасывания лекарственных средств, проникновения в клетки или в клеточные органеллы и прохождения через ГЭБ и плацентарный барьер. Благодаря амфифильной природе фосфолипиды образуют двойные слои, характеризующиеся гидрофильной поверхностью и гидрофобной внутренней частью. Вещества могут проникать через такую мембрану тремя разными способами.
а) Диффузия. В зависимости от степени липофильности вещества могут диффундировать непосредственно через двойной липидный слой по градиенту концентрации через мембрану (красные точки). В то же время мембрана практически непроницаема для высокогидрофильных веществ (норадреналина).
б) Пассивный транспорт. Во многих тканях есть транспортные системы для переноса через мембрану веществ, которые самостоятельно не могут через нее пройти. Проникая сквозь мембраны, вещества попадают внутрь клеток и в клеточные отделы, где имеется потребность в них. Эти транспортные системы расположены в мембранах и являются более или менее специфичными для определенной группы веществ.
Пассивный транспорт через мембрану не требует энергии. Каналы или белки-переносчики обеспечивают возможность гидрофильным веществам проникать через мембраны. Примерами являются потенциал- или лиганд-контролируемые ионные каналы (потенциалзависимые Na + -каналы, Са 2+ -каналы) и аквапорины.
Аквапорины — специальные транспортные белки, которые обеспечивают прохождение воды через гидрофобную клеточную мембрану во многих тканях организма.
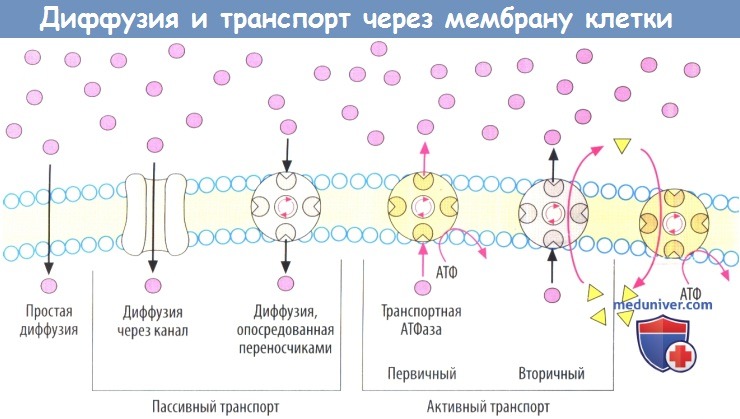
в) Активный транспорт. Многие транспортные процессы в организме осуществляются с прямым или непрямым использованием энергии аденозинтрифосфата (АТФ). Энергия АТФ особенно необходима, когда транспорт веществ через клеточную мембрану осуществляется против градиента концентрации, т. е. с затратой энергии.
В первичном активном транспорте участвуют белки, которые самостоятельно расщепляют АТФ (АТФазы) и таким образом обеспечивают транспорт веществ. Примерами являются Na + /K + -АТФаза или H + /K + -АТФаза.
Некоторые белки первичного активного транспорта выступают в роли мишеней для лекарственных средств; так, гликозиды наперстянки ингибируют Na + /K + -АТФазы] Ингибиторы протонной помпы снижают продукцию кислоты в желудке за счет ингибирования действия H + /K + -АТФазы.
г) При вторичном активном транспорте необходимо функциональное взаимодействие котранспортера с первичным АТФ-зависимым транспортером, В таком случае источником энергии, необходимой для транспорта вещества, служит движение ионов по градиенту концентрации. Градиент Na + обычно служит донором энергии. За поддержание градиента данного иона отвечает, в свою очередь, Na + /К + -АТФаза.
Многие нейромедиаторы и анионные или катионные переносчики используют клеточные градиенты Na + в качестве источника энергии.
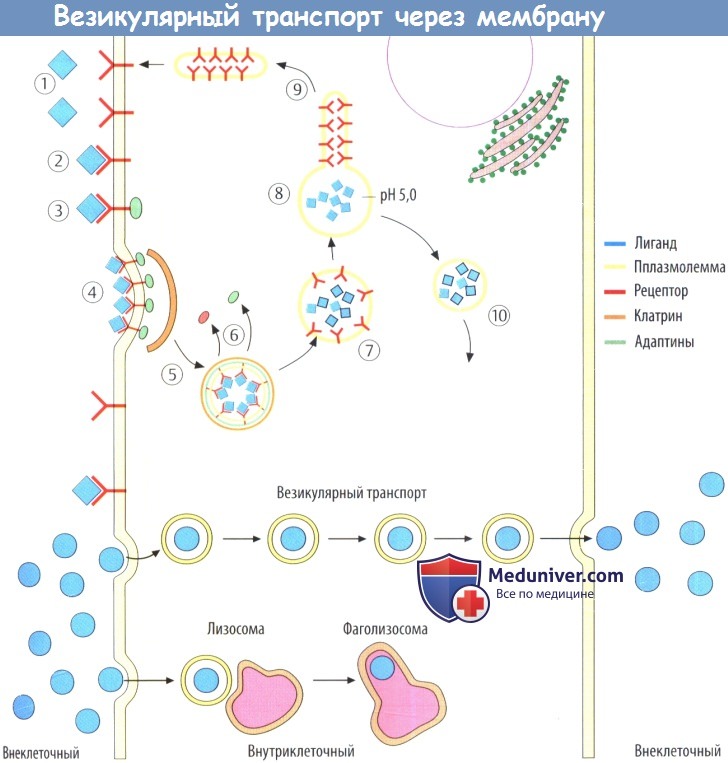
д) Трансцитоз (везикулярный транспорт). Вновь образованные везикулы захватывают растворенные во внеклеточной жидкости вещества и затем переносят их через цитоплазму. В некоторых случаях везикулы (фагосомы) сливаются с лизосомами дообразования фаголизосом, а переносимые вещества метаболизируются.
е) Эндоцитоз, опосредованный рецепторами. Лекарственное средство связывается в первую очередь с рецепторами на поверхности мембраны, а цитозольные участки рецепторов взаимодействуют со специальными белками (адаптины). Комплексы лекарственного вещества с рецептором мигрируют вдоль мембраны и соединяются с другими комплексами на основе клатринзависимого процесс. Область поврежденной мембраны инвагинирует и в конце концов отслаивается до образования обособленной везикулы.
Везикула охватывает клатрин и адаптин, что приводит к образованию ранней эндосомы. Внутри нее повышается концентрация протонов, вызывая диссоциацию комплекса «лекарственное средство-рецептор». Далее участки несущей рецептор мембраны отделяются от эндосомы. Они возвращаются обратно в плазмолемму в то время как эндосома направляется в органеллы мишени.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Способ проникновения липофильных неполярных молекул лекарственных веществ через клеточные мембраны
Фармакокинетика — всасывание, распределение, депонирование, превращения и выведение лекарственных веществ.
Все эти процессы связаны с проникновением лекарственных веществ через клеточную (цитоплазматическую) мембрану. Основные способы проникновения веществ через клеточную мембрану: пассивная диффузия, фильтрация, активный транспорт, облегченная диффузия, пиноцитоз.
Пассивная диффузия — проникновение веществ через мембрану в любом ее месте по градиенту концентрации (если с одной стороны мембраны концентрация вещества выше, чем с другой стороны, вещество проникает через мембрану в сторону меньшей концентрации). Так как мембраны состоят в основном из ли-пидов, путем пассивной диффузии через клеточную мембрану легко проникают липофильные неполярные вещества, т.е. вещества, которые хорошо растворимы в липидах и не несут электрических зарядов. Наоборот, гидрофильные полярные вещества (вещества, хорошо растворимые в воде и имеющие электрические заряды) путем пассивной диффузии через мембрану практически не проникают.
Многие лекарственные вещества являются слабыми электролитами — слабокислыми соединениями или слабыми основаниями. В растворе часть таких веществ находится в неионизированной (неполярной) форме, а часть — в виде ионов, несущих электрические заряды. Ионизация кислых соединений происходит путем их диссоциации.
Ионизация оснований происходит путем их протонирования.
Путем пассивной диффузии через мембраны проникает неиони-зированная (неполярная) часть слабого электролита. Таким образом, пассивная диффузия слабых электролитов обратно пропорциональна степени их ионизации.
В кислой среде увеличивается ионизация оснований, а в щелочной среде — ионизация кислых соединений. Однако при этом следует учитывать показатель рКа — отрицательный логарифм константы ионизации. Численно рКа равен рН, при котором ионизирована половина молекул соединения.
Значения рКа для разных кислот и разных оснований могут существенно различаться. Можно предположить, например, что ацетилсалициловая кислота (аспирин) при рН 4,5 будет мало диссоциировать. Однако для ацетилсалициловой кислоты рКа = 3,5, и результат получается неожиданным.
Для определения степени ионизации используют формулу Henderson — Hasselbalch :
Следовательно, при рН 4,5 ацетилсалициловая кислота почти полностью диссоциирована.
Фильтрация. В клеточной мембране имеются водные каналы (водные поры), через которые проходит вода и могут проходить растворенные в воде гидрофильные полярные вещества, если размеры их молекул не превышают диаметра каналов. Этот процесс называют фильтрацией.
Так как через водные каналы цитоплазматической мембраны нет постоянного однонаправленного движения воды, ряд авторов считают, что через водные каналы гидрофильные полярные вещества
проникают путем пассивной диффузии по градиенту концентрации (пассивная диффузия в водной фазе).
Однако диаметр водных каналов цитоплазматической мембраны очень мал — 0,4 нм, поэтому большинство лекарственных веществ через эти каналы не проходят.
Фильтрацией называют также прохождение воды и растворенных в ней веществ через межклеточные промежутки. Путем фильтрации через межклеточные промежутки проходят гидрофильные полярные вещества. Степень их фильтрации зависит от величины межклеточных промежутков.
В эндотелии сосудов мозга межклеточные промежутки отсутствуют и фильтрация большинства лекарственных веществ невозможна. Эндотелий сосудов мозга образует барьер, который препятствует проникновению гидрофильных полярных веществ из крови в мозг, — гематоэнцефалический барьер.
В некоторых областях головного мозга имеются «дефекты» гематоэнцефалического барьера, через которые возможно прохождение гидрофильных полярных веществ. Так, в area postrema продолговатого мозга гидрофильные полярные вещества могут проникать в триггер-зону рвотного центра.
Некоторые гидрофильные полярные вещества проникают через гематоэнцефалический барьер путем активного транспорта (например, леводопа).
Липофильные неполярные вещества легко проходят через гематоэнцефалический барьер путем пассивной диффузии.
В эндотелии сосудов периферических тканей (мышцы, подкожная клетчатка, внутренние органы) межклеточные промежутки достаточно велики и большинство гидрофильных полярных лекарственных веществ легко проходят через них путем фильтрации. При внутривенном введении эти вещества быстро проникают в ткани. При подкожном, внутримышечном введении вещества проникают из тканей в кровь и распространяются по организму.
В желудочно-кишечном тракте промежутки между клетками эпителия слизистой оболочки невелики и фильтрация веществ ограничена, поэтому в желудочно-кишечном тракте гидрофильные полярные соединения всасываются плохо. Так, гидрофильное полярное соединение неостигмин (прозерин) под кожу вводят в дозе 0,0005 г, а для получения сходного эффекта при приеме внутрь требуется доза 0,015 г.
Липофильные неполярные вещества в желудочно-кишечном тракте хорошо всасываются путем пассивной диффузии.
Активный транспорт — транспорт лекарственных веществ через мембраны с помощью специальных транспортных систем. Такими транспортными системами обычно являются функционально активные белковые молекулы, встроенные в цитоплазматическую мембрану. Лекарственное вещество, имеющее аффинитет к транспортной системе, соединяется с местами связывания этой системы с одной стороны мембраны; затем происходит кон-формация белковой молекулы и вещество высвобождается с другой стороны мембраны.
Активный транспорт избирателен, насыщаем, требует затрат энергии, может происходить против градиента концентрации.
Облегченная диффузия— перенос вещества через мембраны специальными транспортными системами по градиенту концентрации без затрат энергии.
Пиноцитоз — впячивания клеточной мембраны, окружающие молекулы вещества и образующие вакуоли, которые проникают через клетку и высвобождают вещество с другой стороны клетки.
1. Всасывание (абсорбция)
При большинстве путей введения лекарственные вещества, прежде чем они попадут в кровь, проходят процесс всасывания.
Различают энтеральные (через пищеварительный тракт) и парентеральные (помимо пищеварительного тракта) пути введения лекарственных веществ.
Энтеральные пути введения — введение веществ под язык, внутрь, ректально. При этих путях введения вещества всасываются в основном путем пассивной диффузии. Поэтому хорошо всасываются липофильные неполярные вещества и плохо — гидрофильные полярные соединения.
При введении веществ под язык (сублингвально) всасывание происходит быстро и вещества попадают в кровь, минуя печень. Однако всасывающая поверхность невелика и таким путем можно вводить только высокоактивные вещества, назначаемые в малых дозах. Например, сублингвально применяют таблетки нитроглицерина, содержащие 0,0005 г нитроглицерина; действие наступает через 1—2 мин.
При назначении веществ внутрь ( per os ) лекарственные средства (таблетки, драже, микстуры и др.) проглатывают; всасывание веществ происходит в основном в тонком кишечнике.
Из тонкого кишечника вещества через систему воротной вены попадают в печень и только затем — в общий кровоток. В печени многие вещества подвергаются превращениям (биотрансформация); некоторые вещества выделяются из печени с желчью. В связи с этим в кровь может попасть лишь часть вводимого вещества; остальная часть подвергается элиминации при первом прохождении (пассаже) через печень.
Лекарственные вещества могут неполностью всасываться в кишечнике, подвергаться метаболизму в стенке кишечника. Поэтому часто используют более общий термин — «пресистемная элиминация».
Количество неизмененного вещества, попавшего в общий кровоток, в процентном отношении к введенному количеству обозначают термином «биодоступность». Например, биодоступность про-пранолола 30%. Это означает, что при приеме внутрь в дозе 0,01 г (10 мг) только 0,003 г (3 мг) неизмененного пропранолола попадает в кровь.
Для определения биодоступности лекарственное вещество вводят в вену (при внутривенном введении биодоступность вещества — 100%). Через определенные интервалы времени определяют концентрации вещества в плазме крови и строят кривую изменения концентрации вещества во времени. Затем ту же дозу вещества назначают внутрь, определяют концентрации вещества в крови и строят кривую концентрация-время (рис. 1).
Измеряют площади под кривыми — AUC ( Area Under the Curve ). Биодоступность — F ( Fraction ) определяют как отношение AUC при назначении внутрь к AUC при внутривенном введении и обозначают в процентах
При одинаковой биодоступности двух веществ скорость их поступления в общий кровоток может быть различной. Соответственно различными будут время достижения пиковой концентрации, максимальная концентрация в плазме крови, величина фармакологического эффекта. В связи с этим вводят понятие «биоэквивалентность». Биоэквивалентность двух веществ означает сходные биодоступность, пик действия, характер и величину фармакологического эффекта.
Некоторые лекарственные средства вводят ректально (в прямую кишку) в виде ректальных суппозиториев (свечей) или лекарственных клизм. При этом 50% вещества после всасывания попадает в кровь, минуя печень.
Рис. 1. Биодоступность лекарственного вещества
Биодоступность ( F — Fraction ) определяется как отношение площадей под кривыми
концентрация — время ( AUC ) при приеме вещества внутрь и введении внутривенно.
Парентеральные пути введения — введение веществ, минуя пищеварительный тракт. Наиболее употребительные парентеральные пути введения — в вену, под кожу, в мышцы.
При внутривенном введении лекарственное вещество сразу попадает в кровь; действие вещества развивается очень быстро, обычно в течение 1—2 мин. Чтобы не создавать в крови слишком высокой концентрации вещества, большинство лекарственных средств перед внутривенным введением разводят в 10—20 мл изотонического (0,9%) раствора натрия хлорида или изотонического (5%) раствора глюкозы и вводят медленно — в течение нескольких минут. Нередко лекарственные вещества в 250—500 мл изотонического раствора водят в вену капельно, иногда в течение многих часов.
В вену нельзя вводить масляные растворы и взвеси (суспензии) в связи с опасностью закупорки сосудов (эмболии). Однако внутривенно иногда вводят небольшие количества гипертонических растворов (например, 10—20 мл 40% раствора глюкозы), которые быстро разводятся кровью.
При внутримышечном введении (чаще всего в мышцы ягодицы) вещества могут всасываться путем пассивной диффузии и путем фильтрации ( через межклеточные промежутки в эндотелии кровеносных сосудов). Таким образом, внутримышечно можно вводить и липофильные неполярные, и гидрофильные полярные соединения.
В мышцы нельзя вводить гипертонические растворы и раздражающие вещества. В то же время, в мышцы вводят масляные растворы и взвеси (суспензии). При введении взвеси в мышце создается депо препарата, из которого лекарственное вещество может медленно и длительно всасываться в кровь.
При подкожном введении (в подкожную жировую клетчатку) вещества всасываются так же, как и при внутримышечном введении, но более медленно, так как кровоснабжение подкожной клетчатки меньше, чем кровоснабжение скелетных мышц. Под кожу иногда вводят масляные растворы и взвеси. Однако по сравнению с введением в мышцы масляные растворы и взвеси медленнее всасываются и могут образовывать инфильтраты.
Из других путей введения лекарственных средств в клинической практике используют ингаляционное введение (вдыхание газообразных веществ, паров летучих жидкостей, аэрозолей), введение веществ под оболочки мозга, внутриартериальное введение и некоторые другие.
При попадании в общий кровоток липофильные неполярные вещества распределяются в организме относительно равномерно, а гидрофильные полярные вещества — неравномерно, Препятствиями для распределения гидрофильных полярных веществ являются, в частности, гисто-гемагпические барьеры, т.е. барьеры, отделяющие некоторые ткани от крови. К таким барьерам относятся гематоэн-цефалический, гематоофтальмический и плацентарный барьеры.
Гематоэнцефалический барьер образован слоем эндотелиальных клеток капилляров мозга, в котором отсутствуют межклеточные промежутки. Гематоэнцефалический барьер препятствует проникновению гидрофильных полярных веществ из крови в ткани мозга. При воспалении мозговых оболочек проницаемость гематоэнцефа-лического барьера повышается.
Гематоофтальмический барьер препятствует проникновению гидрофильных полярных веществ из крови в ткани глаз.
Плацентарный барьер во время беременности препятствует проникновению ряда веществ из организма матери в организм плода.
Для характеристики распределения лекарственного вещества используют кажущийся объем распределения — Vd ( Volume of distribution ).
В системе однокамерной фармакокинетической модели ,
где D — доза, Со — начальная концентрация. Поэтому кажущийся объем распределения можно определить как гипотетический объем жидкостей организма, в котором после внутривенного введения, при условии мгновенного и равномерного распределения концентрация вещества равна его концентрации в плазме крови. Vd определяют в литрах или л/кг.
Если для условного человека с массой тела 70 кг Vd = 3 л (объем плазмы крови ), это означает, что вещество находится в плазме крови, не проникает в форменные элементы крови и не выходит за пределы кровеносного русла.
Vd = 15 л означает, что вещество находится в плазме крови (3 л), в межклеточной жидкости (12 л) и не проникает в клетки тканей.
Vd = 40 л (общее количество жидкости в организме) означает, что вещество распределено во внеклеточной и внутриклеточной жидкости.
Vd = 400 — 600 -1000 л означает, что вещество депонировано в периферических тканях и его концентрация в крови низкая. Например, для имипрамина (трициклический антидепрессант) Vd = 23 л/кг, т.е. примерно 1600 л. В связи с этим концентрация имипрамина в крови очень низкая и при отравлении имипрамином гемодиализ не эффективен.
При распределении лекарственного вещества в организме часть вещества может задерживаться (депонироваться) в различных тканях. Из «депо» вещество высвобождается в кровь и оказывает фармакологическое действие. Липофильные вещества могут депонироваться в жировой ткани. Так, средство для внутривенного наркоза тиопентал-натрий вызывает наркоз, который продолжается 15—20 мин. Кратковременность действия связана с тем, что 90% тиопентала-натрия депонируется в жировой ткани. После прекращения наркоза наступает посленаркозный сон, который продолжается 2—3 ч и связан с действием препарата, высвобождаемого из жирового депо.
Антибиотики из группы тетрациклинов на длительное время депонируются в костной ткани. Тетрациклины не рекомендуют назначать детям до 8 лет, так как, депонируясь в костной ткани, они могут нарушать развитие скелета.
Многие вещества депонируются в крови, связываясь с белками плазмы крови. В соединении с белками плазмы вещества не проявляют фармакологической активности. Однако часть вещества высвобождается из связи с белками и оказывает фармакологическое действие. Вещества, которые более прочно связываются с белками, могут вытеснять вещества с меньшей прочностью связывания. Действие вытесненного вещества при этом усиливается, так как увеличивается концентрация в плазме крови его свободной (активной) формы. Например, сульфаниламиды, салицилаты могут таким образом усиливать действие назначаемых одновременно непрямых антикоагулянтов. При этом свертываемость крови может чрезмерно снижаться, что ведет к кровотечениям.
Большинство лекарственных веществ в организме подвергается превращениям (биотрансформации). Различают метаболическую трансформацию (окисление, восстановление, гидролиз) и конъюгацию (ацетилирование, метилирование, образование соединений с глюкуроновой кислотой и др.). Соответственно, продукты превращений называют метаболитами и конъюгатами. Обычно вещество подвергается сначала метаболической трансформации, а затем конъюгации. Метаболиты, как правило, менее активны, чем исходные соединения, но иногда оказываются активнее (токсичнее) исходных веществ. Конъюгаты обычно малоактивны.
Большинство лекарственных веществ подвергается биотрансформации в печени под влиянием ферментов, локализованных в эндоплазматическом ретикулуме клеток печени и называемых микросомальными ферментами (в основном изоферменты цитохрома Р-450).
Эти ферменты действуют на липофильные неполярные вещества, превращая их в гидрофильные полярные соединения, которые легче выводятся из организма. Активность микросомальных ферментов зависит от пола, возраста, заболеваний печени, действия некоторых лекарственных средств.
Так, у мужчин активность микросомальных ферментов несколько выше, чем у женщин (синтез этих ферментов стимулируется мужскими половыми гормонами). Поэтому мужчины более устойчивы к действию многих фармакологических веществ.
У новорожденных система микросомальных ферментов несовершенна, поэтому ряд лекарственных веществ (например, хлорамфеникол) в первые недели жизни назначать не рекомендуют в связи с их выраженным токсическим действием.
Активность микросомальных ферментов печени снижается в пожилом возрасте, поэтому многие лекарственные препараты лицам старше 60 лет назначают в меньших дозах по сравнению с лицами среднего возраста.
При заболеваниях печени активность микросомальных ферментов может снижаться, замедляется биотрансформация лекарственных средств, усиливается и удлиняется их действие.
Известны лекарственные вещества, индуцирующие синтез микросомальных ферментов печени, например, фенобарбитал, гризеофульвин, рифампицин. Индукция синтеза микросомальных ферментов при применении указанных лекарственных веществ развивается постепенно (примерно в течение 2 нед). При одновременном назначении с ними других препаратов (например, глюкокортикоидов, противозачаточных средств для приема внутрь) действие последних может ослабляться.
Некоторые лекарственные вещества (циметидин, хлорамфени-кол и др.) снижают активность микросомальных ферментов печени и поэтому могут усиливать действие других препаратов.
5. Выведение (экскреция)
Большинство лекарственных веществ выводится из организма через почки в неизмененном виде или в виде продуктов биотрансформации. В почечные канальцы вещества могут поступать при фильтрации плазмы крови в почечных клубочках. Многие вещества секретируются в просвет проксимальных канальцев. Транспортные системы, которые обеспечивают эту секрецию, малоспецифичны, поэтому разные вещества могут конкурировать за связывание с транспортными системами. При этом одно вещество может задерживать секрецию другого вещества и таким образом задерживать его выведение из организма. Например, хинидин замедляет секрецию дигоксина, концентрация дигоксина в плазме крови повышается, возможно проявление токсического действия дигоксина (аритмии и др.).
Липофильные неполярные вещества в канальцах подвергаются обратному всасыванию (реабсорбции) путем пассивной диффузии. Гидрофильные полярные соединения мало реабсорбируются и выводятся почками.
Выведение (экскреция) слабых электролитов прямо пропорционально степени их ионизации (ионизированные соединения мало реабсорбируются). Поэтому для ускоренного выведения кислых соединений (например, производных барбитуровой кислоты, салицилатов) реакцию мочи следует изменять в щелочную сторону, а для выведения оснований — в кислую.
Кроме того, лекарственные вещества могут выделяться через желудочно-кишечный тракт (выделение с желчью), с секретами потовых, слюнных, бронхиальных и других желез. Летучие лекарственные вещества выделяются из организма через легкие с выдыхаемым воздухом.
У женщин в период кормления грудью лекарственные вещества могут выделяться молочными железами и с молоком попадать в организм ребенка. Поэтому кормящим матерям не следует назначать лекарства, которые могут неблагоприятно воздействовать на ребенка.
Биотрансформация и экскреция лекарственных веществ объединяются термином «элиминация». Для характеристики элиминации используют константу элиминации — ке1 (ке) и период полуэлиминации — t 1/2 .
Константа элиминации показывает, какая часть вещества элиминируется в единицу времени. Например, внутривенно введено вещество А в дозе 10 мг; ке1 = 0,1/ч. Через 1 ч в плазме крови останется 9 мг, через 2 ч — 8,1 мг.
Период полуэлиминации — t 1/2 — время, за которое концентрация вещества в плазме крови снижается наполовину. В основное время элиминации t 1/2 не зависит от дозы вещества и одинаков в разное
Другими словами, Clt показывает, какая часть объема распределения освобождается от вещества в единицу времени.
Для оптимального терапевтического эффекта и для предупреждения токсического действия необходимо поддерживать в плазме крови постоянную (стационарную) терапевтическую концентрацию лекарственного вещества. Стационарную концентрацию обозначают как Css ( steady — state concentration ). В справочниках и руководствах по фармакологии приводят значения средних терапевтических концентраций для наиболее употребительных лекарственных веществ.
Определяют также минимальную терапевтическую концентрацию (минимальную эффективную концентрацию) — Css min и максимальную терапевтическую концентрацию (максимальную безопасную концентрацию) — Css max , выше которой концентрации становятся токсическими. Интервал между Css min и Css max соответствует терапевтической широте (рис. 2). Чем больше терапевтическая широта лекарственного средства, тем легче его использовать в практической медицине. Наоборот, при малой терапевтической широте увеличивается вероятность попадания в зону токсических концентраций.
Для поддержания средней терапевтической концентрации лекарственного вещества можно вводить раствор этого вещества внутривенно капельно. При этом концентрация вещества в плазме крови сначала повышается быстро, затем медленнее и, наконец, устанавливается стационарная концентрация, при которой скорость введения вещества равна скорости его элиминации (биотрансформация + экскреция). Скорость введения определяют по формуле
Однако значительно чаще лекарственные вещества назначают внутрь или в виде отдельных инъекций. В этих случаях целесообразно сначала вводить нагрузочную дозу для быстрого достижения терапевтической концентрации, а затем назначать малые дозы, которые поддерживают терапевтическую концентрацию, — поддерживающие дозы.
Источник




