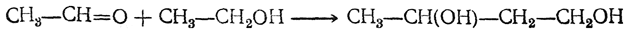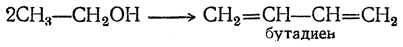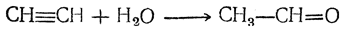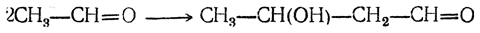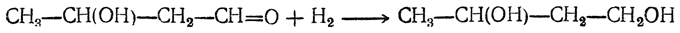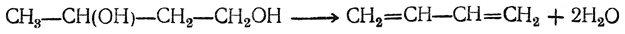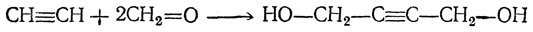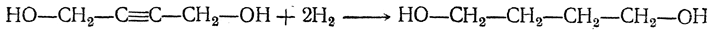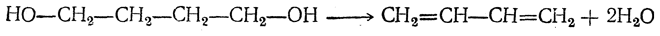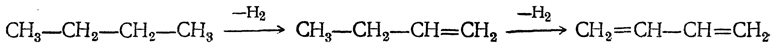- Получение алкадиенов
- Получение алкадиенов
- 1. Дегидрирование алканов
- 2. Синтез Лебедева
- 3. Дегидратация двухатомных спиртов
- 4. Дегидрогалогенирование дигалогеналканов
- Бутадиен-1,3, или дивинил
- Основы химии и технологии мономеров
- Calendar
- Книга в формате PDF
- Главы:
- Страницы
- 4.1 Бутадиен-1,3
- 4.1.1. Способ С.В. Лебедева
- 4.1.3. Получение бутадиена из ацетилена
- Синтез бутадиена через альдоль (альдольный метод)
- Синтез бутадиена через бутиндиол
- Синтез бутадиена через димеризацию ацетилена
- Пиролиз углеводородного сырья
- Параметр
Получение алкадиенов
Алкадиены – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствуют две двойные связи между атомами углерода С=С.
Общая формула алкадиенов CnH2n-2 (как у алкинов, а также циклоалкенов), где n ≥ 3.
Наличие двух двойных связей между атомами углерода очень сильно влияет на свойства углеводородов. В этой статье мы подробно остановимся на свойствах, способах получения и особенностях строения алкадиенов.
Получение алкадиенов
1. Дегидрирование алканов
Отщепление водорода от бутана — это промышленный способ получения дивинила. Реакция протекает при нагревании в присутствии оксида хрома (III):

Изопрен получают каталитическим дегидрированием изопентана (2-метилбутана):
2. Синтез Лебедева
Н агревание этанола в присутствии катализатора (смесь оксидов Al2O3, MgO, ZnO) – это промышленный способ получения дивинила из этанола (синтез Лебедева).
При этом образуются бутадиен-1,3, вода и водород:
3. Дегидратация двухатомных спиртов
Под действием серной кислоты вода отщепляется от бутандиола-1,3. При этом образуется дивинил и вода:
4. Дегидрогалогенирование дигалогеналканов
Под действием спиртовых растворов щелочей протекает отщепление атомов галогена и водорода и образуются вода, соль и алкадиен.
При этом атомы галогенов в дигалогеналкане должны располагаться не у одного и не у соседних атомов углерода.
1,3-Дихлорбутан реагирует со спиртовым раствором гидроксида калия с образованием бутадиена-1,3:
Источник
Бутадиен-1,3, или дивинил
Бутадиен-1,3, или дивинил, СН2=СН—СН=СН2 представляет собой газ, конденсирующийся при —4,5° С. Вследствие громадного технического значения бутадиена-1,3 как одного из важнейших исходных мономеров для производства синтетических каучуков было разработано много способов его получения, в том числе и промышленных.
Бутадиен образуется при термическом разложении различных органических веществ; в небольших количествах содержится в газах, получаемых пиролизом нефтепродуктов и каменного угля. Он может быть получен пиролизом циклогексана и других углеводородов нефти, пиролизом циклогексанола, дегидратацией 1,3-бутиленгликоля, а также конденсацией альдегида и спирта в присутствии глинозема как катализатора (И. И. Остромысленский). В последнем случае, вероятно, промежуточно образуется 1,3-бутиленгликоль
который сразу же дегидратируется. Другой способ получения бутадиена из спирта состоит в окислении этанола в ацегальдегид, который конденсируют в альдоль; восстановление альдоля дает 1,3-бутиленгликоль.
Первым технически целесообразным путем получения бутадиена из спирта является способ С. В. Лебедева, впервые осуществленный в промышленных масштабах в СССР в 1932 г. и в дальнейшем получивший широкое распространение. По С. В. Лебедеву спирт непосредственно превращается в бутадиен при пропускании его паров при 400—500° С над катализатором, обладающим одновременно дегидрирующим и дегидратирующим действием. Суммарно процесс выражается уравнением
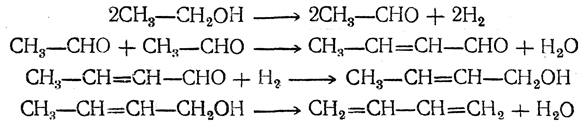
Вероятно, механизм этой реакции (М. Я. Каган, Ю. Д. Горин) таков:
Можно получать дивинил, в том числе и в промышленном масштабе, на основе ацетилена. Более старый метод синтеза из ацетилена может быть представлен следующей схемой:
Позднее был предложен следующий путь: 1. Получение 1,4-бутиндиола конденсацией ацетилена и формальдегида (с Сu2Сl2 в качестве катализатора):
2. Гидрирование 1,4-бутиндиола в 1,4-бутандиол:
3. Дегидратация 1,4-бутандиола в дивинил либо непосредственно
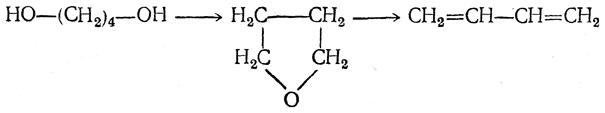
либо с промежуточным выделением тетрагидрофурана
В настоящее время самым эффективным методом получения дивинила является каталитическое дегидрирование природного бутана, а также бутиленов, содержащихся в газах термической переработки нефти. Реакция проводится над различными алюмо-хромовыми катализаторами при 500—650° С. В зависимости от применяемых катализаторов бутан может быть превращен в бутадиен либо сразу, либо в две стадии
причем для каждой стадии требуются свои катализаторы и условия реакции. Эти методы, разрабатывавшиеся одновременно в СССР и в США, в настоящее время осуществляются как промышленные.
Хлорпроизводное дивинила — 2-хлорбутадиен-1,3, или хлоропрен, СН2—СН—ССl=СН2 может быть получен присоединением молекулы хлористого водорода к винилацетилену, получаемому при пропускании ацетилена через солянокислые растворы медных солей. Хлоропрен — жидкость с характерным эфирным запахом, несколько напоминающим запах бромистого этила; т. кип. 59,4°С, относительная плотность 0,9533 (при 20°С). Подобно дивинилу, но значительно легче, хлоропрен полимеризуется в каучукоподобные вещества — синтетические каучуки, выпускаемые в СССР под названием наирит, а в США — под названием неопрен.
Полихлоропреновые каучуки обладают рядом ценных физико-химических свойств — стойкостью к атмосферным воздействиям, к солнечному свету, к различным маслам и химическим агентам, а также негорючестью, благодаря чему они нашли очень широкое применение.
Источник
Основы химии и технологии мономеров
«Основы химии и технологии мономеров», Н.А. Платэ, Е.В. Сливинский, 2002 г. (pdf-версия книги, 5 Мб.)
Calendar
-
Ноябрь 2021
Пн Вт Ср Чт Пт Сб Вс « Мар 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30
—>
Книга в формате PDF
Главы:
Страницы
4.1 Бутадиен-1,3
Бутадиен-1,3 (дивинил) СН2=СН—СН=СН2 – бесцветный газ с характерным неприятным запахом с темп. кип. 268,59 К.
Бутадиен – типичный диеновый углеводород с сопряженными двойными связями, легко полимеризуется и сополимеризуется со стиролом, нитрилами или эфирами акриловой или метакриловой кислот, винил- и метилвинилпиридинами, винил- и винилиденхлоридами, изобутиленом, изопреном и др. Бутадиен является основным мономером, применяемым в современном промышленном производстве синтетических каучуков. На бутадиене базируется производство подавляющего большинства синтетических каучуков общего назначения: стереорегулярные 1,4,-цис-бутадиеновые, бутадиен-стирольные, бутадиен-метилстирольные, ряд синтетических каучуков специального назначения – бутадиен-нитрильные, бутадиен- метилвинилпиридиновые и др. Помимо производства синтетических каучуков, бутадиен применяется в промышленном масштабе для производства синтетических смол, адиподинитрила (в производстве полиамидов) и себациновой кислоты.
Впервые процесс получения бутадиена из этилового спирта был разработан С.В. Лебедевым (СССР). Впоследствии он получил развитие в США.
Процесс производства бутадиена по реакции ацетилена с формальдегидом (способ Реппе) впервые был реализован в Германии. Затем были разработаны процессы получения бутадиена через альдольную конденсацию ацетальдегида (Германия) и дегидратацией и дегидрированием этанола (Советский Союз, США). В настоящее время бутадиен получают из нефтяного сырья выделением из фракции С4 парового крекинга и дегидрированием бутана и частично бутена, также содержащихся во фракции С4 парового крекинга.
4.1.1. Способ С.В. Лебедева
На первых заводах синтетического каучука, построенных в Советском Союзе еще в начале 30-х годов, бутадиен получали по способу С.В. Лебедева путем каталитического разложения этилового спирта. На основе этого процесса в СССР впервые в мире было создано промышленное производство синтетического каучука. Процесс проводили в одну стадию:
Качественный состав продуктов реакции при превращении этанола в бутадиен свидетельствует о том, что в процессе протекают реакции конденсации, дегидрирования и дегидратации. Эти реакции проводят в одну стадию за счет использования полифункционального оксидного катализатора. Таким образом, в условиях превращения этанола реализуются следующие реакции:
дегидрирование спирта до ацетальдегида
конденсации ацетальдегида в альдоль с последующим отщеплением воды и образованием кротонового альдегида
восстановление карбонильной группы кротонового альдегида водородом, отдаваемым этиловым спиртом, с образованием кротилового спирта и ацетальдегида
дегидратация кротилового спирта, сопровождающаяся перегруппировкой двойных связей с образованием бутадиена
Превращение спирта в бутадиен протекает при 633-653 К на неподвижном оксидном катализаторе. В качестве побочных продуктов образуются органические соединения различных классов: углеводороды, спирты, эфиры, альдегиды и др.
Теоретический выход бутадиена составляет 58,7%, однако, вследствие протекания побочных реакций он обычно бывает несколько ниже, но остается близким к теоретическому. Основным недостатком процесса является низкая селективность. Достоинство способа – сравнительная простота аппаратурного оформления технологического процесса. В настоящее время этот процесс в основном потерял промышленное значение.
4.1.2. Способ И.И. Остромысленского
Другой способ получения бутадиена, предложенный русским химиком И.И. Остромысленским еще в 1915 г., был реализован в США в годы Второй мировой войны. В отличие от способа С.В. Лебедева этот процесс протекает в две стадии.
на первой стадии дегидрированием этанола получают ацетальдегид:
На второй стадии смесь спирта и ацетальдегида в мольном соотношении 3:1 пропускают над катализатором (оксид тантала на силикагеле):
Селективность процесса – 63,9% от теоретической.
По этой технологии дегидрирование осуществляют при 523-573 К. В качестве катализатора используют медь, нанесенную на асбестовое волокно. В качестве промоторов к катализатору добавляют 5 % оксида кобальта и 2% оксида хрома (в расчете на медь). Выход ацетальдегида на пропущенный этанол составляет 30-40% при селективности
92%. Основными побочными продуктами являются масляный альдегид, этилацетат и уксусная кислота.
Вторая стадия получения бутадиена по этому способу представляет собой совместное превращение этанола и ацетальдегида в присутствии в качестве катализатора оксида тантала, нанесенного на силикагель, при 603-623 К и атмосферном давлении. Синтез бутадиена протекает через стадию образования кротонового альдегида:
В годы Второй мировой войны по методу Остромысленского в США выпускалось
60% всего бутадиена, использованного для производства синтетического каучука.
После 1952 г. все заводы, использовавшие этот процесс, были закрыты из-за их нерентабельности.
4.1.3. Получение бутадиена из ацетилена
В Германии часть бутадиена производилась из ацетилена, который получали из карбида кальция. Были разработаны два многостадийных процесса:
— синтез бутадиена через альдоль – этот способ осуществлялся на заводах е фирмы «И.Г. Фарбениндустри»;
— синтез бутадиена через бутиндиол – этот способ был реализован, в частности, на заводе в г. Людвигсгафене фирмой БАСФ.
Синтез бутадиена через альдоль (альдольный метод)
Альдольный метод включает четыре стадии: гидратацию ацетилена до ацетальдегида, конденсацию ацетальдегида в альдоль, гидрирование альдоля до бутиленгликоля, дегидратацию бутиленгликоля в бутадиен.
Гидратация ацетилена в течение ряда лет являлась основным методом получения ацетальдегида, однако в последнее время этот процесс вытесняется методами, базирующимися на более дешевом сырье – этилене.
В промышленности используют метод получения ацетальдегида из ацетилена гидратацией в жидкой фазе в присутствии ртутных катализаторов (реакция Кучерова). Впервые в промышленном масштабе она была реализована в присутствии раствора сульфата двухвалентной ртути в серной кислоте:
СН?СН + H2O СН3СНО DН = 142 кДж/моль
Сульфат ртути образуется непосредственно в реакторе гидратации из металлической ртути. Соль ртути образует с ацетиленом сложные промежуточные соединения, которые разлагаются на ацетальдегид и сульфат ртути. В связи с тем, что катализатор постепенно теряет активность, часть ртути выводится из реактора в виде шлама, а в реактор периодически вводят свежую металлическую ртуть. Синтез осуществляют при температуре
373 К и давлении 0,25 МПа. Выход бутадиена достигает 90-97% от теоретического.
Жидкофазная гидратация ацетилена проводится при 348-368 К в присутствии 10-20% (мас.) серной кислоты и 0,5-1,0% (мас.) ртутного катализатора (в пересчете на HgО).
Высокая токсичность ртути привела к необходимости разработки процесса парофазной гидратации ацетилена над нертутными катализаторами. Наибольшую активность и стабильность проявляет кадмийкальцийфосфатный катализатор. Катализатор представляет собой смесь средних фосфатов кальция и кадмия, которая содержит некоторое количество кислых фосфатов при мольном соотношении (СаО + СdО):Р2О5, равном 2,8. Процесс проводят при 623 К. На поверхности катализатора в ходе процесса накапливаются смолистые вещества. Регенерацию катализатора осуществляют смесью воздуха и водяного пара при 673-703 К.
Конденсация ацетальдегида в альдоль проводится в присутствии 8-12%-ных растворов щелочи при атмосферном давлении и комнатной температуре:
Выход альдоля составляет
50% на пропущенный и 84-88% на превращенный ацетальдегид.
Гидрирование альдоля в бутиленгликоль
проводят при 328-343 К и давлении 30,0 МПа. В качестве катализаторов используют нанесенные на оксид алюминия или оксид кремния металлы: Со, Ni, Cu и другие.
Процесс дегидратации бутиленгликоля с получением бутадиена
осуществляют при 543-553 К и атмосферном давлении в присутствии разбавителя – водяного пара. В качестве катализатора используют кокс или графит, пропитанные фосфорной кислотой. Выход бутадиена на этой стадии
47% за один проход или 97% от теоретического.
Синтез бутадиена через бутиндиол
В годы второй мировой войны в Германии был разработан и реализован в промышленности синтез бутадиена на основе ацетилена через бутиндиол. Бутиндиольный метод включает взаимодействие ацетилена и формальдегида с образованием 2-бутиндиола-1,4 и последующее гидрирование его в бутилендиол и бутандиол; бутандиол дегидрируют в бутадиен.
Основную стадию – конденсацию ацетилена с формальдегидом с образованием 2-бутиндиола-1,4 (метод Реппе) проводят при 373 К и 0,5 МПа.
СН?СН + 2СН2О НОСН2-С?С-СН2ОН DН = 231 кДж/моль
В качестве катализатора используют ацетиленид меди, нанесенный на силикагель. Формальдегид используют в виде 8%-ного водного раствора. Выход бутиндиола достигает по ацетилену около 80% и по формальдегиду около 90%.
Синтез бутиндиола протекает в две стадии.
На первой стадии образуется пропаргиловый спирт, который в присутствии катализатора присоединяет вторую молекулу формальдегида:
На второй стадии бутиндиол гидрируется с образованием бутандиола:
Гидрирование водного раствора бутиндиола проводят при 423-473 К и 30 МПа в присутствии медноникельхромового катализатора (9% меди, 90% никеля, 1% хрома, носитель – силикагель). Селективность образования бутандиола достигает 98%.
На третьей стадии бутандиол подвергают дегидратации с образованием тетрагидрофурана:
Дегидратация осуществляется в жидкой фазе в присутствии кислого катализатора (фосфорная кислота) при
533-548 К и 7,0 МПа.
На заключительной стадии проводят дегидратация тетрагидрофурана с образованием бутадиена:
Процесс проводят при 543-553 К и 0,1 МПа в присутствии в качестве катализатора дигидрофосфата натрия NaН2РО4, нанесенного на кокс или графит.
Метод Реппе в отличие от альдольного способа не получил широкого распространения ввиду сложности технологии.
Синтез бутадиена через димеризацию ацетилена
Этот метод включает димеризацию ацетилена с последующим гидрированием винилацетилена в бутадиен:
метод, несмотря на относительную простоту технологии, не нашел промышленного применения главным образом из-за взрывоопасности реакционных смесей, в состав которых входит ацетилен.
Пиролиз углеводородного сырья
Техническая возможность получения бутадиена пиролизом нефтяных фракций была показана В.Б. Бызовым в России в 1916 г.
При пиролизе любого углеводородного сырья, а особенно легких бензинов, в качестве побочного продукта образуется бутадиен, количество которого зависит от целей и условий проведения процесса. Если целевым продуктом пиролиза является не только этилен, но и пропилен и бутены, то выход бутадиена может достигать 5% (мас.) на пропущенное сырье, а содержание его во фракции С4 может колебаться от 20 до 60% (мас.).
4.1.4. Промышленные способы получения бутадиена
из бутана или бутена-1
Производство бутадиена из углеводородов С4 (н-бутан и н-бутены) методами каталитического дегидрирования является основным направлением в современной технологии получения бутадиена. В промышленности используют различные технологические варианты получения бутадиена дегидрированием углеводородов С4. Применяемые процессы можно условно разделить на следующие группы: дегидрирование бутана в бутены, дегидрирование бутенов; одностадийное дегидрирование бутана в бутадиен.
Характерной особенностью реакций дегидрирования с образованием олефинов является ограничение степени превращения условиями равновесия. Реакции дегидрирования всегда являются эндотермическими и, следовательно, равновесие в сторону образования ненасыщенных углеводородов должно сдвигаться с повышением температуры. Степень превращения углеводородов возрастает с повышением температуры и понижением давления. На практике при температурах выше 773-823 К даже в отсутствие катализаторов предельные углеводороды претерпевают реакции изомеризации, крекинга и др. Поэтому процесс дегидрирования бутана проводят при температурах до 923-973 К, т.е. при температурах более низких, чем термодинамически оптимальные. Применение катализаторов позволяет достигнуть высокой скорости процесса при относительно низкой температуре, когда еще не существенен вклад побочных реакций. Ввиду обратимости реакций дегидрирования –гидрирования и, следовательно, способности катализаторов ускорять обратимые реакции в обоих направлениях, эти реакции катализируются одними и теми же соединениями.
При дегидрировании вследствие отщепления водорода всегда происходит увеличение объема газа и понижение давления благоприятствует повышению степени конверсии. По этой причине процессы дегидрирования проводят при давлении, близком к атмосферному, а в некоторых случаях процесс осуществляют в вакууме.
Иногда вместо применения вакуума предпочтительнее разбавлять реакционную массу газом, инертным в условиях реакции, или паром, что также приводит к снижению парциальных давлений реагентов и возрастанию равновесной степени конверсии. Снижение парциального давления позволяет также понизить температуру реакции и, следовательно, уменьшить образование побочных продуктов.
Важным параметром при проведении реакции дегидрирования является время контакта реакционной смеси с катализатором. Рис. 4.1 иллюстрирует влияние температуры и времени реакции на содержание бутенов.
Рис. 4.1. Зависимость содержания н-бутенов при каталитическом дегидрировании н-бутана от температуры и времени реакции
Максимальный выход олефинов не соответствует рассчитанной равновесной концентрации при соответствующей температуре: он всегда значительно ниже. С увеличением времени реакции выше оптимального выход олефинов уменьшается, так как увеличивается вклад побочных реакций.
Работы по каталитическому дегидрированию н-бутана по двухстадийному варианту: н-бутан ® н-бутен ® бутадиен были начаты в США в 1920-х годах. В Советском Союзе фундаментальные исследования в этой области проводили С.В. Лебедев, Н.И. Шуйкин, А.А. Баландин, Б.А. Казанский и др.
Дегидрирование углеводородов С4-С5 в олефины и диены
Дегидрирование бутана в бутен осуществляется в «кипящем слое» алюмохромового катализатора при температуре в реакторе 838-853 К.
Бутены выделяют экстрактивной ректификацией водным ацетоном или диметилформамидом (ДМФА). Бутены дегидрируют в реакторах с неподвижным слоем катализатора и с подводом тепла за счет разбавления исходной смеси водяным паром при 853-893 К на хромкальцийникельфосфатном катализаторе. Общий выход бутадиена – 60% (мас.) от теоретического.
В промышленности США и Западной Европы используется также одностадийный способ дегидрирования бутана до бутадиена по Гудри. По этому способу дегидрированию подвергают бутан-бутеновую смесь в соотношении 60:40 при 873 К и
1,225 кПа в периодических реакторах с неподвижным слоем алюмохромового катализатора без внешнего теплообмена. Продолжительность процесса 7-10 мин. Регенерацию катализатора проводят выжиганием отложившегося кокса в потоке воздуха. Из продуктов дегидрирования выделяют бутадиен и бутан-бутеновую фракцию, которую направляет далее в рецикл с добавлением в нее свежего бутана. Выход бутадиена составляет до 14% (мас.) на пропущенный и до 54% (мас.) в расчете на превращенный бутан.
Оптимальная глубина дегидрирования н-бутана (
30% за проход) достигается при температуре выше 773 К, а для дегидрирования бутенов при атмосферном давлении равновесная глубина превращения даже при температуре 903 К не превышает 30%, что не приемлемо для промышленности. Увеличить выход целевого продукта можно путем снижения парциального давления, например при проведении реакции при 823 К и парциальном давлении 10,1 кПа, что соответствует разбавлению бутена в соотношении 1:10.
Как правило, катализаторы дегидрирования н-бутана состоят из оксида хрома на оксиде алюминия. В качестве промотирующих добавок используют оксиды калия, кремния или бериллия. Общее содержание добавляемых оксидов составляет 1-5%. Промотирующее влияние оказывают также некоторые оксиды лантанидов, например Pr6O11 или Nd2O3. В алюмохромовых катализаторах, получаемых пропиткой g-А12О3 оксид хрома находится в виде a-Сr2О3, имеющего корундовую структуру, которая образуется при нагревании СrО3 в присутствии кислорода воздуха.
окислительное дегидрирование бутана и бутиленов
отличительная особенность окислительного дегидрирования заключается в том, что равновесие реакции практически полностью смещено вправо. Это позволяет проводить процесс при относительно низких температурах – 753 К. промышленное значение имеют следующие способы окислительного дегидрирования бутана и изопентана до бутадиена и изопрена: дегидрирование в присутствии иода, кислорода и поглотителей иодида водорода (иодное дегидрирование); каталитическое дегидрирование в присутствии кислорода.
Иодное дегидрирование. Наибольший интерес представляет процесс иодного дегидрирования н-бутана:
При этом очень важно создание надежных методов рекуперации (возвращене в технологический цикл в качестве реагента) и рециркуляции иода, стоимость которого в десятки раз превышает стоимость мономеров. Эффективное решение этой задачи состоит в практически необратимом связывании НI в зоне реакции оксидами или гидроксидами щелочных металлов:
В качестве поглотителя могут быть использованы оксиды марганца.
Регенерация иода осуществляется кислородом:
Из побочных реакций следует отметить образование иодидов и крекинг углеводородов.
При иодном дегидрировании равновесные глубины превращения н-бутана значительно выше, чем при обычном дегидрировании. Так, при 823 К и одном и том же начальном парциальном давлении
30,3 кПа (при иодном дегидрировании такое парциальное давление создается при мольном соотношении С4Н10:I2=1:2) равновесные расчетные составы имеют следующие значения:
При обычном дегидрировании, % (мол.) 28 64 8
При иодном дегидрировании, % (мол.) 9,5 63 27,5
Таким образом, при иодном дегидрировании, т.е. при связывании водорода в виде HI, равновесные выходы бутадиена существенно увеличиваются по сравнению с выходами при обычном дегидрировании, а равновесные выходы бутенов в обоих случаях сопоставимы. Увеличение соотношения I2:С4Н10 приводит к резкому повышению равновесного выхода бутадиена: при увеличении этого соотношения от 1 до 4 при 823 К выход возрастает с 13 до 77%. Влияние остальных параметров аналогично их влиянию при обычном дегидрировании: равновесные выходы бутадиена увеличиваются с повышением температуры и с уменьшением парциального давления бутана.
Окислительное дегидрирование н-бутана можно осуществлять и в присутствии катализаторов, например молибдата кобальта. Однако предложенные на сегодня катализаторы пока недостаточно эффективны.
Каталитическое дегидрирование. Реакция окислительного дегидрирования бутенов в бутадиен практически необратима, и поэтому можно достигнуть практически полного превращения бутенов:
Основной побочной реакцией является предельное окисление (горение) углеводородов с образованием СО2 и Н2О. В процессе окислительного дегидрирования бутенов протекают побочные реакции, приводящие к образованию кислородсодержащих соединений: фурана, формальдегида, ацетальдегида, акролеина, метакролеинов, муравьиной, уксусной, пропионовой и малеиновой кислот. Реакцию осуществляют при 723-773 К.
Окислительное дегидрирование олефинов до диолефинов можно проводить в присутствии например кальцийникельфосфатных или оксидных катализаторов или тех же катализаторов, что и при обычном дегидрировании, в качестве которых используют вольфрамат висмута и фосфат висмута, смесь оксидов олова и сурьмы, висмутмолибденовые и другие.
Одностадийное дегидирование бутана в бутадиен
Одностадийный процесс дегидрирования алканов:
имеет очевидные преимущества перед двухстадийным процессом ввиду отсутствия необходимости разделения газовых смесей после каждой стадии и более низких энерго- и капитальных затрат. На рис. 4.2 представлена зависимость состава равновесной смеси при дегидрировании бутана в бутены и бутадиен от температуры и давления.
Рис. 4.2. Зависимость состава равновесной смеси при дегидрировании бутана в бутены и бутадиен от температуры и давления
Сплошные линии – 0,1 МПа, штриховые – 0,01 МПа.
1 – бутан; 2 – бутены; 3 – бутадиен
Термодинамические расчеты показывают, что равновесный выход диена существенно возрастает с повышением температуры и с уменьшением парциального давления алкана. Поскольку повышение температуры связано с потерей селективности реакции, одностадийное получение диенов из алканов было реализовано в условиях вакуумного дегидрирования. В одностадийном процессе дегидрирования используют алюмохромовые катализаторы, содержащие 18-30% оксида хрома.
Фирма «Гудри» (США) впервые реализовала процесс получения бутадиена из бутана в одну стадию (аналогично процессу получения изопрена из изопентана). В присутствии алюмохромового катализатора протекают побочные превращения бутана, бутенов и бутадиена. Применение алюмохромового катализатора исключает использование водяного пара в качестве разбавителя. Принципиальная технологическая схема этого процесса, который проводят под вакуумом (0,015-0,020 МПа) в стационарном слое катализатора, приведена на рис. 4.3.
Рис. 4.3. Принципиальная технологическая схема процесса одностадийного дегидрирования бутана
1 – испаритель; 2 – трубчатая печь; 3 – топка; 4 – реакторы; 5 – котел-утилизатор; 6 – скруббер; 7 – холодильник; 8 – турбокомпрессор; 9 – абсорбер; 10 – десорбер; 11, 12 – ректификационные колонны; 13 – узел экстрактивной ректификации.
Потоки: I – свежий бутан; II – возвратная бутан-бутиленовая фракция; III – воздух; IV – топливный газ; V – линия вакуума; VI – сброс в атмосферу; VII – отдувкн в топливную сеть; VIII – углеводороды С3 на сжигание; IX – фракция С4-С12; X – бутадиен
Сырье – смесь бутана и возвратной бутан-бутеновой фракции – испаряется в испарителе 1 и при 313 К поступает в трубчатую печь 2. Перегретые пары сырья со скоростью 240 ч -1 направляют в реактор 4, где при 863-898 К и остаточном давлении 11,3-22,7 кПа происходит процесс дегидрирования. Реактор представляет собой горизонтальный цилиндрический аппарат диаметром 6 м и длиной 12 м. Полный рабочий цикл продолжается 21 мин. 30 с., дегидрирование – 8 мин. 15 с., продувка паром, опорожнение реактора – 2 мин. 35 с. Из реакторного блока контактный газ подают в орошаемый охлаждающим маслом скруббер 6, в котором его охлаждают до 328 К, и затем в блок выделения бутадиена.
Конверсия бутана в одностадийном процессе составляет
20%, а выход бутадиена 50-55% на превращенное сырье. Контактный газ содержит 37-39% бутана, 23-25% бутенов, 12-13% бутадиена.
Основные параметры процессов дегидрирования алкенов С4-С5 приведены ниже:
Параметр
бутенов
изопентенов
Выделение бутадиена
Во всех процессах бутадиен получается в смеси с другими углеводородами, близкими к нему по летучести. Выделение из таких смесей концентрированного бутадиена, используемого для производства каучука, является весьма сложной задачей. Для стереоспецифической полимеризации необходим бутадиен, тщательно очищенный от примесей других углеводородов диенового и ацетиленового ряда и соединений неуглеводородного характера. В России для стереоспецифической полимеризации применяется бутадиен с концентрацией не ниже 99% (масс.) и содержанием примесей в нем не выше (% мас.):
(в расчете на азот)
В табл. 4.2 приведен углеводородный состав продуктов дегидрирования бутана, бутенов и фракции С4 пиролиза бензина.
Таблица 4.2. Углеводородный состав продуктов дегидрирования бутана, бутенов и фракции С4 пиролиза бензина ( в % (мас.))
| Компонент | Дегидрирование бутана | Дегидрирование бутенов | Пиролиз бензина | ||||
| обычное на алюмохромовом катализаторе | вакуумное на алюмохромовом катализаторе | окисли-тельное с иодом и акцептором | обычное на кальций-никель-фосфатном катализаторе | окислительное на фосфор-висмут-молибденовом катализаторе | средний при 1033 К | жесткий при 1123 К | |
| С1-С3 | 9,48 | 4,75 | 9,20 | 2,45 | 0,05 | 1,1 | 0,31 |
| Изобутан | 22,45 | 2,05 | 0,10 | 0,40 | 0,25 | 2,5 | 6,68 |
| н-Бутан | 50,60 | 47,35 | 14,50 | 7,30 | 8,50 | 9,3 | |
| Изобутен | 1,90 | 5,5 | 1,50 | 8,55 | — | 29,0 | 23,98 |
| Бутен-1 | 10,40 | 9,90 | 2,90 | 18,30 | 4,80 | 14,0 | 6,27 |
| Бутен-2 | 23,30 | 15,75 | 7,80 | 29,32 | 16,80 | 10,0 | 7,75 |
| Бутадиен | 1,50 | 14,00 | 63,10 | 32,95 | 68,80 | 32,7 | 50,08 |
| С5 | 0,31 | 0,63 | 0,70 | 0,50 | 0,74 | 0,5 | 0,6 |
| Вредные примеси | |||||||
| Пропин | 0,002 | 0,005 | 0,20 | 0,013 | 0,003 | 0,24 | 0,86 |
| Бутин-1 | 0,005 | 0,005 | 0,07 | 0,040 | — | 0,11 | — |
| Аллен | — | 0,003 | 0,04 | 0,015 | 0,008 | 0,17 | — |
| Метилаллен | 0,003 | 0,025 | 0,09 | 0,09 | — | 0,04 | — |
| Циклопентадиен | 0,04 | 0,02 | 0,2 | 0,1 | 0,03 | 0,03 | — |
Для выделения бутадиена из различных бутадиенсодержащих фракций в промышленности используют два метода: экстрактивную ректификацию с различными полярными агентами и хемосорбцию медноаммиачноацетатными растворами.
При экстрактивной ректификации в качестве разделяющих агентов используют N-метилпирролидон, диметилформамид и диметилацетамид.
Хемосорбция основана на образовании комплексных соединений ненасыщнных углеводородов (преимущественно диенов) с солями металлов переменной валентности. Промышленное применение для выделения бутадиена хемосорбцией нашел способ с использованием водноаммиачного раствора ацетата одновалентной меди. Взаимодействие бутадиена и бутенов с медно-аммиачным раствором происходит с образованием комплексов:
Процесс связывания бутадиена носит характер вытеснения молекулы аммиака из внутренней координационной сферы центрального атома молекулой углеводорода.
Технологические схемы установок хемосорбции включают три основные стадии:
— поглощение, на которой бутадиен вместе с небольшим количеством других ненасыщенных углеводородов растворяется в экстрагенте;
— обогащение, при котором бутены удаляются из раствора;
— десорбция, при которой бутадиен практически полностью отгоняется из раствора.
Обогащение бутадиена осуществляется за счет подачи части десорбированного бутадиена противотоком к насыщенному хемосорбенту, в результате чего поглощенные бутилены замещаются в комплексе на бутадиен.
Десорбция бутадиена может осуществляться за счет разрушения комплекса нагреванием или уменьшением парциального давления бутадиена в системе путем создания вакуума или продувкой хемосорбента инертным газом или паром
This entry was posted on Понедельник, Январь 10th, 2011 at 10:02 дп and is filed under Без рубрики. You can follow any responses to this entry through the RSS 2.0 feed. Both comments and pings are currently closed.
Comments are closed.
Copyright © 2008 — Основы химии и технологии мономеров — Powered by WordPress — Designed By Free WordPress Themes / Coded: Auto Loan Quote
Источник