- Способ применения ароматических углеводородов
- Ароматические углеводороды (Арены)
- Формула и соединения
- Строение
- Изомеры
- Свойства
- Физические
- Химические
- Получение
- Применение
- Распределение по фракциям нефти
- Гибридные соединения
- Cодержание аренов в нефтях России
- Арены — классификация, виды и особенности строения ароматических углеводородов
- Особенности структуры
- Физические и химические свойства
- Классификация и номенклатура
- Области применения
- Влияние на человека
Способ применения ароматических углеводородов
Ароматические углеводороды – важнейшее сырье для синтеза ценных веществ.
Бензол С6Н6 — хороший растворитель. Бензол в качестве добавки улучшает качество моторного топлива.
Он также используется как исходный продукт для получения различных ароматических соединений – нитробензола, хлорбензола, анилина, фенола, стирола, из которых в свою очередь получают лекарства, пластмассы, красители, ядохимикаты и многие другие органические вещества.
Толуол С6Н5-СН3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ).
Ксилолы С6Н4(СН3)2 в виде смеси трех изомеров (орто- , мета- и пара-ксилолов) – технический ксилол – применяется как растворитель и исходный продукт для синтеза многих органических соединений.
Изопропилбензол (кумол) С6Н4-СН(СН3)2 – исходное вещество для получения фенола и ацетона.
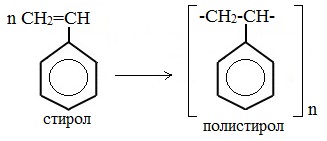
Винилбензол (стирол) C6H5-CН=СН2 используется для получения ценного полимерного материала полистирола, т.к. очень легко полимеризуется.
Особенно ценна его способность к совместной полимеризации с бутадиеном, в результате которой получают различные сорта бутадиенстирольных каучуков (жаро- и морозоустойчивые, прочные на износ, высокоэластичные, устойчивые к маслам). Из них изготовляют шины, ленты для транспортеров, эскалаторов, облегченную микропористую подошву.
Источник
Ароматические углеводороды (Арены)
Формула и соединения
АРЕНЫ (АрУ)– карбоциклические соединения, содержащие в молекуле специфическую систему чередующихся двойных и одинарных связей (сопряженных π-связей).
Общая формула CnH2n-6
Ароматические углеводороды (Арены) являются ненасыщенными циклическими соединениями и представлены в нефтях следующими углеводородами:
- моноциклическими (бензольными) – СnНn;
- бициклическими (нафталиновыми) – СnНn-2;
- трициклическими (антраценовыми) – СnНn-4
- тетрациклическими (пиреновыми) – СnНn-6.
В основном все они представлены алкилпроизводными изомерами и содержатся во фракциях нефти в соответствии с их температурами кипения.
В среднем для нефтей характерно следующее соотношение этих групп углеводородов:
- бензольные – 67%,
- нафталиновые – 18%,
- фенантреновые – 8%,
- пиреновые – 5%,
- прочие – 2%.
Строение
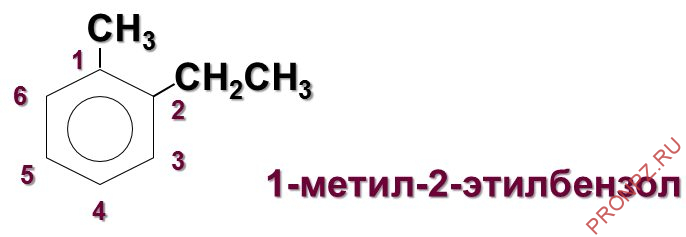
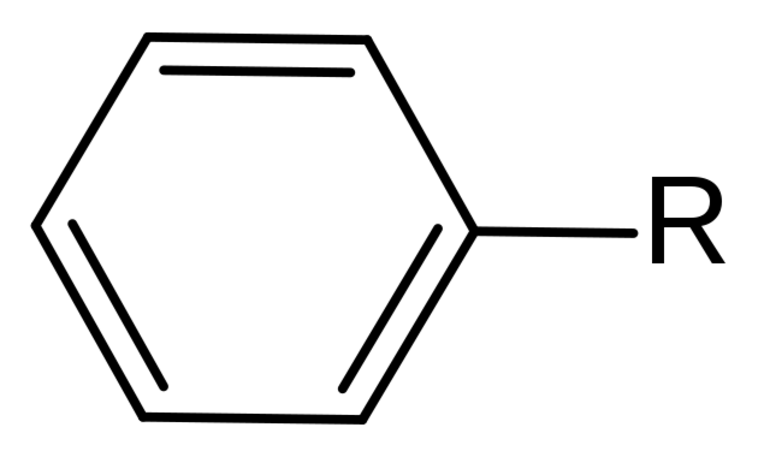
Основой названия ароматического углеводорода с небольшим заместителем является бензол. Атомы в ароматическом кольце нумеруют, начиная от старшего заместителя к младшему по кратчайшему пути.
Строение аренонов представлено бензолом и его гомологами – продуктами замещения одного или более атомов водорода в молекуле бензола на углеводородные остатки.
Гомологи – вещества, относящиеся к одному классу соединений, имеющие сходные химические свойства и отличающиеся на одну или несколько СН2 групп.
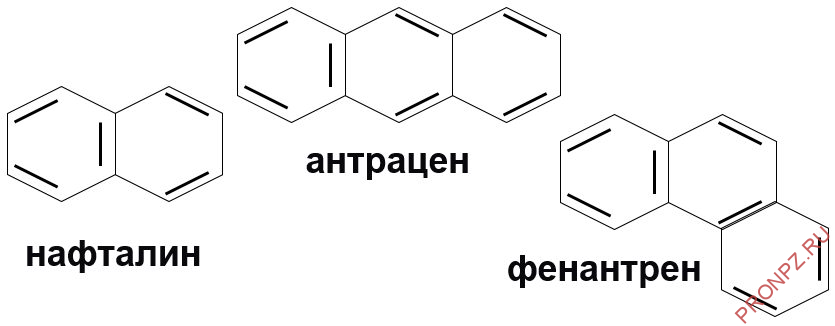
Существуют также соединения, молекулы которых содержат несколько циклических структур:
Изомеры
Для гомологов бензола характерна изомерия положения нескольких заместителей.
Свойства
Физические
К характерным свойствам следует отнести:
- высокую плотность (880 – 900 кг/м 3 ),
- большой показатель преломления (1,5 – 1,55)
- минимальное соотношение Н:С (5 – 8 %), т.е. низкие энергетические свойства.
Физические свойства ароматических углеводородов существенно зависят от числа, места и молекулярной массы боковых заместителей и числа циклов. Такое резкое отличие их свойств часто используют для разделения этих углеводородов физическими методами.
Бензол и его простейшие гомологи в обычных условиях – токсичные жидкости с характерным запахом. Они плохо растворяются в воде, но хорошо в органических растворителях.
Первые члены гомологического ряда бензола (например, толуол, этилбензол и др.) – бесцветные жидкости со специфическим запахом. Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ.
Все арены горят коптящим пламенем ввиду высокого содержания углерода в их молекулах.
Химические
Для аренов наиболее характерны реакции электрофильного замещения –
- галогенирование,
- нитрование,
- сульфирование,
- алкилирование (получение хлорбензола, нитробензола, этилбензола др. соединений).
При высоких парциальных давлениях водорода в присутствии катализаторов арены насыщаются до нафтенов.
Получение
Ароматические углеводороды нефтяного происхождения (содержащиеся в природной нефти и образующиеся во вторичных процессах термокаталитической переработки фракций нефти) являются основным исходным сырьем для огромного числа нефтехимических производств получения ценных продуктов.
Из общего производства аренов в мире 29 млн. т/г. (2005-е годы) 87-92% вырабатывалось из нефти.
Применение
Бензол в основном идет на производство этилбензола, из которого каталитическим дегидрированием при 600 °С получают стирол – исходный мономер для производства каучуков и ценных полимеров:
Для производства других ценных продуктов – фенола и ацетона пользуют кумол (изопропилбензол), который окисляют в пероксид, разложением которого кислотой получают фенол и ацетон.
Из кумола каталитическим дегидрированием получают такой ценный мономер для производства каучуков, как α-метилстирол.
Значение АрУ в нефтепродуктах различно. Так, в бензинах присутствие (до 30% масс.) желательно и необходимо, так как придает бензинам хорошие моторные свойства – повышает детонационную стойкость. С этой целью в товарные бензины часто добавляют толуол или ксилолы.
В авиационных керосинах содержание АрУ ограничивают (в зависимости от марки топлива) 10-20% масс. из-за их низкой теплоты сгорания и способности давать нагар в двигателе сгорании. Допустимое количество АрУ обусловлено необходимостью иметь авиакеросины с повышенной плотностью.
В дизельных топливах содержание АрУ ограничивают из-за их нагарообразующих свойств и плохой воспламеняемости является очень важной характеристикой этих топлив. В маслах высокомолекулярные и алкилсодержащие АрУ с боковыми цепями изомерного строения – нежелательный компонент, так как они ухудшают вязкостно-температурную характеристику масел (индекс вязкости) и обусловливают образование лаково-смолистых отложений на трущихся поверхностях. АрУ удаляют из масел в процессе очистки масляных дистиллятов и деасфальтизатов. Остаются в маслах лишь АрУ с длинными боковыми цепями и “гибридные” полициклические углеводороды, в которых преобладают насыщенные циклы, поскольку свойства углеводородов приближаются соответственно к свойствам алканов и цикланов.
Распределение по фракциям нефти
Распределение АрУ по фракциям нефтей зависит от степени ароматизированности нефти, выражающейся в ее плотности.
- В легких нефтях, богатых алканами, АрУ представлены в основном легкими моно- и бициклическими, и их общее содержание максимально в начальных фракциях и снижается к более высококипящим.
- В нефтях средней плотности, богатых нафтеновыми углеводородами, распределение АрУ более равномерно, а в тяжелых смолистых нефтях картина обратная: содержание АрУ в низкокипящих фракциях невелико и нарастает в высококипящих.
- В бензиновых фракциях нефти (30-200 °С) содержатся в основном бензольные АрУ (С6-C9).
- В керосиновых фракциях (150-300 °С) кроме бензольных присутствуют нафталиновые АрУ (С10-С16), а в тяжелых дистиллятных фракциях (350-500 °С) – главным образом нафталиновые и антраценовые.
- В остатках нефти (выше 500 °С) концентрируются полициклические АрУ с числом циклов от трех до семи, причем “чистые” АрУ здесь уступают место “гибридным”, сочетающим в себе насыщенные и ненасыщенные циклы.
Простейшие из них (индан, тетралин, флуорен и другие би- и трициклические соединения) содержатся в керосино-газойлевых фракциях нефти (150 – 350 о С).
Гибридные соединения
В «гибридных» соединениях ароматические циклы имеют обычно метильные заместители, а нафтеновые – более длинные боковые цепи.
В остальных фракциях нефти (выше 500 о С) и особенно в составе смол и асфальтенов концентрируются полициклические АрУ с числом циклов 4 и более, такие как пирен, хризен, бенз-α-пирен и другие, являющиеся канцерогенными веществами.
Cодержание аренов в нефтях России
Общее содержание аренов в нефтях России (с учетом «гибридных») составляет 35 – 40 % – для тяжелых нафтено – ароматических нефтей и около 20 % – для высокопарафинистых.
Источник
Арены — классификация, виды и особенности строения ароматических углеводородов
Особенности структуры
Термин «ароматический» присвоен классу до того, как был обнаружен физический механизм, определяющий ароматичность. Его придумали просто потому, что многие арены имеют сладкий запах. Бензольным кольцом называют конфигурацию из шести атомов углерода. Оно присуще почти всем представителям класса, которые могут быть моноциклическими и полициклическими.
Некоторые, не основанные на бензоле соединения, называемые гетероаренами, следуют правилу Хюккеля, также называются ароматическими. В них по меньшей мере один атом углерода заменён одним из гетероатомов кислорода, азотом или серой. Примером таких веществ является гетероциклическое соединение фуран с пятичленным кольцом и атомом кислорода. А также пиридин с шестичленным кольцом и азотом.
Простейшим представителем гомологического ряда аренов является бензол (С6Н6). Его структурный вид — это плоская молекула в форме правильного шестиугольника. В ней все углерод-углеродные связи имеют одинаковую длину. Молекулярное строение включает 6 p-электронов делокализованных выше и ниже плоскости кольца. Такая особенность делает бензол очень стабильным. Следующий — это метилбензол (толуол), у которого один из атомов водорода присоединён к кольцу и заменён метильной группой — С6Н5СР3. К характерным свойствам ароматических углеводородов относятся:
- обладают ароматичностью;
- все соединения имеют изомерию боковых цепей;
- имеют высокое соотношение углерода и водорода;
- легко горят;
- подвергаются реакциям электрофильного и нуклеофильного ароматического замещения.
Реакция, которая образует соединения арена из полностью или частично ненасыщенного предшественника, называется просто — ароматизацией. Существует много лабораторных способов синтеза аренов. Например, ароматизация циклогексанов и других алифатических колец. В таких реакциях реагенты представляют собой катализаторы, используемые в гидрировании, такие как платина, палладий и никель. Для получения ареновых соединений в качестве сырья используют нефть и нефтепродукты.
Физические и химические свойства
Летучие ароматические углеводороды легко воспламеняются и горят ярким, коптящим пламенем, оставляя мало углеродного остатка. Помимо горения, выделяют следующие физические свойства аренов:
- Точка кипения. Поскольку на бензольной молекуле нет постоянного диполя, единственное притяжение между ними — дисперсионные силы Ван-дер-Ваальса. Бензол кипит при 80 °C, что значительно выше, чем у других углеводородов схожего молекулярного размера (например, пентана и гексана). Метилбензол кипит при 111 °C. Это большая молекула и она имеет постоянный диполь.
- Точка плавления. Бензол плавится при 5,5 °C, толуол при -95 °C. Молекулы должны эффективно упаковываться в твёрдом теле, если они хотят наилучшим образом использовать свои молекулярные силы. Метильная группа, торчащая в метилбензоле, имеет тенденцию нарушать плотность упаковки. Поэтому температура плавления у него ниже.
- Растворимость в воде. Арены таким свойством не обладают. Бензол довольно большой по сравнению с водной молекулой. Надо сказать, что для растворения бензольному соединению пришлось бы разорвать множество существующих водородных связей между частицами воды. При этом нужно ещё сломать дисперсионные силы. Оба этих занятия стоят большого количества энергии.
Основными типами химических реакций с участием ароматических колец являются присоединение, окисление и замещение. Последняя — самая распространённая. Химические свойства аренов:
- Ароматическое замещение. Один заместитель в ареновом кольце, обычно водород, заменяется другим. Двумя основными типами являются электрофильное и нуклеофильное ароматическое замещение. А также нитрирование, например, салициловой кислотой, алкилирование и другие.
- Сочетание. Здесь металл катализирует связь между двумя фрагментами формального радикала. Обычно такие реакции с аренами приводят к образованию новых углерод-углеродных связей. Например, алкиларенов, виниларенов, биарилов, анилинов (углерод-азотные связи) или арилоксисоединений (углерод-кислород).
- Гидрирование. Эта реакция создаёт насыщенные кольца. Например, соединение резорцин, гидрированное никелем Ренея в присутствии одного гидроксида натрия, образует энолы, которые алкилируются йодистым метилом до 2-метил-1,3-циклогександиона.
- Присоединение. Реакция циклоприсоединения не распространена.
- Деароматизация. В органической химии представляет собой реакцию, при которой продукты утрачивают ароматичность. Здесь арены выступают реагентами.
Ароматические соединения обладают высокими показателями поглощения и преломления УФ и видимой части спектра.
Классификация и номенклатура
Многие производные бензола приобрели довольно тривиальные названия. Например, имя для C6H5 — фенил. Более сложные кольцевые системы, имеющие два и более бензольных кольца, имеют несистематические наименования и нелогичные системы нумерации. Они описаны как многоядерные ароматические углеводороды.
Три наиболее важных — нафталин, антрацен и фенантрен. Названия, которые были даны этим и другим сложным типам соединений, по большей части неинформативны в отношении их структур. Классификацию аренов можно представить в виде таблицы:
| Системы π-связи, кол-во π-электронов | Представители | Пояснения |
|---|---|---|
| 2 | производные катиона (перхлорат циклопропенилия) | |
| 6 | бензол и гомологичные соединения | |
| дианион циклобутадиена | ||
| пирол, фуран и др. | ||
| циклопентадиен-анион | ||
| 10 | нафталин | конденсированные бензольные кольца, широко встречающиеся в природе |
| азулен | входит в состав эфирных масел | |
| азонин | ||
| индол | распространены в природе | |
| пурин | содержат атомы азота | |
| 14 | фенантрен | такие соединения называют полиценами |
| [14]-аннулен | ||
| от 15 и более | кекулен | |
| коронен | антиароматичен, его π-электронная система 18 внешних и 6 внутренних электронов | |
| 18-аннулен |
Если бензольное кольцо не может расположиться в плоскости, один его атом выводится из неё. При этом он сохраняет sp3-гибридизацию, а также не принимает участия в сопряжении. Такие соединения классифицируются как гомоароматичные.
Типичный представитель — трисгомоциклопропенильный катион. Ещё один вид — спироароматичные системы, которые подчиняются правилу Хюккеля. Примером служит [4,2]спирарен.
Области применения
Многие, возможно, и не слышали о бензоле и его производных, но скорее всего все сталкивались с продуктами, производимыми с ним каждый день. Пластмассы, моющие средства, пестициды и даже красители, используемые для окрашивания одежды, пищевых и фармацевтических продуктов, изготавливаются с применением бензольных соединений.
Молекулы производных бензола довольно универсальны и сегодня широко используются в промышленности. Первым стоит выделить этилбензол. Заменяет один из атомов водорода, присоединённых к кольцу, этильной группой. Естественным образом содержится в каменноугольной смоле и нефти. Из него производят чернила, пестициды, краски и другие химикаты. Однако основное применение этилбензола заключается в производстве стирола, а затем полистирола:
- Стирол. Используется для изготовления латекса и синтетического каучука. Можно посмотреть на нижнюю часть придверного коврика, который обычно есть в каждом доме. Его резиновая подложка, скорее всего, сделана из стирол-бутадиенового каучука — типа стирола. Он также используется для конвейерных лент, напольных покрытий, изоляции проводов и даже для резиновых обувных подошв.
- Полистирол. Изготовлен из стирола. Является распространённым материалом для производства упаковки для пищевых продуктов, одноразовых стаканчиков, контейнеров.
В какой-то момент большинство людей принимает аспирин для лечения головной боли, ушибов или снижения температуры. Этот препарат на самом деле сделан с применением фенола, ещё одним производным бензола. Он также используется в изготовлении пластмасс, взрывчатых веществ и красителей, используемых для одежды и пищевых продуктов (азокраситель). Сам фенол часто применяется в качестве антисептика и дезинфицирующего средства в бытовых чистящих составах, конечно, в низких концентрациях. Кстати, это соединение было одним из первых антисептических средств для, применённых в хирургии Джозефом Листером.
Ещё одним универсальным производным бензола является анилин. Используется для производства многих продуктов, как и предыдущие представители. Например, входит в состав ацетаминофена, или тиленола, другого безрецептурного обезболивающего средства. Применяется в процессах деревообработки. Все яркие элементы мебели изготовлены с его участием.
Толуол в настоящее время часто используется в качестве заменителя бензола, например, как присадка к топливу. Свойства обоих растворителей похожи, но этот менее токсичен и имеет более широкий диапазон содержания жидкости. Бензол также используют в качестве бензиновой добавки, он повышает октановое число и снижает детонацию.
Все ароматические соединения проявляют уникальные химические и физические свойства благодаря своей дополнительной стабильности. Применение аренов довольно масштабно и распространяется на многие отрасли промышленности. Например, фенантрен является промежуточным продуктом различных синтетических процессов для производства красителей, взрывчатых веществ и лекарств. Катехин (пирокатехол) — один из ключевых компонентов фотографического проявителя.
Влияние на человека
Ароматические углеводороды выделяются главным образом в результате антропогенных процессов, например, из-за неполного сгорания органического топлива. Их нахождению в окружающей среде способствуют такие природные явления, как извержение вулканов и лесные пожары. Арены присутствуют в окружающей среде в виде частиц или в газообразной форме, в зависимости от их летучести. В атмосфере эти соединения реагируют с другими загрязнителями, такими как диоксид серы, оксид азота и озон.
На людей воздействует смесь ароматических углеводородов в газообразной или дисперсной формах. Некоторые арены считаются канцерогенами, вдыхание которых несёт потенциальный риск для здоровья. Это связанно с возникновением рака лёгких. Основными источниками токсичных выбросов являются:
- Отопление и приготовление пищи путём сжигания и пиролиза угля, нефти, газа, мусора и древесины.
- Выбросы от промышленной деятельности. Например, при производстве первичного алюминия и кокса, резиновых шин и цемента, битума и асфальта, тепла и электроэнергии, сжигании отходов.
- Мобильные источники. Выхлопные газы от транспортных средств, включая автомобили, железные дороги, корабли, самолёты и другие.
- Сельское хозяйство. Ароматические соединения образуются в результате открытого сжигания биомассы.
Ароматические углеводороды могут попасть в организм человека в процессе дыхания, при употреблении пищи или воды, а также через кожные покровы. Они транспортируются во все органы и ткани, которые содержат жировые клетки.
При многократном длительном воздействии арены накапливаются в печени, почках, селезёнке и даже яичниках, вызывая рост раковых клеток. Помимо этого, соединения могут способствовать развитию сердечно-сосудистых заболеваний.
Источник