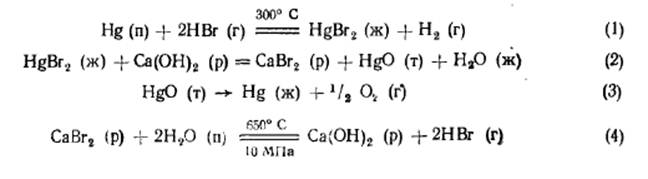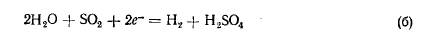Аммиак: получение и свойства
Аммиак
Строение молекулы и физические свойства
В молекуле аммиака NH3 атом азота соединен тремя одинарными ковалентными полярными связями с атомами водорода:
Геометрическая форма молекулы аммиака — правильная треугольная пирамида. Валентный угол H-N-H составляет 107,3 о :
У атома азота в аммиаке на внешнем энергетическом уровне остается одна неподеленная электронная пара. Эта электронная пара оказывает значительное влиение на свойства аммиака, а также на его структуру. Электронная структура аммиака — тетраэдр , с атомом азота в центре:
Аммиак – бесцветный газ с резким характерным запахом. Ядовит. Весит меньше воздуха. Связь N-H — сильно полярная, поэтому между молекулами аммиака в жидкой фазе возникают водородные связи. При этом аммиак очень хорошо растворим в воде, т.к. молекулы аммиака образуют водородные связи с молекулами воды.
Способы получения аммиака
В лаборатории аммиак получают при взаимодействии солей аммония с щелочами. Поск ольку аммиак очень хорошо растворим в воде, для получения чистого аммиака используют твердые вещества.
Например , аммиак можно получить нагреванием смеси хлорида аммония и гидроксида кальция. При нагревании смеси происходит образование соли, аммиака и воды:
Тщательно растирают ступкой смесь соли и основания и нагревают смесь. Выделяющийся газ собирают в пробирку (аммиак — легкий газ и пробирку нужно перевернуть вверх дном). Влажная лакмусовая бумажка синеет в присутствии аммиака.
Видеоопыт получения аммиака из хлорида аммония и гидроксида кальция можно посмотреть здесь.
Еще один лабораторный способ получения аммиака – гидролиз нитридов.
Например , гидролиз нитрида кальция:
В промышленности аммиак получают с помощью процесса Габера: прямым синтезом из водорода и азота.
Процесс проводят при температуре 500-550 о С и в присутствии катализатора. Для синтеза аммиака применяют давления 15-30 МПа. В качестве катализатора используют губчатое железо с добавками оксидов алюминия, калия, кальция, кремния. Для полного использования исходных веществ применяют метод циркуляции непровзаимодействовавших реагентов: не вступившие в реакцию азот и водород вновь возвращают в реактор.
Более подробно про технологию производства аммиака можно прочитать здесь.
Химические свойства аммиака
1. В водном растворе аммиак проявляет основные свойства (за счет неподеленной электронной пары). Принимая протон (ион H + ), он превращается в ион аммония. Реакция может протекать и в водном растворе, и в газовой фазе:
Таким образом, среда водного раствора аммиака – щелочная. Однако аммиак – слабое основание . При 20 градусах один объем воды поглощает до 700 объемов аммиака.
Видеоопыт растворения аммиака в воде можно посмотреть здесь.
2. Как основание, аммиак взаимодействует с кислотами в растворе и в газовой фазе с образованием солей аммония.
Например , аммиак реагирует с серной кислотой с образованием либо кислой соли – гидросульфата аммония (при избытке кислоты), либо средней соли – сульфата аммония (при избытке аммиака):
Еще один пример : аммиак взаимодействует с водным раствором углекислого газа с образованием карбонатов или гидрокарбонатов аммония:
Видеоопыт взаимодействия аммиака с концентрированными кислотами – азотной, серной и и соляной можно посмотреть здесь.
В газовой фазе аммиак реагирует с летучим хлороводородом. При этом образуется густой белый дым – это выделяется хлорид аммония.
NH3 + HCl → NH4Cl
Видеоопыт взаимодействия аммиака с хлороводородом в газовой фазе (дым без огня) можно посмотреть здесь.
3. В качестве основания, водный раствор аммиака реагирует с растворами солей тяжелых металлов , образуя нерастворимые гидроксиды.
Например , водный раствор аммиака реагирует с сульфатом железа (II) с образованием сульфата аммония и гидроксида железа (II):
4. Соли и гидроксиды меди, никеля, серебра растворяются в избытке аммиака, образуя комплексные соединения – аминокомплексы.
Например , хлорид меди (II) реагирует с избытком аммиака с образованием хлорида тетрамминомеди (II):
Гидроксид меди (II) растворяется в избытке аммиака:
5. Аммиак горит на воздухе , образуя азот и воду:
Если реакцию проводить в присутствии катализатора (Pt), то азот окисляется до NO:
6. За счет атомов водорода в степени окисления +1 аммиак может выступать в роли окислителя , например в реакциях с щелочными, щелочноземельными металлами, магнием и алюминием . С металлами реагирует только жидкий аммиак.
Например , жидкий аммиак реагирует с натрием с образованием амида натрия:
Также возможно образование Na2NH, Na3N.
При взаимодействии аммиака с алюминием образуется нитрид алюминия:
2NH3 + 2Al → 2AlN + 3H2
7. За счет азота в степени окисления -3 аммиак проявляет восстановительные свойства. Может взаимодействовать с сильными окислителями — хлором, бромом, пероксидом водорода, пероксидами и оксидами некоторых металлов. При этом азот окисляется, как правило, до простого вещества.
Например , аммиак окисляется хлором до молекулярного азота:
Пероксид водорода также окисляет аммиак до азота:
Оксиды металлов , которые в электрохимическом ряду напряжений металлов расположены справа — сильные окислители. Поэтому они также окисляют аммиак до азота.
Например , оксид меди (II) окисляет аммиак:
2NH3 + 3CuO → 3Cu + N2 + 3H2O
Источник
Сырье для производства аммиака. Синтез аммиака из азотводородной смеси (АВС)



Технологические свойства аммиака.
Аммиак (NH3) – бесцветный газ с резким запахом и температурой кипения —33,4˚С и температурой плавления —77,8˚С Аммиак хорошо растворим в воде (750 литров в литре воды), ограниченно растворим в органических растворителях.
При взаимодействии с водой аммиак образует гидраты следующего состава:
Незначительное количество растворенных в воде молекул аммиака ионизирует в результате реакции:
Степень диссоциации 0.004.
Жидкий аммиак растворяет щелочные и щелочноземельные металлы, фосфор, серу, иод и многие другие неорганические и органические соединения.
При температуре 1300 °С аммиак диссоциирует на азот и водород:
Сухой аммиак образует с воздухом взрывчатые смеси, пределы взрываемости которых зависят от температуры.
Мировое производство аммиака составило в 1980 году более 90 млн. тонн.
Первый заводпо производствуаммиака был пущен в 1913 году с производительностью 25 т в сутки.
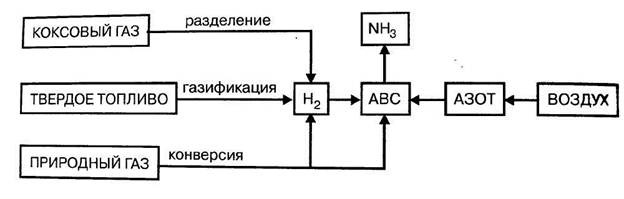
Сырьем в производстве аммиака является азотоводородная смесь (АВС) состава N2:H2 = 1:3. Ресурсы атмосферного азота практически неисчерпаемы, поэтому производство аммиака определяется в основном способом производства водорода.
Рисунок 4.3. – Сырьевые ресурсы производства аммиака.
Азот получают ректификацией (перегонкой) сжиженного атмосферного воздуха.
Водороддля синтеза аммиака может быть получен:
1. разделением обратного коксового газа,
2. газификацией твердого топлива,
3. конверсией природного газа (метана или его газообразных гомологов),
4. конверсией оксида углерода с водяным паром,
5. крекингом метана
6. электролизом либо термическим разложением воды
Основное значение имеют методы конверсии метана и оксида углерода, а также разделение коксового газа.
Для перспективных планов широкого применения водорода в промышленных и энергетических целях планируется его крупномасштабное производство из воды – самого дешевого сырья, запасы которого неограниченны. Существующие и разрабатываемые методы производства водорода из воды делятся на три группы:
1. электролиз воды
2. термохимические методы
3. комбинированные термо-и электрохимические методы.
ЭЛЕКТРОЛИЗ – наиболее освоенный метод производства водорода из воды, в настоящее время он используется в небольших масштабах при наличии дешевой электроэнергии. Электрохимические процессы основаны на взаимных превращениях электрической энергии в химическую и наоборот. Достоинства электрохимических процессов – их простота в аппаратурном оформлении, малостадийность технологического процесса, высокая чистота получаемых продуктов, надостижимая для химических способов и др. Основной недостаток электролиза – высокий расход электроэнергии, стоимость которой составляет основную долю в себестоимости продуктов – более 90 %. Более того, при промышленном электролизе водных растворов коэффициент использования энергии – не более 50 – 60%, что еще более повышает стоимость продуктов электролиза. При получении водорода электролизом воды применяют в качестве электролита водные растворы кислот, щелочей или солей, так как электропроводность чистой воды ничтожно мала – при 18 °С удельная электропроводность воды составляет (2-6)×10 -10 См ×м -1 . Чаще всего применяют щелочные электролиты, наименее агрессивные для конструкционных материалов электролизеров. Выделение водорода происходит на катоде по реакции:
Суммарный КПД производства водорода электролизом воды с использованием электроэнергии, вырабатываемой атомной станцией, составляет не более 20 – 30 %, и это отрицательно сказывается на себестоимости водорода. Снижение себестоимости электролитического водорода может быть достигнуто совершенствованием конструкции электролизеров, их удешевлением, и, что амое главное, применением дешевой электроэнергии. Как основная перспектива, рассматривается возможность питания водородных электролизеров «провальной» энергией атомных станций, т.е. использованием электроэнергии в те периоды, когда станции недогружены, например, в ночные часы.
Термохимический метод получения водорода основан на разложении воды с помощью тепловой энергии, которую предполагается получать от атомных реакторов с гелиевым охлаждением, используя теплоту газового теплоносителя на выходе из реактора. Непосредственное разложение воды по реакции

неосуществимо, так как при необходимой для этого высокой температуре (около 1000 °С) константа равновесия реакции ничтожно мала (10 -6 ). Реализация процесса возможна заменой реакции прямого разложения воды термохимическим циклом, состоящим из нескольких стадий, для каждого из которых значения константы равновесия были бы приемлемы для практики. Разработано и предложено множество термохимических циклов для разложения воды при температурах, доступных с точки зрения использования теплоты охлаждающих газов ядерных реакторов. В большинстве из предложенных циклов промежуточные вещества имеют высокое сродство к водороду, либо к кислороду – это галогены, элементы IV группы (сера), металлы II группы (Mg, Ca. Ba) и переходные элементы с переменной степенью окисления (V, Fe). Ниже приведен один из примеров термохимического цикла реакций, ведущих к разложению воды на H2 и O2:
Весь термохимический цикл разложения воды представляет собой замкнутый цикл, так как все исходные реагенты отделяются от продуктов реакции и возвращаются в цикл, за исключением воды, расходуемой на образование водорода и кислорода. Максимальная температура реакций не превышает 700 °С и может быть обеспечена теплоносителем на выходе их атомного реактора на уровне 800 — 900 °С.
В настоящее время ни один из предложенных термохимических циклов еще не реализован в промышленности и значение КПД циклов, а так же расчеты затрат на получение водорода этим методом пока не определены.
Комбинированный метод производства водорода заключается в комбинировании термо- и электрохимических стадий процесса. Ожидаемые преимущества комбинированного метода состоят в том, что могут быть использованы достоинства каждого из рассмотренных способов: электрохимический хорошо освоен, имеет простое аппаратурное оформление, а термохимический более экономичен, но мало освоен и включает стадии, трудные для промышленного осуществления.
Примером может служить сернокислотный комбинированный цикл получения водорода и кислорода из воды. Это двухступенчатый процесс, включающий 2 стадии
1. термохимическая – эндотермическая реакция, осуществляемая при 900 °С
2. низкотемпературный электрохимический процесс:
Последняя реакция может быть реализована только путем электролиза, так как ее константа равновесия и теоретическим выход водорода чрезвычайно малы. Источником энергии для комбинированной установки может служить атомный газовый реактор, снабжающий отбросной теплотой термохимическую стадию и электроэнергией электрохимическую стадию. Расчетные затраты для комбинированной установки меньше, чем для прямого электролиза воды. Суммарный КПД процесса должен составить 35 – 37 %. По мнению специалистов комбинирование термохимических и электрохимических стадий – наиболее перспективное направление крупномасштабного производства водорода из воды.
Основным методом получения водорода для синтеза аммиака является каталитическая конверсия метана. Сырьём для этого метода служит природный и попутный газ, содержащий до 90-98% метана.
Источник