- Опыт № 33. Получение уксусной кислоты из ацетата натрия
- Получение уксусной кислоты и опыты с ней
- Описание презентации по отдельным слайдам:
- Охрана труда
- Библиотечно-библиографические и информационные знания в педагогическом процессе
- Охрана труда
- Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
- Общая информация
- Похожие материалы
- Урок по математике «Геометрические фигуры. Признаки и характеристики предметов»
- Сценарий открытого мероприятия, посвящённого 75-летию Победы в Великой Отечественной войне: «Памяти павших будьте достойны!»
- Возможности и риски педагогической диагностики
- Презентация на тему : «Этологическая теория»
- Мастер-класс для воспитателей «Нетрадиционные техники лепки»
- Презентация на тему: Электрический ток. Анализ опасности поражения током
- «Вред и польза жевательной резинки»
- Статья «Нетрадиционные формы обучения столяров»
- Вам будут интересны эти курсы:
- Оставьте свой комментарий
- Безлимитный доступ к занятиям с онлайн-репетиторами
- Подарочные сертификаты
- Ацетат натрия
- Содержание
- Область применения
- Способы получения
- Характерные реакции
- Влияние на организм
Опыт № 33. Получение уксусной кислоты из ацетата натрия
20% раствор серной кислоты
Гидрокарбонат натрия (NaHCO3)
В пробирку помещают 3 г (0,037 моль) кристаллического ацетата натрия и приливают 5 мл 20% раствор серной кислоты (0,012 моль), вносят в пробирку кипятильный камешек и закрывают пробкой с газоотводной трубкой. Свободный конец газоотводной трубки погружают в другую пробирку, опущенную в стаканчик с холодной водой. Реакционную смесь осторожно нагревают, уксусная кислота перегоняется с парами воды и конденсируется в холодной пробирке (серная кислота с парами воды не перегоняется).
Полученный дистиллят испытывают на универсальную индикаторную бумагу (кислая среда). После этого к дистилляту добавляют небольшое количество кристаллической соды (NaHCO3), наблюдается энергичное выделение углекислого газа.
Уксусная кислота восстанавливает угольную кислоту из её соли, при этом наблюдается выделение углекислого газа.
Опыт № 34. Получение и гидролиз ацетата железа (III)
Раствор хлорида железа (III)
В пробирку помещают 2 г (0,024 моль) ацетата натрия, растворяют в 3 мл воды, добавляют 2-3 капли раствора хлорида железа (III), при встряхивании жидкость окрашивается в красно-бурый цвет благодаря образованию ацетата железа (III). В пробирку добавляют еще 1 мл воды и кипятят. В результате гидролиза соли образуется коричнево-красный осадок основной соли ацетата железа:
Опыт № 35. Устойчивость уксусной кислоты к действию окислителей
5% раствор уксусной кислоты
10% раствор серной кислоты
1% раствор перманганата калия
К 1 мл 5%-ного раствора уксусной кислоты (8,3∙10 -4 моль) прибавляют 0,5 мл 1%-ного раствора перманганата калия (6,3∙10 -6 моль) и 1 мл 10%-ного раствора серной кислоты (1∙10 -3 моль). Обесцвечивания перманганата калия не наблюдается, что указывает на устойчивость уксусной кислоты к окислению.
Опыт № 36. Окисление муравьиной кислоты
10% раствор серной кислоты
Раствор перманганата калия
В пробирку с газоотводной трубкой наливают 1 мл (0,026 моль) муравьиной кислоты, 1 мл 10% раствора серной кислоты (0,0011 моль) и 4 мл раствора перманганата калия. Газоотводную трубку погружают в пробирку с раствором известковой воды. Реакционную смесь осторожно нагревают, поместив в пробирку кипятильные камешки для равномерного кипения. Раствор сначала буреет, затем обесцвечивается. Образовавшаяся угольная кислота распадается на воду и углекислый газ, который с известковой водой в пробирке образует белый осадок карбоната кальция СаСО3.
Опыт № 37. Разложение муравьиной кислоты
Концентрированная серная кислота
В пробирку, снабженную пробкой с газоотводной трубкой, наливают 3 мл (0,078 моль) муравьиной кислоты, добавляют 3 мл (0,055 моль) концентрированной серной кислоты и нагревают на слабом огне. Конец газоотводной трубки помещают в пламя второй горелки. Муравьиная кислота разлагается с выделением оксида углерода (II):
При поджигании оксид углерода сгорает голубоватым пламенем до углекислого газа.
Опыт № 38. Окисление олеиновой кислоты перманганатом калия (реакция Вагнера)
1% раствор перманганата калия
10% раствор гидроксида натрия
В пробирку наливают 2 мл разбавленного раствора 1% перманганата калия (1,27∙10 -4 моль), прибавляют 0,5 мл 10% раствора гидроксида натрия (1.25∙10 -3 моль) и 3-4 капли олеиновой кислоты. Пробирку закрывают и энергично встряхивают. Раствор перманганата калия изменяет свою окраску. Происходит окисление олеиновой кислоты в диоксистеариновую (две гидроксильные группы присоединяются по месту двойной связи):
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).
Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.
Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Источник
Получение уксусной кислоты и опыты с ней
Описание презентации по отдельным слайдам:
Описание слайда:
Практическая работа
«Получение уксусной кислоты
и опыты с ней»
Подготовила учитель химии Бердова Н.Ю.
Описание слайда:
Описание слайда:
.
Помните, что любое вещество может быть опасным, если обращаться с ним неправильно
Описание слайда:
Вещества не должны храниться вместе с пищевыми продуктами.
Описание слайда:
Не склоняйтесь над сосудом с кипящей жидкостью.
Описание слайда:
Перед началом эксперимента внимательно ознакомьтесь с инструкциями
Описание слайда:
Не работай с треснутой или посудой
Описание слайда:
Цель работы: Получить уксусную кислоту и изучить её свойства.
Реактивы и оборудование: ацетат натрия, серная кислота (конц.), уксусная кислота, магний (порошок), цинк, гидроксид натрия, карбонат натрия, фенолфталеин, универсальная индикаторная бумага, прибор для получения и собирания кислоты, спиртовка, пробирку, вата, спички.
Описание слайда:
Опыт 1. Получение уксусной кислоты.
В пробирку с ацетатом натрия прибавить 1- 2 мл концентрированной серной кислоты. Закрыть пробирку пробкой с газоотводной трубкой, конец которой опустите в другую пробирку вход в пробирку прикрыть ваткой, смотрите рисунок:
Смесь в пробирке осторожно нагревайте до тех пор, пока в приёмнике – пробирке не собёрётся 1 -2 мл жидкости. Прекратите нагревание, закройте спиртовку.
Опустите в пробирку с образовавшейся жидкости универсальную индикаторную бумагу. Как изменился цвет индикатора? Почему? Запишите уравнение диссоциации уксусной кислоты.
Опишите запах, образовавшейся жидкости? Соблюдайте осторожность при определении запаха! Составьте уравнение данной химической реакции.
Ход работы
Описание слайда:
Опыт 2. Взаимодействие уксусной кислоты с металлами.
Посмотрите видео-опыт «Взаимодействие уксусной кислоты с металлами»
В одну пробирку положите гранулу цинка, в другую порошок магния. В обе пробирки прилейте 1 мл уксусной кислоты. Что наблюдаете? Сравните скорость этих реакций? Запишите соответствующие уравнения химических реакций, назовите продукты, укажите тип реакции.
Описание слайда:
Описание слайда:
Опыт 3. Взаимодействие уксусной кислоты с основаниями.
Посмотрите видео-опыт «Взаимодействие уксусной кислоты с основаниями»
В пробирку налейте 1 мл гидроксида натрия и добавьте 1 каплю фенолфталеина. Что наблюдаете? Почему?
Затем добавьте к содержимому пробирки уксусную кислоту. Почему происходит обесцвечивание? Запишите УХР, назовите продукты.
Описание слайда:
Описание слайда:
Опыт 4. Взаимодействие уксусной кислоты с солями слабых неорганических кислот.
Посмотрите видео-опыт «Взаимодействие уксусной кислоты с карбонатом натрия»
В пробирку налейте 1 мл карбоната натрия и по каплям добавьте уксусную кислоту. Что наблюдаете? Почему?
Запишите УХР, назовите продукты.
Описание слайда:
Описание слайда:
Оформите работу в виде таблицы
Сделайте общий вывод о проделанной работе.
Описание слайда:
УРОК ОКОНЧЕН
СПАСИБО ЗА УРОК
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Курс повышения квалификации
Охрана труда
- Сейчас обучается 97 человек из 44 регионов
Курс профессиональной переподготовки
Библиотечно-библиографические и информационные знания в педагогическом процессе
- Сейчас обучается 336 человек из 66 регионов
Курс профессиональной переподготовки
Охрана труда
- Сейчас обучается 172 человека из 48 регионов
Ищем педагогов в команду «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
Общая информация
Международная дистанционная олимпиада Осень 2021
Похожие материалы
Урок по математике «Геометрические фигуры. Признаки и характеристики предметов»
Сценарий открытого мероприятия, посвящённого 75-летию Победы в Великой Отечественной войне: «Памяти павших будьте достойны!»
Возможности и риски педагогической диагностики
Презентация на тему : «Этологическая теория»
Мастер-класс для воспитателей «Нетрадиционные техники лепки»
Презентация на тему: Электрический ток. Анализ опасности поражения током
«Вред и польза жевательной резинки»
Статья «Нетрадиционные формы обучения столяров»
Не нашли то что искали?
Воспользуйтесь поиском по нашей базе из
5309447 материалов.
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Безлимитный доступ к занятиям с онлайн-репетиторами
Выгоднее, чем оплачивать каждое занятие отдельно
Рособрнадзор откажется от ОС Windows при проведении ЕГЭ до конца 2024 года
Время чтения: 1 минута
В проекте КоАП отказались от штрафов для школ
Время чтения: 2 минуты
Правительство предложило потратить до 1 млрд рублей на установку флагов РФ у школ
Время чтения: 1 минута
Российский совет олимпиад школьников намерен усилить требования к олимпиадам
Время чтения: 2 минуты
Минпросвещения разрабатывает образовательный минимум для подготовки педагогов
Время чтения: 2 минуты
Спортивные и творческие кружки должны появиться в каждой школе до 2024 года
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Источник
Ацетат натрия
| Ацетат натрия | |
|---|---|
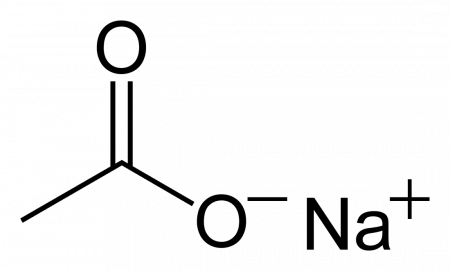 | |
| Систематическое наименование | sodium acetate (ИЮПАК) sodium ethanoate (систематическое) ацетат натрия натрия этаноат натрий уксуснокислый |
| Хим. формула | C2H3O2Na |
| Рац. формула | CH3COONa |
| Состояние | белый гигроскопичный порошок |
| Молярная масса | 82.03 грамм/моль (безводная форма) 136.08 грамм/моль (тригидрат) г/моль |
| Плотность | 1,45 г/см³ |
| Температура | |
| • плавления | 328 °C |
| • разложения | 324 °C |
| Удельная теплота плавления | 264—289 кДж/кг |
| Растворимость | |
| • в воде | 76 г/100 мл |
| Рег. номер CAS | 127-09-3 |
| PubChem | 517045 |
| Рег. номер EINECS | 204-823-8 |
| SMILES | |
| Кодекс Алиментариус | E262 |
| ChEBI | 32954 |
| ChemSpider | 29105 |
| Токсичность | ирритант, малотоксичен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, кристаллы со слабым солёным вкусом и уксусным запахом, производится и применяется в промышленных масштабах.
Содержание
Область применения
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
Также ацетат натрия является источником углерода для бактерий, выращиваемых на питательной среде.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
Ацетат натрия также используется в быту как составная химических грелок (англ. heating pad ) или химических обогревателей (англ. Hand warmer ), применяется как составная часть смеси «горячего льда» (англ. «hot ice» ), при кристаллизации ацетата натрия выделяется тепло — это экзотермический процесс. При нагреве тригидрата ацетата натрия (имеющего точку плавления в 58 °C) до 100 °C (обычно ёмкость с ним кладут в кипящую воду) он расплавляется (вернее, растворяется в собственной кристаллизационной воде) и переходит в водный раствор ацетата натрия. При охлаждении этого раствора образуется перенасыщенный раствор ацетата натрия в воде. Этот раствор прекрасно переохлаждается до комнатной температуры без образования твёрдой фазы, затем нажатием на металлический диск в ёмкости образуется центр кристаллизации, который, вырастая, заставляет перенасыщенный раствор переходить в твёрдую фазу тригидрата ацетата натрия. Этот процесс сопровождается значительным выделением тепла (экзотермическая реакция), теплота фазового перехода составляет 264-289 кДж/кг.
На этом свойстве основан довольно красивый химический опыт — «горячий лёд».
Способы получения
- В лабораторных условиях ацетат натрия образуется при взаимодействии уксусной кислоты, например, с карбонатом натрия, гидрокарбонатом натрия или гидроксидом натрия.
CH3COOH + NaHCO3 ⟶ CH3COONa + H2O + CO2↑
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 г гидрокарбоната натрия реагируют с 750 г 8%-го винного уксуса (или же с 86 г 70%-й уксусной эссенции) с образованием 82 г ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия. Для получения тригидрата ацетата натрия без выпаривания необходимо смешать 84 г гидрокарбоната натрия (пищевой соды) с 86 г 70%-ной уксусной кислоты и 10 г воды.
- Также ацетат натрия может быть получен и в ходе экзотермической реакции растворения металлического натрия в уксусной кислоте:
2CH3COOH + 2Na ⟶ 2CH3COONa + H2↑ + Q
Характерные реакции
Ацетат натрия может быть использован для образования сложного эфира по реакции с алкилгалогенидами, такими как, например, бромэтан:
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
2CH3COONa → Na2CO3 + (CH3)2CO 
Влияние на организм
Ацетат натрия может всасываться в организм при проглатывании. Является ирритантом. LD50 25956 мг/кг. По другим данным из того же источника: LD50(крысы, орально): 3500 мг/кг, LD50(мыши, орально): 4960 мг/кг.
Источник

















