Постгеномная эра. Получение трансгенных животных
В наши дни трансгенные организмы перестают быть редкостью и значение их для биологии и медицины трудно переоценить. Искусственное включение практически любого интересующего исследователей гена позволяет физиологам изучать на трансгенных животных различные отклонения в гомеостазе организма, иммунной системе, в эмбриогенезе и во многих других случаях
Получение трансгенных животных
Исследования в биомедицине сосредоточены в основном на том, чтобы создать широкий спектр моделей заболеваний человека, включая такие, как атеросклероз, диабет, гипертонию, болезнь Альцгеймера, ретинобластому, онкологические и многие другие заболевания. Модели трансгенных животных, как правило мышей, позволяют изучать механизмы развития и лечения болезней человека.
Трансгенные мыши являются также незаменимой модельной системой и для тестирования генетических конструкций перед получением сельскохозяйственных трансгенных животных-биореакторов, способных с молоком продуцировать белки человека.
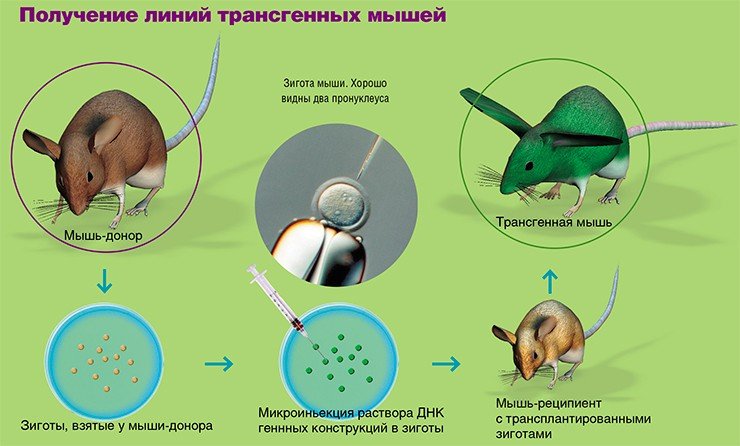
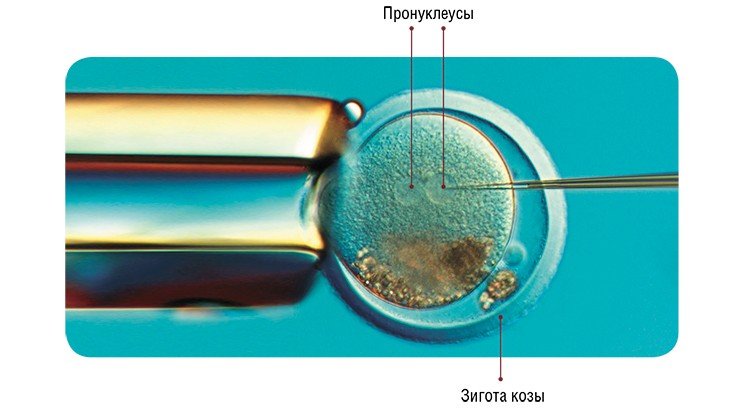
Наиболее широко используемый метод введения трансгена – микроинъекция в пронуклеусы (мужское и женское ядро) зиготы в тот момент, когда спермий проник в яйцеклетку, и пронуклеусы готовятся к слиянию. Суть метода заключается во введении в мужской пронуклеус с помощью микроманипулятора со стеклянным капилляром (диаметр кончика 1 мкм) раствора экзогенной (чужеродной) ДНК (500—1000 копий гена). Эта процедура проводится под микроскопом со специальной оптикой, позволяющей видеть пронуклеусы в трехмерном измерении.
Эффективность интеграции трансгенов в геном, т. е. число трансгенных животных от общего числа родившихся при использовании данного метода в зависимости от вида животных колеблется незначительно. Так, у мышей этот показатель составляет 5—15 %, у свиней – 10—15 %, у кроликов – 10 %, у овец, коз и коров – 5—10 %.
Можно выделить следующие этапы получения трансгенных животных:
1) получение зигот от гормонально стимулированных самок;
2) микроиньекция раствора ДНК генных конструкций в мужской пронуклеус зиготы;
3) трансплантация проинъецированных зигот самкам-реципиентам, подготовленным для вынашивания беременности;
4) анализ родившихся потомков на присутствие трансгена методом полимеразной цепной реакции (ПЦР-анализ);
5) анализ трансгенных животных по наследованию трансгена, экспрессии рекомбинантного белка, его биологической активности; необходимо узнать, активен ли встроенный трансген, передается ли он потомкам, обладает ли белок всеми биологическими свойствами его природного аналога и соответствует ли уровень продукции биотехнологическим целям;
6) создание линии (стада) трансгенных животных для научных или биотехнологических целей.
Животные-биореакторы
Получение терапевтически ценных белков человека в молоке трансгенных животных – одно из перспективных направлений современной биотехнологии. Стратегия создания сельскохозяйственных молочных животных в качестве биореакторов основана на введении в управляемую регуляторными элементами одного из «генов молока» коровы, козы или овцы комбинированной генетической конструкции, содержащей последовательность ДНК человека, кодирующую необходимый белок. Согласно этой стратегии, такие трансгенные животные способны синтезировать на высоком уровне белок человека исключительно в молочной железе и секретировать его в молоко, которое в свою очередь становится источником для выделения белка человека.
В настоящее время имеются примеры успешного применения этой технологии, и созданы трансгенные козы, овцы, кролики, свиньи – продуценты человеческих белков: -антитрипсина, сывороточного реактивного белка С, антитромбина, факторов VIII и IX свертываемости крови, лактоферрина, кальцитонина и др. (Wall et al., 1997; Rudolph, 1999; Гольдман и др., 2002).
Фармакологический рынок рекомбинантных белков, полученных из молока трансгенных домашних животных оценивается в 1 млрд долл. в настоящее время и прогнозируется его развитие до 18,6 млрд долл. к 2013 г. (Niemann и др., 2007).
Тестирование новых генно-инженерных конструкций, как правило, производится на трансгенных мышах из-за того, что большинство крупных животных – потенциальных продуцентов лекарственных белков человека имеют длительный репродуктивный период и к тому же дорого обходятся. Анализ генетических конструкций на трансгенных мышах позволяет быстро отобрать из них наиболее перспективные как по уровню продукции заданного белка, так и по его биологическим свойствам.
Проекты по получению трансгенных биореакторов, как правило, состоят из трех частей: создание генетической конструкции, включающей ген человека под управлением регуляторных областей одного из «молочных генов» (например, казеиновых), тестирование ее на трансгенных мышах и, наконец, введение отобранных конструкций в геном молочных животных.
Получение эффективного продуцента – большая удача и гарантия в относительно сжатые сроки создания стада его потомков, обеспечивающих рынок ценным фармакологическим продуктом. При таком стаде создается лаборатория по выделению и очистке рекомбинантного белка, который передается в соответствующие фарминституты для тестирования, проведения его предклинических и клинических испытаний и разрешения применения получаемого лекарства в медицинской практике.
Опыт ведущих фармакологических фирм США, Канады и Англии показывает, что такие проекты длятся около 10 лет при высоком уровне финансирования. С сожалением можно отметить, что в России таких технологий практически нет, как и инфраструктуры для их развития, а это означает, что биологически ценные белки человека мы будем покупать за рубежом. А таких белков уже около 60 (Rudolph, 1999).
К тому же досадно, что российские ученые получили и протестировали на трансгенных мышах несколько эффективных генных конструкций для целей биотехнологии (Завадская и др., 2001; Дворянчиков и др., 2005; Гольдман и др., 1998; Zakharova et al., 2006), однако современных биотехнологических ферм в России нет, и эти разработки пока не используются в полной мере.
Скорее как исключение следует отметить два биотехнологических проекта, развивающихся в России.
В рамках российско-бразильского проекта, о котором рассказывается выше, участвуют Институт цитологии и генетики СО РАН, Институт молекулярной генетики РАН, Государственный университет Рио де Жанейро (UFRJ) и Университет штата Сеара (UECE), в июле 2006 г. получена трансгенная коза с геном Г-КСФ человека, конструкция предварительно была протестирована на трансгенных мышах (Dvoryanchikov et al., 2005). Статья, посвященная получению трансгенной козы опубликована в Журнале Академии наук Бразилии (Freitas et al., 2007). Осенью 2007 г. эксперимент успешно повторен, и в марте 2008 г. родились три трансгенных козленка, из которых сейчас успешно подрастают только двое – Камилла и Августин.
Второй биотехнологический проект на козах, известный нам пока только из популярной прессы, развивается в совместном российско-белорусском проекте с генетической конструкцией лактоферрина человека. Лактоферрин содержится в женском грудном молоке и является природным антибиотиком, защищающим детский организм от всевозможных болезней. Государственными заказчиками программы выступают Федеральное агентство по науке и инновациям России и Национальная академия наук Белоруссии. Основные исследования проводят специалисты Института биологии гена РАН и Научно-практического центра НАН Белоруссии по животноводству. В конце 2007 г. ученые сумели получить двух трансгенных козлят, которые несут ген лактоферрина человека.
Гольдман И. Л. и др. Лактоферин: свойства и перспективы биотехнологического производства // Биотехнология. 1998. № 4. С. 3—16.
Гольдман И. Л. и др. Трансгенные козы в мировой фармаиндустрии ХХI века // Генетика. 2002. Т. 38, № 1. С. 5—21.
Завадская Е. С. и др. Получение рекомбинантного эндостатина в молоке трансгенных мышей // Генетика. 2001. Т. 37. С. 1207—1212.
Dvoryanchikov G. A. et al. Secretion of Biologicaly Active Human Granulocyte Colony-Stimulating Factor (G-CSF) in Milk of transgenic Mice // Russian J. of Genetics. 2005. V. 41, N. 10. P. 1088—1094.
Freitas V. J. et al. Production of transgenic goat (Capra hircus) with human Granulocyte Colony Stimulating Factor (hG-CSF) gene in Brazil // Ann. Braz. Acаd. Sci. 2007. V. 79 N. 4. P. 585—592.
Hubel K. et al. Clinical applications of granulocyte colony-stimulating factor: an update and summary // Ann. Hematol. 2003. V. 82. P. 207—213.
Niemann H. et al. Transgenic farm animals: an update // Reprod. Fertil. Dev. 2007. № 19. 762 р.
Wall R. J. et al. Transgenic dairy cattle: genetic engineering on a large scale // J. Dairy Sci. 1997. V. 80. P. 2213—2224.
Wall R. J. Transgenic livestock: progress and prospects for the future // Theriogenology. 1996. V. 45. P. 57.
Zakharova E. S. et al. Transcription and mRNA splicing of the human lactoferrin gene controlled by the regulatory region of the bovine alphaS1 casein gene in the mammary gland of transgenic mice and in mouse embryonic stem cells // Dokl. Biochem. Biophys. 2006. N. 411. P. 336—338.
Фотоматериалы получены совместно с участником проекта Л. Е. Андреевой (к. б. н., с. н. с. Института молекулярной генетики РАН (Москва)).
Источник
Трансгенные животные: технологии получения
В отличие от растений, где существует возможность получения целого фертильного растения из одной трансформированной соматической клетки и вегетативное размножение, получение трансгенных животных — очень сложный и длительный процесс.
Используемая стратегия состоит в следующем:
1. Клонированный ген вводят в ядро оплодотворенной яйцеклетки.
2. Оплодотворенные яйцеклетки с экзогенной ДНК имплантируют в рецепиентную женскую особь (поскольку успешное завершение развития эмбриона млекопитающих в иных условиях невозможно).
3. Отбирают потомков, развившихся из имплантированных яйцеклеток, которые содержат клонированный ген во всех клетках.
4. Скрещивают животных, которые несут клонированный ген в клетках зародышевой линии, и получают новую генетическую линию.
Эксперименты по генетической модификации многоклеточных организмов путем введения в них трансгенов требуют много времени. Тем не менее, трансгеноз стал мощным инструментом для исследования молекулярных основ экспрессии генов млекопитающих и их развития, для создания модельных систем, позволяющих изучать болезни человека, а также для генетической модификации клеток молочных желез животных с целью получения с молоком важных для медицины белков. Был даже предложен новый термин «фарминг» (pharming), относящийся к процессу получения из молока трансгенных домашних животных аутентичных белков человека или фармацевтических препаратов.
Использование молока целесообразно потому, что оно образуется в организме животного в большом количестве и его можно надаивать по мере надобности без вреда для животного. Вырабатываемый молочной железой и секретируемый в молоко новый белок не должен при этом оказывать никаких побочных эффектов на нормальные физиологические процессы, протекающие в организме трансгенного животного, и подвергаться посттрансляционным изменениям, которые, по крайней мере, близки к таковым в клетках человека. Кроме того, его выделение из молока, которое содержит и другие белки, не должно составлять большого труда.
Несмотря на то, что первые трансгенные сельскохозяйственные животные были получены в 1985 г. введением экзогенной ДНК в пронуклеус зигот, до настоящего времени не разработано эффективного метода, который бы мог быть использован для создания генетически модифицированных животных независимо от вида и от целей эксперимента. Разработка новых эффективных методов переноса генов в эмбриональные и соматические клетки животных, а также совершенствование существующих подходов остается актуальной задачей.
Среди большого разнообразия способов внедрения экзогенной ДНК в геном животного можно выделить следующие, которые нашли широкое применение в практике трансгеноза:
— метод микроинъекции,
— опосредованный ретровирусами перенос генов,
— использование модифицированньгх эмбриональных стволовых клеток,
— перенос трансформированных ядер генеративных и соматических клеток,
— использование спермиев и сперматогониев как переносчиков ДНК.
Среди других способов доставки экзогенной ДНК в организм животных можно отметить использование липосом, аденовирусных векторов, а также метод высокоскоростной инъекции. Однако эти методы не нашли широкого применения вследствие их недостаточной стабильности, а также отсутствия интеграции трансгена в геном.
Микроинъекции рекомбинантной ДНК в оплодотворенные ооциты многоклеточных животных пока остаются наиболее популярным способом введения чужих генов в организм животных. Несмотря на то, что метод требует высокой квалификации и дорогостоящего оборудования, простота и надежность окупают все его недостатки.
Первой и наиболее хорошо разработанной экспериментальной системой для получения трансгенных животных явилась мышь. Донорных самок мышей с экспериментальной суперовуляцией скрещивают с самцами-производителями, через 12 ч выделяют оплодотворенные яйцеклетки и помещают их в культуру. Далее в больший их двух пронуклеусов (обычно мужской) инъецируют рекомбинантную ДНК (рис. 2.17). Пережившие инъекцию яйцеклетки пересаживают самкам-реципиентам. Только часть трансплантированных ооцитов продолжает развиваться до рождения детенышей.
На частоту интеграции экзогенной ДНК при использовании метода микроинъекции оказывают влияние такие факторы, как чистота вводимого образца, форма и концентрация ДНК, состав буферного раствора для микроинъекции, качество эмбрионов, а также способ пересадки эмбрионов реципиентам (нехирургический, хирургический, лапароскопический).
Трансгенных животных в потомстве идентифицируют различными методами, чаще всего ПЦР, и скрещивают для получения трансгенных линий. Некоторые из трансгенных животных оказываются мозаичными (половые клетки не содержат экзогенной ДНК), поэтому при скрещивании трансгенным оказывается меньшая часть потомства первого поколения, чем расчетные 50 %. В ряде случаев гомозиготные линии получить не удается, поскольку 5-15 % трансгенных инсерций в гомозиготном состоянии летальны, так как инсерция иногда нарушает жизненно-важные части генома.
Точный механизм, обеспечивающий интеграцию инъецированной ДНК в хромосомы клетки-мишени, неизвестен, однако анализ структуры встроенной ДНК позволяет выявить некоторые моменты. Интеграция происходит случайным образом в один хромосомный локус, который может содержать от одного до нескольких тысяч тандемных копий интегрированной ДНК. Около 30 % полученных первичных трансгенных животных, как правило, обнаруживают ту или иную степень мозаичности, что может являться следствием интеграции экзогенной ДНК после завершения первого цикла репликации.
Степень интеграции экзогенной ДНК в геном, т.е. число трансгенных животных от общего числа родившихся животных, при использовании метода микроинъекции в зависимости от вида животных колеблется в незначительных пределах 5-15 % . Наиболее важным с учетом затрат, требующихся для получения одного трансгенного животного, является показатель общей эффективности трансгеноза, который рассчитывается как отношение числа полученных трансгенных животных к общему числу пересаженных эмбрионов, выраженное в процентах. Величина этого показателя для млекопитающих также относительно постоянна и составляет в среднем от
0,5 % у свиней и коров до
Ретровирусные векторы также используются для получения трансгенных животных. Инфицирование предимплантационных эмбрионов рекомбинантными ретровирусами — относительно несложная эффективная процедура.
Восьмиклеточную морулу (рис. 2.18) освобождают от яйцевой оболочки и помещают в культуральную чашку с фибробластами, продуцирующими рекомбинантный ретровирус. Инфицированные эмбрионы, достигшие стадии бластулы, имплантируют псевдобеременным самкам. В результате формируются трансгенные организмы, мозаичные по числу и локализации встроек рекомбинантной ДНК в геном. Поэтому для получения чистых линий далее необходим масштабный аутбридинг.
Недостатком метода является ограничение вставки экзогенной ДНК
8 тнп, вследствие чего трансген может оказаться лишенным прилегающих регуляторных последовательностей, необходимых для его экспрессии, а в некоторых случаях интеграция в исходный локус нестабильна.
Новые лентивирусные векторы (лентивирусы принадлежат семейству ретровирусов) показали свою очень высокую эффективность при доставке ДНК в ооциты и зиготы. Инъекция рекомбинантных лентивирусных конструкций в перивителлиновое пространство свиных зигот и коровьих ооцитов привело к появлению потомства с самой высокой на данный момент долей трансгенных особей. В то же время лентивирусные векторы обладают всеми недостатками ретровирусных: малый размер вставки экзогенной ДНК и множественная интеграция в хозяйский геном, которая может привести к таким нежелательным побочными эффектам, как активация онкогенов и инсерционный мутагенез. Кроме того, для лентивирусных векторов наблюдается высокая степень мозаичности получаемого трансгенного потомства и отдельные факты сайленсинга (инактивации) лентивирусных рекомбинантных последовательностей в полученных трансгенных линиях.
Использование ретровирусных векторов имеет и еще один большой недостаток. Хотя эти векторы создаются так, чтобы они были дефектными по репликации, геном штамма ретровируса (вируса-помощника), который необходим для получения большого количества векторной ДНК, может попасть в то же ядро, что и трансген. Несмотря на все принимаемые меры, ретровирусы-помощники могут реплицироваться в организме трансгенного животного, что совершенно недопустимо, если этих животных предполагается использовать в пищу или как инструмент для получения коммерческого продукта. И поскольку существуют альтернативные методы трансгеноза, ретровирусные векторы редко используются для создания трансгенных животных, имеющих коммерческую ценность.
Модифицированные эмбриональные стволовые клетки могут быть использованы для получения трансгенных животных. Клетки, выделенные из мышиных эмбрионов на стадии бластоцисты, могут пролиферировать в культуре, сохраняя способность к дифференцировке в любые типы клеток, в том числе и в клетки зародышевой линии, при введении в другой эмбрион на стадии бластоцисты (рис. 2.19).
Такие клетки называются плюрипотентными эмбриональными стволовыми клетками (ES). В ES-клетки в культуре можно ввести целевой трансген различными методами (трансфекция, электропорация, ретровирусная инфекция и т.д.) без нарушения их плюрипотентности. Практическое достоинство этой схемы заключается в том, что она дает большие возможности для проведения селекции клеток по определенному параметру. Это может быть число копий трансгена, его локализация или характер экспрессии.
Зная последовательности, окружающие конкретный сайт для желаемой интеграции, можно сконструировать вектор для встраивания целевой ДНК путем гомологичной рекомбинации. Например, заменить какой-либо ген, кодирующий легко идентифицируемый признак с целью селекции, убрав или восстановив его функцию в полученной трансгенной клетке.
Таким же образом получают так называемых нокаутных мышей (knock out) — мышей с направленно инактивированным определенным клеточным геном для исследования его функций. Для осуществления гомологичной рекомбинации вектор конструируют из фрагментов целевого гена, который планируется инактивировать, часть целевого гена при этом заменяется каким-либо селективным маркером для проведения отбора клеток с интегрированной конструкцией.
Отобранные трансгенные ES-клетки можно культивировать и использовать для получения трансгенных животных. Это позволяет избежать случайного встраивания трансгена, характерного для метода микроинъекций и ретровирусных векторных систем.
Все получаемые по такой схеме животные являются мозаиками, поэтому необходима селекционная работа по получению чистых линий. Проблему мозаичности первичных трансгенных животных можно преодолеть пересадкой ядер трансформированных ES-клеток в энуклеированные ооциты, которые затем продолжают свое нормальное развитие. В результате в каждой клетке полученного животного будет содержаться трансген.
К сожалению, плюрипотентные ES-клетки, аналогичные мышиным, пока не обнаружены у других млекопитающих и птиц, но поиски продолжаются.
Перенос ядер трансформированных генеративных и соматических клеток в яйцеклетку, или соматический ядерный перенос (somatic nuclear transfer), еще один способ, используемый в практике трансгеноза. Было показано, что ядра эмбриональных клеток различных животных при переносе в энуклеированную яйцеклетку иногда способны обеспечивать развитие целого нового организма. После непродолжительного культивирования даже ядра из некоторых дифференцированных клеток способны обеспечивать развитие до жизнеспособной особи.
Так, например, знаменитая овечка Долли была клонирована в 1997 г. слиянием культивируемых (3-6 пассажей) клеток эпителия молочной железы (вымени) взрослого шестилетнего животного с лишенной ядра яйцеклеткой (рис. 2.20). Хотя нельзя исключить, что для клонирования случайно была взята недифференцированная клетка, присутствующая в донорском эпителии.
Клонирование Долли из ядра дифференцированной клетки и трех других овец из ядер эмбриональных клеток удалось осуществить благодаря переносу ядер из клеток, находящихся в стадии покоя (G0), и, возможно, особенностям эмбриогенеза этого животного. В зиготах овец в течение первых трех делений, занимающих несколько суток, происходит только репликация ДНК, ни один из генов не экспрессируется. Предполагается, что за это время введенная ДНК освобождается от специфичных для клетки регуляторных белков, а соответствующие гены эмбрионального развития связываются с инициаторными эмбриональными белковыми факторами из цитоплазмы яйцеклетки.
Хотя технологиям клонирования еще очень далеко до совершенствования — клонированная Долли выявляла многие признаки преждевременного старения, это очень многообещающая технология получения трансгенных животных. Даже если имеются различные проблемы с первым поколением, скорее всего, второе поколение не будет иметь недостатков, приобретенных вследствие использования «старого» ядра для яйцеклетки.
Основная проблема, которую нужно решить для того, чтобы создание любых трансгенных животных с помощью метода переноса ядер стало реальным, — это сохранение плюрипотентности клеток в непрерывной культуре. В настоящее время ведутся активные поиски факторов репрограммирования дифференцированных клеток для индукции плюрипотентности. Если это удастся, то генетическое изменение таких клеток и создание трансгенных организмов путем соматического ядерного переноса станет почти рутинной процедурой, а пока это единичные удачные эксперименты.
Искусственные хромосомы как трансгенный вектор. Большинство трансгенов представляют собой кДНК, небольшие гены ( 100 тнп) слишком велики для встраивания в обычные векторы.
Учитывая все это, для трансгеноза стали использовать искусственные дрожжевые хромосомы (YAC), вмещающие фрагменты геномной ДНК длиной от 100 до > 1 000 тнп и искусственные хромосомы человека еще большей емкости (об искусственных хромосомах). Данные эписомальные векторы имеют еще одно преимущество — позволяют избежать эффект положения гена при экспрессии экзогенной ДНК. Уровень экспрессии встроенного гена очень зависит от его хромосомной позиции, например, встраивание в неактивный хроматин (гетерохроматин) интактной хромосомы приводит к инактивации гена.
С помощью искусственных дрожжевых хромосом (YAC), несущих несколько родственных генов или один большой ген, были получены трансгенные мыши путем микроинъекции в пронуклеус оплодотворенной яйцеклетки или трансфекцией ES-клеток. Трансгенные мыши, несущие кластер из пяти функциональных геновв -глобина человека суммарной длиной примерно 250 тнп, экспрессировали все эти гены тканеспецифично и в нужное время -точно так же, как это происходит у человека. Такое соответствие обеспечивалось фланкирующими их последовательностями, которые содержат промотор и другие важные регуляторные элементы. С помощью YAC-трансгеноза были получены мыши, которые синтезировали только человеческие антитела, являющиеся сложной тетрамерной конструкцией из двух пар разных полипептидных цепей.
Искусственные хромосомы человека (human artificial chromosome -HAC), содержащие целиком иммуноглобулиновый локус человека с тяжелыми и легкими цепями, были внедрены в бычьи фибробласты, которые затем использовали для соматического ядерного переноса. Полученные трансхромосомальные телята экспрессировали иммуноглобулины человека в своей крови. Эта система стала важным шагом в направлении животной продукции терапевтических поликлональных антител человека.
Дальнейшие наблюдения за трансгенными животными показали, что рекомбинантные HACs поддерживались в большинстве особей первого поколения в течение нескольких лет. Будут ли полученные искусственные хромосомы соответствующим образом разделяться в процессе мейоза и наследоваться, еще только предстоит выяснить.
Совсем недавно возникла новая перспективная технология для получения животных с выключенными генами — малые интерферирующие РНК (миРНК, siRNA), которые используют для прицельного выключения генов (сайленсинга). РНК-интерференция — консервативный посттранскрипционный регуляторный процесс. Двухцепочечные малые интерферирующие миРНК в 19-23 нуклеотида специфически связываются с комплементарной последовательностью своей матричной мРНК-мишени, направляя ее по пути деградации.
РНК-интерференция является составной частью системы генной регуляции, а именно контролирует/супрессирует трансляцию мРНК из эндогенных и экзогенных вирусных элементов и может быть использована для терапевтических целей. Для транзиентного выключения гена синтетические миРНК трансфецируют в клетки или ранние эмбрионы. Для стабильной генной репрессии последовательность миРНК должна быть инкорпорирована в геном в составе экспрессионной генной конструкции.
Очень эффективна комбинация лентивирусных векторов с миРНК для интеграции в геном. В противоположность классической нокаут-стратегии, которая требует длительного скрещивания для получения чистой линии с инактивированным геном в обоих локусах диплоидного генома, миРНК при интеграции могут легко выключить целевой ген в любой имеющейся линии животных.
Несмотря на разработанный широкий спектр методик получения трансгенных животных, в настоящее время пока отсутствует надежная и эффективная технология трансгеноза животных. Самые большие проблемы связаны с беспорядочным встраиванием экзогенной ДНК в геном при использовании большинства существующих методов. Так что дальнейшие качественные улучшения технологии необходимы в области разработки прицельной модификации клеточных генов и точного встраивания экзогенной ДНК в геном.
Тем более что геномы большинства хозяйственно важных организмов к настоящему времени полностью секвенированы и можно планировать будущую структуру трансгенного организма. Сочетание полностью расшифрованных последовательностей геномов с методами адресной доставки экзогенной ДНК позволит проводить целенаправленное конструирование трансгенных геномов с заранее заданными свойствами.
Источник