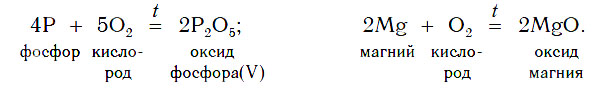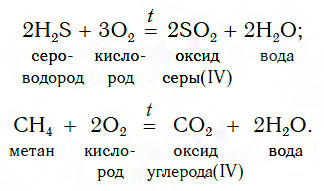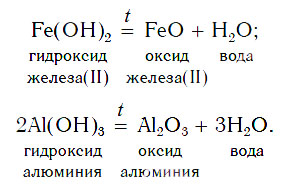- Основные оксиды — получение и химические свойства
- Получение основных оксидов
- Свойства основных оксидов
- Оксиды: классификация, получение и химические свойства
- Классификация оксидов
- Получение оксидов
- Химические свойства оксидов
- Химические свойства основных оксидов
- Урок 33. Получение и применение оксидов
- Получение оксидов
- Применение оксидов
- Основные, амфотерные, кислотные оксиды. Способы получения оксидов. Часть 1
- Основные, амфотерные, кислотные оксиды. Способы получения оксидов. Часть 1
Основные оксиды — получение и химические свойства
Основными называются такие оксиды, которым соответствуют основания. Например, Na2O, CaO являются основными оксидами, так как им соответствуют основания NaOH, Ca(OH)2 .
Получение основных оксидов
- Взаимодействие металла с кислородом:
Этот метод неприменим для щелочных металлов, которые при окислении обычно дают пероксиды и супероксиды, и только литий, сгорая, образует оксид Li2O.
2. Обжиг сульфидов:
Этим методом нельзя получить оксиды щелочных металлов.
3. Разложение нерастворимых оснований (при t):
4. Разложение солей кислородсодержащих кислот — чаще нитратов и карбонатов (при t):
Свойства основных оксидов
Большинство основных оксидов представляет собой твердые кристаллические вещества ионного характера, в узлах кристаллической решетки расположены ионы металлов, достаточно прочно связанные с оксид-ионами О —2 , поэтому оксиды типичных металлов обладают высокими температурами плавления и кипения.
1. Большинство основных оксидов не распадаются при нагревании, исключение составляют оксиды ртути и благородных металлов:
2. Типичные реакции с образованием солей:
| с кислотными оксидами: | BaO + SiO2 = BaSiO3 |
| с амфотерными оксидами: | MgO + Al2O3 = Mg(AlO2)2 |
| с кислотами: | СaО + Н2SО4 = CaSО4 + Н2О |
3. Оксиды щелочных и щелочноземельных металлов непосредственно реагируют с водой:
4. Как и все другие типы оксидов, основные оксиды могут вступать в окислительно-восстановительные реакции:
Источник
Оксиды: классификация, получение и химические свойства
Оксиды — это сложные вещества, состоящие из атомов двух элементов, один из которых — кислород со степенью окисления -2. При этом кислород связан только с менее электроотрицательным элементом.
В зависимости от второго элемента оксиды проявляют разные химические свойства. В школьном курсе оксиды традиционно делят на солеобразующие и несолеобразующие. Некоторые оксиды относят к солеобразным (двойным).
Двойные оксиды — это некоторые оксиды , образованные элементом с разными степенями окисления.
Солеобразующие оксиды делят на основные, амфотерные и кислотные.
Основные оксиды — это оксиды, обладающие характерными основными свойствами. К ним относят оксиды, образованные атомами металлов со степень окисления +1 и +2.
Кислотные оксиды — это оксиды, характеризующиеся кислотными свойствами. К ним относят оксиды, образованные атомами металлов со степенью окисления +5, +6 и +7, а также атомами неметаллов.
Амфотерные оксиды — это оксиды, характеризующиеся и основными, и кислотными свойствами. Это оксиды металлов со степенью окисления +3 и +4, а также четыре оксида со степенью окисления +2: ZnO, PbO, SnO и BeO.
Несолеобразующие оксиды не проявляют характерных основных или кислотных свойств, им не соответствуют гидроксиды. К несолеобразующим относят четыре оксида: CO, NO, N2O и SiO.
Классификация оксидов
Получение оксидов
Общие способы получения оксидов:
1. Взаимодействие простых веществ с кислородом :
1.1. Окисление металлов: большинство металлов окисляются кислородом до оксидов с устойчивыми степенями окисления.
Например , алюминий взаимодействует с кислородом с образованием оксида:
Не взаимодействуют с кислородом золото, платина, палладий.
Натрий при окислении кислородом воздуха образует преимущественно пероксид Na2O2,
Калий, цезий, рубидий образуют преимущественно пероксиды состава MeO2:
Примечания : металлы с переменной степенью окисления окисляются кислородом воздуха, как правило, до промежуточной степени окисления (+3):
Железо также горит с образованием железной окалины — оксида железа (II, III):
1.2. Окисление простых веществ-неметаллов.
Как правило, при окислении неметаллов образуется оксид неметалла с высшей степенью окисления, если кислород в избытке, или оксид неметалла с промежуточной степенью окисления, если кислород в недостатке.
Например , фосфор окисляется избытком кислорода до оксида фосфора (V), а под действием недостатка кислорода до оксида фосфора (III):
Но есть некоторые исключения .
Например , сера сгорает только до оксида серы (IV):
Оксид серы (VI) можно получить только окислением оксида серы (IV) в жестких условиях в присутствии катализатора:
2SO2 + O2 = 2SO3
Азот окисляется кислородом только при очень высокой температуре (около 2000 о С), либо под действием электрического разряда, и только до оксида азота (II):
Не окисляется кислородом фтор F2 (сам фтор окисляет кислород). Не взаимодействуют с кислородом прочие галогены (хлор Cl2, бром и др.), инертные газы (гелий He, неон, аргон, криптон).
2. Окисление сложных веществ (бинарных соединений): сульфидов, гидридов, фосфидов и т.д.
При окислении кислородом сложных веществ, состоящих, как правило, из двух элементов, образуется смесь оксидов этих элементов в устойчивых степенях окисления.
Например , при сжигании пирита FeS2 образуются оксид железа (III) и оксид серы (IV):
Сероводород горит с образованием оксида серы (IV) при избытке кислорода и с образованием серы при недостатке кислорода:
А вот аммиак горит с образованием простого вещества N2, т.к. азот реагирует с кислородом только в жестких условиях:
А вот в присутствии катализатора аммиак окисляется кислородом до оксида азота (II):
3. Разложение гидроксидов. Оксиды можно получить также из гидроксидов — кислот или оснований. Некоторые гидроксиды неустойчивы, и самопроизвольную распадаются на оксид и воду; для разложения некоторых других (как правило, нерастворимых в воде) гидроксидов необходимо их нагревать (прокаливать).
гидроксид → оксид + вода
Самопроизвольно разлагаются в водном растворе угольная кислота, сернистая кислота, гидроксид аммония, гидроксиды серебра (I), меди (I):
2AgOH → Ag2O + H2O
2CuOH → Cu2O + H2O
При нагревании разлагаются на оксиды большинство нерастворимых гидроксидов — кремниевая кислота, гидроксиды тяжелых металлов — гидроксид железа (III) и др.:
4. Еще один способ получения оксидов — разложение сложных соединений — солей .
Например , нерастворимые карбонаты и карбонат лития при нагревании разлагаются на оксиды:
Соли, образованные сильными кислотами-окислителями (нитраты, сульфаты, перхлораты и др.), при нагревании, как правило, разлагаются с с изменением степени окисления:
Более подробно про разложение нитратов можно прочитать в статье Окислительно-восстановительные реакции.
Химические свойства оксидов
Значительная часть химических свойств оксидов описывается схемой взаимосвязи основных классов неорганических веществ.
Химические свойства основных оксидов
Подробно про химические свойства оксидов можно прочитать в соответствующих статьях:
Источник
Урок 33. Получение и применение оксидов
В уроке 33 «Получение и применение оксидов» из курса «Химия для чайников» узнаем как получать оксиды различными способами, а также познакомимся с широким спектром применения оксидов во всех отраслях промышленности и быта.
Получение оксидов
1. Взаимодействие простых веществ с кислородом
Некоторые оксиды образуются в результате сжигания в кислороде (или на воздухе) соответствующих простых веществ. Так можно получить оксиды углерода(IV), серы(IV), фосфора(V), магния и других неметаллов и металлов:
2. Взаимодействие сложных веществ с кислородом
Оксиды можно получать также сжиганием в кислороде (или на воздухе) некоторых сложных веществ, например:
3. Термическое разложение нерастворимых оснований
Применение оксидов
Один из наиболее широко использующихся оксидов — вода H2O, о применении которой в быту, технике и ромышленности вы уже знаете.
Разнообразное применение находят и некоторые другие оксиды. Так, например, из оксида железа(III) Fe2O3, входящего в состав железных руд, в промышленности получают железо, а из оксида алюминия Al2O3 — алюминий. Оксид алюминия применяют также для изготовления искусственных драгоценных камней — рубина и сапфира. Мелкие кристаллы этого оксида применяются также в производстве наждачной бумаги.
Оксид углерода(IV) (углекислый газ) используют в пищевой промышленности для изготовления всех газированных напитков, для увеличения срока сохранности фруктов и овощей. Этим веществом наполняют углекислотные огнетушители. Твердый оксид углерода(IV) под названием «сухой лед» (рис. 117) применяют для хранения мороженого, для сильного охлаждения различных материалов.
Достаточно широко используется и оксид серы(IV) SO2 (сернистый газ). Он находит применение в производстве серной кислоты, для дезинфекции складских помещений, уничтожения вредных насекомых и бактерий, отбеливания бумаги.
Оксид кремния(IV) SiO2 в виде кварцевого песка используется в производстве стекла и бетона. Вместе с оксидом свинца(II) PbO он применяется для изготовления полудрагоценных камней и украшений («кристаллы Сваровски»).
Оксид кальция СaO под названием «негашеная известь» применяют при изготовлении различных строительных материалов. Оксиды некоторых других металлов находят применение в производстве красок. Так, например, Fe2O3 используют для изготовления краски коричневого, Сr2O3 — зеленого, ZnO и TiO2 — белого цветов.
Краткие выводы урока:
- Оксиды образуются при взаимодействии кислорода с простыми и сложными веществами.
- Оксиды можно получить термическим разложением нерастворимых оснований.
- Оксиды находят широкое практическое применение в промышленности и в быту.
- Оксиды — вода H2O и углекислый газ СО2 — участвуют в процессе фотосинтеза.
Надеюсь урок 33 «Получение и применение оксидов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Источник
Основные, амфотерные, кислотные оксиды. Способы получения оксидов. Часть 1
Основные, амфотерные, кислотные оксиды. Способы получения оксидов. Часть 1
Мы продолжаем с вами рассматривать оксиды. Давайте вспомним характерные свойства амфотерных, кислотных, основных оксидов и еще рассмотрим частные случаи (вы с ними можете столкнуться при решении второй части заданий ЕГЭ по химии.
Итак, оксиды – это бинарные соединения (состоящие из двух элементов), содержащих атомы кислорода в степени окисления -2. Мы не рассматриваем сейчас понятие сложных оксидов. С ними познакомимся чуть позже в отдельных статьях для тех, кто хочет знать немного больше, чем на сто баллов ЕГЭ по химии.
Классификация оксидов.
Оксиды делятся на солеобразующие и несолеобразующие. Солеобразующие оксиды – оксиды которые в реакциях с кислотами и щелочами образуют соли. Несолеобразующие оксиды – неиндифферентные оксиды. Таким оксидам соли не соответствуют (примеры несолеобразующих оксидов- монооксид азота, монооксид кремния, угарный газ.
Основные оксиды – оксиды, которые вступают в реакцию с кислотами с образованием солей. Основным оксидам соответствуют гидроксиды. Нетрудно догадаться, что к ним относятся оксиды щелочных и щелочноземельных элементов.
Кислотные оксиды – оксиды, при реакции с щелочами образующие соли. К ним относятся диоксид углерода, оксид фосфора. Вообще этим оксидам соответствуют кислоты. К примеру диоксиду углерода соответствует угольная кислота.
Кислотными оксидами являются все солеобразующие оксиды неметаллов и оксиды металлов в высоких степенях окисления. Кстати, кислотные оксиды имеют еще название ангидридов кислот.
Амфотерные оксиды – оксиды проявляющие свойства и кислотных и основных оксидов. Они вступают в реакции с кислотами и с основаниями с образованием солей. Амфотерным оксидам отвечают амфотерные основания. Амфотерными оксидами являются оксиды металлов в средних степенях окисления (в основном +3, +4).
В случае если металл проявляет разные степени окисления и образует несколько оксидов, то чем выше степень окисления металла, тем более кислотный характер имеет этот оксид.
Химические свойства оксидов
Основные оксиды вступаю в реакцию с водой с образованием оснований, при условии, что последние растворимы. Оксиды, которым соответствуют нерастворимые основания с водой не реагируют. Все основные оксиды вступают в реакцию с кислотами с образованием соли и воды.
Ангидриды в реакции с водой образуют кислоты. Большинство кислотных оксидов реагирует с водой. Но если у нас в наличии оксид нерастворимой кислоты, то такой оксид с водой не реагирует. Со щелочами кислотные оксиды реагируют с образованием соли и воды.
Основные оксиды с кислотными оксидами взаимодействуют между собой образуя соли (к примеру оксид магния в реакции с диоксидом углерода дает карбонат магния).
Получение оксидов
Оксиды в основном можно получить реакцией соединения простого вещества с кислородом при высокой температуре.
Еще один способ получения оксидов – разложение соответствующих кислот и оснований, солей (например, гидроксид меди при нагревании разлагается на оксид меди и воду, а нитрат свинца дает оксид свинца, диоксид азота и кислород.)
Еще один способ получения отдельно взятых оксидов – окисление сложных веществ кислородом.
Частные способы получения оксидов
Как уже было указано выше, оксиды, образующиеся сильно эндотермически, можно получить синтезом из простых веществ. Имеет место для элементов первой-четвертой группы.
К примеру, оксид алюминия мы можем получить синтезом из простых веществ. Если этот процесс заморозить – то он протекает экзотермически (вы, конечно же, помните, что такое экзотермическая реакция). Помним, что у алюминия есть один неспаренный электрон в основном состоянии, а возбуждение атома алюминия с переходом одного электрона на свободные орбитали 3р-подуровня трех неспаренных электронов происходит легко. Это и поясняет. Кстати, почему алюминий трехвалентный.
А теперь давайте посмотрим на классическую реакцию, которая имеет важное значение в топливной промышленности – получение оксида углерода
С(т)+СО2(г)=2СО(г) –энтальпия = 173 кДж
Реакция эндотермическая, значит необходимо повышение температуры для ее успешного протекания. При низких температурных режимах равновесие у нас смещается в сторону разложения монооксида углерода на углерод и углекислый газ. Налицо реакция диспропорционирования. Если мы заглянем в справочные таблицы, то увидим, что температуре порядка 400 градусов и давлении равном атмосферному, равновесие смещено в сторону разложения монооксида углерода практически полностью. А вот если температура у нас порядка 1000 градусов по шкале, то равновесие сдвинуто в сторону образования монооксида. А вот в температурном интервале 400-1000 градусов у нас налицо конкуренция прямой и обратной реакций. Что это значит? А то что если мы возьмем смесь чистого монооксида углерода или смесь диоксида углерода с углем в равных молярных долях и выдержать их при заданной температуре в этом интервале, то и в первом и во втором случае мы получим равновесную смесь угля, диоксида и монооксида углерода. При температуре около 700 градусов – соотношение моноокида углерода и диоксида углерода будут идентичными, но если начать медленно охлаждать СО, который получили при нагревании до 1000 градусов, то равновесие у нас сместится в нужном направлении, концентрация СО постепенно снижается и при достижении 400 градусов в системе уже СО не будет. Но! При температуре ниже 300 градусов, то реакция разложения СО протекает крайне медленно, а при комнатной температуре скорость ее почти равна нулю. Отсюда следует верный вывод: если монооксид углерода, полученный при высокой температуре, резко охладить, то удастся его сохранить при комнатной температуре в метастабильном состоянии. На этом и основан промышленный метод получения СО.
Понятное дело, что намного тяжелее получать те кислородные соединения, которые при обычных условиях существуют только за счет замороженности процесса распада. Классика жанра – оксиды азота.
Как вы думаете почему оксиды азота имеют очень низкую стабильность? Это результат исключительной прочности молекулы азота. Только представьте: образование одного моля молекулы азота из свободных атомов азота сопровождается выделением 945 кДж. Именно поэтому смесь 1 моля азота с 1 и моль кислорода энергетически более выгодное состояние, нежели 2 моль оксида азота. Поэтому, ввиду эндотермичности процесса получения двухвалентного оксида азота, последний может быть получен только при очень высокой температуре. Как вариант – в электрической дуге.
На практике это выглядит так: через трубку с электрической дугой, растянутую магнитным полем в виде диска диаметром в несколько метров, продувают воздух. Скорость продувания воздуха должна быть настолько большой, чтобы результирующая газовая смесь быстро проскакивала зону промежуточных температур, где может пройти обратный процесс – превращение монооксида азота в азот и кислород. Ниже восьмиста градусов процесс распада монооксида азота уже практически заморожен и его в принципе можно сохранить. При температуре 3200 градусов доля выхода NO составляет порядка 4%.
Как видите описанный процесс требует огромных затрат энергии, поэтому, большая часть оксидов азота, требуемых для производства азотной кислоты получают в основном другим способом –каталитическим окислением аммиака. В отсутствие катализатора аммиак горит в кислороде с образованием азота и воды.
На поверхности катализатора из платины или ее сплава с палладием идет иной процесс – образование двухвалентного оксида азота и воды. Соединение NO эндотермичное, а вода – экзотермичное. Сам процесс экзотермичный.
NО легко присоединяет кислород с образованием четырехвалентного оксида азота. Последний в свою очередь растворяется в воде и дает смесь азотной и азотистой кислоты. Азотистая кислота крайне неустойчивая и разлагается по уравнению:
Полученный NO2 вновь может реагировать с водой. Если растворение NO2 в воде происходит в присутствии воздуха, то NO окисляется до NO2, который опять вступает в реакцию с водой. В итоге весь четырехвалентный оксид азота превращается в азотную кислоту.
В следующей статье мы с вами рассмотрим еще один пример как один оксид получают из другого оксида того же элемента.
Источник