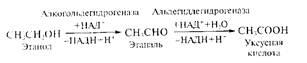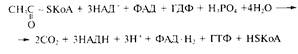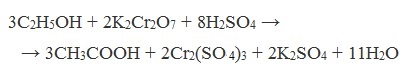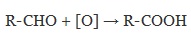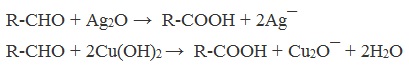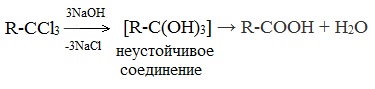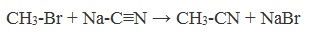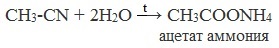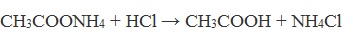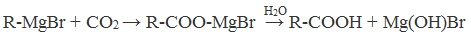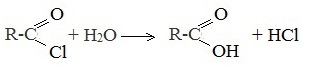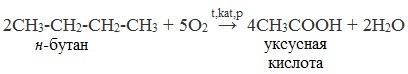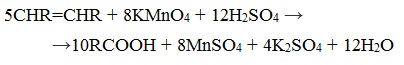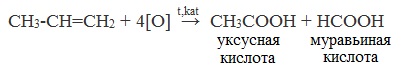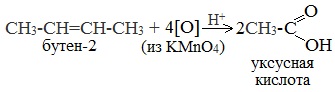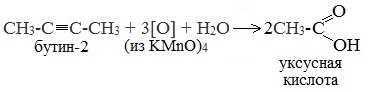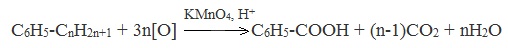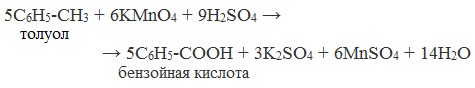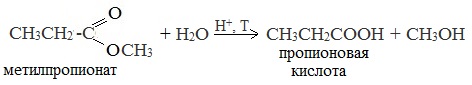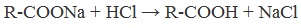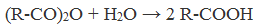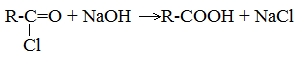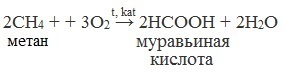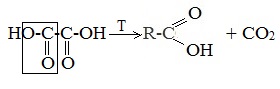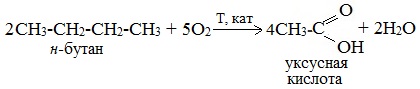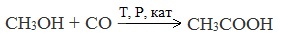ПОЛУЧЕНИЕ ОРГАНИЧЕСКИХ КИСЛОТ
РЕФЕРАТ
Тема: Получение органических кислот.
Группа 342 (ЦБП), д/о
Содержание.
2. Получение органических кислот………………………………………………………………. 3
Микробиологические методы производства аминокислот…………………………………. 8
Введение
В настоящее время биотехнологическими способами в промышленных масштабах синтезируют ряд органических кислот. Из них лимонную, глюконовую, кетоглюконовую и итаконовую кислоты получают лишь микробиологическим способом, молочную, салициловую и уксусную — как химическим, так и микробиологическим способами, а яблочную — химическим и энзиматическим путем.
ПОЛУЧЕНИЕ ОРГАНИЧЕСКИХ КИСЛОТ.
Получение уксусной кислоты. Уксусная кислота имеет наиболее важное значение среди всех органических кислот. Ее используют при выработке многих химических веществ, включая каучук, пластмассы, волокна, инсектициды. Микробиологический способ получения уксусной кислоты состоит в конверсии этанола в уксусную кислоту при участии бактерий штаммов Acetobacter и Gluconobacter:
Процесс идет в анаэробных условиях в режиме непрерывного культивирования продуцента. Для роста бактерии Acetobacter aceti используют питательные среды, содержащие 6-12% этилового спирта, 1 % бактериального гидролизата, 0,05 % дигидрофосфата калия, 0,1% гидрофосфата аммония и 0,05% сульфата магния. Максимальная удельная активность непрерывной культуры Acetobacter aceti (количество микрограммов субстрата, подвергшегося окислению 1мкг биомассы за 1 мин) достигается к 20-м суткам культивирования при концентрации спирта 7 % и составляет 3,0 ед./мг.
Получение лимонной кислоты. Лимонную кислоту широко используют в пищевой, фармацевтической и косметической промышленности. Ею заменяют фосфаты в составе детергентов, так как она полностью метаболизируется живыми организмами. Лимонная кислота образует хелаты с металлами, поэтому ее применяют для их очистки. Объем мирового производства цитрата составляет 400 тыс. т/год. Самый крупный производитель лимонной кислоты США. Производство лимонной кислоты принадлежит к числу старейших промышленных микробиологических процессов: оно было организовано в 1893 г. С этого момента параллельно развитию фундаментальной микробиологии велись изыскания оптимальных продуцентов и технологических вариантов процесса ферментации.
Для промышленного производства лимонной кислоты используют главным образом культуру гриба Acetobacter niger, а также Acetobacter wentii.
Метаболическим источником лимонной кислоты в организме служит цикл трикарбоновых кислот — составная часть цикла Кребса. Суммарное уравнение химических процессов этого цикла следующее:
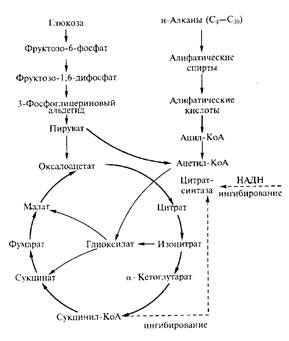
Реакция образования лимонной кислоты, катализируемая цитратсинтазой, открывает цикл Кребса, в котором цитрат постепенно окисляется до щавелево-уксусной кислоты (ЩУК). ЩУК снова конденсируется с ацетил-КоА, так что вновь образуется лимонная кислота (рис.1). Цитратсинтаза определяет скорость реакций, составляющих цикл Кребса. Активность фермента зависит от концентрации ЩУК, содержание которой может поддерживаться за счет функционирования конститутивной пируваткарбоксилазы, обеспечивающей переключение в аэробных условиях процессов гликолиза и глиоксилевого цикла.
Рис. 1. Схема биосинтеза лимонной кислоты
синтазы тормозится НАДН и сукцинил — КоА. Скорость оборота цикла Кребса определяется поддержанием необходимого уровня окисленных форм коферментов дегидрогеназ (НАД + и ФАД; см. уравнение реакции), поэтому высокий выход цитрата получается лишь при условии хорошей аэрации. Накопление в культуральной среде существенных количеств цитрата — промежуточного соединения цикла Кребса — невыгодно для организма и является следствием дисбаланса метаболизма или нарушения его генетической природы. Рост культуры грибов обычно регулируют путем изменения содержания фосфата, ионов марганца, железа и цинка в среде. Дефицит фосфата ведет к сверхпродукции цитрата. Роль ионов металлов не до конца установлена. Считают, что дефицит ионов металлов влияет на свойства клеточных мембран и морфологию гиф.
Процесс ферментации, ведущий к образованию лимонной кислоты, проводят при низких значениях рН (3-4), что облегчает поддержание стерильных условий ферментации и уменьшает возможность образования побочных продуктов. В более щелочной среде происходит накопление щавелевой и глюконовой кислот. Предполагают, что в кислой среде стимулируется гликолиз, что обеспечивает направление потока углерода в цикл Кребса.
Питательные среды для культивирования продуцентов лимонной кислоты в качестве источника углерода содержат дешевое углеводное сырье: мелассу, крахмал и глюкозный сироп. Гриб Acetobacter niger чаще всего выращивают на мелассе. Гриб Trichoderma viride синтезирует значительные количества цитрата из глюкозы, что позволяет использовать для этого процесса целлюлозу. Предложены штаммы бактерий и дрожжей рода Candida, осуществляющие процесс на основе н-парафинов (С9-С30), которые пока широко не внедрены в промышленность.
Существует несколько технологических вариантов промышленного производства лимонной кислоты. Первоначально был разработан вариант процесса, основывающийся на поверхностной ферментации, позднее — на глубинном культивировании. Последнее ведется в две стадии: на первой стадии идет рост мицелия, а на второй, после выхода культуры в стационарную фазу — интенсивный синтез лимонной кислоты. В конце ферментации массу мицелия отделяют путем фильтрования и промывают. Затем при рН
Источник
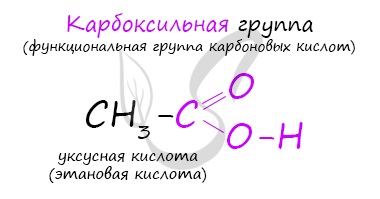
Карбоновые кислоты
Карбоновые кислоты — класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп COOH.
Имеют разнообразное промышленное применение и большое биологическое значение. Общая формула одноосновных карбоновых кислот CnH2nO2 .
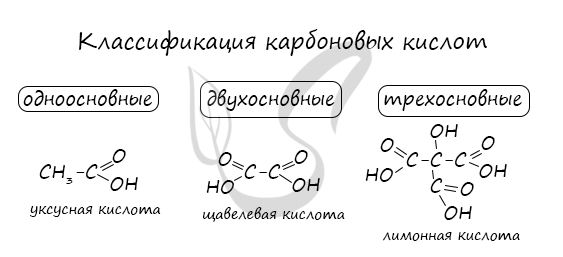
Классификация карбоновых кислот
По количеству карбоксильных групп в молекуле карбоновые кислоты подразделяются на:
- Одноосновные — 1 карбоксильная группа
- Двухосновные — 2 карбоксильных группы
- Трехосновные — 3 карбоксильных группы
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
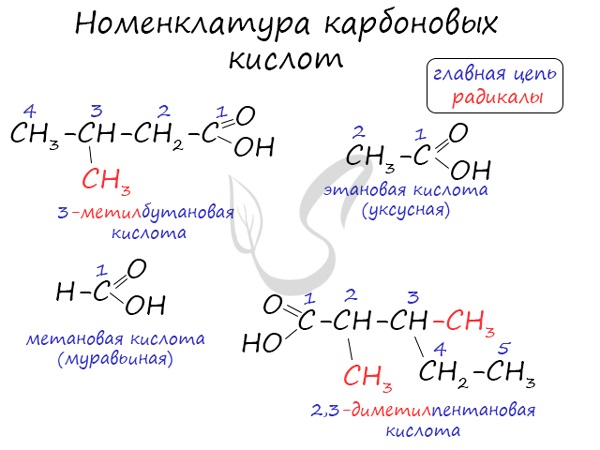
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Многие карбоновые кислоты имеют тривиальные названия. Наиболее известные:
- Метановая — HCOOH — муравьиная кислота
- Этановая — CH3-COOH — уксусная кислота
- Пропановая — C2H5-COOH — пропионовая кислота
- Бутановая — C3H7-COOH — масляная кислота
- Пентановая — C4H9-COOH — валериановая кислота
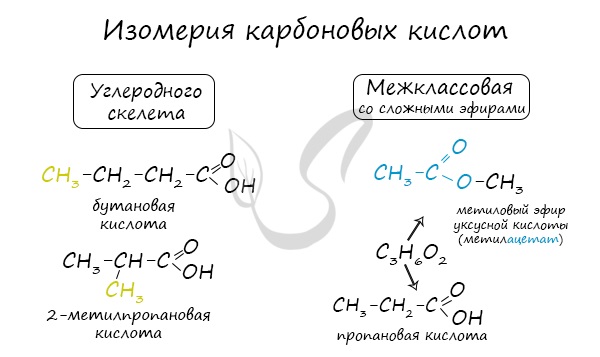
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
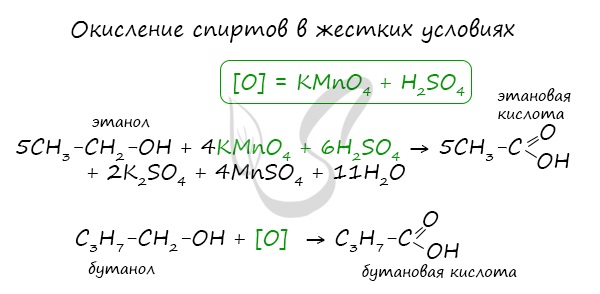
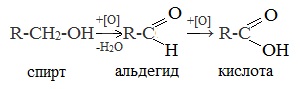
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
При окислении альдегиды образуют соответствующие карбоновые кислоты. Окисление можно проводить качественной реакцией на альдегиды — реакцией серебряного зеркала.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
Окисление альдегидов также может быть успешно осуществлено другим реагентом — свежеосажденным гидроксидом меди II. В результате такой реакции образуется осадок кирпично-красного цвета оксида меди I.
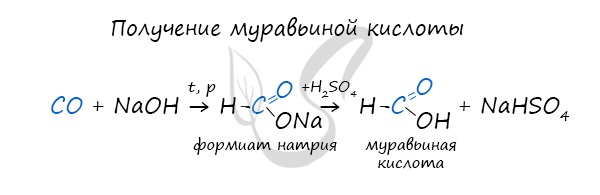
Существует специфический способ получения муравьиной кислоты, который заключается в реакции твердого гидроксида щелочного металла с угарным газом под давлением и температуре 200°С — образуется формиат (соль муравьиной кислоты).
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
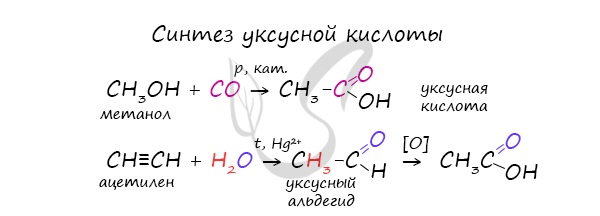
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
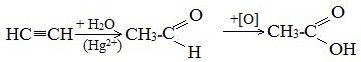
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
Галогенирование происходит по типу замещения в радикале, который соединен с карбоксильной группой. Напомню, что наиболее легко замещается водород у третичного, чуть сложнее — у вторичного, и значительно сложнее — у первичного атома углерода.
Сила карбоновых кислот тем выше, чем меньше электронной плотности сосредоточено на атоме углерода в карбоксильной группе. Поэтому самая слабая из трех кислот — уксусная, чуть сильнее — хлоруксусная, за ней — дихлоруксусная и самая сильная — трихлоруксусная.
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
Сложные эфиры
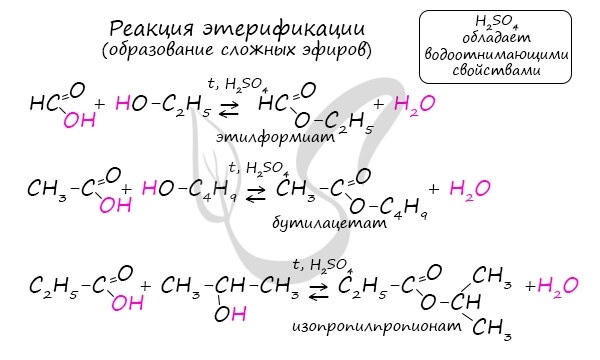
Получение сложных эфиров происходит в реакции этерификации (лат. aether — эфир), заключающейся во взаимодействии карбоновой кислоты и спирта.
Названия сложных эфиров формируются в зависимости от того, какой кислотой и каким спиртом эфир образован. Примеры:
- Метановая кислота + метанол = метиловый эфир метановой кислоты (метилформиат)
- Этановая кислота + этанол = этиловый эфир уксусной кислоты (этилацетат)
- Метановая кислота + этанол = этиловый эфир метановой кислоты (этилформиат)
- Пропановая кислота + бутанол = бутиловый эфир пропионовой кислоты (бутилпропионат)
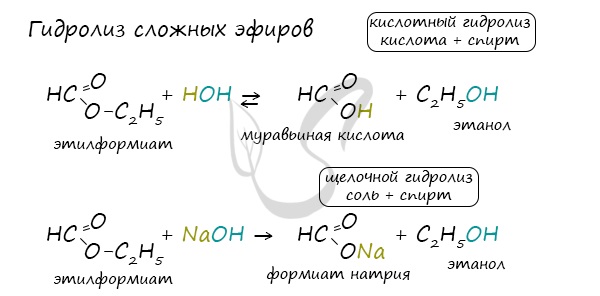
Для сложных эфиров характерной реакцией является гидролиз — их разложение. Возможен щелочной гидролиз, при котором образуется соль кислоты и спирт, и кислотный гидролиз, при котором образуются исходные спирт и кислота.
Кислотный гидролиз протекает обратимо, щелочной — необратимо. Реакция щелочного гидролиза по-другому называется реакция омыления, и напомнит о себе, когда мы дойдем до темы жиров.
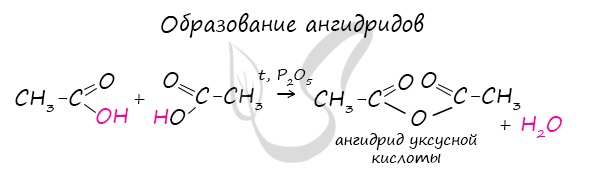
Ангидриды
Ангидриды — химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
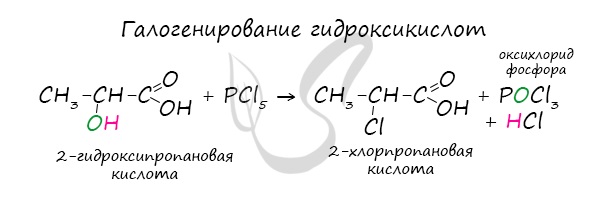
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
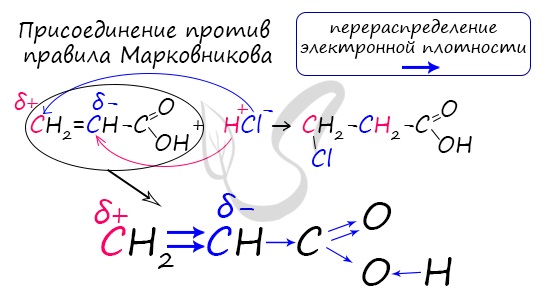
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Способ получения органических кислот
Некоторые карбоновые кислоты встречаются в природе в свободном состоянии (муравьиная, уксусная, масляная, валериановая и др.). Однако, основным источником карбоновых кислот является органический синтез. Рассмотрим основные способы получения карбоновых кислот
Общие способы получения карбоновых кислот
1. Окисление первичных спиртов и альдегидов под действием различных окислителей
В качестве окислителей применяют KMnO4 и K2Cr2O7.
Например:
Для окисления альдегидов используются те же реагенты, что и для спиртов.
При окислении перманганатом калия происходит обесцвечивание фиолетово-розового раствора.
При окислении дихроматом калия — цвет меняется с оранжевого на зеленый.
А также для них характерны реакции «серебряного зеркала» и окисление гидроксидом меди (II) – качественные реакции альдегидов:
2. Гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода
В результате реакции образуются спирты, содержащие три группы ОН у одного атома углерода. Такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
3. Получение карбоновых кислот из цианидов (нитрилов)
Этот способ позволяет наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия:
Образующийся нитрил уксусной кислоты CH3-CN (ацетонитрил, метилцианид) при нагревании гидролизуется с образованием ацетата аммония:
При подкислении раствора выделяется кислота:
4. Использование реактива Гриньяра (по схеме)
5. Гидролиз галогенангидридов кислот
С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту:
В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
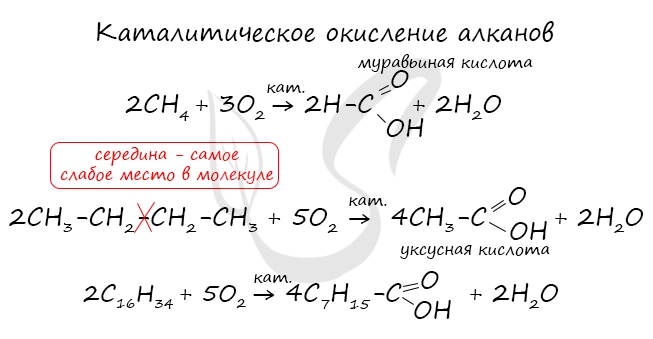
2. Окисление алканов кислородом воздуха ( в присутствии катализаторов – солей марганца или при нагревании под давлением)
Обычно образуется смесь кислот. При окислении бутана единственным продуктом является уксусная кислота:
3. Окисление алкенов и алкинов
При жестком окислении алкенов кипящим раствором KMnO4 в кислой среде происходит полный разрыв двойной связи:
При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты:
4. Окисление гомологов бензола (получение бензойной кислоты)
Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия:
В лаборатории
1. Гидролиз сложных эфиров
При кислотном гидролизе получают карбоновые кислоты и спирты (реакция обратная этерификации):
2. Из солей карбоновых кислот
3. Гидролиз ангидридов кислот
При легком нагревании с водой ангидриды образуют соответствующие карбоновые кислоты:
4. Щелочной гидролиз галоген производных карбоновых кислот
Специфические способы получения важнейших кислот
Способы получения НСООН
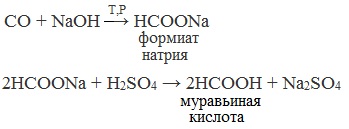
1. Взаимодействие оксида углерода (II) с гидроксидом натрия
Муравьиную кислоту получают нагреванием под давлением гидроксида натрия и оксида углерода (II) под давлением и обработкой полученного формиата натрия серной кислотой:
2. Каталитическое окисление метана
3. Декарбоксилирование щавелевой кислоты
Муравьиную кислоту можно получить при нагревании щавелевой кислоты:
Способы получения СН3СООН
Получение уксусной кислоты для химических целей
1. Синтез из ацетилена
Данный способ получения уксусной кислоты основан на окислении уксусного альдегида, который в свою очередь получают из ацетилена по реакции Кучерова (ацетилен получают из очень доступного сырья — метана):
2. Каталитическое окисление бутана
Большое значение имеет способ получения уксусной кислоты, основанный на окислении бутана кислородом воздуха:
Процесс получения уксусной кислоты из метана является многостадийным (метан – ацетилен – уксусный альдегид – уксусная кислота). Ее получение окислениям будана сокращает число стадий, что дает большой экономический эффект.
3. Каталитическое карбонилирование метанола
Получение уксусной кислоты для пищевых целей
4. Уксуснокислое брожение этанола
Уксусную кислоту для пищевых целей получают уксуснокислым брожением жидкостей, содержащих спирт (вино. пиво):
Источник