Получение, применение натрия и калия.
Натрий получают электролизом расплавленного хлорида натрия или гидроксида натрия. При электролизе расплава NaCl на катоде выделяется натрий:
А на аноде – хлор:
При электролизе расплава NaOH на катоде выделяется натрий (уравнение реакции приведено выше), а на аноде – вода и кислород:
4OH — — 4e — = 2H 2 O + O2
Вследствие дороговизны гидроксида натрия основным современным методом получения натрия является электролиз расплава NaCl.
Калий также можно получить электролизом расплавленных KCl и KOH. Однако этот способ получения калия не нашел распространения из-за технических трудностей (низкий выход по току, трудность обеспечения техники безопасности). Современное промышленное получение калия основано на следующих реакциях:
KCl + Na Û NaCl + K (а)
KOH + Na Û NaOH + K (б)
В способе (а) через расплавленный хлорид калия пропускают пары натрия при 800 0 С, а выделяющиеся пары калия конденсируют. В способе (б) взаимодействие между расплавленным гидроксидом калия и жидким натрием осуществляется противотоком при 440 0 С в реакционной колонне из никеля1.
Этими же способами получают сплав калия с натрием, который применяется как жидкий металлический теплоноситель в атомных реакторах.
Сплав калия с натрием используется также в качестве восстановителя в производстве титана.
Калий и его соединения широко используются в различных отраслях хозяйства. Пероксид элемента № 19 необходим при получении некоторых красителей, при гидролизе крахмала, производстве пороха, отбелке тканей. Регенерация воздуха в космических кораблях и подводных лодках осуществляется с помощью все тех же пероксидов натрия и калия. Без едких щелочей не сваришь мыло. Причем самое лучшее-жидкое туалетное, а также специальные медицинские сорта получают, используя едкий калий. Поташ в больших количествах идет на производство стекла.
Физические свойства.
Поскольку в атомах щелочных металлов один внешний электрон приходится на 4 и более свободные орбитали, а энергия ионизации атомов низкая, то между атомами металлов возникает металлическая связь. Для вещества с металлической связью характерны металлический блеск, пластичность, мягкость, хорошая электрическая проводимость и теплопроводность. Такими свойствами обладают калий и натрий.
Натрий и калий – серебристо-белые металлы, плотность первого – 0,97г/см 3 , второго – 0,86 г/см 3 , очень мягкие, легко режутся ножом.
Природный натрий состоит из одного изотопа 

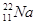
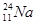

Химические свойства.
Атомы натрия и калия при химическом взаимодействии легко отдают валентные электроны, переходя в положительно заряженные ионы: Na + и K + . Оба металла – сильные восстановители.
На воздухе натрий и калий быстро окисляются, поэтому их хранят под слоем керосина. Они легко взаимодействуют со многими неметаллами – галогенами, серой, фосфором и др. Бурно реагируют с водой. С водородом при нагревании образуют гидриды NaH, KH. Гидриды металлов легко разлагаются водой с образованием соответствующей щелочи и водорода:
NaH + H2O = NaOH + H2
При сгорании натрия в избытке кислорода образуется пероксид натрия Na2O2, который взаимодействует с влажным углекислым газом воздуха, выделяя кислород:
2Na2O2 + 2CO2 = 2Na2CO3 + O2
На этой реакции основано применение пероксида натрия для получения кислорода на подводных лодках и для регенерации воздуха в закрытых помещениях.
Едкие щелочи.
Едкими щелочами называются хорошо растворимые в воде гидроксиды. Важнейшие из них NaOH и KOH.
Гидроксид натрия и гидроксид калия – белые, непрозрачные, твердые кристаллические вещества. В воде хорошо растворяются с выделением большого количества теплоты. В водных растворах практически нацело диссоциированы и являются сильными щелочами. Проявляют все свойства оснований.
Твердые гидроксиды натрия и калия и их водные растворы поглощают оксид углерода (IV):
или в иной форме:
OH — + CO2 = HCO
2OH — + CO2 = CO 
В твердом состоянии на воздухе NaOH и KOH поглощают влагу, благодаря чему используются как осушители газов.
В промышленности гидроксид натрия и гидроксид калия получают электролизом концентрированных растворов соответственно NaCl и KCl. При этом одновременно получаются хлор и водород. Катодом служит железная сетка, анодом – графит.
Схему электролиза (на примере KCl) следует представлять так, KCl полностью диссоциирует на ионы K + и Cl — . При прохождении электрического тока к катоду подходят ионы K + , к аноду – хлорид-ионы Cl — . Калий в ряду стандартных электродных потенциалов расположен до алюминия, и его ионы восстанавливаются (присоединяют электроны) гораздо труднее, чем молекулы воды. Ионов же водорода H + в растворе очень мало. Поэтому на катоде разряжаются молекулы воды с выделением молекулярного водорода:
Хлорид-ионы в концентрированном растворе легче отдают электроны (окисляются), чем молекулы воды, поэтому на аноде разряжаются хлорид-ионы:

2Cl — – 2e — = Cl2 1
Аналогично протекает электролиз раствора NaCl. Раствор, содержащий NaOH и NaCl, подвергается упариванию, в результате чего выпадает в осадок хлорид натрия (он имеет намного меньшую растворимость и она мало изменяется с температурой), который отделяют и используют для дальнейшего электролиза. Гидроксид натрия получают в очень больших количествах. Он является одним из важнейших продуктов основной химической промышленности. Применяют его для очистки нефтяных продуктов – бензина и керосина, для производства мыла, искусственного шелка, бумаги, в текстильной, кожевенной, химической промышленности, а также в быту (каустик, каустическая сода).
Более дорогой продукт – гидроксид калия – применяется реже, чем NaOH.
Соли натрия и калия.
Натрий образует соли со всеми кислотами. Почти все его соли растворимы в воде. Важнейшие из них – хлорид натрия (поваренная соль), сода и сульфат натрия.
Хлорид натрия NaCl – необходимая приправа к пище, используется для консервирования пищевых продуктов, а также служит сырьем для получения гидроксида натрия, хлора, соляной кислоты, соды и др.
Сульфат натрия Na2SO4 применяется в производстве соды и стекла. Из водных растворов кристаллизуется десятиводный гидрат Na2SO4 * 10H2O, называемый глауберовой солью. Глауберова соль применяется в медицине как слабительное. Соли натрия (ионы натрия) окрашивают пламя горелки в желтый цвет. Это очень чувствительный метод для обнаружения натрия в соединениях.
Калийные соли используют главным образом как калийные удобрения. Соли калия (ионы калия) окрашивают пламя горелки в фиолетовый цвет. Однако в присутствии даже ничтожных количеств соединений натрия фиолетовый цвет маскируется желтым. В этом случае его можно заметить через синее стекло, поглощающее желтые лучи.
Список использованной литературы.
Источник
Калий и натрий
- Краткая характеристика и нахождение в природе.
- История открытия.
- Физические свойства.
- Химические свойства.
- Едкие щелочи. Соли металлов.
- Способы получения и область применения.
- Краткая характеристика и нахождение в природе.
Натрий и калий относятся к числу довольно распространенных элементов.
Содержание натрия в земной коре составляет 2,64%, калия – 2,6%.
В свободном виде калий и натрий в природе не встречаются. Эти щелочные металлы входят в состав различных соединений. Одним из таких соединений является – хлорид натрия NaCl (образует залежи каменной соли — Донбасс, Соликамск, Соль-Илецк и др).
Также хлорид натрия содержится в морской воде и соляных источниках.
Калийные соли также присутствуют в морской воде, но в значительно меньших количествах. Обычно калийные соли содержат верхние слои залежей. Самые большие в мире запасы калийных солей находятся на Урале в районе Соликамска. В Белоруссии (г.Солигорск) открыты крупные залежи калийных солей
Мы не случайно рассматриваем натрий и калий вместе, сходные своими физическими свойствами, они и открыты были одновременно.
В 1807 г. Дэви, путем электролиза слегка увлажненных твердых щелочей, были получены свободные металлы — калий и натрий. В то время они получили названия — потассий (Potassium) и содий (Sodium).
В следующем году Гильберт, издатель известных «Анналов физики»,
предложил именовать новые металлы калием и натронием (Natronium).
Позднее Берцелиус сократил последнее название до «натрий» (Natrium).
Вообще, название «натрий» (англ. и франц. Sodium, нем. Natrium) происходит от древнего слова, распространенного в Египте, у древних греков (vixpov) и римлян и соответствует древнееврейскому нетер (neter).
В древнем Египте натроном, или нитроном называли щелочь, получаемую не только из природных содовых озер, но и из золы растений. Ее употребляли для мытья, изготовления глазурей, при мумификации
трупов. В конце XVIII в. Клапрот ввел для минеральной щелочи
название натрон (Natron), а для растительной — кали (Kali).
Известно, что в начале XIX в. в России натрий называли содием.
Что касается слова калий, то оно происходит от арабского термина
алкали (щелочные вещества, именуемые в средние века “щелочные соли”). В то время их еще не отличали друг от друга и называли именами, имевшими сходное значение: натрон, боракс, варек т. д. Слово кали (qila) впервые встречается в 850 г. у арабских писателей, затем начинает употребляться слово Qali (al-Qali), которое обозначало продукт, получаемый из золы некоторых
растений. В России, в первой четверти XIX в., калий назывался потассий, поташ, а также поташий. В 1828 г. в химической литературе наряду с названием поташ уже встречается название кали (едкое кали, кали соляный и др.).
Название калий стало общепринятым во всем мире после выхода в свет учебника Гесса.
Калий и натрий – серебристо-белые металлы, с плотностью
K = 0,86 г/см3, Na = 0,97г/см3,
Эти металлы очень мягкие, режутся ножом.
Обладают всеми свойствами, присущими веществам с металлической связью, а именно: металлический блеск, пластичность, мягкость, хорошая электрическая проводимость и теплопроводность.
Это обусловлено тем, что в атомах щелочных металлов один внешний электрон приходится на 4 и более свободные орбитали, а энергия ионизации атомов низкая, в следствии чего между атомами металлов возникает металлическая связь.
В природе натрий состоит из одного изотопа
калий – из двух стабильных изотопов
При химическом взаимодействии, атомы калия и натрия легко отдают валентные электроны, переходя в положительно заряженные ионы: K+ и Na+. Оба металла являются сильными восстановителями.
Быстро окисляются на открытом воздухе, поэтому необходимо хранить калий и натрий под слоем керосина.
Реакция с водой — бурная. Эти металлы легко взаимодействуют со многими неметаллами –серой, фосфором, галогенами и др.
Образуют гидриды NaH, KH, взаимодействуя с водородом, при нагревании. Эти гидриды легко разлагаются водой с образованием
соответствующей щелочи и водорода:
NaH + H2O = NaOH + H2
При сгорании натрия в избытке кислорода образуется пероксид натрия Na2O2, который в свою очередь взаимодействует с влажным углекислым газом воздуха, выделяя кислород:
2Na2O2 + 2CO2 = 2Na2CO3 + O2
На этой реакции основано применение пероксида натрия для получения кислорода на
подводных лодках и для регенерации воздуха в закрытых помещениях.
Едкие щелочи. Соли металлов.
Едкими щелочами называются хорошо растворимые в воде гидроксиды. Важнейшие из них NaOH и KOH.
Гидроксид натрия и гидроксид калия – белые, непрозрачные, твердые
кристаллические вещества. В воде хорошо растворяются с выделением большого количества теплоты. В водных растворах практически нацело диссоциированы и являются сильными щелочами. Проявляют все свойства оснований.
Твердые гидроксиды натрия и калия и их водные растворы поглощают оксид углерода (IV):
NaOH + CO2 = NaHCO3
2NaOH + CO2 = Na2CO3 + H2O
или в иной форме:
2OH- + CO2 = CO + H2O
В твердом состоянии на воздухе NaOH и KOH поглощают влагу, благодаря чему используются как осушители газов.
В промышленности гидроксид натрия и гидроксид калия получают электролизом концентрированных растворов соответственно NaCl и KCl. При этом одновременно получаются хлор и водород. Катодом служит железная сетка, анодом – графит.
Схему электролиза (на примере KCl) следует представлять так, KCl полностью диссоциирует на ионы K+ и Cl-. При прохождении электрического тока к катоду подходят ионы K+, к аноду – хлорид-ионы Cl-. Калий в ряду стандартных электродных потенциалов расположен до алюминия, и его ионы восстанавливаются
(присоединяют электроны) гораздо труднее, чем молекулы воды. Ионов же водорода H+ в растворе очень мало. Поэтому на катоде разряжаются молекулы воды с выделением молекулярного водорода:
2H2O + 2e- = H2 + 2OH-
Хлорид-ионы в концентрированном растворе легче отдают электроны (окисляются), чем молекулы воды, поэтому на аноде разряжаются хлорид-ионы:
Общее уравнение электролиза раствора в ионной форме:
2H2O + 2e- = H2 + 2OH- 1
2Cl- + 2H2O электролиз H2 + 2OH- + Cl2
2KCl + 2H2O электролиз H2 + 2KOH + Cl2
Аналогично протекает электролиз раствора NaCl. Раствор, содержащий NaOH и NaCl, подвергается упариванию, в результате чего выпадает в осадок хлорид натрия (он имеет намного меньшую растворимость и она мало изменяется с температурой), который отделяют и используют для дальнейшего электролиза. Гидроксид натрия получают в очень больших количествах. Он является одним из важнейших продуктов основной химической промышленности. Применяют его для очистки нефтяных продуктов – бензина и керосина, для производства мыла, искусственного шелка, бумаги, в текстильной, кожевенной, химической промышленности, а также в быту (каустик,каустическая сода).
Более дорогой продукт – гидроксид калия – применяется реже, чем NaOH.
Соли калия и натрия.
Практически все соли калия и натрия растворимы в воде.
Натрий способен образовывать соли со всеми кислотами.
Наиболее распространенными и используемыми в быту и промышленности являются – хлорид натрия NaCl (поваренная соль), сода и сульфат натрия Na2SO4.
Рассмотрим каждую из них в одельности.
Хлорид натрия NaCl – используется для консервирования пищевых продуктов, в качестве приправы при приготовлении пищи, является сырьем в промышленности при получения гидроксида натрия, хлора, соляной кислоты, соды и др.
Сульфат натрия Na2SO4 – используется в промышленности для приготовления глауберовой соли, путем кристаллизации десятиводного гидрата Na2SO4 * 10H2O.
Глауберова соль применяется в медицине как слабительное.
Соли натрия и калия (ионы натрия и калия), применяются при качественном обнаружении натрия и калия в соединениях.
Соли натрия окрашивают пламя горелки в желтый цвет.
Соли калия окрашивают пламя горелки в фиолетовый цвет.
Это очень чувствительный метод. Единственный его минус то, что в присутствии даже ничтожных количеств натрия в соединениях фиолетовый цвет маскируется желтым. В этом случае используют синее стекло, поглощающее желтые лучи.
Калийные соли используют главным образом как калийные удобрения.
- Получение и область применения.
Натрий получают в процессе электролиза расплавленного хлорида натрия или гидроксида натрия.
При электролизе расплава гидроксида натрия NaOH на катоде выделяется натрий:
а на аноде – вода и кислород:
4OH- — 4e- = 2H2O + O2
При электролизе расплава хлорида натрия NaCl на катоде выделяется натрий:
А на аноде – хлор:
Предпочтительнее, с экономической точки зрения, вследствие дороговизны гидроксида натрия,использовать в качестве основного метода электролиз расплава NaCl.
Также как и натрий, калий можно получить в процессе электролиза хлорида калия KCl и гидроксида калия KOH.
Но этот способ не получил широкого распространения, т.к. в процессе электролиза возник ряд технических трудностей, в том числе, трудность обеспечения техники безопасности.
На сегодняшний день получение калия в промышленности основано на следующих реакциях:
1. KCl + Na Ы NaCl + K
При получении калия этим способом, через расплавленный хлорид калия пропускают пары натрия при 8000С, а выделяющиеся пары калия конденсируют.
2. KOH + Na Ы NaOH + K
Здесь взаимодействие между расплавленным гидроксидом калия и жидким натрием осуществляется противотоком при температуре 4400С в реакционной колонне из никеля.
Также этими способами можно получать сплав калия с натрием. Этот сплав применяется:
в атомных реакторах, как жидкий металлический теплоноситель.
в качестве восстановителя при производстве титана.
Широко используют калий и его соединения в различных отраслях хозяйства:
- при получении некоторых красителей,
- при гидролизе крахмала,
- при производстве пороха,
- при отбелке тканей.
С помощью пероксидов натрия и калия проводится регенерация воздуха в космических кораблях и подводных лодках.
Поташ в больших количествах идет на производство стекла. Используя едкий калий производят самое лучшее — жидкое туалетное мыло.
1. “Пособие по химии для поступающих в вузы”. Г.П.Хомченко. 1976 г.
2. “Основы общей химии”. Ю.Д.Третьяков, Ю.Г.Метлин. Москва “Просвещение” 1980 г.
Ошибка в тексте? Выдели её мышкой и нажми 
Остались рефераты, курсовые, презентации? Поделись с нами — загрузи их здесь!
Источник


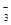

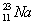 В природе натрий состоит из одного изотопа
В природе натрий состоит из одного изотопа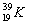 калий – из двух стабильных изотопов
калий – из двух стабильных изотопов


