- Технология получения карбида бора
- Способ получения карбида бора плазмохимическим методом Российский патент 2018 года по МПК C01B32/991
- Описание патента на изобретение RU2648421C2
- Похожие патенты RU2648421C2
- Реферат патента 2018 года Способ получения карбида бора плазмохимическим методом
- Формула изобретения RU 2 648 421 C2
Технология получения карбида бора
Карбид бора – В4С (торговая марка тетрабор) и изделия на его основе широко применяются в различных отраслях техники и промышленности, в порошковой металлургии, для изготовления конструкционной керамики (броневых плит, облицовочной брони кабин самолетов, вертолетов), противоударной одежды (бронежелетов), а также в атомной энергетике в качестве поглотителей тепловых нейтронов в регулируемых стержнях ядерных реакторов. В металлообрабатывающей отрасли В4С используется в шлифовально-полировочных операциях.
Температура плавления карбида В4С 2450 о С. Образование В4С из элементов представлено реакцией
и сопровождается изменением энергии Гиббса
∆G 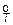
В соответствии с ГОСТ 5744-74 промышленность производит карбид бора, предназначенный для использования в свободном виде на шлифовально-полировальных операциях и для других указанных выше целей. Карбид бора поставляется в виде шлифзерна (номер 16), шлифовального порошка (номера 12, 10, 8, 6, 5, 3) и микропорошка (М40, М28, М20, М14, М10, М7, М5) по ГОСТ 3647-71. По химическому составу карбид бора должен удовлетворять требованиям ГОСТ 5744-74 (табл. 17.7).
Таблица 17.7. Химический состав, %, карбида бора
| Номер зернис-тости | В4С, не менее | Вобщ, не менее | В2О3, не более | Собщ, не более | Номер зернис- тости | В4С, не менее | Вобщ, не менее | В2О3, не более | Собщ, не более |
| 91,6 | 0,5 | М40,М14 | 92,0 | 0,20 | |||||
| 12-16 | 93,0 | 0,45 | М10, М7 | 84,0 | 0,25 | ||||
| 5-3 | 90,0 | 0,40 | М5 | 84,0 | 0,25 |
Химизм процесса в общем виде может быть представлен реакцией
являющейся суммой низкотемпературного превращения ортоборной кислоты
4Н3ВО3 
и основной высокотемпературной реакции
∆G 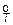
Условие ∆G 
Исходя из данных термодинамики, кинетики и механизма этого сложного процесса, разработан* процесс получения карбида бора с использованием ортоборной кислоты и углеродистого восстановителя в дуговой печи специально разработанной конструкции (рис. 17.5).
Разработана новая конструкция дуговой электропечи для выплавки карбида бора. Как следует из рис. 17.5, дуговая электропечь с установленной мощностью трансформатора 2000 кВ∙А имеет два металлических нефутерованных кожуха. Наружный кожух стационарный, внутренний – подвижный. Наружный кожух имеет диаметр 2 м и высоту 2 м, а внутренний – диаметр 1,6 м, высоту 1,2. Наружный кожух устанавливается на тележку – подину, а внутренний – подвешивается та тягах и может перемещаться по вертикали по ходу плавки карбида бора, для чего имеется механизм перемещения этого кожуха. Наружный кожух по верхней кромке переходит в так называемый ложный кожух, представляющий собой секционный
* Порада А.Н., Гасик М.И. Электротермия неорганических материалов. – М.: Металлургия, 1990. – 232с.
раструб высотой 0,5 м с верхним диаметром 3,1 м. Подина на тележке выкладывается из графитированных блоков сечения 0,4х0,4 м. Электропитание печи производится от трехфазного трансформатора типа ЭТМК 3200/10 мощностью 2000 кВ∙А, имеющего 12 ступеней напряжения на низкой стороне от 69,6 В до 145 В при токе 7–10 кА. Электроды используются графитированные диаметром 300 мм.
Рис. 17.5. Общий вид дуговой печи для выплавки карбида бора
1 – трос; 2 – стойка механизма перемещения электрода; 3 – гибкий кабель; 4 – проем; 5 – рукав электрододержателя; 6 – электрод; 7 — подвижный кожух; 8 – наружный кожух; 9 – подина; 10 – выкатная тележка
Подготовленная шихта для выплавки карбида бора засыпается в раструб и поступает в кольцевой зазор между наружным и внутренним кожухами. В процессе плавки внутренний кожух нагревается от электрических дуг реакционного расплава до 600–700 о С, вследствие чего борная кислота плавится, а шихтовая смесь (Н3ВО3 + углерод) приобретает подвижность. При этих температурах происходит дегидратация Н3ВО3 с образованием борного ангидрида В2О3 и Н2Опар. Шихта состоит из ортоборной кислоты Н3ВО3 (ГОСТ 1870-78) и углеродистого восстановителя с весьма малым содержанием золы (≤0,5%). Борная кислота содержит ³99,9% Н3ВО3 (марки А и Б) и ³99,6 (I сорт) ³98,6% (II сорт) Н3ВО3 (марка В). Компоненты шихты тщательно дозируются и в порошкообразном виде поступают в плавку.
Гетерогенный оксидноуглеродный расплав по мере подъема внутреннего кожуха самотеком поступает под электроды в зоны горения электрических дуг, которые практически закрыты этим расплавом. Поступление расплавившейся шихты под электроды регулируется скоростью (частотой) подъема внутреннего кожуха. Поступление шихты – расплава в реакционную зону (под электрические дуги) сообразуется со скоростью восстановительных реакций и, в конечном счете, со скоростью формирования из жидкой карбидборовой фазы блока карбида бора гомогенной структуры, по составу отвечающей формуле В4С.
По окончании плавки электроды, внутренний и ложный кожухи поднимаются, тележка–подина с наплавленным блоком карбида бора (массой 250–300 кг) выкатываются в основной пролет цеха. После охлаждения блока он передается на эстакаду для последующего дробления. Тележка–подина с установленным наружным кожухом закатывается на рабочее место для новой плавки.
Электропечи описанной конструкции и разработанной технологии электроплавки карбида бора позволяют получать блок карбида бора следующего состава, %: 75–77 Вобщ; 1–2 В2О3; 22–24 Собщ; 1–3 Ссвоб; 95–98 В4С.
На 1 т дробленого блока карбида бора расходуется 5,0 т борной кислоты, 1,6 т нефтяного кокса (или стружки от механической обточки графитированных электродов на электродных заводах); 0,15 т графитированных электродов, 18000 кВт∙ч электроэнергии.
Источник
Способ получения карбида бора плазмохимическим методом Российский патент 2018 года по МПК C01B32/991
Описание патента на изобретение RU2648421C2
Заявляемое изобретение относится к области техники получения поликристаллических материалов и может быть использовано для получения поликристаллического карбида бора, в том числе обогащенного одним из его изотопов (например, бором-10).
Карбид бора обладает рядом полезных для технического применения свойств. Высокая твердость дает возможность использовать его в качестве режущего и абразивного инструмента для обработки других материалов. Химическое применение карбида бора определяется его использованием в качестве компонента смесей для диффузионного борирования сталей, результатом которого является повышение твердости и износостойкости поверхности стали со значительным увеличением срока службы изделий. Являясь термодинамически устойчивым соединением, карбид бора применяется в химическом машиностроении в качестве деталей различных агрегатов, работающих в контакте с агрессивными и одновременно абразивными средами. Бор природного изотопного состава содержит два изотопа: бор-10 (19,8%) и бор-11 (80,2%). Первый обладает максимальным из известных для различных нуклидов сечением захвата тепловых нейтронов причем при захвате нейтрона образуются два нерадиоактивных ядра (альфа-частица и литий-7), очень быстро тормозящиеся в среде, а проникающая радиация (гамма-кванты) при этом отсутствует в отличие от аналогичных реакций захвата нейтронов другими нуклидами. Поэтому бор в составе борной кислоты, карбида и других химических соединений применяется в атомных реакторах для регулирования реактивности, а также для биологической защиты от тепловых нейтронов. Кроме того, бор применяется в нейтрон-захватной терапии рака. Эффективность применения бора для указанных целей значительно повышается в случае повышения концентрации изотопа бор-10 (изотопного обогащения).
Известен способ получения карбида бора спеканием элементов (S. Т. Benton and R. David: ‘Methods for preparing boron carbide articles’, US patent no. 3914371, 1975). Способ может быть использован при получении изотопно-обогащенного карбида бора: как правило, используют элементный бор, полученный методом электролиза расплавленных солей (например, US 20100294670 А1). Недостатком способа является высокая стоимость используемого реагента — элементного бора. Еще одним недостатком способа является загрязнение материала примесями, вызванное высокой температурой проведения процесса: в случае метода горячего прессования 1800°C-2200°C.
Известен способ получения карбида бора, основанный на реакции карботермического восстановления борной кислоты или борного ангидрида (F. Schroll and A. Vogt: ‘Electrothermic production of boron carbide’ US patent no. 2163293, 1939). Синтез карбида бора протекает в дуге высокой интенсивности. Дуга постоянного тока протекает между графитовыми электродами. Недостатками способа являются высокая температура синтеза 2300-2500°C и значительные потери бора.
Известен еще один способ получения карбида бора, основанный на реакции карботермического восстановления борной кислоты графитом в печи Ачесона (R.R. Ridgway: ‘Boron carbide and the method of making the same’, US patent no. 1897214, 1933). Недостатками метода также являются высокая температура синтеза и потери бора.
Известен способ получения карбида бора, основанный на реакции карботермического восстановления оксида бора в газовой фазе (В.Z. Dacic, V. Jokanovic, В. Jokanovic and М.D. Dramicanin: ‘Thermodynamics of gas phase carbothermic reduction of boronanhydride’, J. Alloys Compd, 2006, 413, 198-205). К недостаткам метода относится высокая температура синтеза.
Известен способ получения карбида бора, основанный на реакции магний термического восстановления оксида бора в присутствии углерода (Е.G. Gray: ‘Process for the production of boron carbide’, US patent no. 2834651, 1958). К недостаткам метода следует отнести высокую температуру синтеза 1700°C и высокую стоимость магния.
Указанные выше методы относятся к типу «твердофазных». В то же время, если иметь в виду получение карбида бора, обогащенного изотопом бор-10, необходимо исходить из газообразного (летучего) соединения бора, для которого могут использоваться соответствующие известные способы изотопного обогащения (ректификация, центрифугирование). В этой связи представляют интерес методы получения карбида бора, основанные на химическом осаждении из газовой фазы.
Известен способ получения карбида бора химическим осаждением из газовой фазы, основанный на реакции между галогенидами бора и углеводородами в газовой фазе (US 3334967 A 1965). Осаждение карбида бора происходит на горячей подложке в температурном интервале 1800°C-2200°C и при давлении от 13 Па до 26,6 кПа. В качестве летучего углеводорода используется метан. Основным недостатком данного способа является высокая температура синтеза, приводящая к загрязнению карбида бора примесями. Другой недостаток способа связан с дополнительной сложностью аппаратного оформления процесса, проводимого при низком давлении.
Известен другой способ химического осаждения карбида бора из газовой фазы, основанный на реакции хлорида бора с метаном (Deshpande et al. Appl. Phys. Lett. 65 (14), 3 October 1994). В этом способе для активации реакции используется метод химического осаждения из газовой фазы с горячей нитью. Действие температуры подложки на примесный состав в этом методе сводится к минимуму. Недостатком метода, однако, остается ограничение на выбор летучего борсодержащего прекурсора и низкая производительность.
Известен еще способ химического осаждения карбида бора из газовой фазы, основанный на реакции хлорида бора с метаном в лазерном пучке (W.J. Lackey, D. Rosen, С.Е. Duty, D.L. Jean, S.N. Bondi and Т.N. Elkhatib: ‘Laser CVD system design operation, and modeling’, Ceram. Eng. Sci. Proa, 2002, 23, (4), 23-33). Недостатком метода является его сложное аппаратное оформление.
Наиболее близким к заявляемому способом получения карбида бора является восстановление галогенидов бора метаном в плазме высокочастотного разряда при атмосферном давлении (MacKinnon I.M. Wickens A.J. // Chem. and Ind. — 1973. — N 16. — P 800-801). Плазменная горелка представляла собой водоохлаждаемую кварцевую трубу. Максимальный выход хлорида бора в карбид бора составляет 95% и достигается при подаче BCl3 не более 20 л/мин, относительно высоком соотношении Н2:BCl3=8 и стехиометрическом соотношении между метаном и хлоридом СН4:BCl3=1:4. Мощность разряда составляла 30 кВт. Энерговклад при данных условиях на 1 моль газовой смеси составил 230 кДж/моль. Получаемый карбид представлял собой порошок со средним размером частиц 0,4 мкм. Недостатком способа является загрязнение целевого продукта примесями, поступающими из материала плазменной горелки, а также недолговременная работа плазменной горелки в результате использования водяного охлаждения.
Упомянутое решение взято в качестве прототипа.
В рассмотренных выше способах получения карбида бора химическим осаждением из газовой фазы в качестве исходного борсодержащего соединения применялся треххлористый бор. Для получения карбида бора, обогащенного изотопом бор-10, необходимо иметь треххлористый бор с соответствующей степенью обогащения. Известен метод его обогащения методом ректификации, который, однако, не позволяет достигать высоких степеней обогащения и характеризуется низкой производительностью. Применение для этого соединения центробежного метода обогащения может быть также недостаточно эффективным ввиду наличия у хлора нескольких изотопов. С другой стороны, наличие у бора химически устойчивого газообразного при обычных условиях фторида BF3 позволяет использовать для получения высоких концентраций изотопа бор-10 хорошо развитую «фторидную» технологию изотопного обогащения (фтор в отличие от хлора моноизотопен).
Однако способы синтеза карбида бора из фторида бора, в том числе изотопно-обогащенного в плазме высокочастотного разряда нам не были известны.
Задачей, на решение которой направлено заявляемое изобретение, является разработка технологии прямого получения поликристаллического карбида бора, в том числе изотопно-обогащенного из его трифторида и метана плазмохимическим осаждением из газовой фазы. Другой задачей, на решение которой направлено изобретение, является снижение энергозатрат за счет создания высокочастотного разряда с достаточно высокой плотностью энергии, сохранение химической и изотопной чистоты получаемого поликристаллического карбида бора за счет того, что разряд локализован в объеме и не контактирует со стенками разрядной камеры, упрощение технологии синтеза карбида бора в том числе изотопно-обогащенного, а именно разработка плазмохимической технологии получения карбида бора при атмосферном давлении, что позволяет отказаться от применения дорогостоящего вакуумного оборудования.
Сущность изобретения заключается в том, что осаждение поликристаллического карбида бора ведут в высокочастотном разряде из водорода, фторида бора и метана на электродах, выполненных в виде подложек, контактирующих с концентрированной в малом объеме плазмой атмосферного давления. При этом разработаны условия осаждения поликристаллического карбида бора, а именно проведение процесса при давлении 70,7-100 кПа (0,7-1 атм), соотношении потоков H2:BF3 не менее 2,6 и BF3:CH4 от 5 до 6 и общей скорости потоков Н2, BF3 и СН4 — 1000 см 3 /мин. Мощность разряда составляет 500 Вт. Эти условия обеспечивают выход поликристаллического карбида бора 95% и энергозатраты, равные 10 кДж/моль.
Опытным путем было установлено, что при давлении менее 70,7 Па (0,7 атм) происходит снижение производительности образования карбида бора вследствие изменения условий существования разряда приблизительно в два раза. При давлении выше 100 кПа (1 атм) требуется увеличения подводимой к разряду мощности, что приводит к увеличению энергозатрат.
Опытным путем было установлено также, что проведение реакции при соотношении потоков Н2 и BF3 не менее 2,6 является оптимальным для максимально возможного выхода карбида бора (до 95%) и максимально возможной производительности способа (1 г/час). При соотношении потоков Н2 и менее 2,6 выход карбида бора снижается приблизительно в 2 раза, а при соотношении потоков Н2 и BF3 более 2,6 снижается производительность способа в два раза. Проведение реакции при соотношении потоков BF3 и СН4 менее 5 наблюдается образование свободного углерода в виде сажи, а при соотношении потоков BF3 и CH4 более 6 — резкое снижение выхода карбида бора.
Кроме того, опытным путем было установлено, что электроды, выполненные в виде подложек, образуют и удерживают в стационарном состоянии плазменный разряд атмосферного давления, который обеспечивает условия для образования поликристаллического карбида бора, в том числе обогащенного одним из изотопов бора, как на поверхности электродов в виде компактных поликристаллов. Опытным путем установлено, что температура электродов в процессе образования карбида бора составляет 800-1200°C. Ниже 800°C осаждения карбида бора на поверхности электродов не наблюдается. При температуре выше 1200°C происходит распыление осажденного материала с поверхности электрода.
Все упомянутые признаки являются существенными, так как каждый из них необходим, а вместе они достаточны для решения поставленной задачи — разработка технологии прямого получения поликристаллического карбида бора из его трифторида бора, в том числе обогащенного одним из изотопов бора, водорода и метана, плазмохимическим осаждением из газовой фазы. Для получения карбида бора, обогащенного изотопом бор-10, необходимо лишь заменить исходный фторид изотопно-обогащенным, предварительно пассивировав внутренние стенки аппаратуры этим газом во избежание изотопного разбавления.
Производительность предлагаемого способа составляет не менее 1 г/час и выход поликристаллического карбида бора 95% из его трифторида с энергозатратами 10 кДж/моль, в то время как в прототипе карбида бора природного состава получают из трихлорида бора с выходом 95% и энергозатраты составляют 230 кДж/моль.
В связи с вышеизложенным предлагаемую технологию можно рекомендовать для организации соответствующего производства.
Пример. Получение поликристаллического карбида бора природного изотопного состава. В реактор из кварцевого стекла помещаются соосные цилиндрические электроды сечением 10 мм на расстоянии 10 мм. Реактор откачивают до остаточного давления 0,1 Па, наполняют водородом и зажигают разряд. Подводимая мощность составляет 500 Вт. Образующаяся низкотемпературная плазма очищает внутреннюю поверхность реактора от влаги и других адсорбированных примесей. Затем, путем подачи водорода в реактор, разряд выводится на рабочее давление 100 кПа (атмосферное давление), после чего реализуют режим горения разряда в потоке водорода. При переходе к атмосферному давлению плазменный разряд сжимается и стабилизируется на концах электродов. После чего в реактор подают реакционную смесь — фторид бора, метан и водород в соотношении потоков водорода, фторида бора и метана 2,6:1,0:0,18 и общем расходе плазмообразующей смеси 500 см 3 /мин. Образование поликристаллического карбида бора происходит на нагретых до Т=900°C электродах, а также в объеме разряда. По окончании процесса синтеза в реактор подается инертный газ и гасится разряд. Реактор продувается потоком инертного газа, после чего открывается. Выгрузка образцов осуществляется в специально подготовленном боксе с инертной атмосферой. Скорость осаждения карбида бора составляет 1 г/ч. Содержание типичных примесей в полученном карбиде бора представлено в таблице 1.
Наряду с карбидом бора с бором природного изотопного состава таким образом можно получать и другие изотопные разновидности поликристаллического карбида бора.
Предложенный способ позволяет получать в непрерывном режиме изотопные модификации поликристаллического карбида бора в количестве, достаточном для их использования в вышеупомянутых областях науки и техники.
Похожие патенты RU2648421C2
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения обогащенного изотопа бор-10 | 2019 |
| RU2720774C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОТОПНО-ОБОГАЩЕННОГО ГЕРМАНИЯ | 2011 |
| RU2483130C1 |
| Способ получения изотопных разновидностей элементарного германия с высокой изотопной и химической чистотой | 2016 |
| RU2641126C2 |
| Способ получения наноразмерных структур молибдена | 2014 |
| RU2610583C2 |
| ПИРОЛИТИЧЕСКИЙ РОМБОЭДРИЧЕСКИЙ НИТРИД БОРА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
| RU2167224C1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНИЯ И ЕГО СОЕДИНЕНИЙ И ЛИНИЯ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2012 |
| RU2525415C1 |
| СПОСОБ ДЕЗАКТИВАЦИИ ЭЛЕМЕНТА КОНСТРУКЦИИ ЯДЕРНОГО РЕАКТОРА | 2018 |
| RU2711292C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОИЗОТОПНОГО КРЕМНИЯ SI | 1999 |
| RU2155158C1 |
| СПОСОБ ПРЯМОГО ПОЛУЧЕНИЯ ПОЛИКРИСТАЛЛИЧЕСКОГО КРЕМНИЯ ИЗ ПРИРОДНОГО КВАРЦА И ИЗ ЕГО ОСОБО ЧИСТЫХ КОНЦЕНТРАТОВ | 2012 |
| RU2516512C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИРОЛИТИЧЕСКОГО НИТРИДА БОРА | 1999 |
| RU2160224C1 |
Реферат патента 2018 года Способ получения карбида бора плазмохимическим методом
Изобретение относится к получению поликристаллического карбида бора. Карбид бора получают плазмохимическим синтезом в высокочастотном разряде в реакторе, содержащем электроды, выполненные в виде подложек для осаждения карбида бора. Синтез проводят при мощности разряда 500 Вт в плазме атмосферного давления при подаче в реактор потоков водорода, фторида бора и метана. Соотношение потоков H2:BF3 составляет 2,6, соотношение потоков BF3:CH4 составляет 5,5. Предложенный способ позволяет получить в непрерывном режиме изотопные модификации поликристаллического карбида бора. 1 з.п. ф-лы, 1 табл.
Формула изобретения RU 2 648 421 C2
1. Способ получения карбида бора плазмохимическим синтезом в высокочастотном разряде в реакторе, содержащем электроды, выполненные в виде подложек для осаждения карбида бора, при этом синтез проводят при мощности разряда 500 Вт в плазме атмосферного давления при подаче в реактор потоков водорода, фторида бора и метана при общей скорости потоков 1000 см 3 /мин и при соотношении потоков H2:BF3, равном 2,6, и соотношении потоков BF3:CH4, равном 5,5.
2. Способ по п.1, отличающийся тем, что температура электродов при осаждении карбида бора составляет 800-1200°C.
Источник