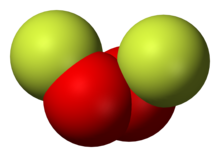
- Фторид кислорода
- Содержание
- Открытие
- Систематическое название
- Физические свойства
- Получение
- Химические свойства
- Взаимодействие с металлами
- Применение
- Токсичность
- Упоминания в литературе
- Фтористый кислород — Oxygen fluoride
- СОДЕРЖАНИЕ
- Синтез
- Дифторид кислорода (OF 2 )
- Дифторид кислорода (O 2 F 2 )
- Дифторид триоксигена или дифторид озона (O 3 F 2 )
- Фторпероксил
- Общее получение дифторидов полиоксида
- Воздействие на озон
- Гиперголический пропеллент
- Смотрите также
- Рекомендации
- Внешние ссылки
Фторид кислорода
Фторид кислорода
| Фторид кислорода(II) | |
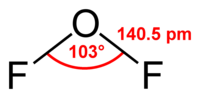 | |
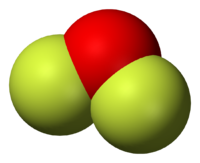 | |
| Общие | |
|---|---|
| Систематическое наименование | Фторид кислорода (II) |
| Химическая формула | OF2 |
| Отн. молек. масса | 54 а. е. м. |
| Физические свойства | |
| Плотность вещества | 1,59 г/см³ |
| Состояние (ст. усл.) | бледно-жёлтый газ |
| Термические свойства | |
| Температура плавления | -224 °C |
| Температура кипения | -145 °C |
| Температура разложения | выше 200 °C |
| Критическая точка | -58°C, 49 атм |
| Энтальпия (ст. усл.) | -25,2 кДж/моль |
| Классификация | |
| номер CAS | 7783-41-7 |
Фторид кислорода(II), дифторид кислорода, OF2. Представляет собой бесцветный газ, конденсирующийся при охлаждении в светло-желтую (в толстых слоях золотисто-желтую) жидкость. Фторид кислорода(II) имеет раздражающий запах несколько отличающийся от запаха фтора (смесь запаха хлорной извести и озона).
Содержание
Открытие
Дифторид кислорода был открыт впервые в 1927 году Лебо и Дамьеном, а спустя некоторое время подробно изучен Руффом и Менцелем.
Систематическое название
В литературе иногда это соединение называют оксидом фтора (F2O). Однако, это неверно, так как атом фтора более электроотрицателен чем кислород, и по правилам IUPAC это соединение должно называться именно фторид кислорода (OF2).
Физические свойства
Жидкий фторид кислорода неограниченно смешивается с жидкими озоном, фтором, кислородом. Плохо растворяется в холодной воде (примерно 7:100 по объёму). При этом достаточно хорошо растворяет воздух.
Молекула обладает слабым дипольным моментом, равным 0,3 Дб
Получение
- Получение фторида кислорода(II) до сих пор проводят по так называемому «щелочному» способу пропусканием газообразного фтора в 2% (0,5 нормальный) водный раствор гидроксида натрия (NaOH). Помимо фторида кислорода(II) в реакции происходит образование перекиси водорода, и озона:
2F2 + 2NaOH = OF2 + 2NaF + H2O
- Возможно также получение фторида кислорода(II) электролизомводного раствора HF.
- При горении воды в атмосфере фтора также частично образуется дифторид кислорода и пероксид водорода. Это происходит за счёт протекания радикальных реакций:
F2 + H2O → 2HF + O· — инициация свободных радикалов 2O· → O2 — доминирующий процесс O· + H2O → H2O2 O· + F2 → F2O
Химические свойства
Дифторид кислорода весьма энергичный окислитель, и в этом отношении напоминает фтор, но реакции с участием фторида кислорода(II) требуют более высокой энергии активации, поскольку на первой стадии происходит образование атомарного кислорода. Термическое разложение фторида кислорода(II) представляет собой мономолекулярную реакцию с энергией активации 41 ккал/моль и начинается только при температуре выше 200°C.
При растворении в горячей воде, подвергается гидролизу. В щелочной среде разложение протекает достаточно быстро.
Смесь паров дифторида кислорода и воды взрывоопасна:
Фторид кислорода(II) не действует на сухое стекло и кварц, но действует (интенсивно) на металлическую ртуть — что исключает применение ртути в приборах с фторидом кислорода(II). На смазку для газовых кранов фторид кислорода(II) действует очень медленно.
Взаимодействие с металлами
На меди, платине, золоте, серебре, фторид кислорода(II) образует лишь тончайшие защитные пленки фторидов, что позволяет использовать эти металлы в контакте с фторидом кислорода(II) при комнатной температуре. При повышении температур до 250°C проиходит дальнейшее окисление металлов. Наиболее подходящими металлами для работы с дифторидом кислорода являются алюминий и магний. Нержавеющие стали, никель, монель-металл, магниевомедный сплав (92/8), латунь и медь, также мало изменяются в весе при воздействии фторида кислорода(II) в течение 1-1,5 недели при 100 °C.
Применение
Благодаря высокой энергии активации разложения фторида кислорода(II), последнюю можно сравнительно безопасно смешивать с многими углеводородами, водородом, моноокисью углерода и прочими веществами, что чрезвычайно важно в практическом плане использования фторида кислорода(II) в качестве высокоэффективного окислителя ракетного топлива. Так как фторид кислорода(II) не взрывается при смешивании с горючими материалами и при нагревании (сам по себе) то ее применение вполне безопасно.
Имели значительный успех опыты применения фторида кислорода(II) в газодинамических химических лазерах. Имея лучшие показателе нежели фтор, фторид кислорода(II) способен занять достойное место в качестве компонента для боевого лазерного оружия высокой мощности.
Токсичность
Фторид кислорода(II) весьма токсичен и по силе превышает фосген, с другой стороны он гораздо ядовитей чем фтор, так как вызывает сильнейшее раздражение тканей организма, очень глубоко проникает и растворяется в них (глубже чем фтор), затрудняет дыхание.
Упоминания в литературе
В фантастической новелле Роберта Л. Форварда «Камелот 30К», дифторид кислорода был использован как биохимический растворитель для живых форм Солнечой системы
Источник
Фтористый кислород — Oxygen fluoride
Кислородные фториды являются соединениями из элементов кислорода и фтора с общей формулой O п F 2 , где п известны = от 1 до 6. Много различных фторидов кислорода:
Фториды кислорода являются сильными окислителями с высокой энергией и могут выделять свою энергию мгновенно или с контролируемой скоростью. Таким образом, эти соединения привлекли большое внимание как потенциальные топлива в реактивных двигательных установках .
СОДЕРЖАНИЕ
Синтез
Вот некоторые методы синтеза и реакции трех наиболее распространенных фторидов кислорода — дифторида кислорода (OF 2 ), дифторида кислорода (O 2 F 2 ) и дифторида озона (O 3 F 2 ).
Дифторид кислорода (OF 2 )
Распространенный препаративный метод включает фторирование гидроксида натрия :
OF2 + 2NaF + H2O>>>»> 2 F 2 + 2 NaOH ⟶ ИЗ 2 + 2 NaF + ЧАС 2 О <\ Displaystyle <\ ce <2f2 + 2naoh ->OF2 + 2NaF + H2O>>> 
OF 2 представляет собой бесцветный газ при комнатной температуре и желтую жидкость при температуре ниже 128 К. Дифторид кислорода имеет раздражающий запах и ядовит. Количественно реагирует с водными галогенкислотами с образованием свободных галогенов :
2Cl2 + 2HF + 2H2O>>>»> ИЗ 2 + 4 HCl ⟶ 2 Cl 2 + 2 HF + 2 ЧАС 2 О <\ Displaystyle <\ ce 
Он также может вытеснять галогены из их солей. Это одновременно эффективный фторирующий агент и сильный окислитель . При взаимодействии с ненасыщенными фторидами азота с помощью электрического разряда это приводит к образованию трифторида азота , оксидов фторидов и других оксидов.
Дифторид кислорода (O 2 F 2 )
O 2 F 2 выпадает в осадок в виде коричневого твердого вещества при УФ-облучении смеси жидких O 2 и F 2 при -196 ° C. Он также кажется стабильным только при температуре ниже -160 ° C. Общий метод получения многих фторидов кислорода — это газофазный электрический разряд в холодных контейнерах, включая O 2 F 2 .
[<\text
Обычно это оранжево-желтое твердое вещество, которое быстро разлагается до O 2 и F 2, близкое к своей нормальной температуре кипения около 216 K.
O 2 F 2 бурно реагирует с красным фосфором даже при -196 ° C. Взрывы также могут произойти, если для смягчения реакции использовать фреон-13 .
Дифторид триоксигена или дифторид озона (O 3 F 2 )
O 3 F 2 — вязкая жидкость кроваво-красного цвета. Он остается жидким при 90 К, поэтому его можно отличить от O 2 F 2 , температура плавления которого составляет около 109 К.
Как и другие фториды кислорода, O 3 F 2 является эндотермическим и разлагается при температуре около 115 K с выделением тепла, которое дается следующей реакцией:
O2 + 2O2F2>>>»> 2 О 3 F 2 ⟶ О 2 + 2 О 2 F 2 <\ Displaystyle <\ ce <2 o3f2 ->O2 + 2O2F2>>> 
С O 3 F 2 безопаснее работать, чем с озоном , и он может испаряться, термически разлагаться или подвергаться воздействию электрических искр без каких-либо взрывов. Но при контакте с органическими веществами или окисляемыми соединениями он может взорваться или взорваться. Таким образом, добавление даже одной капли дифторида озона к твердому безводному аммиаку приведет к легкому взрыву, когда оба они имеют температуру 90 К.
Фторпероксил
Фторпероксил — это такая молекула, как OOF, химическая формула которой O 2 F и стабильна только при низкой температуре. Сообщается, что его получают из атомарного фтора и дикислорода.
О 2 + F ⟶ О 2 F <\ displaystyle <\ rm
Общее получение дифторидов полиоксида
| Уравнение реакции | F 2 : O 2 по объему | Текущий | Температура ванны (° C) |
|---|---|---|---|
O2F2>>>»> О 2 + F 2 ↽ — — ⇀ О 2 F 2 <\ displaystyle <\ ce  O2F2>>>»> O2F2>>>»> | 1: 1 | 10–50 мА | |
2O3F2>>>»> 3 О 2 + 2 F 2 ↽ — — ⇀ 2 О 3 F 2 <\ displaystyle <\ ce <3o2 + 2f2 2o3f2>>>  2O3F2>>>»> 2O3F2>>>»> | 2: 3 | 25–30 мА | |
O4F2>>>»> 2 О 2 + F 2 ↽ — — ⇀ О 4 F 2 <\ displaystyle <\ ce <2o2 + f2 o4f2>>>  O4F2>>>»> O4F2>>>»> | 1: 2 | 4-5 мА |