- Фосфат кальция
- Характеристики и физические свойства фосфата кальция
- Получение фосфата кальция
- Химические свойства фосфата кальция
- Применение фосфата кальция
- Примеры решения задач
- Структура фосфата кальция (Ca3 (PO4) 2), свойства, образование и использование
- Структура фосфата кальция
- Остальная часть семьи
- Фосфат кальция, характеристика, свойства и получение, химические реакции
- Фосфат кальция, характеристика, свойства и получение, химические реакции.
- Краткая характеристика фосфата кальция:
- Физические свойства фосфата кальция:
- Получение фосфата кальция:
Фосфат кальция
Характеристики и физические свойства фосфата кальция
Существует в виде двух полиморфных модификаций: моноклинной и гексагональной.
Рис. 1. Фосфат кальция. Внешний вид.
Основные характеристики фосфата кальция приведены в таблице ниже:
Молярная масса, г/моль
Плотность, г/см 3
Температура плавления, o С
Растворимость в воде (20 o С), % (масс.)
Получение фосфата кальция
Лабораторные способы получения фосфата кальция предполагают действие ортофосфорной кислоты на соли кальция (1) или гидроксид кальция (2):
Химические свойства фосфата кальция
Фосфат кальция – это средняя соль, образованная сильным основанием – гидроксидом кальция (Ca(OH)2) и слабой кислотой – ортофосфорной (H3PO4). В водном растворе гидролизуется. Гидролиз протекает по аниону (теоретически возможны вторая и третья ступень). Наличие анионов ОН — свидетельствует о щелочном характере среды.
3Ca 2+ + 2PO4 3- + HOH ↔ HPO4 2- + 3Ca 2+ + OH — ;
Для фосфата кальция характерны все свойства солей:
— взаимодействие с сильными минеральными кислотами
— взаимодействие с солями, в результате которого одним из продуктов реакции является нерастворимое в воде соединение
— разложение при нагревании
Применение фосфата кальция
Фосфат кальция нашел применение в качестве добавки при производстве кормов для КРС и домашних птиц. Его используют при производстве минеральных удобрений, керамики и стекла. В пищевой промышленности фосфат кальция известен как добавка Е341 – разрыхлитель.
Примеры решения задач
| Задание | Вычислите массу фосфата кальция, который может прореагировать с концентрированным раствором соляной кислоты объемом 100 мл (массовая доля HCl 34%, плотность 1,168 кг/л). |
| Решение | Запишем уравнение реакции: |
Найдем массу раствора соляной кислоты, а также массу растворенного вещества HCl в нем:
msolution =0,1 × 1,168 = 0,1168 кг = 116,8г.
msolute (HCl) = ω (HCl) / 100% ×msolution;
msolute (HCl) = 34 / 100% × 116,8 = 39,712 г.
Рассчитаем количество моль соляной кислоты (молярная масса равна 36,5 г/моль):
n(HCl) = m (HCl) / M (HCl);
n (HCl) = 39,712 / 36,5 = 1,088 моль.
Согласно уравнению реакции n (HCl) :n (Ca3(PO4)2) =6: 1. Значит,
Тогда масса фосфата кальция, вступившего в реакцию будет равна (молярная масса – 310 г/моль):
| Задание | Какая масса оксида фосфора (V) образуется в ходе реакции термического разложения фосфата кальция массой 46 г? |
| Решение | Запишем уравнение реакции термического разложения фосфата кальция: |
Рассчитаем количество вещества фосфата кальция (молярная масса – 310 г/моль):
Согласно уравнению реакции n(Ca3(PO4)2) :n(P2O5) =1:1 . Тогда количество моль оксида фосфора (V) будет равно:
Найдем массу образовавшегося оксида фосфора (V) (молярная масса – 284 г/моль):
Источник
Структура фосфата кальция (Ca3 (PO4) 2), свойства, образование и использование
фосфат кальция неорганическая и третичная соль, химическая формула которой Ca3(РО4)2. Формула утверждает, что состав этой соли составляет 3: 2 для кальция и фосфата, соответственно. Это можно увидеть непосредственно на нижнем изображении, где показан катион Ca 2+ и анион ПО4 3- . На каждые три КА 2+ Есть два ПО4 3- взаимодействуя с ними.
С другой стороны, фосфат кальция относится к ряду солей, которые варьируются в зависимости от соотношения Ca / P, а также от степени гидратации и pH. На самом деле существует много типов фосфатов кальция, которые существуют и могут быть синтезированы. Однако, буквально следуя номенклатуре, фосфат кальция относится только к трикальцию, упомянутому выше..
Все фосфаты кальция, включая Са3(РО4)2, Они однотонные с легкими сероватыми тонами. Они могут быть зернистыми, мелкими, кристаллическими и иметь размеры частиц около микрометров; и даже были получены наночастицы этих фосфатов, с помощью которых были разработаны биосовместимые материалы для костей..
Эта биосовместимость связана с тем, что эти соли находятся в зубах и, короче, в костных тканях млекопитающих. Например, гидроксиапатит представляет собой кристаллический фосфат кальция, который, в свою очередь, взаимодействует с аморфной фазой той же соли.
Это означает, что существуют аморфные и кристаллические фосфаты кальция. По этой причине разнообразие и множество вариантов не удивительны при синтезе материалов на основе фосфатов кальция; материалы, свойства которых исследователи интересуются каждый день во всем мире, чтобы сосредоточиться на восстановлении костей.
- 1 Структура фосфата кальция
- 1.1 Аморфный фосфат кальция
- 1.2 Остальная часть семьи
- 2 Физические и химические свойства
- 2.1 Имена
- 2.2 Молекулярный вес
- 2.3 Физическое описание
- 2.4 Вкус
- 2.5 Точка плавления
- 2.6 Растворимость
- 2.7 Плотность
- 2.8 Показатель преломления
- 2.9 Стандартная энтальпия тренировки
- 2.10 Температура хранения
- 2,11 рН
- 3 Обучение
- 3.1 Нитрат кальция и гидрофосфат аммония
- 3.2 Гидроксид кальция и фосфорная кислота
- 4 использования
- 4.1 В костной ткани
- 4.2 Биокерамические цементы
- 4.3 Врачи
- 4.4 Другое
- 5 ссылок
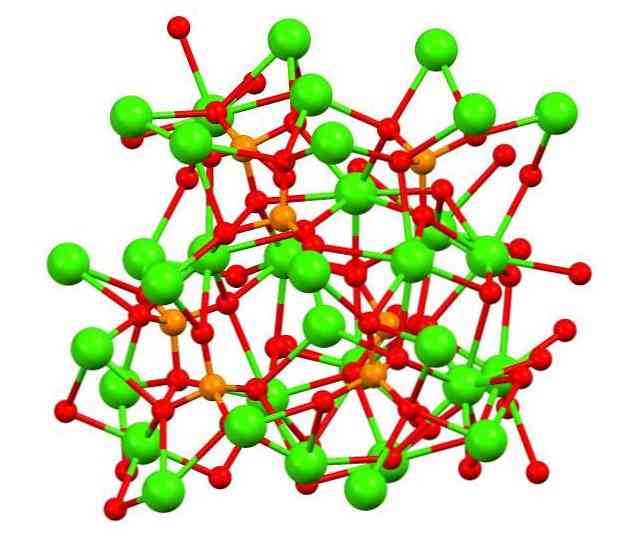
Структура фосфата кальция
Верхнее изображение показывает структуру трехосновного каликофосфата в странном минерале whitlockite, который может содержать магний и железо в качестве примесей.
Хотя на первый взгляд это может показаться сложным, необходимо уточнить, что модель предполагает ковалентное взаимодействие между атомами кислорода фосфатов и металлическими центрами кальция.
В порядке представления это действительно, однако, взаимодействия являются электростатическими; катионы Са 2+ привлекаются к анионам ПО4 3- (Са 2+ — O-PO3 3- ). Имея это в виду, понятно, почему на изображении кальций (зеленые сферы) окружен отрицательно заряженными атомами кислорода (красные сферы).
Когда есть так много ионов, это не оставляет симметричное расположение или образец видимым. Ca3(РО4)2 Принимает при низких температурах (Т — и HPO4 2- в АШП. Эти ионы образуются при гидролизе одного из фосфатов:
В результате истинная структура АШП становится более сложной, состав ее ионов которой представлен формулой: Ca9(РО4)6-х(HPO4)х(ОН)х. «Х» указывает на степень гидратации, так как если х = 1, то формула будет такой: Ca9(РО4)5(HPO4) (ОН).
Различные структуры, которые могут иметь PCA, зависят от молярных отношений Ca / P; то есть относительного количества кальция и фосфата, которые изменяют весь их результирующий состав.
Остальная часть семьи
На самом деле фосфаты кальция представляют собой семейство неорганических соединений, которые, в свою очередь, могут взаимодействовать с органической матрицей..
Другие фосфаты получают «просто» путем замены анионов, которые сопровождают кальций (ПО4 3- , HPO4 2- , H2ПО4 — , Огайо — ), а также тип примесей в твердом теле. Таким образом, до одиннадцати или более фосфатов кальция, каждый со своей структурой и свойствами, могут возникать естественным или искусственным путем..
Ниже приведены некоторые фосфаты и их соответствующие структуры и химические формулы:
-Водород кальций фосфат дигидрат, CaHPO4H 2H2O: моноклинный.
-Кальция дигидрофосфат моногидрат, Ca (H)2ПО4)2∙ H2O: триклиника.
-Безводный кислый фосфат, Ca (H)2ПО4)2: триклиника.
-Ocalcium гидрофосфат (OCP), Ca8H2(РО4)6: триклиника Является предшественником в синтезе гидроксиапатита.
Источник
Фосфат кальция, характеристика, свойства и получение, химические реакции
Фосфат кальция, характеристика, свойства и получение, химические реакции.
Фосфат кальция – неорганическое вещество, имеет химическую формулу Ca3(PO4)2.
Краткая характеристика фосфата кальция:
Фосфат кальция – неорганическое вещество бесцветного либо белого цвета, соль металла кальция и ортофосфорной кислоты.
Фосфат кальция представляет собой бесцветные кристаллы.
Химическая формула фосфата кальция Ca3(PO4)2.
Фосфат кальция существует в виде двух модификациях (α и β), отличающихся физическими свойствами (плотностью и температурой плавления). α-модификация фосфата кальция имеет моноклинную сингонию. β-модификация фосфата кальция имеет гексагональная сингонию.
Плохо растворим в воде. В отличие от многих химических веществ растворимость фосфата кальция падает с увеличением температуры.
Не растворим в жидком аммиаке, ацетоне, диэтиловом эфире, этаноле и пр. органических растворителях.
В пищевой промышленности используется 3 типа фосфатов кальция, согласно степени замещения атомов водорода:
– добавка Е341(i) – ортофосфат кальция 1-замещенный (Monocalcium ortophosphate) с химической формулой Ca(Н2PO4)2;
– добавка Е341(ii) – ортофосфат кальция 2-замещенный (Dicalcium ortophosphate) с химической формулой CaНPO4;
– добавка Е341(iii) – ортофосфат кальция 3-замещенный (Tricalcium ortophosphate) с химической формулой Ca3(PO4)2.
Фосфат кальция широко распространён в природе. Входит в состав минералов фосфорита, апатита, гидроксиапатита. Фосфаты кальция содержатся в коровьем молоке. В организме человека кальций существует в основном в виде фосфатов кальция. Кости человека на семьдесят процентов состоят из фосфатов кальция. Зубная эмаль тоже состоит в основном из гидроксиапатитов (соединений фосфата кальция).
Физические свойства фосфата кальция:
| Наименование параметра: | Значение: |
| Химическая формула | Ca3(PO4)2 |
| Синонимы и названия иностранном языке | calcium phosphate (англ.) |
кальций фосфорнокислый (рус.)
кальция ортофосфат (рус.)
трикальций фосфат (рус.)
Получение фосфата кальция:
Фосфат кальция получают из минералов, в которых он содержится: фосфорита, апатита, гидроксиапатита.
Фосфат кальция также получают в результате следующих химических реакций:
- 1. взаимодействием оксида кальция и ортофосфорной кислоты:
- 2. взаимодействием гидроксида кальция и ортофосфорной кислоты:
- 3. взаимодействием фосфата лития и хлорида кальция:
- 4. взаимодействием фосфата натрия и хлорида кальция:
- 5. разложения гидроортофосфата кальция:
Источник