- Способ получения бета-каротина
- ПОЛУЧЕНИЕ КАРОТИНОВ ИЗ ВОДОРОСЛИ DUNALIELLA SALINA
- Вводная часть
- Природные источники каротиноидов и их использование
- Способы получения бета-каротина из природного сырья
- Преимущества использования водоросли Dunaliella salina в качестве источника каротиноидов
- Биология и систематика водоросли
- Оценка запасов каротиноидов в водоемах соляных промыслов Крымского полуострова
- Предыдущий опыт получения каротина в условиях соленых лиманов юга Украины
- Ведущие производители и примеры продукции с содержанием каротина, получаемого из водоросли Dunaliella salina
- Заключение
Способ получения бета-каротина
Владельцы патента RU 2295874:
Изобретение относится к биотехнологии и может быть использовано в пищевой и фармацевтической промышленности, а также в сельском хозяйстве. Способ получения бета-каротина предусматривает экстракцию бета-каротина из мицеллиальной массы, отделение от экстракта суспензии кристаллов бета-каротина в липидах. Далее осуществляют алкоголиз спиртом полученных в суспензии липидов в соотношении 1:2-1:5 при температуре кипения в присутствии катализатора. В качестве катализатора используют алкоголят щелочного металла. Полученные после фильтрации кристаллы бета-каротина два-три раза промывают спиртом в соотношении 1:1,5-1:3. Изобретение позволяет повысить выход целевого продукта, снизить расход спирта и реагентов, сократить технологический процесс. 1 з.п. ф-лы, 2 табл.
Предлагаемое изобретение относится к биотехнологии и может быть использовано в пищевой и фармацевтической промышленности, в сельском хозяйстве.
Бета-каротин — ценнейший продукт для обогащения пищевой продукции, получения витаминных и лекарственных препаратов, предназначенных для повышения защитных функций организма, лечения заболеваний желудочно-кишечного тракта, ожогов, пролежней, трофических язв и др., а также используемый в качестве добавки в корм животных.
Известен способ получения бета-каротина (RU 2032667, 6 МПК С 07 С 403/24, 1995), предусматривающий получение бета-каротина путем конденсации ретинилтрифенилфосфониевой соли, полученной из ретинилацетата и трифенилфосфина с ретиналем в спирте, в присутствии едкой щелочи, при этом ретинилтрифенилфосфониевую соль вводят в виде гидросульфата, а ретиналь — в виде гидрохинонового комплекса при соотношении ретинилацетата и едкой щелочи 1:(3÷3,5).
К суспензии трифенилфосфина в этаноле при перемешивании в атмосфере азота последовательно добавляют концентрированную серную кислоту и ретинилацетат. Смесь при 20°С перемешивают в течение 18-20 ч. Полученный спиртовой раствор фосфониевой соли добавляют одновременно с раствором гидроокиси калия в этаноле к суспензии ретиненгидрохинонового комплекса в этаноле, охлажденной до — 14°С. Реакционную смесь перемешивают при 0-5°С в течение 4 час. Выпавшие кристаллы бета-каротина отфильтровывают, промывают этанолом, водой, потом вновь этанолом, сушат в вакууме при 60°С в течение 4 час.
Недостатки: длительность технологического процесса, использование едкой щелочи, концентрированной серной кислоты, необходимость тщательного отмывания реагентов, потребность в значительных объемах этанола, воды, потребность в обеспечении жестких режимов, потери бета-каротина.
За ближайший аналог принят способ получения кристаллического бета-каротина по патенту RU №2168913, А 23 L 1/302.
Бета-каротин извлекают из мицеллиальной массы путем экстракции неполярным органическим растворителем при температуре 90°С. Полученный экстракт фильтруют, бета-каротин кристаллизуют при температуре 15°С, суспензию кристаллов очищают в спиртовом растворе щелочи концентрацией 40-120 г/л в соотношении 1:8÷1:12, добавляют равное количество воды, доводят до кипения, фильтруют. После этого полученные кристаллы вновь промывают спиртовым раствором щелочи, затем — спиртом, до отрицательной реакции на фенолфталеин. Заключительный этап — высушивание полученного бета-каротина в токе инертного газа в вакууме.
Недостатки: использование значительных объемов щелочи влечет за собой удлинение технологического процесса в связи с необходимостью отмывания кристаллов бета-каротина от трудноудаляемой щелочи, которое сопровождается потерями бета-каротина.
Задачи: упрощение способа получения бета-каротина с одновременным сохранением его качества, повышение выхода целевого продукта по сравнению с прототипом, снижение расхода спирта и реагентов, сокращение технологического процесса.
Существенной новизной предлагаемого способа является то, что при получении бета-каротина из мицеллиальной массы после отделения от экстракта кристаллического бета-каротина в виде суспензии ее липиды подвергают алкоголизу спиртом в соотношении фракций 1:2÷1:5 при температуре кипения в присутствии катализатора, преимущественно алкоголята щелочного металла, а полученные после фильтрации кристаллы бета-каротина 2-3 раза промывают легкокипящим спиртом в соотношении 1:1,5÷1:3. Завершают процесс сушкой бета-каротина в токе инертного газа в вакууме.
Техническим результатом являются следующие показатели:
| № п/п | Показатели | Способ получения бета-каротина, патент №2168913 | Способ получения бета-каротина по предлагаемому способу |
| 1 | 2 | 3 | 4 |
| 1 | Выход бета-каротина, % | 99,74 | 99,84 |
| 2 | Расход спирта, мл | 500 | 240 |
| 3 | Продолжительность технологического цикла, мин | 120 | 30 |
| 4 | Масса кристаллов в суспензии, г | 6,549 | 5,752 |
| 5 | Потери бета-каротина в процессе очистки, г | 0,017 | 0,009 |
| 6 | Расход щелочи, используемой в технологическом процессе, 1 цикл, г | 80,0 | 24,0 |
| 7 | Чистота бета-каротина | tпл=180÷182°C | tпл=180÷182°С |
Липиды суспензии переводят в форму растворимых в спирте эфиров, используя процесс алкоголиза, в присутствии катализатора реакции, в качестве которого используют алкоголят щелочного металла.
Процесс проводят при температуре кипения с обратным холодильником до получения гомогенной среды над кристаллами, после чего систему охлаждают до 40-50°С и отфильтровывают, создав в аппарате над жидкой фазой среду инертного газа. Кристаллы отмывают от остатков эфиров спиртом, сушат в вакууме в среде инертного газа.
Пример 1. Суспензию бета-каротина в липидах в количестве 20 г обработали этиловым спиртом в присутствии алкоголята калия, при температуре кипения в соотношении суспензия: спирт 1:2, полученные эфиры отделили фильтрацией, кристаллы бета-каротина промыли этиловым спиртом в соотношении 1:1,5 дважды промыли в соотношении 1:2, высушили в токе инертного газа при остаточном давлении (40 мм рт.ст.)≈5,3 кПа.
Пример 2. Суспензию бета-каротина в липидах в количестве 20 г обрабатывают метиловым спиртом в присутствии алкоголята натрия, при температуре кипения, в соотношении суспензия: спирт 1:4, полученные эфиры отделили фильтрацией, кристаллы бета-каротина трижды промыли в соотношении 1:3, высушили в токе инертного газа при остаточном давлении (40 мм рт.ст.)≈5,3 кПа.
| Количество липидов в суспензии, г | Количество кристаллов в суспензии, г | Количество летучих компонентов, г | Количество кристаллов после очистки, г | Потери бета-каротина, г | Температура плавления кристаллов, °С |
| 13,721 | 6,109 | 0,17 | 6,096 | 0,013 | 180-182 |
| 13,886 | 5,924 | 0,19 | 5,913 | 0,011 | 180-182 |
Таким образом, способ позволяет повысить выход бета-картина, сократить технологический процесс, избавиться от работы с большими расходами щелочи и необходимости ее длительного отмывания, улучшить условия работы персонала, исключить применение воды для промывки, что сокращает потери спирта при последующей регенерации растворов.
1. Способ получения бета-каротина, включающий экстракцию его из мицеллиальной массы и последующую обработку целевого продукта, отличающийся тем, что после отделения от экстракта суспензии кристаллов бета-каротина в липидах смесь подвергают алкоголизу спиртом в соотношении 1:2-1:5 при температуре кипения в присутствии катализатора в виде алкоголята щелочного металла, полученные после фильтрации кристаллы бета-каротина 2-3 раза промывают спиртом в соотношении 1:1,5-1:3.
2. Способ по п.1, отличающийся тем, что бета-каротин после промывания легкокипящим спиртом сушат в вакууме в токе инертного газа.
Источник
ПОЛУЧЕНИЕ КАРОТИНОВ ИЗ ВОДОРОСЛИ DUNALIELLA SALINA
В УСЛОВИЯХ КРЫМСКИХ СОЛЕВЫХ ПРОМЫСЛОВ
Авторы:
Давидович Николай Александрович, канд.биол.наук, старший научный сотрудник
Стюпан Андрей Витальевич
Вводная часть
Каротин (от латинского carota – морковь) – жёлто-оранжевый пигмент, синтезируемый бактериями, грибами, водорослями, высшими растениями. Его присутствие объясняет желтую, оранжевую, красную окраску плодов, корнеплодов, листьев растений.
По своей химической природе каротин – это непредельный углеводород из группы терпеноидов. Эмпирическая формула С40H56, молекулярный вес 536,9. Химический синтез β-каротина был осуществлен в 1956 г. Различают несколько изомерных форм каротина, среди них наиболее известен β-каротин (бета-каротин). Структурная формула β-каротина:
Нерастворим в воде, но хорошо растворяется в органических растворителях; относятся к липофильным соединениям, т. е. растворим в маслах. В кристаллическом виде он имеет фиолетовокрасную окраску, в масляном растворе – от желтой до оранжевой.
Растворы каротиноидов в органических растворителях при спектрофотометрических исследованиях дают характеристические полосы поглощения в основном в видимой области спектра, а стереоизомеры показывают их также и в ультрафиолетовой области. Это один из наиболее точных показателей, используемых при идентификации этих веществ. Характерной является также особенность каротиноидов избирательно абсорбироваться на минеральных и некоторых органических абсорбентах, что позволяет разделять их при помощи методов хроматографирования. Для отдельных каротиноидов характерны некоторые специфические реакции, в том числе цветные.
Следует учитывать, что каротиноиды в чистом виде отличаются высокой лабильностью – они весьма чувствительны к воздействию солнечного света, кислорода воздуха, нагреванию, воздействию кислот и щелочей. Под влиянием этих неблагоприятных факторов они подвергаются окислению и разрушению. В тоже время, входя в состав различных комплексов, они проявляют намного большую стабильность.
Наравне с черно-коричневыми меланинами, каротины являются самыми распространенными пигментами в природе: за год в масштабах Земли их синтезируется около 100 млн. тонн (более 3 тонн в секунду). В природе каротиноиды могут находиться в различных состояниях: в свободном виде они чаще встречаются в пластидах растений, мышечной ткани рыб, яйцах птиц, в виде эфиров жирных кислот – в хроматофорах и эпидермальных структурах растений, в форме каротин-протеинов – в эпидермальных тканях животных и т. д.
Животные (в том числе и человек) не способны синтезировать каротиноиды de novo, их поступление зависит только от источников питания. Усвоение каротиноидов, как и других липидов, происходит в дуоденальной области тонкого кишечника. Под влиянием желудочно-кишечной среды (например кислотности желудочного сока), наличия специфических рецепторов протеинов каротиноиды могут разрушаться окислителями или энзимами или метаболизировать, как например β-каротин в витамин А. Позвоночные в процессе пищеварения способны расщеплять молекулу β -каротина на две молекулы витамина А. Поэтому β-каротин называют также провитамином А. Провитаминные свойства β-каротина и его окислительное преобразование в витамин А являются общими для всех животных.
Каротин, являющийся провитамином витамина А, крайне важен в питании человека, он незаменим для зрения, роста, репродукции, защиты от различных бактериальных и грибковых заболеваний, нормального функционирования кожи и слизистых. Бета-каротин характеризуется наибольшей известной в природе способностью к дезактивации синглетного кислорода. Последний обладает высокой химической активностью, влияет на процессы, связанные с разрушением различных веществ на свету, ответственен за повреждение ДНК в живых организмах, влияет на процессы старения кожи и т.д. Среднее естественное (без биологических добавок) потребление каротина с пищей в разных странах составляет 1,8-5,0 мг/сутки. Согласно методическим рекомендациям по нормам рационального питания «НОРМЫ физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации» от 18 декабря 2008 г. (МР 2.3.1.2432 -08) 1 физиологическая потребность в бета-каротине для взрослых – 5 мг/сутки (вводится впервые). 6 мкг бета-каротина эквивалентны 1 мкг витамина А. Верхний допустимый уровень потребления бета-каротина не установлен; длительный прием бета-каротина не сопровождается какими-либо побочными эффектами. При избытке каротина в организме наблюдается состояние гиперкаротинемии – однако, в отличие от избыточного витамина А, каротин малотоксичен. Бета-каротин зарегистрирован в качестве пищевой добавки Е160a.
Всемирный рынок каротиноидов в 2000 г. оценивался в $786 млн., в том числе пищевое применение – $209 млн., кормовые добавки – $462 млн., фармацевтическая и косметическая продукция – $115 миллионов. Как ожидается, рынок каротиноидов возрастет до $919 млн. к 2015 г 2. Бета-каротин составляет около трети всего рынка каротиноидов. Стоимость синтетического β-каротина порядка 500 долларов США/кг.
Следует указать на то, что каротин, полученный из природных источников относится к натуральным продуктам, потребность в которых возрастает с каждым годом.
Природные источники каротиноидов и их использование
Красители бывает натурально-идентичными (синтетическими) или натуральным (природными).
Природные источники каротиноидов очень многообразны, многие из них довольно широко используются для получения каротиноидсодержащих продуктов. В странах с тропическим климатом источником получения каротиноидсодержащих продуктов служат красное пальмовое масло и клубни батата. Довольно богаты каротиноидами плоды цитрусовых, абрикосы, хурма. Из источников, присущих средним широтам, в том числе и климатическим зонам Украины, можно выделить плоды моркови, тыквы, томатов, сладкого перца, облепихи, шиповника, рябины. При этом ряд каротиноидсодержащих препаратов на основе природного растительного сырья выпускается украинской фармацевтической промышленностью. В частности, выпускается масло шиповника (содержит не менее 0,6 г/л каротиноидов), масло из плодов облепихи (содержание каротиноидов составляет не менее 1,8 г/л).
Среди натуральных красителей наиболее востребованный – бета-каротин (Е160а). Согласно последним данным, на данный пигмент тратиться около 30% от общего объема средств, расходуемых производителями пищевых продуктов на закупки натуральных красителей.
Один из наиболее ценных источников натурального бета-каротина – водоросль D. salina, из которой получают краситель, содержащий в своем составе 96% этого пигмента. Смесь каротинов из пальмового масла содержит 35% альфа-каротина и 65% – бета-каротина. По своей природе бета-каротин — жирорастворимый пигмент. Его искусственно доводят до формы вододисперсной эмульсии. Для напитков необходимы высокостойкие кислотоустойчивые эмульсии бета-каротина. Если в процессе хранения эмульсия разрушается, то обычно на горлышке бутылки образуется окрашенное кольцо. Во избежание проявления такого порока необходимо применять краситель с эмульгирующей системой, подобранной в соответствии с особенностями производства и состава напитка. В качестве эмульгаторов используются полисорбат 80, сорбитан моноолеат, камеди, эфиры сахарозы (по отдельности или в различных сочетаниях). Светостойкость бета-каротина приемлема для напитков в прозрачной упаковке, однако она очень ослабляется в присутствии кислорода и усиливается при добавлении аскорбиновой кислоты.
Следующий по объемам мирового потребления краситель из группы каротиноидов – паприка (Е160с). Его доля на рынке в денежном выражении – 20%. Пигменты паприки получают из олеорезинов сладкого перца Capsicum annum L.
Пигменты паприки по своей природе жирорастворимы. Их вододисперсные эмульсии выпускаются в формах, пригодных для получения как прозрачных, так и с различной степенью замутненности растворов. Пигменты паприки чувствительны к свету и кислороду, но не чувствительны к рН. Для их стабилизации могут использоваться аскорбиновая кислота, альфатокоферол и экстракт розмарина. Хорошо очищенный краситель при дозировках, необходимых для окрашивания, не придает продуктам ощутимых посторонних привкусов и запахов.
Также к группе каротиноидов относится желто-оранжевый натуральный краситель аннато (Е160b), получаемый из семян растения Bixa orellana. Родина аннато – Центральная и Южная Америка. Аннато – легко культивируемое дерево, которое достигает периода плодоношения в 4-5 лет и дает урожай в течение 20 лет. Аннато является одним из наиболее экономически значимых натуральных красителей в мире. Крупнейшими производителями семян аннато являются Перу, Бразилия и Кения, а крупнейшими импортерами – США, Япония и Европа.
Жирорастворимый пигмент биксин экстрагируют из семян аннато этанолом или маслом. Водорастворимый пигмент норбиксин получают методом щелочного гидролиза биксина. Водный раствор аннато производится в виде щелочного раствора с рН, равным 10,5, поэтому при работе с ним необходимо соблюдать меры предосторожности. Недавно был исследован путь преобразования каротиноида ликопина (красный пигмент томата) в биксин. В настоящее время ведутся работы по выведению биксинпродуцирующих помидоров. Биксин слабо растворим в маслах – 0,1–0,3% (в/в). Он чувствителен к pH, при понижении которого оттенок смещается от желто-оранжевого до розового. Кислотность не влияет на стабильность этого пигмента. Биксин имеет хорошую термос табильность при температуре, не превышающей 100°C, но быстро разрушается при температуре свыше 125°C. Биксин устойчив к окислению, но чувствителен к свету, как и другие каротиноиды. Для увеличения стабильности в красители на основе биксина добавляют антиоксиданты.
Доля биксина на рынке натуральных красителей – 7%. Водорастворимый норбиксин выпускается в стандартной (устойчивой при рН около 4) и специальной кислотоустойчивой (до рН 2,5) формах. Также на основе биксина производятся вододисперсные эмульсии, позволяющие получать замутненные растворы.
Способы получения бета-каротина из природного сырья
Наиболее старым, но все еще используемым, является способ производства из моркови. Способ отличается крайне высокой трудоемкостью и низкой рентабельностью: для получения 1 кг каротина кристаллического необходимо переработать около 15 т моркови, т .е. это равно ее сбору с 1 га при средней урожайности.
На Украине преобладающая часть 80% бета-каротина производится сейчас из биомассы мукорового гриба Blakeslea trispora. В производстве используются отходы мукомольной, консервной и мясомолочной промышленности. Каротин экстрагируют из биомассы гриба органическим растворителем в растительном масле, либо получаемую биомассу высушивают без экстракции. В первом случае степень извлечения каротина более высокая, до 50%. Во втором случае получают порошок с содержанием бета-каротина 6-7%. Себестоимость получения продукта и по этой технологии высокая.
Преимущества использования водоросли Dunaliella salina в качестве источника каротиноидов
Красители на основе бета-каротина натурального происхождения имеют более высокую стабильность, чем натурально-идентичные. Кроме того, в натурально-идентичном и микробилогическом (бактериальном и фунгинальном) бета-каротине часть пигмента находится в форме труднорастворимых кристаллов. Каротин имеет много изомерных форм; синтетическиый вариант не позволяет добиться необходимого соотношения изомеров, в точности повторяющего природный комплекс. Это же относиться и к сопутствующим каротиноидам, включая каротины и ксантофиллы.
Содержание β-каротина может достигать 10% от сухой массы водоросли, что является наиболее высоким показателем по сравнению с другими продуцентами β-каротина.
В условиях, благоприятных для роста и размножения, клетки D. salina имеют зеленую окраску и содержат лишь около 0,3 % β -каротина от сухой массы, т.е. столько же сколько листья растений и клетки других некаротиноносных водорослей. Только в условиях, задерживающих рост и размножение клеток, в последних аккумулируется β -каротин в виде оранжевых масляных глобул расположенных в межтилакоидных промежутках хлоропласта. Среди параметров, регулирующих процессы роста, размножения и каротинообразования, первоочередное значение имеют интенсивность света, концентрация осмотически действующих солей, температура и содержание в среде биогенных элементов. Чем выше освещенность, тем интенсивнее каротинообразование. Избыточному накоплению β -каротина в ее клетках способствуют также повышенная концентрация осмотически действующих солей в среде обитания (до 5 М NaCl), экстремальные температуры (выше или ниже ростового оптимума), недостаток биогенных элементов в питательной среде (особенно голодание по азоту). Таким образом, биосинтез β-каротина в клетках микроскопичаской водоросли Dunaliella salina — легко регулируемый процесс, а значит себестоимость β -каротина, получаемого из водорослей, выращенных в нестерильных условиях под открытым небом в будущем будет снижаться на основе дальнейшего совершенствования технологического процесса.
Биология и систематика водоросли
Dunaliella salina Teod. (дуналиелля солоноводная) – одноклеточная жгутиковая микроводоросль (рис. 1) из отдела Зеленых водорослей.
Рис. 1 Dunaliella salina Teodoresco, видимая под микроскопом при разных увеличениях. Длина масштабного отрезка 20 мкм.
- Царство (Kingdom) Plantae
- Класс (Class) Chlorophyceae
- Отдел (Division) Chlorophycota
- Порядок (Order) Volvocales
- Семейство (Family) Dunaliellaceae
- Род (Genus) Dunaliella
- Вид (Species) Dunaliella salina
Род Dunaliella включает 29 солоноводных, морских, пресноводных и почвенных видов; 6 из них найдены на территории Украины исключительно в соленых водоемах. Хорошо известна Dunaliella salina – дуналиелла солоноводная, развивающаяся в гипергалинных водоемах юга Украины, включая степной Крым. В массовом количестве она вызывает красное “цветение”, особенно выраженное в период летнего испарения воды из мелководных лагун. Иногда на поверхности таких лагун образуется солевой концентрат в виде пластинок из кристаллов соли4. Таким образом, Dunaliella salina в состоянии жить в рапе, в которой достигнута точка насыщения и происходит кристаллизация и осаждение солей.
Клетки водоросли разнообразной формы: овальные, эллипсоидные, яйцевидные, грушевидные, иногда шаровидные, цилиндрические или веретеновидные; радиально- или билатерально симметричные, редко дорсивентральные или слегка ассиметричные. Размеры клеток весьма разнообразны. Длина может быть от 5 мк до 29 мк, ширина от 4 мк до 20 мк; объём клеток от 70 куб.мк до 4500 куб.мк5. Хлоропласт по цвету чаще всего зелёный, иногда жёлтый или бурый. По форме хлоропласт обычно чашевидный с пиреноидом и глазком, реже без них.
В отличие от многих других водорослей, клетки дуналиелли лишены целлюлозной или пектиновой оболочки и окружены лишь тонкой эластичной протоплазматической мембраной (плазмалеммой). По обе стороны от папиллы, на выпуклом апикальном конце клетки прикреплены два жгутика, с обычной микроструктурой (9 + 2 микротрубочки). Обычно жгутики одинаковой длины, равной или превышающей длину клетки. У молодых, только что разделившихся клеток один из жгутиков может быть короче другого. Как и вся клетка, жгутики покрыты протоплазматической мембраной. Клетки водоросли способны двигаться благодаря веслоподобным движениям жгутиков. Дуналиелля проявляет ярко выраженный положительный фототаксис.
Для Dunaliella salina характерны как бесполый, так и половой типы размножения. Первый является преобладающим. Деления клеток продольное. Последовательность деления органелл строго не детерминирована и легко нарушается, особенно в старых культурах. При этом образуются уродливые формы. В неблагоприятных условиях дуналиелла способна образовывать цисты бесполого происхождения. Цисты имеют шаровидную форму, толстую двойную оболочку и гранулированное содержимое, освобождение которого при прорастании происходит через щель в оболочке. Перед прорастанием цисты, её содержимое красного цвета зеленеет и делится с образованием 2-4 клеток. Половой процесс у Dunaliella salina — гологамного типа. Копуляция может происходить как на свету, так и в темноте. В результате слияния двух клеток образуется неподвижная зигота, покрытая оболочкой (иногда слоистой). Перед прорастанием происходит редукционное деление с образованием 2-32 клеток. Количество последних зависит от размеров зиготы и условий, в которых она развивалась.
Исследование биологии D. salina и экологических факторов, вызывающих ее переход к активному накоплению β-каротина в естественных условиях, показало, что биосинтез этого соединения является приспособительной реакцией организмов в ответ на экстремальные условия роста, к которым относятся изменения солености и минерального состава среды, температуры и освещенности, а также сочетания комплекса указанных параметров.
Оценка запасов каротиноидов в водоемах соляных промыслов Крымского полуострова
Нами были исследованы несколько водоемов солевых промыслов Крымского полуострова и юга Украины, в частности Сакского (Рис.2), Сивашского и Херсонского сольпромов.
Рис. 2. Сакский сольпром. Вид бассейнов для садки соли с высоты 2 км. Белого цвета – выпаренная соль; красно-коричневый цвет бассейнов обусловлен в значительной степени высокой концентрацией в рапе клеток Dunaliella
В Таблице 2 представлены средние данные по ряду наблюдений за 2007 год. Всего было обработано 90 проб. Наиболее адекватными для оценки численности водоросли в течение года являются ее модальные значения, которые оказались в пределах 19 – 37 млн.кл/л.
Таблица 2. Средние и модальные значения численности (млн.кл./л) Dunaliella salina в исследуемых водоемах Херсонского сольпрома
Содержание каротинов в клетке в значительной мере зависит от размера клетки и условий роста. По 80 определениям мы нашли, что содержание каротинов в среднем составляло 0,69 нанограмм /клетку при очень широком варьировании от 0,03 до 31,26 нг/кл. Заметим, что сильное варьирование исходных параметров не позволяет с большой вероятностью события оценить содержание каротинов в расчете на клетку для каждого конкретного случая. Кроме того, использовать полученное среднее значение для оценки содержания каротинов в литре воды по данным о численности клеток в исследуемых водоемах не вполне корректно также по той причине, что зависимость концентрации каротинов (мг/л) от концентрации клеток (млн.кл./л) в воде, как выяснилось, носит нелинейный характер (рис. 3) и хорошо описывается уравнением:
Рис. 3. Зависимость концентрации каротинов (мг/л) от концентрации клеток (млн.кл./л) в исследованных водоемах.
где х – концентрация клеток, млн.кл./л; у – концентрации каротинов, мг/л.
Приняв во внимание модальные концентрации клеток в водоемах, и воспользовавшись полученным уравнением, получим, что “обычное” (наиболее часто встречающееся) содержание каротинов в этих водоемах (по взятым пробам) составляет 3,42 – 4,51 мг/л.
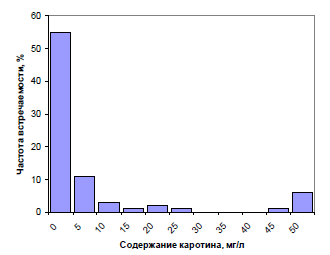
Фактическое распределение содержания каротина в 1 л воды по частоте встречаемости в 80 пробах из исследуемых водоемов, представленное на рис. 4, подтверждает сделанный расчет.
Рис. 4. Распределение содержания каротина (мг/л) по частоте встречаемости в 80 пробах из исследуемых водоемов.
Таким образом, на одном квадратном метре бассейна при средней толщине слоя рапы 25 см текущее содержание каротина будет равняться 855 – 1128 мг, что соответствует 8,6 – 11,3 кг/га. Подчеркнем, что такое содержание каротина является типичным для водоемов соляных промыслов в их “естественном” состоянии, направленном на получение и добычу соли, когда не ставится цель получения каротина как продукта производства. Иногда (6% случаев) в естественных условиях в водоемах достигались очень высокие концентрации каротинов, превышавшие 50 мг/л, из них в двух случаях – более 100 мг/л при концентрации клеток более 3 млрд./л.
Практика показывает, что концентрацию каротинов в рапе можно повысить в десятки и сотни раз при использовании следующих технологических приемов:
- управляемое (в имеющихся водоемах) выращивание водоросли с использованием оптимальных режимов солености, внесения биогенных элементов и регулирования состава солей;
- инициация накопления каротинов в клетках водорослей при изменении должным образом режимов солености, освещенности слоя (регулирование толщины слоя воды), концентрации биогенных элементов (особенно азота);
- защита популяции водоросли от хищников (рачок Artemia salina) путем изменения солености;
- отстаивание, с использованием явления фототаксиса водорослей;
- флотация.
Дальнейшее соосаждение каротина с гидроокисью магния позволяет еще больше увеличить концентрацию каротина и получить продукт (пасту), допускающую длительное хранение каротина без разложения. Это очень важно, если учесть сезонность вегетации водоросли в естественных водоемах; открывается возможность последующей переработки пасты и извлечения из нее каротина в зимние, менее загруженные месяцы.
Предыдущий опыт получения каротина в условиях соленых лиманов юга Украины
Метод массового культивирования D. salina с целью полупромышленного получения β-каротина был впервые положен в основу создания экспериментального каротинового хозяйства площадью 0,5 га на базе Сакского химического завода в Крыму в 1965-1968 гг (Рис. 56). Для выращивания водоросли использовалась дешевая хлормагниевая рапа и удобрения (суперфосфат, аммиачная селитра, калийная соль и др.) Опытное хозяйство располагало пятнадцатью 200-литровыми пластиковыми лотками, четырьмя однокубовыми и четырьмя пятикубовыми бетонированными бассейнами, в которых размножали посевной материал, а также рядом промышленных бассейнов с земляным дном (рис. 5), в которых проходил второй этап – накопление каротина. Опыты, проведенные в этом хозяйстве в 1965-1968 гг., показали возможность получения на юге Украины до 120 кг каротина/га за вегетационный сезон (7 месяцев).
Ведущие производители и примеры продукции с содержанием каротина, получаемого из водоросли Dunaliella salina
Массовое культивирование Dunaliella salina с целью получения бета-каротина осуществляется сегодня в Австралии, Израиле, Испании, Китае, США. Крупнейшие в мире биотехнологические фирмы: Betatene Pty Ltd на юге Австралии и Western Biotechnology Pty Ltd на западе Австралии, входящие в международную корпорацию Cognis7, имеют пруды для выращивания Dunaliella площадью более 800 гектар (рис. 6)..
В США Cyanotech Inc. (рис. 7) и Microbio Resources, Inc. (San Diego, Калифорния, США), производят каждая по 1,5 т β-каротина в год из биомассы дуналиелли. Имеются данные о том, что компания Microbio Resources инвестировала в развитие мощностей по выращиванию Dunaliella и получению из нее каротина свыше 15 млн. долларов США
Крупные производители бета-каротина имеются также в Индии (Arora aromatics, Uttar Pradesh) и Китае (Shandong Binzhou Tianjian Biotechnology Co., Ltd.)8. Например, фирма Arora aromatics готова ежемесячно поставлять 5 тонн порошка (сухой биомассы) Dunaliella.
Массовое производство каротина налажено в Израиле (компания Nature Beta Technologies9).
В Украине и России единственным на сегодняшний день (по заявлению самой фирмы) производителем натуральных каротиноидов из гриба Blakeslea является группа «НПП «ВИТАН» 10. Фирма производит и реализует такую продукцию как:
- Биомасса бета-каротина с содержанием бета-каротина 6-7%.
- Биомасса ликопина с содержанием ликопина 3-5%.
- Масляные растворы бета-каротина в рафинированном дезодорированном подсолнечном масле, в которых содержится от 0,2 до 1,0% бета.
- Масляная суспензия бета-каротина 2,5. 30%
- Кристаллы бета-каротина 95%
- Диетическая добавка «Каренол+», содержит 0,2% раствора бета-каротина в подсолнечном масле.
- Масло каротиновое содержит 0,015% бета-каротина, растворенного в подсолнечном масле.
Заключение
Мировой опыт получения каротинов из солоноводной одноклеточной водоросли Dunaliella salina показывает не только возможность, но и перспективность этого биотехнологического направления. Условия водоемов Крыма и юга Украины обеспечивают достаточную сырьевую базу для производства каротина. Грамотно используемые технологические приемы в состоянии существенно повысить выход конечного продукта. Предыдущий, в целом положительный опыт выращивания водоросли в опытно-промышленных масштабах свидетельствует о реальности данного проекта.
Источник