- Соли алюминия: получение и свойства
- Соли алюминия
- Нитрат и сульфат алюминия
- Комплексные соли алюминия
- Гидролиз солей алюминия
- Алюминаты
- Получение алюминия
- Производство и получение алюминия
- Получение глинозема
- Бокситовая руда
- Получение глинозема из бокситовых руд
- Получение алюминия электролизом
- Получение рафинированного алюминия
- Рафинирование методом трехслойного электролиза
Соли алюминия: получение и свойства
Соли алюминия
Нитрат и сульфат алюминия
Нитрат алюминия при нагревании разлагается на оксид алюминия, оксид азота (IV) и кислород:
Сульфат алюминия при сильном нагревании разлагается аналогично — на оксид алюминия, сернистый газ и кислород:
Комплексные соли алюминия
Для описания свойств комплексных солей алюминия — гидроксоалюминатов, удобно использоваться следующий прием: мысленно разбейте тетрагидроксоалюминат на две отдельные молекулы — гидроксид алюминия и гидроксид щелочного металла.
Например , тетрагидроксоалюминат натрия разбиваем на гидроксид алюминия и гидроксид натрия:
Na[Al(OH)4] разбиваем на NaOH и Al(OH)3
Свойства всего комплекса можно определять, как свойства этих отдельных соединений.
Таким образом, гидроксокомплексы алюминия реагируют с кислотными оксидами .
Например , гидроксокомплекс разрушается под действием избытка углекислого газа. При этом с СО2 реагирует NaOH с образованием кислой соли (при избытке СО2), а амфотерный гидроксид алюминия не реагирует с углекислым газом, следовательно, просто выпадает в осадок:
Аналогично тетрагидроксоалюминат калия реагирует с углекислым газом:
По такому же принципу тетрагидроксоалюминаты реагирует с сернистым газом SO2:
А вот под действием избытка сильной кислоты осадок не выпадает, т.к. амфотерный гидроксид алюминия реагирует с сильными кислотами.
Например , с соляной кислотой:
Правда, под действием небольшого количества ( недостатка ) сильной кислоты осадок все-таки выпадет, для растворения гидроксида алюминия кислоты не будет хватать:
Аналогично с недостатком азотной кислоты выпадает гидроксид алюминия:
Комплекс разрушается при взаимодействии с хлорной водой (водным раствором хлора) Cl2:
2Na[Al(OH)4] + Cl2 → 2Al(OH)3↓ + NaCl + NaClO
При этом хлор диспропорционирует.
Также комплекс может прореагировать с избытком хлорида алюминия. При этом выпадает осадок гидроксида алюминия:
Если выпарить воду из раствора комплексной соли и нагреть образующееся вещество, то останется обычная соль-алюминат:
Гидролиз солей алюминия
Растворимые соли алюминия и сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. чуть-чуть:
I ступень: Al 3+ + H2O = AlOH 2+ + H +
II ступень: AlOH 2+ + H2O = Al(OH )2 + + H +
Однако сульфиды, сульфиты, карбонаты алюминия и их кислые соли гидролизуются необратимо, полностью, т.е. в водном растворе не существуют, а разлагаются водой:
Более подробно про гидролиз можно прочитать в соответствующей статье.
Алюминаты
Соли, в которых алюминий является кислотным остатком (алюминаты) — образуются из оксида алюминия при сплавлении с щелочами и основными оксидами:
Для понимания свойств алюминатов их также очень удобно разбить на два отдельных вещества.
Например, алюминат натрия мы разделим мысленно на два вещества: оксид алюминия и оксид натрия.
NaAlO2 разбиваем на Na2O и Al2O3
Тогда нам станет очевидно, что алюминаты реагируют с кислотами с образованием солей алюминия :
KAlO2 + 4HCl → KCl + AlCl3 + 2H2O
NaAlO2 + 4HCl → AlCl3 + NaCl + 2H2O
Под действием избытка воды алюминаты переходят в комплексные соли:
Источник
Получение алюминия
Производство и получение алюминия
Металлический алюминий получают в три стадии:
- Получение глинозема (Al2O3) из алюминиевых руд;
- Получение алюминия из глинозема;
- Рафинирование алюминия.
Получение глинозема
Около 95 % всего глинозема получают из бокситовых руд.
Бокситовая руда
Боксит (фр. bauxite) (по названию местности Baux на юге Франции) – алюминиевая руда, состоящая из гидроксидов алюминия, оксидов железа и кремния, сырьё для получения глинозёма и глинозёмосодержащих огнеупоров. Содержание глинозёма в промышленных бокситах колеблется от 40 % до 60 % и выше. Используется также в качестве флюса в чёрной металлургии.
Рисунок 1 – Бокситовая руда
Обычно бокситы представляют собой землистую глиноподобную массу, которая может иметь полосчатую, пизолитовую (гороховидную) либо однородную текстуру. В обычных условиях выветривания полевые шпаты (минералы, составляющие большую часть земной коры и являющиеся алюмосиликатами) разлагаются с образованием глин, но в условиях жаркого климата и высокой влажности конечным продуктом их разложения могут оказаться бокситы, т. к. подобная обстановка благоприятствует выносу щелочей и кремнезёма, особенно из сиенитов или габбро. Бокситы перерабатывают в алюминий поэтапно: сначала получают оксид алюминия (глинозём), а затем металлический алюминий (электролитическим способом в присутствии криолита).
Основные примеси в бокситах это Fe2O3, SiO2, TiO2. К малым примесям бокситов относят: Na2O, K2O, CaO, MgO, редкоземельные элементы, Cr, P, V, F, органика.
Обычно бокситы классифицируют:
- по цвету;
- по основному минералу (чаще они бывают смешанными);
- по возрасту.
Основными критериями качества алюминиевой руды являются :
- Кремниевый модуль (Мsi = Al2O3/SiO2 (% масс.)). Чем больше кремниевый модуль тем лучше качество (Мsi = 7);
- Содержание железа в пересчете на Fe2O3. Если содержание Fe2O3около 18 % масс., то боксит считается высокожелезистым. Чем больше содержание железа труднее добыть бокситы;
- Содержание серы. Наличие большого количества серы усложняет переработку боксита;
- Содержание карбонатов в пересчете на CO3 (2-) . Наличие большого количества карбонатов усложняет переработку боксита.
- в производстве глинозема;
- в производстве абразивных материалов;
- в производстве огнеупорных материалов;
- в качестве флюса для выплавки мартеновской стали;
- для сушки газов и чистки нефти от серы;
- в качестве красителя.
На сегодняшний день главными поставщиками боксита являются:
- Австралия – там находятся также огромные залежи Fe, Au, U, Ni, Co, Cuи др. Выгоднее покупать сырье у Австралии, чем перерабатывать свое.
- Гвинея – У России есть несколько купленных мест.
- Центральная Америка: Гайана, Ямайка, Суриман.
- Бразилия.
В Европе все месторождения истощены. Осуществляются поставки бокситов из Греции, но данное сырье является сырьем низкого качества.
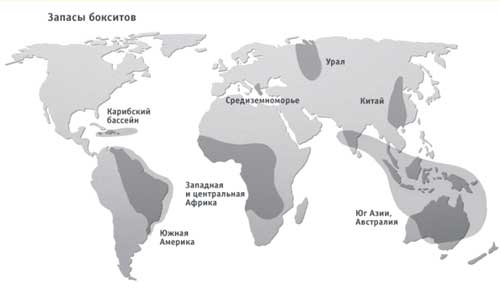
Рисунок 2 – Запасы бокситов в мире
Ниже представлен основных месторождений алюминиевых руд в России.
- Первое месторождение было открыто в 1914 г. под Сант-Петербургов, рядом с городом Тихвин. На данном месторождении было построено 6 заводов. Самый большой — это Волховский алюминиевый завод. На сегодняшний день Тихвинское месторождение истощено и работает в основном на привозном сырье.
- В 1931 г. было открыто уникальное Северо-Уральское месторождение высококачественных бокситов (СУБР). Оно послужило базой для строительства в 1939 г. Уральского алюминиевого завода (УАЗ). А на основе Южно-уральского бокситового рудника (ЮУБР) был построен Богословский алюминиевый завод (БАЗ).
- Североонежское месторождение находится по дороге на Кольский полуостров. В Плане есть, но дата строительства неизвестна.
- Висловское месторождение – чистоглинистое месторождение каолитного типа. Для глинозема не используется.
- Тиманское месторождение (Республика Коми, Варкута). Канадцы заинтересованы в данном месторождении, поэтому планируют строительство заводов («Коми Суал» — холдинг).
Получение глинозема из бокситовых руд
Поскольку алюминий амфотерен, глинозем получают тремя способами:
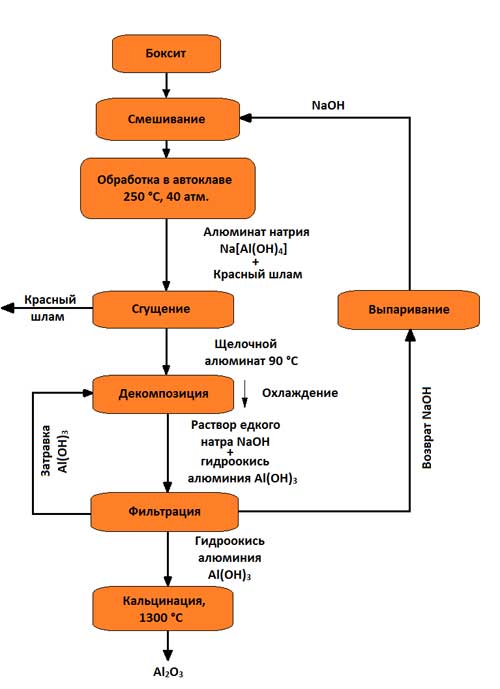
Наибольшее распространение имеет щелочной способ (метод К. И. Байера, разработанный в России в конце позапрошлого столетия и применяемый для переработки высокосортных бокситов с небольшим количеством (до 5 – 6 %) кремнезема). С тех пор техническое выполнение его было существенно улучшено. Схема производства глинозема по способу Байера представлена на рисунке 3.
Рисунок 3 – Схема получения глинозема по способу Байера
Сущность способа состоит в том, что алюминиевые растворы быстро разлагаются при введении в них гидроокиси алюминия, а оставшийся от разложения раствор после его выпаривания в условиях интенсивного перемешивания при 169 – 170 °С может вновь растворять глинозем, содержащийся в бокситах. Этот способ состоит из следующих основных операций:
1. Подготовки боксита, заключающийся в его дроблении и измельчении в мельницах; в мельницы подают боксит, едкую щелочь и небольшое количество извести, которое улучшает выделение Al2O3; полученную пульпу подают на выщелачивание;
2. Выщелачивания боксита (в последнее время применяемые до сих пор блоки автоклав круглой формы частично заменены трубчатыми автоклавами, в которых при температурах 230 – 250 °С (500 – 520 К) происходит выщелачивание), заключающегося в химическом его разложении от взаимодействия с водным раствором щелочи; гидраты окиси алюминия при взаимодействии со щелочью переходят в раствор в виде алюмината натрия:
содержащийся в боксите кремнезем взаимодействует со щелочью и переходит в раствор в виде силиката натрия:
в растворе алюминат натрия и силикат натрия образуют нерастворимый натриевый алюмосиликат; в нерастворимый остаток переходят окислы титана и железа, предающие остатку красный цвет; этот остаток называют красным шламом. По окончании растворения полученный алюминат натрия разбавляют водным раствором щелочи при одновременном понижении температуры на 100 °С;
3. Отделения алюминатного раствора от красного шлама обычно осуществляемого путем промывки в специальных сгустителях; в результате этого красный шлам оседает, а алюминатный раствор сливают и затем фильтруют (осветляют). В ограниченных количествах шлам находит применение, например, как добавка к цементу. В зависимости от сорта бокситов на 1 т полученной окиси алюминия приходится 0,6 – 1,0 т красного шлама (сухого остатка);
4. Разложения алюминатного раствора. Его фильтруют и перекачивают в большие емкости с мешалками (декомпозеры). Из пересыщенного раствора при охлаждении на 60 °С (330 К) и постоянном перемешивании извлекается гидроокись алюминия Al(OH)3. Так как этот процесс протекает медленно и неравномерно, а формирование и рост кристаллов гидроокиси алюминия имеют большое значение при ее дальнейшей обработке, в декомпозеры добавляют большое количество твердой гидроокиси – затравки:
5. Выделения гидроокиси алюминия и ее классификации; это происходит в гидроциклонах и вакуум-фильтрах, где от алюминатного раствора выделяют осадок, содержащий 50 – 60 % частиц Al(OH)3. Значительную часть гидроокиси возвращают в процесс декомпозиции как затравочный материал, которая и остается в обороте в неизменных количествах. Остаток после промывки водой идет на кальцинацию; фильтрат также возвращается в оборот (после концентрации в выпарных аппаратах – для выщелачивания новых бокситов);
6. Обезвоживания гидроокиси алюминия (кальцинации); это завершающая операция производства глинозема; ее осуществляют в трубчатых вращающихся печах, а в последнее время также в печах с турбулентным движением материала при температуре 1150 – 1300 °С; сырая гидроокись алюминия, проходя через вращающуюся печь, высушивается и обезвоживается; при нагреве происходят последовательно следующие структурные превращения:
200 °C – 950 °С – 1200 °С.
В окончательно прокаленном глиноземе содержится 30 – 50 % α-Al2O3 (корунд), остальное γ-Al2O2.
Этим способом извлекается 85 – 87 % от всего получаемого глинозема. Полученная окись алюминия представляет собой прочное химическое соединение с температурой плавления 2050 ° С [7].
Получение алюминия электролизом
Электролитическое восстановление окиси алюминия, растворенной в расплаве на основе криолита, осуществляется при 950-970 °С в электролизере. Электролизер состоит из футерованной углеродистыми блоками ванны, к подине которой подводится электрический ток. Выделившийся на подине, служащей катодом, жидкий алюминий тяжелее расплава соли электролита, поэтому собирается на угольном основании, откуда его периодически откачивают (рисунок 4). Сверху в электролит погружены угольные аноды, которые сгорают в атмосфере выделяющегося из окиси алюминия кислорода, выделяя окись углерода (CO) или двуокись углерода (CO2). На практике находят применение два типа анодов:
- самообжигающиеся аноды Зедерберга, состоящие из брикетов, так называемых «хлебов» массы Зедерберга (малозольный уголь с 25 – 35 % каменноугольного пека), набитых в алюминиевую оболочку; под действием высокой температуры анодная масса обжигается (спекается);
- обожженные, или «непрерывные», аноды из больших угольных блоков (например, 1900 × 600 × 500 мм массой около 1,1 т).
Рисунок 4 – Схема электролизера
Сила тока на электролизерах составляет 150 000 А. Они включаются в сеть последовательно, т. е. получается система (серия) – длинный ряд электролизеров.
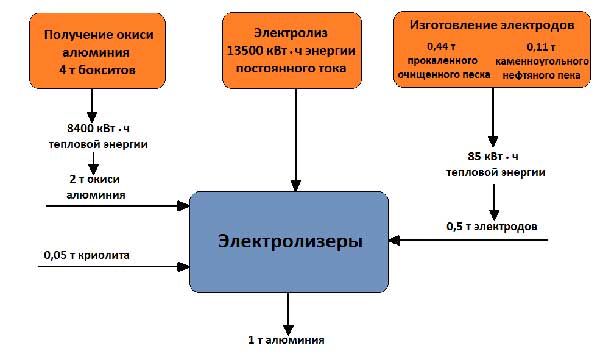
Рабочее напряжение на ванне, составляющее 4 – 5 В, значительно выше напряжения, при котором происходит разложение окиси алюминия, поскольку в процессе работы неизбежны потери напряжения в различных частях системы. Баланс сырья и энергии при получении 1 т алюминия представлен на рисунке 5.
Рисунок 5 – Баланс сырья и энергии при получении 1 т алюминия
Вреакционном сосуде окись алюминия превращается сначала в хлорид алюминия. Затем в плотно изолированной ванне происходит электролиз AlCl3, растворенного в расплаве солей KCl, NaCl. Выделяющийся при этом хлор отсасывается и подается для вторичного использования; алюминий осаждается на катоде.
Преимуществами данного метода перед существующим электролизом жидкого криолитоглиноземного расплава (Al2O3, растворенная в криолите Na3AlF6) считают: экономию до 30 % энергии; возможность применения окиси алюминия, которая не годится для традиционного электролиза (например, Al2O3 с высоким содержанием кремния); замену дорогостоящего криолита более дешевыми солями; исчезновение опасности выделения фтора [7].
Получение рафинированного алюминия
Для алюминия рафинирующий электролиз с разложением водных солевых растворов невозможен. Поскольку для некоторых целей степень очистки промышленного алюминия (Al 99,5 – Al 99,8), полученного электролизом криолитоглиноземного расплава, недостаточна, то из промышленного алюминия или отходов металла путем рафинирования получают еще более чистый алюминий (Al 99,99 R). Наиболее известен метод рафинирования — трехслойный электролиз.
Рафинирование методом трехслойного электролиза
Одетая стальным листом, работающая на постоянном токе (рисунок 6) ванна для рафинирования состоит из угольной подины с токоподводами и теплоизолирующей магнезитовой футеровки. В противоположность электролизу криолитоглиноземного расплава анодом здесь служит, как правило, расплавленный рафинируемый металл (нижний анодный слой). Электролит составляется из чистых фторидов или смеси хлорида бария и фторидов алюминия и натрия (средний слой). Алюминий, растворяющийся из анодного слоя в электролите, выделяется над электролитом (верхний катодный слой). Чистый металл служит катодом. Подвод тока к катодному слою осуществляется графитовым электродом.
Рисунок 6 — Схема электролизера с передним горном для рафинирования алюминия (по Фульда — Гинзбергу)
1 – алюминиевый расплав; 2 – электролит; 3 – рафинированный алюминий высокой частоты; 4 – катод из графита; 5 – магнезитовая стена; 6 – передний горн; 7 – изолирующий слой; 8 – боковая изоляция; 9 – угольная подина; 10 – анодный токопровод; 11 – изоляция подины; 12 – железный короб; 13 – крышка
Ванна работает при 750 – 800 °С, расход электроэнергии составляет 20 кВт ч на 1 кг чистого алюминия, т. е. несколько выше, чем при обычном электролизе алюминия.
Металл анода содержит 25 – 35 % Cu; 7 – 12 % Zn; 6 – 9 % Si; до 5 % Fe и незначительное количество марганца, никеля, свинца и олова, остальное (40 – 55 %) – алюминий. Все тяжелые металлы и кремний при рафинировании остаются в анодном слое. Наличие магния в электролите приводит к нежелательным изменениям состава электролита или к сильному его ошлакованию. Для очистки от магния шлаки, содержащие магний, обрабатывают флюсами или газообразным хлором.
В результате рафинирования получают чистый алюминий (99,99 %) и продукты сегрегации (зайгер-продукт), которые содержат тяжелые металлы и кремний и выделяются в виде щелочного раствора и кристаллического остатка. Щелочной раствор является отходом, а твердый остаток применяется для раскисления.
Рафинированный алюминий имеет обычно следующий состав, %: Fe 0,0005 – 0,002; Si 0,002 – 0,005; Cu 0,0005 – 0,002; Zn 0,0005 – 0,002; Mg следы; Al остальное.
Рафинированный алюминий перерабатывают в полуфабрикат в указанном составе или легируют магнием (таблица 1).
Таблица 1 – Химический состав алюминия повышенной чистоты и первичного алюминия по DIN 1712, лист 1
Источник