- Лабораторные способы получения неорганических веществ
- Получение углекислого газа в лаборатории
- Получение угарного газа в лаборатории
- Получение сероводорода в лаборатории
- Получение аммиака в лаборатории
- Получение азотной кислоты в лаборатории
- Получение ортофосфорной кислоты в лаборатории
- Получение кремния в лаборатории
- Получение кислорода в лаборатории
- Получение водорода в лаборатории
- Получение хлора в лаборатории
- Получение хлороводорода в лаборатории
- Добавить комментарий Отменить ответ
- Способы получения алканов
- Способ получение любого получения
- Таблица Менделеева
- Универсальная таблица растворимости
- Коллекция таблиц к урокам по химии
- Общая характеристика и способы получения металлов
- Пирометаллургия
- Гидрометаллургия
- Электрометаллургия
Лабораторные способы получения неорганических веществ
Основные способы получения (в лаборатории) конкретных веществ, относящихся к изученным классам неорганических соединений.
Лабораторные способы получения веществ отличаются от промышленных:
| Лабораторные способы получения веществ | Промышленные способы получения веществ |
| Реагенты могут быть редкими и дорогими | Реагенты распространенные в природе и дешевые |
| Условия реакции мягкие, без высоких давлений и сильного нагревания | Условия реакции могут быть довольно жесткими, допустимы высокие давления и температуры |
| Как правило, реагенты — жидкости или твердые вещества | Реагенты — газы или жидкости, реже твердые вещества |
Получение углекислого газа в лаборатории
Углекислый газ CO2 в лаборатории получают при помощи аппарата Киппа при взаимодействии соляной кислоты с мелом или мрамором:
Получение угарного газа в лаборатории
В лаборатории угарный газ проще всего получить, действуя концентрированной серной кислотой на муравьиную кислоту:
HCOOH → H2O + CO
Получение сероводорода в лаборатории
Сероводород в лаборатории легко получить действием разбавленной серной кислоты на сульфиды металлов, например, сульфид железа (II):
Эта реакция также проводится в аппарате Киппа.
Получение аммиака в лаборатории
Аммиак в лаборатории получают при нагревании смеси солей аммония с щелочами.
Например , при нагревании смеси хлорида аммония с гашеной известью:
Эти вещества тщательно перемешивают, помещают в колбу и нагревают.
Получение азотной кислоты в лаборатории
Азотную кислоту в лаборатории получают действием концентрированной серной кислоты на кристаллический нитрат натрия и калия при небольшом нагревании:
При этом менее летучая кислота вытесняет более летучую кислоту из соли.
При более сильном нагревании образуется сульфат натрия, но и образующаяся азотная кислота разлагается.
Получение ортофосфорной кислоты в лаборатории
При взаимодействии ортофосфата кальция с серной кислотой при нагревании образуется ортофосфорная кислота:
Получение кремния в лаборатории
В лаборатории кремний получают при взаимодействии смеси чистого песка с порошком магния:
2Mg + SiO2→ 3MgO + Si
Получение кислорода в лаборатории
Кислорода в лаборатории можно получить при разложении целого ряда неорганических веществ.
Чаще всего в лаборатории кислород получают разложением перманганата калия:
Выделяющийся кислород можно собрать вытеснением воздуха:
Также кислород можно собирать методом вытеснения воды:
Обнаружить кислород можно очень просто: тлеющая лучинка вспыхивает в атмосфере кислорода.
Кислород можно получить также разложением пероксида водорода:
Реакция катализируется оксидом марганца (IV) MnO2.
Разложение бертолетовой соли KClO3 — еще один способ получения кислорода в лаборатории:
2KClO3 → 2KCl + 3O2
Реакция также протекает в присутствии катализатора, оксида марганца (IV) MnO2.
Получение водорода в лаборатории
Водород в лаборатории можно получить различными методами.
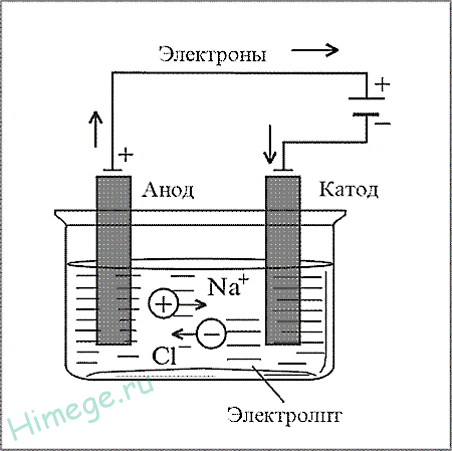
Под действием электрического тока вода разлагается на водород и кислород:
При взаимодействии минеральных кислот (не сильных окислителей) с активными металлами и металлами средней активности также образуется водород.
Например , соляная кислота реагирует с цинком с образованием водорода:
Zn + 2HCl → ZnCl2 + H2
Собирать водород можно методом вытеснения воздуха, так как водород — гораздо более легкий газ, чем воздух.
Также для собирания водорода подходит метод вытеснения воды, так как водород плохо растворим в воде:
Водород выделяется также при взаимодействии активных металлов (расположенных в ряду активности до магния) с водой.
Например , натрий активно реагирует с водой с образованием водорода:
2Na + 2H2O → 2NaOH + H2
Получение хлора в лаборатории
Стр. 162в лаборатории можно получить различными методами.
Под действием электрического тока вода разлагается на водород и кислород:
При взаимодействии минеральных кислот (не сильных окислителей) с активными металлами и металлами средней активности также образуется водород.
Получение хлороводорода в лаборатории
Стр. 162в лаборатории можно получить различными методами.
Под действием электрического тока вода разлагается на водород и кислород:
Добавить комментарий Отменить ответ
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.
Источник
Способы получения алканов
1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета.
| Например, хлорметан реагирует с натрием с образованием этана:
Хлорэтан взаимодействует с натрием с образованием бутана: Реакция больше подходит для получения симметричных алканов. При проведении синтеза со смесью разных галогеналканов образуется смесь разных алканов.
|