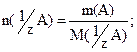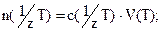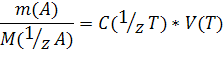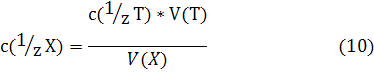Лекция 5. Общие приемы титрования. Закон эквивалентов. Расчеты в титриметрическом анализе.
Ключевые слова: метод пипетирования, метод отдельных навесок, прямое титрование, обратное титрование, титрование заместителя, закон эквивалентов.
В титриметрическом анализе концентрацию определяемого вещества рассчитывают по известным объемам реагирующих веществ и известной концентрации титранта. Титрование, как при определении концентрации, так и при выполнении анализов можно проводить двумя различными методами:
1. Метод пипетирования: навеску исходного (или анализируемого) вещества растворяют в мерной колбе, разбавляют водой до метки и тщательно перемешивают. Пипеткой отбирают отдельные порции раствора (аликвоты), переносят в колбу для титрования и титруют рабочим раствором.
2. Метод отдельных навесок:навеску исходного (или анализируемого) вещества растворяют в произвольном объеме растворителя в колбе для титрования, целиком оттитровывая полученный раствор.
В титриметрии используют три способа титрования: прямое, обратное и титрование заместителя.
В случае прямого титрования определяемое вещество А в процессе титрования непосредственно реагирует с раствором титранта В:
А + В ® продукты реакции.
Расчет результатов титриметрического анализа основан на законе эквивалентов, в соответствии с которым вещества реагируют между собой в строго определенных эквивалентных количествах. В точке эквивалентности:
Это важное следствие из закона эквивалентов применяется при всех расчетах в титриметрии. Массу вещества А, вступившего в реакцию, рассчитывают для метода отдельных навесок по формуле 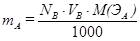
В том случае, если для анализа берут не весь раствор анализируемого вещества Vмк, а только часть его – аликвоту — Vп (метод пипетирования), предыдущее уравнение умножают на отношение (Vмк/Vп).
Обратное титрование (титрование по остатку) используется в тех случаях, когда реакция между веществами А и В протекает медленно или нет подходящего индикатора для фиксирования точки эквивалентности. В этом случае к раствору определяемого вещества А добавляют точно отмеренный, но заведомо избыточный объем титранта В и после завершения реакции между ними остаток вещества В оттитровывают рабочим раствором D.
А + В(избыток) ® продукты реакции + В(остаток),
В(остаток) + D ® продукты реакции.
Количество молей эквивалентов определяемого вещества — nэкв(А) — в этом случае равно разности между количеством молей эквивалентов веществ В и D:
nэкв(А) = [nэкв(В) – nэкв(D)], откуда 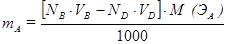
Например, количественное определение солей аммония нельзя провести прямым титрованием щелочью из-за отсутствия скачка на кривой титрования. Поэтому к анализируемому раствору добавляют точное количество щелочи (избыток). Остаток щелочи титруют рабочим раствором соляной кислоты.
Титрование заместителя (заместительное титрование) применяют в том случае, когда невозможно провести прямое титрование. В этом случае сначала проводят реакцию определяемого вещества А с избытком вспомогательного реагента D, в результате чего получается соединение А‘(заместитель), способное реагировать с титрантом В в строго эквивалентном соотношении:
А + D ® продукты реакции + А’,
А’ + В ® продукты реакции.
Количество молей эквивалентов при титровании заместителя А’ всегда равно количеству моль эквивалентов титранта В и равно количеству молей эквивалентов определяемого вещества А:
Расчет массы тА осуществляется по формуле, аналогичной формуле, используемой для расчетов результата прямого титрования.
Например, невозможно анализировать окислители прямым титрованием раствором йодида калия. В данном случае применяется метод замещения, в результате которого один окислитель замещается другим окислителем – йодом, а последний титруется тиосульфатом натрия.
Затраченный на титрование объем Na2S2O3 эквивалентен выделившемуся в первой реакции I2, а последний эквивалентен K2Cr2O7. Расчет массы или нормальности K2Cr2O7 основан на законе эквивалентов:
Контрольные вопросы
1. В чем суть метода пипетирования и метода отдельных навесок?
2. Сформулируйте закон эквивалентов.
3. Охарактеризуйте способ прямого титрования и приведите для него формулы расчета результатов анализа.
4. Охарактеризуйте способ обратного титрования и приведите для него формулы расчета результатов анализа.
5. Охарактеризуйте способ титрования заместителя и приведите для него формулы расчета результатов анализа.
Список рекомендуемой литературы
1. Васильев В.П. Аналитическая химия. Кн. 1. Титриметрические и гравиметрический методы анализа. — М.: Дрофа, 2005. — С. 60 – 88.
2. Харитонов Ю.Я. Аналитическая химия (аналитика): учебник для вузов. В 2 кн. Кн. 2. Количественный анализ. Физико-химические (инструментальные) методы анализа. – М.: Высшая школа, 2001. – С. 76 — 80.
Источник
III. Методы отдельных навесок и пипетирования
При проведении титрования можно брать либо определенную массу анализируемого вещества, либо точно отмеренный объем анализируемого раствора. В соответствии с этим различают два подхода: метод отдельных навесок и метод пипетирования.
1) В методе отдельных навесок взвешивают на аналитических весах точную навеску m(А) вещества А, количественно переносят ее в колбу для титрования, растворяют, прибавляя в колбу некоторое количество растворителя, и титруют полученный раствор. При этом объем титруемого раствора можно не измерять. n( 1 /zT) = n( 1 /zA) – закон эквивалентов.
Получают:
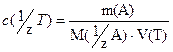
Титрование проводят заданное число раз (
2) В методе пипетирования отбирают с помощью калиброванной пипетки аликвоту — точно измеренный объем V(Х) анализируемого раствора вещества X с неизвестной молярной концентрацией эквивалента с( 1 /zХ) и титруют аликвоту стандартным раствором титранта с молярной концентрацией эквивалента с( 1 /zТ).
Пусть на титрование затрачен объем титранта V(Т).
n( 1 /zX) = n( 1 /zТ) по закону эквивалентов.
Определив концентрацию анализируемого раствора, можно рассчитать массу m(Х) вещества X во всем анализируемом растворе:
где Vк — объем всего анализируемого раствора в мерной колбе (объем
мерной колбы).
Если известна масса от исходной навески, содержащей определяемый компонент X, которая была растворена в мерной колбе при приготовлении анализируемого раствора, можно вычислить массовую долю W(X) определяемого компонента X в исходной анализируемой навеске:
Классификация методов титриметрического анализа.
Наиболее распространенная классификация титриметрических методов основана на различных типах используемых реакций.
1) Кислотно-основное титрование (метод нейтрализации) — титрование, основанное на реакции переноса протонов от одной реагирующей
частицы к другой в растворе. Различают ацидиметрию и алкалиметрию.
Ацидиметрия (ацидиметрическое титрование) — определение веществ титрованием стандартным раствором кислоты.
Алкалиметрия (алкалиметрическое титрование) — определение веществ титрованием стандартным раствором сильного основания.
2) Окислителъно-восстановительное титрование (редоксметрия) -титрование, сопровождаемое переходом одного или большего числа
электронов от иона-донора или молекулы (восстановителя) к акцептору
(окислителю).
3) Осадительное титрование — такое титрование, когда титруемое вещество при взаимодействии с титрантом выделяется из раствора в виде осадка.
4) Комплексиметрическое титрование — титрование вещества раствором такого соединения, которое образует с титруемым веществом слабодиссоциирующий растворимый комплекс.
Разновидностью комплексиметрического титрования является комплексонометрическое титрование (комплексонометрия) — такое титрование, когда титруемое вещество при взаимодействии с титрантом — раствором комплексонов — образует комплексонаты металлов.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Методы отдельных навесок и пипетироваиия



При проведении титрования можно брать либо определенную массу анализируемого вещества, либо точно отмеренный объем анализируемого раствора. В соответствии с этим различают два подхода: метод отдельных навесок и метод пипетирования
В методе отдельных навесоквзвешивают на аналитических весах точную навеску т(А) вещества А, количественно переносят ее в колбу для титрования, растворяют, прибавляя в колбу некоторое количество растворителя, и титруют полученный раствор. При этом объем титруемого раствора можно не измерять.
Пусть на титрование раствора вещества А затрачен объем V(Т) титранта с неизвестной молярной концентрацией эквивалента c (1/zТ). Поскольку А и Т реагируют в эквивалентных соотношениях, то их эквивалентные количества равны п(1/z А) = п(1/z Т). Эти эквивалентные количества можно выразить в виде
n (1/z А) = m(A) /M(1/z A) , п(1/z Т) = с(1/z Т)V(Т),
где М(1/z А) — молярная масса эквивалента вещества А. Левые части этих уравнений равны; значит, равны и правые части:
Отсюда с(1/z Т) = т(А) /М(1/z А)V(Т).
Титрование проводят заданное число раз (обычно от двух до пяти), каждый раз взвешивая новую навеску вещества А.
В методе пипетированияотбирают с помощью калиброванной пипетки аликвоту — точно измеренный объем V(Х) анализируемого раствора вещества X с неизвестной молярной концентрацией эквивалента с(1/z Х) и титруют аликвоту стандартным раствором титранта с молярной концентрацией эквивалента с(1/z Т).
Пусть на титрование затрачен объем титранта V(Т). Тогда, поступая аналогично изложенному выше в при выводе формулы получим
Определив концентрацию анализируемого раствора, можно по формуле рассчитать массу т(Х) вещества X во всем анализируемом растворе:
т(Х) = с(1/z Х )M (1/z Х )V к
где Vк — объем всего анализируемого раствора в мерной колбе (объем мерной колбы).
Если известна масса т исходной навески, содержащей определяемый компонент X, которая была растворена в мерной колбе при приготовлении анализируемого раствора, можно вычислить массовую долю W(Х) определяемого компонента X в исходной анализируемой навеске:
Классификация методов титриметрического анализа
Наиболее распространенная классификация титриметрических методов основана на различных типах используемых реакций.
1) Кислотно-основное титрование (метод нейтрализации)— титрование, основанное на реакции переноса протонов от одной реагирующей частицы к другой в растворе. Различают ацидиметрию и алкалиметрию.
Ацидиметрия (ацидиметрическое титрование)— определение веществ титрованием стандартным раствором кислоты.
Алкалиметрия (алкалиметрическое титрование)— определение веществ титрованием стандартным раствором сильного основания.
2) Окислительно-восстановительное титрование (редоксметрия)— титрование, сопровождаемое переходом одного или большего числа электронов от иона-донора или молекулы (восстановителя) к акцептору(окислителю).
3) Осадительное титрование— такое титрование, когда титруемое вещество при взаимодействии с титрантом выделяется из раствора в виде осадка.
4) Комплексиметрическое титрование— титрование вещества раствором такого соединения, которое образует с титруемым веществом слабодиссоциирующий растворимый комплекс.
Разновидностью комплексиметрического титрования является комплексонометрическое титрование (комтексонометрия) — такое титрование,когда титруемое вещество при -взаимодействии с титрантом —раствором комплексонов — образует комплексонаты металлов.
Виды титрования, применяемые в титриметрическом анализе
В титриметрическом анализе применяют прямое титрование, обратное титрование и косвенное титрование, или титрование по заместителю (заместительное титрование).
Прямое титрование — это такое титрование, когда определяемое вещество непосредственно титруется стандартным раствором титранта или наоборот. Расчет результатов прямого титрования проводится аналогично описанному
выше при характеристике метода пипетирования

где все обозначения соответствуют принятым ранее, причем объем мерной колбы Vк измеряется в литрах, а объем той же мерной колбы Vk — в миллилитрах: Vк’ = 1000 Vк.
Обратное титрование (титрование по остатку) — титрование непрореагировавшего вещества, которое прибавлено в избытке к анализируемому раствору в виде стандартного раствора. К аликвотной доле анализируемого раствора объемом V(Х)n прибавляют в избытке точно известный объем V(Т1) стандартного раствора вещества Т 1 с молярной концентрацией эквивалента с (1/z Т1). Определяемое вещество X реагирует с Т, нацело. Затем непрореагировавший избыток вещества Т, оттитровывают стандартным раствором титранта Т2. Схема реакций при обратном титровании:
X + Т1 = Продукты реакции,
Т1 + Т2 = Продукты реакции,
Расчет концентрации с(1/z Х) определяемого вещества X. Вещество Т1 реагирует с X и Т2, поэтому
здесь все обозначения соответствуют принятым ранее.
Источник