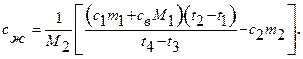- ОПРЕДЕЛЕНИЕ УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ ЖИДКОСТИ ПРИ ПОМОЩИ ЭЛЕКТРОКАЛОРИМЕТРА
- Удельная теплоемкость вещества
- Нагревание и охлаждение
- Виды теплопередачи
- Теплопроводность
- Конвекция
- Излучение
- Удельная теплоемкость: понятие и формула для расчета
- Таблица удельных теплоемкостей
- Исследовательский домашний эксперимент «Удельная теплоемкость»
- План 1-го занятия
- Беседа
- Теоретическая модель исследования
- Лабораторный практикум / 1-ая физическая лаборатория / 65 — Определение удельной теплоёмкости жидкости методом лучеиспускания / 65 — Определение удельной теплоёмкости жидкости методом лучеиспускания
ОПРЕДЕЛЕНИЕ УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ ЖИДКОСТИ ПРИ ПОМОЩИ ЭЛЕКТРОКАЛОРИМЕТРА



МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ
УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ИЖЕВСКАЯ ГОСУДАРСТВЕННАЯ СЕЛЬСКОХОЗЯЙСТВЕННАЯ
АКАДЕМИЯ»
Лаборатория механики и молекулярной физики №1(213а)
ЛАБОРАТОРНАЯ РАБОТА №12
ОПРЕДЕЛЕНИЕ УДЕЛЬНОЙ ТЕПЛОЁМКОСТИ ЖИДКОСТИ ПРИ ПОМОЩИ ЭЛЕКТРОКАЛОРИМЕТРА
Отредактировал: Кораблев Г.А.
ЛАБОРАТОРНАЯ РАБОТА №12
ОПРЕДЕЛЕНИЕ УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ ЖИДКОСТИ ПРИ ПОМОЩИ ЭЛЕКТРОКАЛОРИМЕТРА
Цель работы: ознакомление с калориметрическим методом определения удельной теплоемкости жидкости.
Приборы и принадлежности:1) два электрокалориметра с термометрами; 2) исследуемая жидкость; 3) вода.
Количество теплоты, необходимое для нагревания тела на один градус, называется теплоёмкостью данного тела, измеряется в СИ: Дж/К. Количество теплоты, необходимое для нагревания единицы массы вещества на один градус, называется удельной теплоемкостью вещества и обозначается буквой суд, измеряется в СИ: Дж/(кг . К). Количество теплоты, необходимое для нагревания одного моля вещества на один градус, называется молярной теплоемкостью вещества и обозначается буквой См, измеряется в СИ: Дж/(моль . К). Удельная и молярная теплоёмкости связаны между собой соотношением См = М . суд, где М – молекулярная масса данного вещества.
В данной работе определяется удельная теплоёмкость жидкости при помощи электрокалориметра. Метод электрокалориметра состоит в следующем: два калориметра, сделанных из одинакового материала, содержат различные жидкости. В первом калориметре находится вода, удельная теплоёмкость которой известна, а во втором – жидкость, удельную теплоёмкость которой требуется определить (см. рис. 1).
В оба калориметра опущены спирали, имеющие одинаковое электрическое сопротивление R. Если соединить спирали последовательно и пропустить через них электрический ток, то сила тока I, проходящего через обе спирали, будет одинакова. При этом спирали, нагреваясь, через некоторое время t передадут жидкостям равные количества теплоты 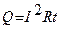
Количество теплоты, полученное калориметром с исследуемой жидкостью:
Q2 = (c2m2 + cжM2) . (t4 – t3) (2)
В формулах (1) и (2) введены следующие обозначения: М1 и М2 – массы воды и исследуемой жидкости в калориметрах; m1 и m2 – массы калориметров (вместе с мешалками); с1 и с2 – их теплоемкости; сж – теплоёмкость исследуемой жидкости, св – теплоёмкость воды, t1 и t2 – температура воды в начале и в конце опыта; t3 и t4 – температуры исследуемой жидкости в начале и в конце опыта.
Приравнивая Q1 и Q2, получим формулу для расчета удельной теплоёмкости исследуемой жидкости:
Для избежания ошибок, связанных с возможным незначительным изменением сопротивлений нагревателей, измерение удельной теплоёмкости жидкости проводят несколько раз.
Для уменьшения потерь на отдачу теплоты в окружающую среду, нагревание жидкостей, налитых в калориметры, рекомендуется проводить не выше, чем на 6-7 0 С, а для получения точного результата не ниже, чем на 4-5 0 С.
Источник
Удельная теплоемкость вещества
О чем эта статья:
Нагревание и охлаждение
Эти два процесса знакомы каждому. Вот нам захотелось чайку, и мы ставим чайник, чтобы нагреть воду. Или ставим газировку в холодильник, чтобы охладить.
Логично предположить, что нагревание — это увеличение температуры, а охлаждение — ее уменьшение. Все, процесс понятен, едем дальше.
Но не тут-то было: температура меняется не «с потолка». Все завязано на таком понятии, как количество теплоты. При нагревании тело получает количество теплоты, а при нагревании — отдает.
- Количество теплоты — энергия, которую получает или теряет тело при теплопередаче.
В процессах нагревания и охлаждения формулы для количества теплоты выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
В этих формулах фигурирует и изменение температуры, о котором мы сказали выше, и удельная теплоемкость, речь о которой пойдет дальше.
А вот теперь поговорим о видах теплопередачи.
Виды теплопередачи
- Теплопередача — это физический процесс передачи тепловой энергии от более нагретого тела к менее нагретому.
Здесь все совсем несложно, их всего три: теплопроводность, конвекция и излучение.
Теплопроводность
Тот вид теплопередачи, который можно охарактеризовать, как способность тел проводить энергию от более нагретого тела к менее нагретому.
Речь о том, чтобы передать тепло с помощью соприкосновения. Признавайтесь, грелись же когда-нибудь возле батареи. Если вы сидели к ней вплотную, то согрелись вы благодаря теплопроводности. Обниматься с котиком, у которого горячее пузо, тоже эффективно.
Порой мы немного перебарщиваем с возможностями этого эффекта, когда на пляже ложимся на горячий песок. Эффект есть, только не очень приятный. Ну а ледяная грелка на лбу дает обратный эффект — ваш лоб отдает тепло грелке.
Конвекция
Когда мы говорили о теплопроводности, мы приводили в пример батарею. Теплопроводность — это когда мы получаем тепло, прикоснувшись к батарее. Но все вещи в комнате к батарее не прикасаются, а комната греется. Здесь вступает конвекция.
Дело в том, что холодный воздух тяжелее горячего (холодный просто плотнее). Когда батарея нагревает некий объем воздуха, он тут же поднимается наверх, проходит вдоль потолка, успевает остыть и спуститься обратно вниз — к батарее, где снова нагревается. Таким образом, вся комната равномерно прогревается, потому что все более горячие потоки сменяют все менее холодные.
Излучение
Пляж мы уже упоминали, но речь шла только о горячем песочке. А вот тепло от солнышка — это излучение. В этом случае тепло передается через волны.
Обоими способами. То тепло, которое мы ощущаем непосредственно от камина (когда лицу горячо, если вы расположились слишком близко к камину) — это излучение. А вот прогревание комнаты в целом — это конвекция.
Удельная теплоемкость: понятие и формула для расчета
Формулы количества теплоты для нагревания и охлаждения мы уже разбирали, но давайте еще раз:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
В этих формулах фигурирует такая величина, как удельная теплоемкость. По сути своей — это способность материала получать или отдавать тепло.
С точки зрения математики удельная теплоемкость вещества — это количество теплоты, которое надо к нему подвести, чтобы изменить температуру 1 кг вещества на 1 градус Цельсия:
Удельная теплоемкость вещества
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Также ее можно рассчитать через теплоемкость вещества:
Удельная теплоемкость вещества
c — удельная теплоемкость вещества [Дж/кг*˚C]
C — теплоемкость вещества [Дж/˚C]
Величины теплоемкость и удельная теплоемкость означают практически одно и то же. Отличие в том, что теплоемкость — это способность всего вещества к передаче тепла. То есть формулу количества теплоты для нагревания тела можно записать в таком виде:
Количество теплоты, необходимое для нагревания тела
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Таблица удельных теплоемкостей
Удельная теплоемкость — табличная величина. Часто ее указывают в условии задачи, но при отсутствии в условии — можно и нужно воспользоваться таблицей. Ниже приведена таблица удельных теплоемкостей для некоторых (многих) веществ.
Источник
Исследовательский домашний эксперимент «Удельная теплоемкость»
Цель исследования: определить удельную теплоемкость воды, используя бытовые приборы учета потребления газа и электроэнергии.
Задачи исследования:
- провести опыт;
- вычислить значение удельной теплоемкости воды;
- оценить погрешность результата;
- сформулировать выводы.
План 1-го занятия
- Вводная беседа.
- Методика эксперимента.
- Техника безопасности.
- Оценка погрешности.
- Формулировка выводов.
Беседа
В природе не было бы ни весны, ни осени, если бы вода не обладала высокой удельной теплоемкостью.
Вода является незаменимым терморегулятором планеты. Благодаря большой теплоемкости мирового океана сглаживаются температурные переходы от зимы к лету и наоборот, что позволяет живым организмам постепенно приспосабливаться к новым сезонным условиям.
Высокая удельная теплоемкость воды способствует медленному нагреванию и охлаждению. Обитающие в воде организмы предохранены от резких колебаний температуры, приспосабливаясь к ритмическим колебаниям – суточным, сезонным, годовым. Вода в атмосфере оказывает смягчающее влияние на погодно-климатические условия.
Лучший иллюстратор большой теплоемкости воды — обыкновенный чайник. Если его пустым поставить на огонь, он быстро раскалится. А если наполнить водой, то за то же время он лишь слегка нагреется.
Так как теплоемкость воды высока, то она эффективно и быстро заберет излишки энергии. Поэтому вода широко применяется в производстве как удобный и доступный охладитель.
Да и дома мы наверняка знаем, что самый эффективный способ охладить сваренные вкрутую яйца или горячую сковородку – ополоснуть струей холодной воды.
Высокая удельная теплоемкость воды способствует её применению в отопительной системе, в медицинских грелках, в атомных реакторах.
Из-за высокой удельной теплоемкости воду широко используют в быту и технике. Например, в отопительных системах, для охлаждения обрабатываемых деталей.
Теоретическая модель исследования
Количество теплоты, необходимое для нагревания тела или выделяемое им при охлаждении, вычисляется по формуле Q = сm(t2— t1).
Из этой формулы можно выразить удельную теплоемкость: с = Q/(m ∙ Δt), где Δt = (t2 — t1).
Измерив начальную температуру воды и зная температуру кипения, можно определить изменение температуры Δt. Количество теплоты, необходимое для нагревания воды, определяется по расходу электроэнергии и газа (предварительно все другие потребители нужно отключить).
Перечень необходимого оборудования: бытовой мерный стакан, чайник, электрический чайник, прибор учета потребления газа, прибор учета потребления электроэнергии.
Последовательность действий:
- налить в чайник определенное количество воды;
- измерить начальную температуру воды;
- зафиксировать показание прибора учета;
- довести воду до кипения;
- зафиксировать показание прибора учета.
Оценка погрешности:
- Абсолютная погрешность: разность между точным значением и полученным результатом.
- Относительная погрешность: отношение абсолютной погрешности к точному значению.
- Какими факторами обусловлена погрешность?
Регистрация и обработка полученных данных:
а) Опыт с использованием электроэнергии
начальная температура воды t1, °С
конечная температура воды t2, °С
Источник
Лабораторный практикум / 1-ая физическая лаборатория / 65 — Определение удельной теплоёмкости жидкости методом лучеиспускания / 65 — Определение удельной теплоёмкости жидкости методом лучеиспускания
Определение удельной теплоёмкости жидкости методом лучеиспускания.
Нагретое тело, помещенное в среду с более низкой температурой, теряет тепло, излучая его в окружающую среду. Этот процесс можно описать эмпирическим законом Ньютона:
dQ = α · ( T − T 0 ) dt
— количество тепла dQ , отданное телом за небольшой отрезок времени dt , пропорционально разности температуры тела T и температуры окружающей среды T 0 ; коэффициент пропорциональности α — коэффициент теплоотдачи — определяется свойствами излучающей поверхности. Закон Ньютона достаточно хорошо выполняется при небольших (несколько градусов) разностях температур T − T 0 . Излучение ведет к уменьшению внутренней энергии тела и, если эта энергия определяется только хаотическим (тепловым) движением атомов и молекул тела (в частности, не протекают никакие химические реакции, не происходит изменение агрегатного состояния вещества и т.п.), то можно записать
где C — теплоёмкость тела и dT — изменение его температуры.
Из формул (1) и (2) следует
α ( T − T 0 ) dt = − CdT .
Измерив скорость охлаждения тела, можно вычислить его теплоёмкость, если известен коэффициент теплоотдачи α . Этот коэффициент можно определить, исследуя охлаждение другого тела, принятого за эталонное, теплоёмкость которого известна, а поверхность имеет те же свойства, что и поверхность исследуемого тела. На этом и основан способ определения удельной теплоёмкости жидкости методом лучеиспускания.
Исследуемую жидкость наливают в сосуд, изготовленный из теплопроводного материала, нагревают, а затем наблюдают её остывание, происходящее благодаря излучению. Фиксируют зависимость температуры жидкости и внешней среды от времени.
Пусть за время dt температура жидкости изменилась на dT . Тогда, согласно формуле (3),
α ( T − T 0 ) dt = − ( cm +ω ) dT .
Здесь m — масса жидкости, c — её удельная теплоёмкость и ω — тепловой эквивалент сосуда, в который она налита. Интегрируя обе части равенства, получим уравнение, описывающее охлаждение жидкости от температуры T 1 до T 2 , происходящее за промежуток времени от t 1 до t 2 :
α ( T − T 0 ) dt = − ( cm +ω )( T 2 − T 1 ) .
Левую часть равенства можно упростить, если считать, что величина коэффициента α не меняется за время остывания, т.е. не зависит от температур T и T 0 (в действительности это верно лишь приблизительно). Вынося α за знак
α ( T − T 0 ) dt = − ( cm +ω )( T 2 − T 1 ) ,
S = Z ( T − T 0 ) dt .
Величину интеграла S можно определить графически. Начертим график зависимости температур T и T 0 от времени (рис.1). Из рисунка видно, что S равно площади, заключенной между кривыми T ( t ), T 0 ( t ) и прямыми t = t 1 и t = t 2 .
Чтобы определить коэффициент α , проделываем такие же измерения с эталонной жидкостью. Её наливаем в такой же сосуд, что и исследуемую жидкость, — этим достигаются одинаковые условия теплоотдачи для обеих жидкостей. Для эталонной жидкости получим аналогичные соотношения:
α · S э = − ( c э m э +ω )( T 2э − T 1э ) ,
S э = ( T − T 0 ) dt ,
( c э m э +ω )( T 1э − T 2э )
Подставляя это значение α в уравнение (5), будем иметь:
Экспериментальная установка и измерения.
В нашей работе измеряется удельная теплоёмкость керосина. Эталонной жидкостью служит вода.
Калориметр, предназначенный для данной работы, состоит из трёх цилиндрических сосудов, вставленных один в другой. Первый, наружный массивный сосуд закрыт эбонитовой крышкой. К крышке снизу привинчен второй сосуд с зачерненной внутренней поверхностью. В этом втором сосуде на шелковых нитях подвешено эбонитовое кольцо, на котором помещается третий, внутренний, сосуд с блестящей полированной наружной поверхностью.
Жидкость наливается во внутренний сосуд. Между первым (наружным) и вторым сосудом налита вода, играющая роль окружающей среды. Излучение происходит через прослойку воздуха между третьим (внутренним) и вторым сосудами.
В крышке наружного сосуда калориметра сделано отверстие для термометра, измеряющего температуру среды, принимающей излучение. В середине крышки имеется круглый вырез, в который вставляется внутренний сосуд. Вырез, в свою очередь, закрывается эбонитовой крышкой, в которую вставляется термометр, измеряющий температуру исследуемой жидкости, и мешалка.
Нагревание внутреннего сосуда с жидкостью производится на водяной бане, которая представляет из себя кастрюлю с припаянным к ней держателем для термометра. Кастрюля наполняется водой и ставится на электроплитку, а в кастрюлю помещают внутренний сосуд калориметра с исследуемой жидкостью.
Внимание! Ни в коем случае нельзя ставить сосуд с керосином прямо на плитку, без водяной бани.
После того, как сосуд с жидкостью нагреется до нужной температуры, его вынимают из водяной бани и, тщательно обтерев наружную поверхность, помещают в калориметр. Наблюдают зависимость температуры жидкости и внешней среды от времени. Время измеряют секундомером.
Определение водяного эквивалента калориметра. При расчете теплоёмкости нужно знать величину ω , так называемый водяной эквивалент калориметра, учитывающий теплоту, идущую на нагревание калориметра, мешалки и термометра.
Водяным эквивалентом тела называют количество теплоты, нагревающее тело на 1 ◦ C. Водяной эквивалент однородного тела равен массе тела, умноженной на его удельную теплоёмкость. Так как удельная теплоёмкость воды равна единице, то водяной эквивалент тела численно равен такой массе воды, которая нагревается на один градус тем же количеством тепла, что и данное тело. Если известны удельные теплоёмкости материала сосуда калориметра и других его вспомогательных частей, то водяной эквивалент калориметра определяется так:
ω = m 1 c 1 + m 2 c 2 + m 3 c 3 ,
где m 1 и c 1 -масса и удельная теплоёмкость материала сосуда, m 2 и c 2 — масса и удельная теплоёмкость материала мешалки, m 3 и c 3 — масса и удельная теплоёмкость материала термометра.
Водяной эквивалент калориметра определяется опытным путём. Взвесим внутренний сосуд калориметра. Пусть его масса будет M 0 . Наполним его водой приблизительно до половины и снова взвесим. Пусть теперь масса его будет M 1 . Тогда разность M ′ = M 1 − M 0 даст массу воды. Поместим внутренний сосуд калориметра во внешний, опустим в воду термометр и определим её температуру. Пусть эта температура равна T ′ . Возьмём горячую воду, определим её температуру и нальем в калориметр. Перемешаем воду и, когда установится стационарное состояние, определим окончательную температуру смеси. Пусть температура горячей воды равна T ′′ и окончательная температура равна T . Снова взвешиваем внутренний сосуд калориметра. Если теперь его масса M 2 , то M ′′ = M 2 − M ′ будет масса прибавленной горячей воды. Составим уравнение теплового баланса. Горячая вода потеряла M ′′ c 0 ( T − T ′ ) калорий. Холодная вода и калориметр получили ( M ′ c 0 +ω )( T − T ′ ) калорий (здесь c 0 — удельная теплоёмкость воды). Следовательно
M ′′ c 0 ( T ′′ − T ) = ( M ′ c 0 +ω )( T − T ′ )
ω = c M ′′ T ′′ − T − M ′ .
Обратите внимание: при определении водяного эквивалента калориметра и при измерениях скорости охлаждения жидкости термометр нужно всегда опускать в жидкость на одну и ту же глубину (подумайте — почему?).
1. Поставьте кастрюлю с водой на плитку, чтобы вода успела нагреться, пока вы занимаетесь взвешиванием.
2. Определите водяной эквивалент калориметра, как описано выше. Горячую воду возьмите из кастрюли. Сначала проводим измерения с водой:
3. Помещаем внутренний сосуд с водой (и с термометром) в водяную баню. Конечно, масса воды должна быть предварительно измерена. Сосуд нагреваем градусов до 90.
4. Вынимаем сосуд из водяной бани, тщательно обсушиваем (подумайте — зачем?) и помещаем в калориметр. Закрываем крышку наружного сосуда.
5. Выжидаем, когда термометр внутреннего сосуда покажет градусов 85. Затем измеряем и записываем зависимость от времени температуры внутреннего сосуда и температуры водяной защиты (внешней среды). Измерения ведём, пока температура не упадёт градусов до 60.
6. Вынимаем сосуд, выливаем воду, тщательно обсушиваем. Проводим измерения с керосином:
7. Наливаем во внутренний сосуд калориметра керосин, взвешиваем его и вычисляем массу налитого керосина.
8. Далее поступаем с сосудом, наполненным керосином так же, как с сосудом, наполненным водой.
1. Постройте график зависимости температуры воды и внешней среды от времени и такой же график — для керосина. Обратите внимание: так как в дальнейшем вам нужно будет вычислять отношение S / S э (см. формулу (8)) или произведение α S (см. формулу (5)), в которую неявно входит то же отношение, то оба графика должны быть начерчены в одном масштабе! (Если использовать один масштаб неудобно, то можно взять и разные масштабы, но тогда нужно определить масштабный коэффициент, приводящий графики к одному масштабу);
2. Определите коэффициент α в законе Ньютона. Для этого выберите на графике для воды отрезок времени от t 1 до
t 2 и определите (подсчитывая клеточки на миллиметровой бумаге) площадь S э . Вычислите α по формуле (7) .
3. Определите α несколько раз, используя разные участки графика. Постарайтесь ответить на вопросы:
— Остаётся ли коэффициент теплоотдачи постоянным в исследованном вами интервале температур?
— Если нет, то от каких величин он зависит: T , T 0 или от разности T − T 0 ? Если нужно — начертите график;
— Какие условия (температура, время) выгоднее всего выбрать при определении площади S по графику для керосина (дайте обоснование).
4. По графику для керосина определите площадь S . Рассчитайте теплоёмкость керосина.
5. Сделайте расчёт теплоёмкости, пользуясь разными участками графика.
6. Подведите итог:
— Насколько хорошо выполняется закон Ньютона?
— Какую величину коэффициента α вы использовали при расчете теплоёмкости керосина? Почему?
— Какое получено окончательное значение теплоемкости керосина?
Источник