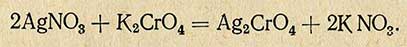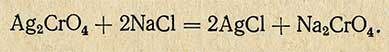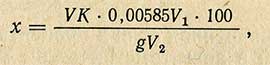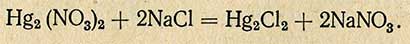- Способ определения раствора соли натрий
- 1. ОТБОР И ПОДГОТОВКА ПРОБ
- 2. ОПРЕДЕЛЕНИЕ ХЛОРИСТОГО НАТРИЯ АРГЕНТОМЕТРИЧЕСКИМ МЕТОДОМ
- Определение поваренной соли (хлорида натрия)
- Аргентометрический метод
- Меркурометрический метод
- Приготовление реактивов
- Определение количества хлористого натрия (NaCl) в поваренной соли
Способ определения раствора соли натрий
Методы определения поваренной соли
Food concentrates. Methods for determination of salt
Дата введения 1979-01-01
ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 24 августа 1977 г. N 2028
Ограничение срока действия снято по протоколу N 3-93 Межгосударственного совета по стандартизации, метрологии и сертификации (ИУС 5-6-93)
ИЗДАНИЕ с Изменением N 1, утвержденным в апреле 1984 г. (ИУС 8-84).
Настоящий стандарт распространяется на пищевые концентраты, в рецептуру которых входит поваренная соль (хлористый натрий), и устанавливает методы ее определения.
1. ОТБОР И ПОДГОТОВКА ПРОБ
1.1. Отбор и подготовку проб для лабораторных испытаний проводят по ГОСТ 15113.0-77.
2. ОПРЕДЕЛЕНИЕ ХЛОРИСТОГО НАТРИЯ АРГЕНТОМЕТРИЧЕСКИМ МЕТОДОМ
2.1. Сущность метода
Метод основан на титровании хлористого натрия в нейтральной среде раствором азотнокислого серебра в присутствии хромовокислого калия в качестве индикатора. Метод применяется при разногласиях в оценке качества продукции.
2.2. Аппаратура, реактивы и материалы
Весы лабораторные общего назначения по ГОСТ 24104-88*.
* С июля 2002 г. введен в действие ГОСТ 24104-2001 (здесь и далее).
Печь муфельная электрическая.
Бюретки вместимостью 25 см .
Воронки стеклянные по ГОСТ 25336-82.
Капельницы лабораторные стеклянные по ГОСТ 25336-82, вместимостью 10, 25 см .
Колбы мерные по ГОСТ 1770-74, вместимостью 100 и 250 см .
Колбы конические по ГОСТ 25336-82, вместимостью 100, 150, 250 см .
Пипетки вместимостью 10, 20 и 50 см .
Стаканчики стеклянные вместимостью 0,3-0,5 и 10 см .
Тигли фарфоровые по ГОСТ 9147-80.
Гидроокись (гидроксид) натрия по ГОСТ 4328-77 или гидроокись (гидроксид) калия по ГОСТ 24363-80.
Натрий хлористый по ГОСТ 4233-77.
Серебро азотнокислое, х.ч., по ГОСТ 1277-75, 0,1 моль/дм раствор.
Спирт этиловый ректификованный по ГОСТ 5962-67*.
* На территории Российской Федерации действует ГОСТ Р 51652-2000 (здесь и далее).
Фенолфталеин по НД, 1%-ный спиртовой раствор.
Бумага фильтровальная по ГОСТ 12026-76.
Вода дистиллированная по ГОСТ 6709-72.
Калий хромовокислый по ГОСТ 4459-75, х.ч., 10%-ный раствор.
(Измененная редакция, Изм. N 1)
2.3. Подготовка к испытанию
2.3.1. Приготовление 0,1 моль/дм раствора азотнокислого серебра
17 г химически чистого азотнокислого серебра, взвешенного с погрешностью не более ±0,01 г, растворяют в 1000 см дистиллированной воды. Титр приготовленного раствора устанавливают через 7-10 дней по химически чистому дважды перекристаллизованному хлористому натрию. Для этого в стеклянный стаканчик вместимостью 0,3-0,5 см берут навеску хлористого натрия 0,1-0,2 г с погрешностью не более ±0,0001 г и, опустив стаканчик в коническую колбу, растворяют навеску в 25-30 см дистиллированной воды.
Раствор хлористого натрия титруют 0,1 моль/дм раствором азотнокислого серебра в присутствии 0,5 см 10%-ного раствора хромовокислого калия при непрерывном перемешивании содержимого колбы до появления не исчезающей при взбалтывании красноватой окраски.
Титр 0,1 моль/дм раствора азотнокислого серебра вычисляют по формуле

где — масса навески хлористого натрия, г;
— молярная масса азотнокислого серебра;
— молярная масса хлористого натрия;
— объем раствора азотнокислого серебра, израсходованный на титрование, см .
Поправку 0,1 моль/дм раствора азотнокислого серебра получают делением установленного титра раствора на титр точно 0,1 моль/дм раствора азотнокислого серебра, т.е. 0,01699 г/см .
Титр 0,1 моль/дм раствора азотнокислого серебра устанавливают по двум-трем навескам хлористого натрия. Допускаемые расхождения между параллельными определениями не должны превышать 0,001 г/см .
Приготовленный раствор хранят в склянке из темного сте
2.3.2. Приготовление водной вытяжки из продуктов, дающих слабоокрашенную водную вытяжку
Навеску массой от 5 до 25 г (в зависимости от предполагаемого содержания соли) берут из пробы продукта в небольшой стаканчик с погрешностью не более ±0,01 г и количественно переносят через воронку в мерную колбу вместимостью 250 см , смывая частицы продукта дистиллированной водой. Содержимое колбы доливают водой до 3/4 объема, взбалтывают и при испытании продуктов растительного происхождения нагревают на кипящей водяной бане в течение 15 мин. При анализе продуктов, богатых крахмалом или белками, содержимое колбы выдерживают при 30 °С в течение 30 мин при частом взбалтывании.
Затем содержимое колбы охлаждают, доводят до метки дистиллированной водой, взбалтывают и фильтруют через складчатый бумажный фильтр в сухую коническую колбу.
2.3.3. Приготовление водной вытяжки из продуктов, дающих интенсивно окрашенную водную вытяжку
Навеску массой 5-25 г из пробы продукта берут с погрешностью не более ±0,01 г в фарфоровый тигель и осторожно обугливают до тех пор, пока содержимое тигля не будет легко распадаться от надавливания стеклянной палочкой.
Обугленное вещество охлаждают, количественно переносят через воронку в мерную колбу вместимостью 250 см , смывая тигель несколько раз дистиллированной водой. Колбу доливают до 3/4 объема горячей дистиллированной водой и выдерживают 15 мин в кипящей водяной бане при периодическом взбалтывании. Содержимое колбы охлаждают, доводят дистиллированной водой до метки, перемешивают, фильтруют через складчатый бумажный фильтр в сухую коническую колбу.
2.4. Проведение испытания
20-25 см фильтрата, приготовленного по п.2.3.2 или 2.3.3, переносят пипеткой в коническую колбу вместимостью 250 см , нейтрализуют 0,1 моль/дм раствором щелочи в присутствии фенолфталеина, прибавляют 0,5 см 10%-ного раствора хромовокислого калия и титруют 0,1 моль/дм раствором азотнокислого серебра. Содержимое колбы непрерывно перемешивают и заканчивают титрование при появлении не исчезающей при взбалтывании красноватой окраски жидкости.
2.5. Обработка результатов
Массовую долю хлористого натрия , %, вычисляют по формуле

где — объем 0,1 моль/дм раствора азотнокислого серебра, израсходованный на титрование, см ;
— коэффициент поправки к титру раствора азотнокислого серебра;

— объем вытяжки, приготовленный из навески, см ;
— масса навески, г;
— объем фильтрата, израсходованный на титрование, см .
За окончательный результат испытания принимают среднеарифметическое результатов двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,2%.
Вычисления проводят с погрешностью не более 0,01%.
Источник
Определение поваренной соли (хлорида натрия)
Поваренная соль — весьма важное вкусовое вещество, вводится как составная часть в рецептуру всех видов концентратов первых и вторых блюд, кулинарных соусов в порошке и сухие завтраки некоторых видов. В этих продуктах содержится от 1 До 15% соли.
Методы, применяемые для определения хлористого натрия, основаны на титровании иона хлора азотнокислым серебром (аргентометрический метод) либо нитратом закисной ртути (меркурометрический метод). Хлористый натрий извлекают водой, чаще непосредственно из навески испытуемого вещества или из обугленной навески продукта, если экстракт, получаемый первым способом, имеет темную окраску.
Аргентометрический метод
Метод основан на следующем принципе: к нейтральному раствору хлорида прибавляют в качестве индикатора несколько капель хромовокислого калия и титруют раствором азотнокислого серебра. При этом образуется красный осадок хромовокислого серебра
Этот осадок исчезает при взбалтывании, так как между хромовокислым серебром и хлористым натрием происходит обменное разложение и образуется нерастворимый осадок хлористого серебра.
В момент превращения всего хлора в хлористое серебро жидкость, над осадком приобретает неисчезающую красноватую окраску, что указывает на конец реакции.
Методика определения. Навеску измельченного продукта от 5 до 25 г (в зависимости от предполагаемого содержания соли) берут в небольшой стаканчик с точностью до 0,01 г и количественно переносят через воронку в мерную колбу емкостью 250 мл, смывая частицы продукта дистиллированной водой. Содержимое колбы доливают водой до 3/4 объема, тщательно взбалтывают и в случае анализа продуктов растительного происхождения нагревают на кипящей водяной бане в течение 15 мин. При анализе веществ, богатых крахмалом или белками, содержимое колбы выдерживают при 30° С в течение 30 мин при частом взбалтывании. После этого содержимое колбы охлаждают, доводят дистиллированной водой до метки, взбалтывают и фильтруют через складчатый фильтр в сухую колбу.
50 мл фильтрата отмеривают пипеткой, переносят в коническую колбу емкостью 250 мл, нейтрализуют 0,1 н. раствором щелочи в присутствии фенолфталеина, прибавляют 0,5 мл 10%-ного раствора хромовокислого калия и титруют 0,1 н. раствором азотнокислого серебра. При титровании содержимое колбы непрерывно перемешивают до появления не исчезающей при взбалтывании красноватой окраски. Если водная вытяжка вещества интенсивно окрашена, то навеску исследуемого продукта берут в фарфоровый тигель и осторожно обугливают до тех пор, пока содержимое тигля не будет легко распадаться от надавливания стеклянной палочкой.
Обугленное вещество охлаждают, количественно переносят через воронку в мерную колбу емкостью 250 мл, смывая тигель несколько раз дистиллированной водой. Колбу доливают до 3/4 объема горячей дистиллированной водой и выдерживают 15 мин в кипящей водяной бане при периодическом взбалтывании. После охлаждения содержимое колбы доводят дистиллированной водой до метки, перемешивают и фильтруют через складчатый фильтр в сухую колбу. 50 мл фильтрата переносят в коническую колбу, нейтрализуют и титруют так же, как указано выше.
Содержание поваренной соли (в %) в обоих случаях рассчитывают по следующей формуле:
где V — количество мл 0,1 н. раствора азотнокислого серебра, пошедшего на титрование; К — коэффициент поправки к титру раствора азотнокислого серебра; 0,00585 — титр азотнокислого серебра, выраженный по хлористому натрию; V1 — объем вытяжки, приготовленной из навески, мл; g — навеска вещества, г; V2 — объем вытяжки, взятой для титрования, мл.
Меркурометрический метод
Принцип метода. При взаимодействии раствора хлорида с раствором нитрата закисной ртути образуется светло-серый нерастворимый осадок однохлористой ртути (каломель):
При количественном определении хлоридов по этому методу в качестве индикатора применяют дифенилкарбазон или бромфеноловый синий.
Методика определения. Приготовление водной вытяжки исследуемого продукта см. «Определение поваренной соли аргентометрическим методом». Из подготовленной вытяжки берут пипеткой 10-20 мл в коническую колбу емкостью 100-150 мл, добавляют концентрированную азотную кислоту из расчета 0,5 мл на 10 мл вытяжки и после взбалтывания 4-6 капель 1%-ного спиртового раствора дифенилкарбазона; раствор титруют 0,1 н. раствором азотнокислой закиси ртути до резкого перехода светло-серой окраски реакционной смеси в голубую или сине-фиолетовую. Если в качестве индикатора применяют бромфеноловый синий, то азотную кислоту не добавляют; к вытяжке приливают 6-8 капель 0,1%-ного водного раствора индикатора и титруют 0,1 н. раствором азотнокислой закиси ртути. При титровании окраска испытуемого раствора изменяется от мутно-зеленоватой через светло-серую к сиреневой, которая указывает на окончание реакции.
Титрование следует проводить в двух параллельных пробах: титрованием первой пробы устанавливают приблизительное количество раствора азотнокислой закиси ртути, идущей на титрование, а на основании этого вторую пробу уже точно оттитровывают раствором азотнокислой закиси ртути, прибавляя индикатор перед концом титрования.
При определении поваренной соли в концентратах, содержащих молоко, в качестве индикатора применяют только дифенилкарбазон. Содержание поваренной соли в процентах вычисляют по формуле, приведенной в аргентометрическом методе. Здесь V соответствует количеству миллилитров 0,1 н. раствора азотнокислой закиси ртути, пошедшей на титрование, а 0,00585 — титру азотнокислой закиси ртути, выраженному по хлористому натрию. Остальные буквы имеют то же значение, что и в приведенной выше формуле.
Приготовление реактивов
1. 0,1 н. раствор азотнокислой закиси ртути. 30 г азотнокислой закиси ртути отвешивают с точностью до 0,1 г и растворяют в 400 мл теплой дистиллированной воды, в которую предварительно приливают 14,1 мл концентрированной азотной кислоты. После растворения реактива общий объем раствора доводят водой до 1 л. Титр раствора устанавливают через сутки после приготовления по навеске хлорида натрия (около 0,15 г), которую растворяют в 10 мл дистиллированной воды и титруют, добавив 0,5 мл концентрированной азотной кислоты и 6-8 капель дифенилкарбазона.
2. 1%-ный раствор дифенилкарбазона. 1 г реактива растворяют в 100 мл 96%-ного спирта, хранят в склянке из темного стекла.
3. 0,1-ный водный раствор бромфенолового синего (см. главу 6).
Источник
Определение количества хлористого натрия (NaCl) в поваренной соли



Метод основан на титровании испытуемого раствора соли азотнокислым серебром (AgNO3). По израсходованному на титрование количеству AgNO3 рассчитывают содержание NaCl.
Образец соли растирают в порошок в фарфоровой ступке. 10г соли взвешивают на аналитических весах. Навеску переносят в химический стакан емкостью 400 см 3 , приливают 200 см 3 дистиллированной воды и ставят на кипящую водяную баню на 20 мин. Затем стакан охлаждают 10 минут и фильтруют раствор в мерную колбу емкостью 500 см 3 через бумажный фильтр.
10 см 3 фильтрата переносят в коническую колбу. Раствор разбавляют до 50 см 3 дистиллированной водой. Туда же добавляют 2-3 капли 10%-ного раствора хромовокислого калия. Полученный раствор титруют раствором азотнокислого серебра при энергичном взбалтывании до момента перехода желто-белого цвета осадка в слабый красновато-бурый цвет, не исчезающий при дальнейшем перемешивании.
Содержание NaCl вычисляют по формуле
где а – объем раствора AgNO3 , израсходованный на титрование, см 3 .
Определите массовую долю влаги, реакцию соли по лакмусу и количество NaCl в пищевой поваренной соли.
Результаты занесите в таблицу 3.4.
| Вид соли | Сорт | Номер помола | Наименование показателей | Характеристика образца | При меча-ние |
| по ГОСТ | фактические |
| Х |
| (3.2) |
| % , |
где V – объем 0,1 н раствора AgNO3, израсходованного на титрование, см 3 ;
К – поправочный коэффициент раствора AgNO3 (коэффициент нормальности для 0,1 н раствора);
0,005845 – титр 0,1 н раствора AgNO3 по хлористому натрию;
mc – навеска соли, пересчитанная на сухое вещество, г;
500 – общий объем исходного раствора, см 3 ;
10 – объем раствора, взятого для определения, см 3 . Примечание: Для определения NaCl в соли «Экстра» (вакуумной) берут навеску соли около 10г и переносят в мерную колбу емкостью 500 см 3 , после чего проводят испытания.
где m – навеска соли, г; Х1 – влажность соли, %;
Сделайте заключение о качестве поваренной соли.
Материальное обеспечение:
1. Натуральные образцы пряностей и поваренной соли.
2. Листы белой бумаги.
3. Аналитические и технические весы.
4. Электроплита, водяные бани.
5. Колбы мерные (500 см 3 ) и конические (100 см 3 ).
6. Химические стаканы, емкостью 200, 400, 500 см 3 .
8. Пинцет медицинский.
9. Стеклянные палочки.
10.Фильтры и лакмусовые бумажки.
11. Сушильный шкаф (t=140-150 о С)
12. Фарфоровые ступки.
14. Серебро азотнокислое (0.1 н раствор).
15. Калий хромовокислый (10%-ный раствор).
Контрольные вопросы
1. Правила приемки и отбора проб пряностей и приправ.
2. Что такое партия, точечная, объединенная и лабораторная пробы?
3. Какие Вы знаете группы и виды пряностей?
4. Какие показатели качества определяют в пряностях?
5. Условия и сроки хранения пряностей и приправ.
6. Классификация пищевой поваренной соли.
7. Правила приемки и показатели качества соли.
8. Дефекты соли, возникающие при хранении и возможность их предупреждения.
9. Порядок определения внешнего вида соли.
10.Порядок определения запаха и вкуса соли.
11.Как повышенное содержание минеральных примесей влияет на органолептические свойства соли?
12.Какие физико-химические показатели контролируют в соли?
13.Виды применяемых упаковок для пряностей и приправ.
Источник