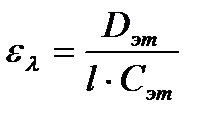Метод калибровочного графика
Для определения концентрации вещества (элемента) в исследуемом растворе используют чаще всего калибровочный (градуировочный) график в координатах А — C (оптическая плотность — концентрация).
Готовят серию стандартных растворов с известной концентрацией вещества. Измеряют оптическую плотность этих растворов, сравнивая интенсивности потока излучения, проходящего через стандартный раствор, с интенсивностью потока излучения, проходящего через раствор сравнения, поглощение которого принимают равным нулю. Строят калибровочный график.
Калибровочная прямая представляет собой прямую линию, которая идет из начала координат.
Затем измеряют оптическую плотность анализируемого раствора и по графику определяют его концентрацию.
Лабораторная работа № 11
ОПРЕДЕЛЕНИЕ МЕДИ (II)
В аммиачных растворах ионы меди образуют комплексные ионы, окрашенные в синий цвет.
Порядок выполнения работы
1. Возьмите 7 мерных колб на 100 мл для приготовления стандартных растворов соли меди (II). Напишите на них стеклографом номера 0, 1, 2, 3, 4, 5, 6.
2. Налейте из бюреткив колбы, начиная с колбы № 1, точное число мл раствора соли меди (II), который содержит 1 мг меди в 1 мл раствора (см. табл. 3) или другие объемы по усмотрению преподавателя.
Таблица 3
Реагенты для фотометрического определения меди (II)
| № колбы | Объем соли меди (II), мл | Концентрация меди (II), мг/мл | Объем раствора аммиака, мл | Оптичес-кая плотность |
| х | х |
3. В каждую колбу добавьтецилиндром по 5 мл 25 % (концентрированного) раствора аммиака, добавьте дистиллированной воды до метки, закройте пробкой, хорошо перемешайте.
4. Измерьте оптическую плотность каждого стандартного раствора и запишите в таблицу 3. Измерение проводится относительно раствора в колбе № 0 (нулевой раствор) в кюветах с b = 34 мм с использованием желтого светофильтра.
5. По результатам постройте калибровочный график на миллиметровой бумаге в координатах А — C.
6. Получите у преподавателя контрольную задачу с неизвестной концентрацией соли меди (II) (колба № х), добавьте 5 мл 25 % раствора аммиака, доведите дистиллированной водой до метки. Закройте пробкой, хорошо перемешайте.
7. Измерьте оптическую плотность контрольного раствора Аx и по калибровочному графику определите концентрацию меди (II) Сх. Узнайте у преподавателя точной значение концентрации раствора и вычислите погрешность измерения.
ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА (III)
Ионы железа (III) образуют с роданид-ионами комплексные соединения кроваво-красного цвета
Fe 3+ + (3 — 6) SCN — = [Fe(SCN)3-6] 0 — (-3)
Окраска растворов неустойчива, поэтому их готовят непосредственно перед измерением оптической плотности.
Порядок выполнения работы
1. Возьмите 6 мерных колб на 100 мл для приготовления стандартных растворов соли железа (III). Напишите на них стеклографом номера 1, 2, 3, 4, 5, 6.
2. Налейте из бюретки в колбы, начиная с колбы № 1, точное число мл раствора соли железа (III), который содержит 0,02 мг железа в 1 мл раствора (см. табл. 4) или данные преподавателя.
3. В каждую колбу цилиндром добавьте по 2 мл разбавленной (1:1) азотной кислоты и по 10 мл 10%-ного раствора роданида аммония NH4SCN. Добавьте дистиллированной воды до метки, закройте пробкой, хорошо перемешайте.
Таблица 4
Реагенты для фотометрического определения железа (III)
| № колбы | Объем соли железа (III), мл | Концентрация железа (III), мг/мл | Объем раствора HNO3, мл | Объем р-ра NH4SCN, мл | Оптич. плотность |
| 0,5 | |||||
| 1,0 | |||||
| 2,0 | |||||
| 3,0 | |||||
| 4,0 | |||||
| 5,0 | |||||
| х | х |
4. Измерьте оптическую плотность каждого стандартного раствора в кюветах с b= 34 мм с использованием синего светофильтра. За “нулевой раствор” возьмите дистиллированную воду. Результаты измерений запишите в таблицу 4.
5. По полученным значениям оптической плотности постройте калибровочный график на миллиметровой бумаге в координатах А — C.
6. Получите у преподавателя контрольную задачу с неизвестной концентрацией соли железа (III) (колба № х), добавьте 2 мл разбавленной (1:1) азотной кислоты, 10 мл раствора роданида аммония, доведите дистиллированной водой до метки. Закройте пробкой, хорошо перемешайте.
7. Измерьте оптическую плотность контрольного раствора Аx и по калибровочному графику определите концентрацию железа (III) Сх. Узнайте у преподавателя точной значение концентрации раствора и вычислите погрешность измерения.
ПОТЕНЦИОМЕТРИЯ
Метод потенциометрии основан на зависимости потенциала электрода, погруженного в раствор, от концентрации определенных ионов в данном растворе (уравнение Нернста). Потенциал применяемого в работе стеклянного электрода зависит от концентрации ионов водорода в растворе, что используется при измерении рН. Стеклянный электрод в паре с электродом сравнения, потенциал которого не зависит от рН, опускают в определяемый раствор и измеряют разность их потенциалов. Вольтметр, применяемый для измерений, имеет шкалу, градуированную как в милливольтах, так и в единицах рН, что позволяет снимать показания рН раствора непосредственно со шкалы прибора.
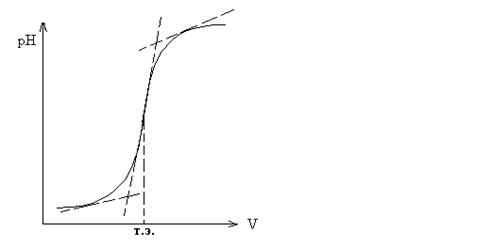
При кислотно-основном титровании добавление каждой порции титранта вызывает изменение рН раствора. На этом основано потенциометрическое титрование. К точному объему определяемого раствора последовательно добавляют небольшие порции стандартного раствора и после каждого добавления измеряется рН. Точку эквивалентности определяют графически (см. рис.1 и 2).
Рис. 1. Интегральная кривая: точка эквивалентности соответствует середине отрезка касательной скачка титрования
Рис. 2 . Дифференциальная кривая: точка эквивалентности соответствует максимуму кривой.
Источник
Способы определения концентрации веществ
1. Определение концентрации вещества с помощью градуировочного (калибровочного) графика.Измеряют оптическую плотность приготовленных стандартных окрашенных растворов и строят градуировочный график: в координатах – оптическая плотность D (ось ординат) – концентрация определяемого вещества – в растворе С (ось абсцисс). При условии выполнения основного закона светопоглощения градуировочный график представляет собой прямую, выходящую из начала координат. Измерив оптическую плотность анализируемого раствора (Dx), по калибровочному графику находят концентрацию определяемого вещества (Cx) (рис. 14).
2. Определение концентрации вещества методом сравнения оптических плотностей эталонного (стандартного) и исследуемого растворов. В этом методе используют два раствора: стандартный с точно известной концентрацией вещества Сэти исследуемый с концентрацией Сх. Последовательно измеряют оптические плотности стандартного Dэт и исследуемого Dx растворов. Концентрацию определяемого вещества Сх находят по формуле:
3. Определение концентрации вещества в растворе по значению молярного коэффициента поглощения. Готовят эталонный раствор исследуемого вещества определенной концентрации Сэт и измеряют значение оптической плотности Dэт этого раствора при длине волны λ. Значение ελ вычисляют по формуле:
Определив значение оптической плотности анализируемого раствора Dх, при той же длине волны находят концентрацию раствора Схпо формуле:

Способом с построением калибровочного графика пользуются при проведении большого количества анализов. Другие способы расчёта Сх используются при проведении единичных анализов.
Дата добавления: 2015-09-11 ; просмотров: 5 | Нарушение авторских прав
Источник
1.4.2 Определение концентрации вещества по калибровочному
Калибровочный или градуировочный график — это зависимость оптической плотности раствора от концентрации растворенного вещества. Для получения его готовят несколько растворов, содержащих определяемое вещество или ион с известными концентрациями, измеряют оптические плотности этих растворов при выбранной или заданной длине волны, по полученным данным строят калибровочный график в координатах 
Рисунок 3 – Калибровочный график
Измеряют оптическую плотность исследуемого раствора 

1.4.3 Определение концентрации веществ в растворах
Метод добавок — это разновидность метода сравнения. Определение концентрации 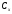

Концентрацию добавки в фотометрируемом растворе можно рассчитать, зная концентрацию и объем стандартного раствора, содержащего определяемый ион и использованного в качестве добавки
Сд 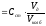
где Сд — концентрация добавки, измеряется в тех же единицах, что и Сст;

моль/мл, г/л, мг/мл, и т.д.);
Vд — объем добавки, мл;

Как установлено в методе сравнения,


где 
растворе, выражается теми же единицами, что и Сд;
Сд — концентрация добавки в исследуемом растворе, может быть выражена
любыми единицами измерения концентрации (моль/л, мг/мл, г/мл, мг/ в
объеме колбы и т. д.);
Ах и А(х+д) — оптические плотности исследуемого раствора и
исследуемого с добавкой соответственно [6, c. 103-104].
1.4.4 Определение концентрации двух веществ при их
Если в растворе имеются два окрашенных вещества А и В, не вступающих в химическую реакцию между собой, то оптическая плотность смеси равна сумме оптических плотностей каждого компонента в отдельности.
Это свойство называется свойством сложения или аддитивности оптической плотности.
При определении концентрации каждого из веществ в смеси можно встретиться с тремя случаями:
I) спектры поглощения определяемых компонентов не накладываются друг на друга (рисунок 4). В этом случае применим принцип дробного анализа, определение концентрации каждого из компонентов проводится с использованием разных светофильтров (для определения количества вещества А — светофильтр «а», для В-светофильтр «в») одним из описанных выше методов анализа (І.4.1, І.4.2, І.4.3);
Рисунок 4 — Спектры поглощения определяемых компонентов не
накладываются друг на друга
2) спектры поглощения определяемых компонентов накладываются друг на друга на протяжении всей видимой области спектра. В этом случае нельзя выбрать таких участков спектра, где можно было бы пренебречь светопоглощением одного из компонентов, т.е. анализ при помощи фотоэлектрокалориметров осуществить практически невозможно. Количественное определение производят при помощи спектрофотометров;
3) спектры поглощения определяемых компонентов частично накладываются друг на друга. В этом случае (рисунок 5) при фотометрировании с различными светофильтрами можно пренебречь светопоглощением одного компонента, например, при фотометрировании с использованием светофильтра «а» можно пренебречь светопоглощением компонента В и считать, что Аa(смеси)=Аa(А).
При фотометрировании смеси с другим светофильтром (в), оптическая плотность смеси равна сумме оптических плотностей компонентов А и В.
Рисунок 5 — Спектры поглощения определяемых компонентов частично
накладываются друг на друга
Для анализа готовят серии стандартных растворов компонентов А и В, измеряют оптические плотности раствора А со светофильтрами «а» и «в», а раствора В — только со светофильтром «в» и строят калибровочные графики:
Рисунок 6 — Калибровочный график для определения концентрации
Рисунок 7 — Калибровочный график для определения концентрации
Затем измеряют оптическую плотность окрашенной смеси компонентов А и В со светофильтром «а» и по измеренному значению Ахa(A) и калибровочному графику Аa(A) = f(C(A))-кривая а на рисунке 6 сразу же находят неизвестную концентрацию Сх (А) компонента А в смеси. Далее, используя кривую «в» на рисунке 6 определяют оптическую плотность раствора компонента А со светофильтром «в» — Ав(А). После этого измеряют оптическую плотность исследуемой смеси компонентов А и В со светофильтром «в». Измеренная величина оптической плотности — суммарная
Так как величина Ав(А) уже известна (см. рисунок 6), то по разности находят Ав(В)
По найденному значению оптической плотности Ав(В) и калибровочному графику «в» рисунок 7, находят неизвестную концентрацию Сх (В) компонента В в исследуемой смеси [6, c. 122-123].
Источник