Методы модификации гуминовых веществ
Изучив различные литературные данные по составу и строению гуминовых веществ, можно заметить, что содержащиеся в них структурные фрагменты (фенольные, карбоксильные, гидроксильные, серо- и азотсодержащие группы) позволяют ожидать, от ГВ высокое сродством к различным органическим экотоксикантам и ионам металлов. Кроме этого, обширный набор функциональных групп открывает широкие спектр возможностей для химических модификаций ГВ.
Преобладающее количество существующих методов модификации гуминовых веществ направлено на изучение их структуры, а не на придание им желаемых химических свойств. Наличие большого количества различных функциональных групп в структуре гуминовых веществ говорит о возможности их модификаций целым рядом различных реагентов. В литературе описаны методы метилирования гуминовых веществ, которые в основном используются для изучения их строения по аналогии с анализом других карбоксил- и гидроксилсодержащих природных и синтетических соединений: углеводов [31,32], жирных кислот [33]. При этом для модификации ГВ используют метилирующие агенты, традиционные для анализа углеводов и жирных кислот: диазометан 35, метилиодид в присутствии окиси серебра [35, 39, 40, 41], метанол в присутствии HСl или BF3 [11, 42] и диметилсульфат [9, 35]. Варьируя методы метилирования и последующей обработки производного, определяют содержание карбоксильных, фенольных и спиртовых групп в структуре ГВ [9].
Реакция метилирования протекает при комнатной температуре, можно варьировать использование растворителей, в качестве растворителя используется и вода. При использовании диазометана в эфирном растворе происходит метилирование как фенольных гидроксилов, так и карбоксильных групп. Как правило, спиртовые группы диазометаном не метилируются [12].
С помощью метилйодида в присутствии оксида серебра удается прометилировать гидроксильные и фенольные группы гуминовых веществ [40].
Метилирование с помощью диметилсульфата приводит к модификации фенольных и спиртовых групп [35].
Ацетилирование гуминовых веществ также проводят с целью определения количества функциональных групп. В качестве ацилирующего агента используют уксусный ангидрид в пиридине, который реагирует с гидроксильными группами всех типов. Исключения составляют третичные спирты и пространственно затрудненные фенолы (три- и более замещенные) [43, 44].
Для увеличения количества кислородсодержащих групп в структуре ГВ используют различные методы окисления ГВ. Продуктами окислительной деструкции гуминовых веществ являются ароматические соединения с различным числом заместителей (COOH-, OH-, OMe-, CHO- группы и др.), а также алифатические кислоты, дикислоты, спирты с длинной цепи С1-С15 [37].
Наиболее подходящим методом для обогащения ГВ кислородсодержащими группами без значительного разрушения молекул является озонирование гуминовых веществ. Озонирование гуминовых веществ проводят озонированным воздухом, содержащим 2,5 об.% озона. В результате модификации таким способом получаются продукты, содержащие от 10 до 30 атомов углерода — в основном ароматические соединения с карбоксильными группами [37, 45].
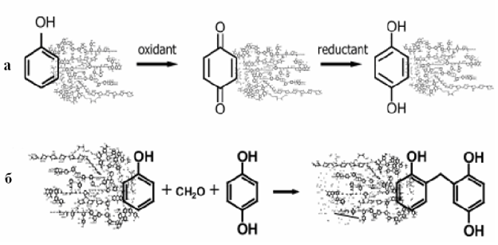
Помимо озонирования направленное обогащение структуры ГВ гидроксильными группами можно осуществить методами гидроксилирования, которые заключаются в окислении фенольных фрагментов ГВ до хинонов с последующим их восстановлением до гидрохинонов (рис. 4 (а). [46].
Реакцию катализируют щавелевой кислотой. Данная модификация также позволяет увеличить количество фенольных групп в структуре ГВ.
Рис.3 Схема модификации ГВ: a – гидроксилирование ГВ; б – сополиконденсация ГВ с гидрохиноном [46]
Гуминовые вещества состоят как из гидрофобных, так и из гидрофильных участков. Наличие большого количества карбоксильных и гидроксильных групп в структуре ГВ является причиной того, что в водных растворах гуминовые вещества отрицательно заряжены [47]. По этой причине гуминовые вещества могут легко взаимодействовать с положительно заряженными группами других органических соединений. В литературе описаны взаимодействия ГВ с различными аминированными поверхностями 52. В кислой среде протонированная аминогруппа реагирует с карбоксильными и фенольными группами ГВ с образованием органических комплексов [49]. В результате взаимодействия карбоксильных и аминогрупп происходит образование солей COO—NH3 +, которые устойчивы лишь при низких значениях рН [54].
Для образования ковалентных связей между ГВ и аминами реакции модификации проводят в органических растворителях. Так, при нагревании ГВ с аминированным силикагелем в ДМФА происходит образование амидных связей в результате взаимодействия карбоксильных групп ГВ с аминогруппами подложки [54].
Кроме того, карбонильные группы ГВ тоже вступают в реакцию с аминами с образованием оснований Шиффа [53].
В литературе так же найдено взаимодействие ГВ с эпоксидами [55]. Реакцию раскрытия эпоксидного цикла катализируют щелочью. Преимуществом применения щелочного катализа является то, что в щелочной среде гуминовые вещества находятся в растворенной форме. Эпоксидный цикл раскрывается под воздействием фенольных групп гуминовых веществ рис.5
Рис.5. Раскрытие эпоксидного цикла при действии фенольных групп ГВ [55]
Количество аминогрупп в структуре гуминовых веществ не велико, по сравнению с карбоксильными и гидроксильными. Но, имеются работы по проведению модификации ГВ по аминогруппам с использованием альдегидов 58. Так например, в работе [56] с целью определения количества аминогрупп в структуре гуминовых веществ проводят модификацию с использованием кротонового альдегида. Реакция проходит гетерофазно с использованием большого избытка альдегида. В результате происходит образование основания Шиффа между аминогруппами ГВ и кротоновым альдегидом.
Из приведенных выше данных следует, что основная часть работ по химической модификации ГВ направлена на изучение структуры ГВ. В то же время важнейшей задачей является получение производных с заданными химическими свойствами, что определяет научную новизну цели, поставленной в данной работе.
В данной работе будут получены гидразиды гуминовых кислот. На основании изучения работ 60 было выяснено, что одним из методов получения гидразидов, самым распространенным и изученным, является гидразинолиз сложных эфиров. Как уже было описано в ГВ между компонентами присутствуют эфирные и сложноэфирные связи.[61] Их наличие дает возможности получать гидразиды ГВ, в частности гидразиды гуминовых кислот.
Так же на примере синтеза пептидов по Т.Курциусу [62] азидным методом (рис. 6) можно спрогназировать хорошие комплексообразущие свойства –СO-NH-NH2 группы. Что безусловно говорит о том, что химические модификации ГВ возможно проводить для получения производных с заданными химическими свойствами.
Рис.6.Азидный метод Т.Курциуса в синтезе пептидов [62]
Источник
Гуминовые вещества — вызов химикам XXI века
Ирина Васильевна Перминова,
доктор химических наук
«Химия и жизнь» №1, 2008
Есть огромный класс природных органических веществ, о котором химики надолго и совершенно незаслуженно забыли. Между тем с точки зрения химии будущего их возможности безграничны, а область их возможного применения очень велика. Речь о гуминовых веществах.
Что такое гуминовые вещества?
Это основная органическая составляющая почвы, воды, а также твердых горючих ископаемых. Гуминовые вещества образуются при разложении растительных и животных остатков под действием микроорганизмов и абиотических факторов среды. В. И. Вернадский в свое время называл гумус продуктом коэволюции живого и неживого планетарного вещества. Более развернутое определение уже в 90-х годах XX века дал профессор кафедры химии почв МГУ Д. С. Орлов: «Гуминовые вещества — это более или менее темноокрашенные азотсодержащие высокомолекулярные соединения, преимущественно кислотной природы». Из этого следует только один вывод: вплоть до сегодняшнего дня определение гуминовых веществ имело скорее философский, чем химический смысл. Причины кроются в специфике образования и строения этих соединений. Откуда же они берутся и что они собой представляют?
Образование гуминовых веществ, или гумификация, — это второй по масштабности процесс превращения органического вещества после фотосинтеза. В результате фотосинтеза ежегодно связывается около 50·10 9 т атмосферного углерода, а при отмирании живых организмов на земной поверхности оказывается около 40·10 9 т углерода. Часть отмерших остатков минерализуется до СO2 и Н2O, остальное превращается в гуминовые вещества. По разным источникам, ежегодно в процесс гумификации вовлекается 0,6–2,5·10 9 т углерода.
В отличие от синтеза в живом организме, образование гуминовых веществ не направляется генетическим кодом, а идет по принципу естественного отбора — остаются самые устойчивые к биоразложению структуры. В результате получается стохастическая, вероятностная смесь молекул, в которой ни одно из соединений не тождественно другому. Таким образом, гуминовые вещества — это очень сложная смесь природных соединений, не существующая в живых организмах.
История изучения гуминовых веществ насчитывает уже более двухсот лет. Впервые их выделил из торфа и описал немецкий химик Ф. Ахард в 1786 году. Немецкие исследователи разработали первые схемы выделения и классификации, а также ввели и сам термин — «гуминовые вещества» (производное от латинского humus — «земля» или «почва»). В исследование химических свойств этих соединений в середине XIX века большой вклад внес шведский химик Я. Берцелиус и его ученики, а потом, в XX веке, и наши ученые-почвоведы и углехимики: М. А. Кононова, Л. А. Христева, Л. Н. Александрова, Д. С. Орлов, Т. А. Кухаренко и другие.

Надо сказать, что к началу XX века интерес химиков к гуминовым веществам резко упал. Понятно почему — было достоверно установлено, что это не индивидуальное соединение, а сложная смесь макромолекул переменного состава и нерегулярного строения (рис. 1), к которой неприменимы законы классической термодинамики и теории строения вещества.
Фундаментальные свойства гуминовых веществ — это нестехиометричность состава, нерегулярность строения, гетерогенность структурных элементов и полидисперсность. Когда мы имеем дело с гуминовыми веществами, то исчезает понятие молекулы — мы можем говорить только о молекулярном ансамбле, каждый параметр которого описывается распределением. Соответственно, к гуминовым веществам невозможно применить традиционный способ численного описания строения органических соединений — определить количество атомов в молекуле, число и типы связей между ними. В какие-то моменты ученым, наверное, казалось, что работать с этими веществами совсем невозможно — они как «черный ящик», в котором все происходит непредсказуемо и каждый раз по-иному.
Чтобы хоть как-то упростить систему, исследователи предложили способ классификации гуминовых веществ, основанный на их растворимости в кислотах и щелочах. Согласно этой классификации, гуминовые вещества подразделяют на три составляющие: гумин — неизвлекаемый остаток, не растворимый ни в щелочах, ни в кислотах; гуминовые кислоты — фракция, растворимая в щелочах и нерастворимая в кислотах (при рН 3 . Однако в сапропеле гораздо больше минеральных примесей, чем в торфе и угле, и он существенно разнообразнее по химическому составу, поэтому нужны более сложные технологии его переработки. С другой стороны, для производства сырья на месте и этот вариант может оказаться полезным. Тем более что в сапропеле нередко уже содержатся различные микроэлементы, которые нужны в качестве удобрений и кормовых добавок. Параллельно при добыче сапропеля удается очистить заиливающиеся озера.
Основной метод, которым выделяют гуминовые вещества, — щелочная экстракция растворами аммиака или гидроксидами калия или натрия. Такая обработка переводит их в водорастворимые соли — гуматы калия или натрия, обладающие высокой биологической активностью. Метод практически безотходный, поэтому его широко используют и в России, и за рубежом. Альтернативный способ предполагает механическое измельчение бурого угля с твердой щелочью, в результате чего получается твердый, растворимый в воде гумат калия и натрия.
Где их использовать
Сначала надо рассказать о той важной роли, которую гуминовые вещества выполняют в биосфере. Они участвуют в структурообразовании почвы, накоплении питательных элементов и микроэлементов в доступной для растений форме, регулировании геохимических потоков металлов в водных и почвенных экосистемах.
К концу XX века, одной из основных проблем которого стало химическое загрязнение окружающей среды, гуминовые вещества, как уже говорилось, начали выполнять роль естественных детоксикантов. Гумусовые кислоты связывают в прочные комплексы ионы металлов и органические экотоксиканты в воде и почве (рис. 3). Известно, что наиболее активен свободный токсикант, связанное вещество не так опасно, поскольку теряет биодоступность.
Во всех моделях биогеохимических циклов загрязняющих веществ, которые создают для того, чтобы оценить опасность, скорость накопления и время жизни ядов в окружающей среде, обязательно надо учитывать их взаимодействие с гумусовыми кислотами. Оно коренным образом меняет и химическое, и токсикологическое поведение вредных веществ. В свое время это дало новый импульс исследованиям — надо же было получить количественные характеристики взаимодействия гумусовых кислот с экотоксикантами.
Химики, вооруженные сложнейшими инструментальными методами, с энтузиазмом принялись за гумусовые вещества. Сегодня в «Chemical Abstracts» каждый год можно найти рецензии на более чем 2000 статей, посвященных этому вопросу. В результате накоплен колоссальный экспериментальный материал. Особо надо отметить тот факт, что наряду с теоретическими изысканиями растет количество прикладных исследований.
В каких областях сегодня применяют гуминовые вещества? Чаще всего — в растениеводстве как стимуляторы роста или микроудобрения. В отличие от аналогичных синтетических регуляторов роста, гуминовые препараты не только влияют на обмен веществ растений.
При систематическом их использовании улучшается структура почвы, ее буферные и ионообменные свойства, становятся активнее почвенные микроорганизмы. Особого внимания заслуживают адаптогенные свойства — гуминовые препараты повышают способность растений противостоять болезням, засухе, переувлажнению, переносить повышенные дозы солей азота в почве. Преимущества гуминовых препаратов заключаются также в том, что они повышают усваивание питательных веществ, а значит, нужно меньше минеральных удобрений без ущерба для урожая.
В последнее время перспективными считают органо-минеральные микроудобрения, содержащие гуматы калия и/или натрия с добавкой Fe, Cu, Zn, Mn, Mo, Co и B в хелатной форме. Особенно они хороши на карбонатных почвах, где, несмотря на высокие концентрации микроэлементов, содержание их в доступной для растений форме невелико. Надо сказать, что обычно для этих же целей применяют микроудобрения на основе синтетических лигандов (ЭДТА, ДТПА, ЭДДГА). Они эффективны, но в их промышленном производстве используют и монохлоруксусную кислоту, и этилендиамин, получаемые из хлорированных углеводородов. Конечно, такое производство небезопасно для человека и окружающей среды. Кроме того, если регулярно вносить удобрения с синтетическими лигандами, то они накапливаются в почве, а это ухудшает ее свойства. Поэтому создание и использование удобрений на основе гуминовых препаратов — куда более безопасная альтернатива.
Другое интересное применение гуминовых веществ — рекультивация загрязненных почв и вод. Их пытаются также применять для очистки и рекультивации территорий, загрязненных органическими веществами и нефтепродуктами, а также тяжелыми металлами. Уже разработаны и используются твердые сорбенты на основе гуминовых веществ.
Наряду со связывающими свойствами гуминовые вещества имеют ярко выраженные поверхностно-активные свойства. Поэтому их добавляют для лучшей растворимости гидрофобных органических веществ (например, нефтепродуктов). Гуминовые вещества входят в состав буровых растворов, а также служат основой растворов, предназначенных для промывания водоносных горизонтов, загрязненных ароматическими веществами. Также для этих целей используют синтетические ПАВ, но, в отличие о них, гуминовые вещества совершенно безопасны для природы.
Другие способы их применения пока остаются экзотикой. Основная причина — та самая гетерогенность структуры, которая, с одной стороны, дает чрезвычайно широкий спектр свойств, а с другой — неспецифичность действия.
Как уйти от этой неспецифичности, создать гуминовые вещества более направленного действия? Например, для рекультивации сред, загрязненных гидрофобными органическими соединениями, нужны гуминовые препараты, обладающие повышенным сродством по отношению к загрязняющим веществам, то есть тоже гидрофобные. А вот при создании микроудобрений на гуминовой основе они, наоборот, должны быть гидрофильными и прекрасно растворяться в воде. Поэтому, чтобы повысить эффективность применения гуминовых препаратов в конкретной области и расширить спектр их применения, надо научиться направленно менять их свойства. Причем получающийся продукт должен быть стабильным, а его свойства воспроизводимыми.
Дизайн гуминовых материалов
Итак, цель — получение гуминовых производных с заданными свойствами (рис. 4, 5). То есть надо найти такой способ их модификации, после которого усиливаются уже имеющиеся положительные свойства и появляются новые. Желательно вдобавок, чтобы такой способ можно было использовать в промышленном масштабе. При решении этой сложной химической проблемы надо, с одной стороны, максимально сохранить гуминовый каркас после серии реакций — в этом залог нетоксичности и устойчивости к биоразложению, а с другой стороны, максимально модифицировать в нужном направлении активные группы. Скажем несколько слов о предлагаемых методах и подходах. Чтобы увеличить растворимость комплексов с металлами в воде, на Химическом факультете МГУ мы провели сульфирование гуминовых веществ. Дело в том, что, когда речь идет о микроудобрениях с гуминовыми кислотами, растворимость комплексов гуминовых веществ с металлами ниже, чем у синтетических аналогов. Чтобы решить эту задачу, мы ввели дополнительные сульфогруппы, после чего, как показали эксперименты, растворимость гуматов железа действительно увеличилась.
Для решения другой задачи — увеличения гидрофобности гуминовых веществ — мы провели кислотный гидролиз гуминовых веществ. Напомним, что гуминовые молекулы состоят из двух строительных блоков, различающихся по химической природе: ароматического каркаса и углеводно-пептидной периферии. При этом известно, что в зависимости от того, какой фрагмент преобладает — гидрофобный ароматический или гидрофильная периферия, — будут сильно изменяться поверхностная активность и способность гуминовых веществ к гидрофобным взаимодействиям. Наши эксперименты подтвердили, что если разложить гуминовые вещества на составляющие, то, например, каркасные фрагменты на 20% лучше связывают пирен, чем исходные препараты.
Совершенно другой тип модификации мы использовали для того, чтобы сделать гуминовые вещества более активными восстановителями. Дело в том, что именно восстановительные свойства определяют способность гуминовых препаратов нейтрализовать окисленные актиниды (например, плутоний). Мы взяли гуминовые вещества, полученные из окисленного угля — как мы уже говорили, основного сырья для промышленного производства гуминовых препаратов. У этих гуминовых веществ самое высокое содержание ароматического углерода (свыше 60%) и нет углеводных фрагментов. К ним мы присоединили различные хиноидные фрагменты с помощью фенолформальдегидной конденсации и получили высокоактивные гуминовые редоксполимеры (рис. 6). Они действительно лучше восстанавливали радионуклиды. Более того, чтобы сделать реакцию «зеленой» при производстве в промышленном масштабе, мы отработали такую реакцию, для проведения которой не нужен токсичный формальдегид. Оказалось, что такой способ позволяет ввести хиноидный фрагмент в гуминовые вещества «по выбору» — достаточно одного незамещенного положения в фенольном фрагменте гуминового каркаса. В результате получается целый набор хиноидно обогащенных гуминовых производных с различными электрохимическими свойствами.
Следующий наш шаг — получение гуминовых производных с повышенной сорбционной способностью на минеральных матрицах (рис. 7). Зачем это нужно? Основное, что останавливает применение гуминовых веществ в природоохранных технологиях: после того как детоксикант вносят в почву и он адсорбирует металл, непонятно, как предотвратить его дальнейшее передвижение. Идеальным решением проблемы было бы заставить гуминовые вещества необратимо прилипать к минеральным поверхностям (например, к песку или глинам). Учитывая, что основная составляющая природных минералов — это кремнезем, то самый удобный способ — создать связь Si—О—Si между гуминовым веществом и минеральной матрицей. Тогда можно получить порошок с поверхностно-активными группами, которые после растворения в водоеме будут прилипать к минеральной поверхности. Вопрос только в том, как это сделать? Казалось бы, все просто: нужно ввести силанольный фрагмент в гуминовый каркас — и дело с концом. Но такие гуминовые вещества в воде будут полимеризоваться, и ничего хорошего из этого не выйдет.
Мы обратились за помощью к коллегам в лабораторию элементоорганических соединений Института синтетических полимерных материалов (ИСПМ) РАН. И решение было найдено: нужно вводить не силанольную группу, а алкоксисилильную. Такое вещество в воде будет гидролизоваться и высвобождать гуминовые вещества с силанольными группами. Сказано — сделано: были получены гуминовые производные (рис. 7), которые с успехом сели на силикагель (модель минеральной поверхности) из водного раствора. Оказалось, что, изменяя степень модификации гуминовых веществ, можно управлять и свойствами, которыми будет обладать гуминовая пленка. По экспериментальным данным, новый препарат сорбирует плутоний почти на 95%.
Конечно, невозможно охватить в одной статье и даже в книге все накопленные данные по существующим способам и перспективам использования гуминовых веществ. Публикации последних лет содержат большое количество оригинальных предложений по новым областям применения гуминовых препаратов. Наряду с растениеводством их все больше используют в медицине, животноводстве и других областях.
Очередная конференция Международного гуминового общества называется «От молекулярного понимания — к инновационным применениям гуминовых веществ». Она пройдет в России (14–19 сентября 2008 года) под эгидой IUPAC, а ее организатор — Химфак МГУ. Это вполне закономерно подтверждает лидерство наших ученых в этой области химии. Кстати, они совершенно уверены, что это сырье будущего. Почему? Потому что гуминовые вещества проявляют уникальные биологические свойства, не нанося никакого вреда природе.
Что еще почитать о гуминовых веществах:
Орлов Д.С. Гумусовые кислоты почв и общая теория гумификации. М.: Изд-во МГУ, 1990.
Варшал Г.М., Велюханова Т. К., Кощеева И.Я. Геохимическая роль гумусовых кислот в миграции элементов. В сб. «Гуминовые вещества в биосфере». М.: Наука, 1993.
Левинский Б.В. Всё о гуматах. Иркутск, 2000.
Лунин В.В., Тундо П., Локтева Е.С. Зеленая химия в России. Изд-во Моск. ун-та, 2004.
Источник