- Хронический атрофический гастрит
- МКБ-10
- Общие сведения
- Причины
- Симптомы
- Осложнения
- Диагностика
- Лечение хронического атрофического гастрита
- Атрофический гастрит — симптомы и лечение
- Определение болезни. Причины заболевания
- Симптомы атрофического гастрита
- Патогенез атрофического гастрита
- Классификация и стадии развития атрофического гастрита
- Осложнения атрофического гастрита
- Диагностика атрофического гастрита
- Лечение атрофического гастрита
- Прогноз. Профилактика
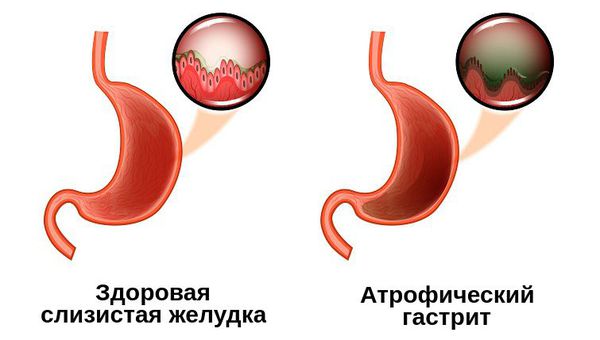
Хронический атрофический гастрит
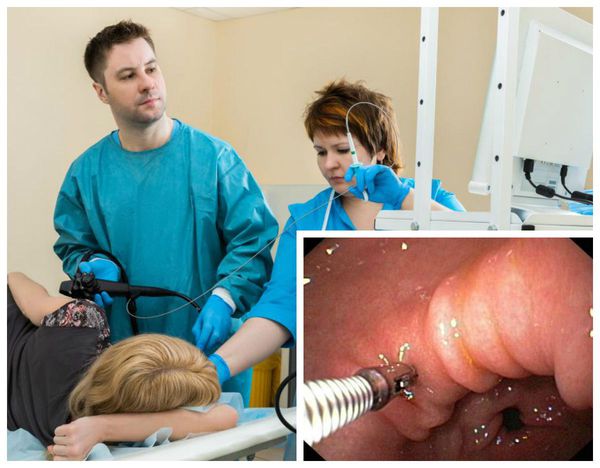
Хронический атрофический гастрит – это заболевание, характеризующееся атрофией желудочных желез, перерождением эпителия желудка в кишечный, умеренно выраженным воспалительным процессом. Проявления зависят от локализации и этиологии атрофических процессов: в основном, это тяжесть в желудке после еды, быстрая насыщаемость, отрыжка, тошнота, неприятный вкус во рту, анемия. Золотой стандарт диагностики — ЭГДС с биопсией слизистой, внутрижелудочная рН-метрия, выявление H.pylori; остальные методы являются вспомогательными. Лечение заключается во введении глюкокортикоидных гормонов, натурального желудочного сока, витамина В12, применении антихеликобактерной схемы терапии.
МКБ-10
Общие сведения
Хронический атрофический гастрит – диагноз морфологический, для верификации которого обязательны результаты ЭГДС. Клинические проявления данной патологии не всегда соответствуют выявляемым при проведении биопсии изменениям. Хронический атрофический гастрит может развиться как на поздних стадиях хеликобактерного гастрита (из-за длительной персистенции инфекции происходит постепенная гибель значительного количества желудочных желез), так и в результате аутоиммунных нарушений в организме (антитела к эпителиальным клеткам желудка вызывают их гибель, постепенно развивается ахлоргидрия).
H.pylori выявляется более чем у 80% населения России, при этом хроническое воспаление слизистой желудка обнаруживается примерно у 50%. Аутоиммунный гастрит у женщин диагностируется в три раза чаще, чем у мужчин, однако является достаточно редким заболеванием. Исследования в области гастроэнтерологии подтверждают, что заболеваемость хроническим гастритом повышается на 1,5% ежегодно.
Причины
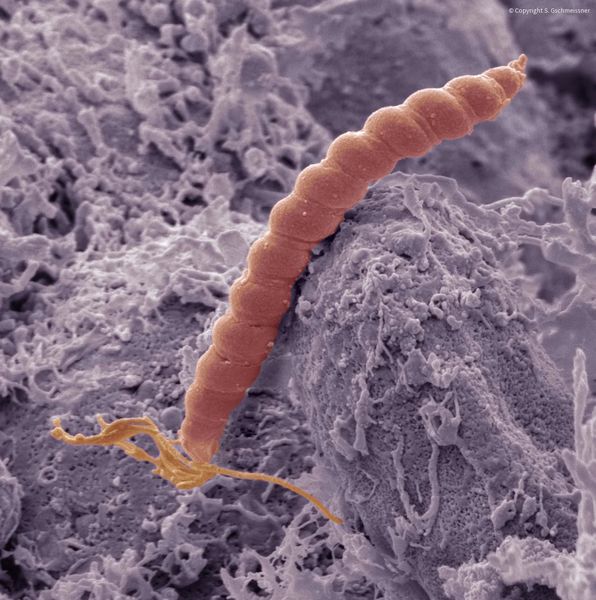
Наиболее значимыми причинами хронического атрофического гастрита являются инфекция H.pylori и аутоиммунные процессы. Атрофия эпителия желудка развивается на поздних стадиях хронического хеликобактер-ассоциированного гастрита. Бактерии сначала колонизируют слизистую антрального отдела, вызывая хронический воспалительный ответ. По мере прогрессирования инфекции процесс распространяется сначала на тело желудка, а затем и на остальные его отделы, инициируя пангастрит. На этой стадии уже четко визуализируются атрофические изменения слизистой, формируется хронический атрофический гастрит. Обычно на данном этапе хеликобактерии перестают выявляться, так как желудочные железы атрофируются, происходит замена желудочного эпителия на кишечный, к которому H.pylori не имеет тропности.
При аутоиммунном гастрите поражение основных желез желудка наблюдается в начале заболевания. Диффузная атрофия эпителия желудка очень быстро прогрессирует, что связано с выработкой аутоантител к микросомальным антигенам париетальных клеток, гастринсвязывающим белкам, внутреннему фактору. Антитела принимают непосредственное участие в деструкции эпителиальных клеток желудка.
Причина образования аутоантител на сегодняшний день не определена, но гастроэнтерологи не исключают наследственной предрасположенности к хроническому атрофическому гастриту. Известно, что для запуска аутоиммунного процесса в эпителии желудка титр антител должен достичь некой критической цифры, индивидуальной для каждого человека. Повлиять на скорость этого процесса могут различные эндогенные и экзогенные провоцирующие факторы:
- Эндогенные факторы: генетические особенности, дуодено-гастральный рефлюкс, эндоинтоксикация, кислородное голодание, хронические инфекции, обменные и эндокринные нарушения, недостаток витаминов (гиповитаминоз), висцеральные рефлекторные реакции при патологии других органов.
- Экзогенные факторы: нарушения питания, вредные привычки (алкоголь, курение), прием некоторых медикаментов, воздействие ионизирующего излучения, инфекционные агенты (бактерии, грибы, паразиты).
Симптомы
Для хронического атрофического гастрита характерны как местные, так и общие проявления. Некоторые симптомы зависят от этиологии заболевания (HP-ассоциированный или аутоиммунный тип) и локализации воспалительного процесса.
При бактериальном генезе хронического атрофического гастрита с локализацией в антральном отделе пациенты предъявляют жалобы на тяжесть в желудке во время или сразу после еды. Если хронический гастрит длительно протекал как гиперацидный, больного могут беспокоить диспепсические нарушения: диарея или запоры, повышенный метеоризм, урчание в животе.
Аутоиммунный гастрит характеризуется тетрадой признаков: аутоиммунный процесс, наличие в крови антител к обкладочным клеткам желудка, В12-фолиеводефицитная анемия, ахлоргидрия. При любом виде хронического атрофического гастрита беспокоят боли в эпигастрии во время или после еды, тошнота, неприятный запах и привкус во рту, отрыжка и срыгивания, жжение в подложечной области или изжога.
Общие проявления выражаются слабостью, раздражительностью, склонностью к артериальной гипотонии, колющими болями в сердце. Для хронического атрофического гастрита характерен демпинг-синдром: после еды возникает резкая слабость, бледность кожи, потливость, сонливость, икота, неустойчивый стул.
Осложнения
При аутоиммунном гастрите антитела поражают не только клетки желудка, но и внутренний фактор Касла, участвующий в метаболизме витамина В12. В результате этого развивается пернициозная анемия, проявляющаяся жжением в языке, симметричными парестезиями в руках и ногах, утомляемостью, сонливостью, депрессией. Помимо В12-дефицитной анемии, хронический аутоиммунный гастрит может осложняться язвенной болезнью желудка и ДПК, ахлоргидрией, раком желудка.
Диагностика
При подозрении на хронический гастрит пациент в обязательном порядке нуждается в консультации гастроэнтеролога и врача-эндоскописта. На первичном приеме назначается ряд анализов и исследований. После получения результатов проводится повторная консультация, на которой обычно и выставляется диагноз хронического атрофического гастрита.
- Лабораторые исследования. Анализ кала на скрытую кровь может быть положительным при наличии изъязвлений в слизистой желудка. В обязательном порядке проводятся исследования с целью обнаружения H.pylori: определение хеликобактер в кале методом ИФА, ПЦР-диагностика, определение антител к хеликобактер в крови, уреазный дыхательный тест.
- Эндоскопия желудка.Эзофагогастродуоденоскопия позволяет выявить атрофию слизистой оболочки желудка. Для подтверждения визуальных изменений проводится эндоскопическая биопсия с морфологическим исследованием биоптатов.
- Дополнительные методы диагностики. Чтобы определить уровень секреции желудочного сока, осуществляется внутрижелудочная pH-метрия. УЗИ органов брюшной полости используется только для дифференциальной диагностики и выявления сопутствующей патологии.
Лечение хронического атрофического гастрита
Перед началом лечения рекомендуется отказаться от вредных привычек (курения, приема алкоголя). Диета не является основным методом терапии хронического атрофического гастрита. Медикаментозное лечение планируется в зависимости от этиологии заболевания (хеликобактерный или аутоиммунный гастрит).
При хроническом атрофическом гастрите, сопровождающемся тяжелыми аутоиммунными нарушениями, показано назначение коротких курсов глюкокортикоидных гормонов в невысоких дозах. После стабилизации процесса и регресса клинических проявлений лечение прекращается. Если секреторная функция желудка не восстановилась, назначают натуральный желудочный сок, прокинетики, ферменты поджелудочной железы. Проводится коррекция В12-дефицитной анемии.
Лечение хеликобактер-ассоциированного хронического атрофического гастрита стандартное: ингибиторы протонной помпы в сочетании с антибактериальными препаратами (кларитромицин, амоксициллин, фуразолидон, метронидазол, тетрациклин), препаратами висмута. Использование препаратов висмута вместо ИПП показано пациентам с пониженной секреторной функцией желудка.
Источник
Атрофический гастрит — симптомы и лечение
Что такое атрофический гастрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Жуковой М. А., гастроэнтеролога со стажем в 22 года.
Определение болезни. Причины заболевания
Атрофический гастрит — это наиболее коварный тип хронического гастрита, при котором изменяются париетальные клетки желудка, из-за чего слизистая оболочка становится тоньше, а железы желудка, вырабатывающие соляную кислоту, атрофируются. Это закономерно приводит к недостаточной выработке соляной кислоты и нарушению переваривания пищи.
Краткое содержание статьи — в видео:
Первоначально заболевание повреждает слизистую оболочку дна желудка (фундального отдела), а затем нарушает продукцию соляной кислоты и пепсиногена, которые обеспечивают желудочное пищеварение [4] .
Так как желудок является начальным звеном пищеварительной системы, нарушение его функции неизбежно влияет на состояние других органов: недостаточно переработанная в механическом и химическом отношении пища нарушает работу тонкого и толстого кишечника, а также поджелудочной железы.
Гастрит с атрофией желёз отличается прогрессирующим течением болезни и более высокой частотой озлокачествления [1] . Известно, что рак желудка не развивается на фоне неизменённой слизистой желудка — ему предшествуют изменения, называемые предраковыми, к которым и относится атрофический гастрит. Длительное течение этой болезни способствует появлению клеток, характерных для тонкого кишечника, вместо желудочных, а избыточное разрастание клеток слизистой провоцирует развитие опухоли.
Атрофический гастрит возникает и прогрессирует по разнообразным причинам, связанным с воздействием на слизистую оболочку желудка. Принято разделять их на две группы — экзогенные (внешние) и эндогенные (внутренние).
Наиболее значимыми факторами развития считаются инфекция Helicobacter pylori (H. pylori) и аутоиммунный гастрит , связанный с выработкой антител к собственным париетальным клеткам [6] . H. Pylori обнаруживают у 80 % с атрофическим гастритом, тогда как аутоиммунный гастрит считается достаточно редким заболеванием. Чаще всего оно встречается у женщин. Он может сопровождаться клиническими проявлениями, а может протекать бессимптомно, т. е. обнаружиться только при гистологическом исследовании после проведения биопсии. При хроническом аутоиммунном гастрите образуются антитела к париетальным клеткам, вырабатывающим соляную кислоту, и внутреннему фактору Касла — белку, который связывает витамин B12, поступающий с пищей, и переводит его в усвояемую форму.
Основной механизм заражения H. pylori неизвестен. Считается, что инфекцией можно заразиться через слюну больного человека, заражённую пищу и воду [13] .
К другим факторам относятся курение и различные алиментарные привычки , вызванные пищевыми погрешностями:
- слишком острые блюда, чересчур холодная или горячая пища;
- злоупотребление алкоголем;
- частое употребление газированных напитков и кофе.
Химические вещества , в т. ч. профессиональные факторы, при длительном воздействии, могут также вызвать атрофию желудка. Согласно исследованиям, наиболее часто гастрит развивается при работе в условиях высокой запылённости и при наличии в воздухе взвеси вредных веществ [3] .
Важную роль в появлении атрофического гастрита играет длительный приём лекарств . Чаще всего он связан с нестероидными противовоспалительными средствами — аспирином , ибупрофеном , диклофенаком , дифлунизалом, пироксикамом , индометацином , кетопрофеном , напроксеном, сулиндаком и др. Также гастрит может развиться после приёма антибиотиков и таких препаратов, как инсулин, сульфаниламид, гормональные препараты, противотуберкулёзные средства. Кроме того, химическое воздействие на слизистую желудка оказывает рефлюкс — процесс заброса агрессивного содержимого кишечника в желудок, вследствие чего повреждается слизистая желудка и развиваются дальнейшие атрофические изменения.
Существенными причинами появления заболевания также являются возрастные изменения: у людей до 30 лет атрофические процессы встречаются в 5 % случаев, до 50 лет — в 30 % случаев, после 50 лет — в 50-70 % случаев. Возможна и генетически обусловленная перестройка слизистой желудка по типу гипо- и атрофии.
К остальным причинам развития атрофического гастрита относят эмоциональные нагрузки, депрессию, сахарный диабет, гипертиреоз, дефицит железа и витамина В12, гипоксию (нехватку кислорода в тканях) при лёгочной и сердечной недостаточности, а также сочетание взаимоусиление нескольких воздействующих факторов [3] .
Симптомы атрофического гастрита
Клиническая картина хронического гастрита связана с местными и общими расстройствами. Часто болезнь может протекать бессимптомно, особенно у людей после 50 лет. Симптомы, как правило, связаны с недостаточной работой желудка и зависят от степени поражения определённого звена пищеварения.
Основными функциями желудка являются:
- временное депонирование (застой) пищи — в среднем еда находится в желудке 3-10 часов, причём жидкость эвакуируется быстро, а жирная пища задерживается дольше;
- частичное переваривание — переработка белков и клетчатки, поступающих с пищей;
- частичное всасывание — усвоение простых углеводов, воды, спиртов;
- моторная функция — перемешивание пищи и проведение её до кишечника;
- бактерицидная функция — связана с действием соляной кислоты, поэтому при снижении её выработки часто возникает дисбактериоз ;
- кроветворная функция, или синтез фактора Касла — гликопротеина, который вырабатывается париетальными клетками желудка, обеспечивает всасывание витамина В12.
При значительном снижении синтеза и отсутствии соляной кислоты возникают следующие местные проявления :
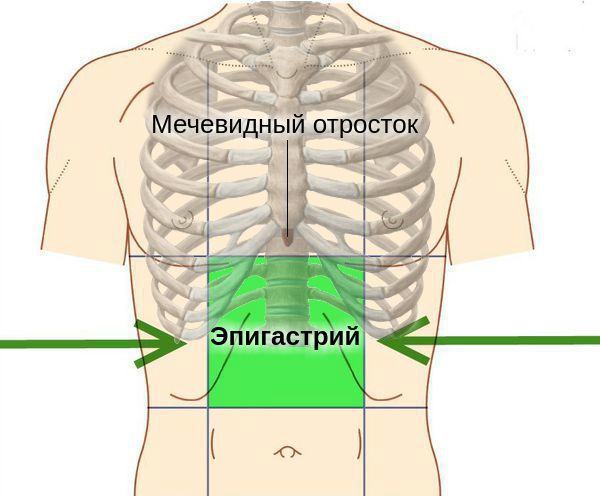
- Симптомы дисперсии (являются ведущим признаком): ухудшение аппетита, отрыжка, тошнота. Возникает чувство тяжести, переполнения в эпигастрии (под мечевидным отростком), распирания в желудке, слюнотечение, неприятный привкус во рту. Может беспокоить жжение в подложечной области, изжога, горечь во рту, свидетельствующая о рефлюксе — забросе желчи из двенадцатиперстной кишки.
- Синдром избыточного бактериального роста часто усугубляет клиническую картину. Как правило, он связан со снижением бактерицидной функции. Проявляется вздутием живота, урчанием, непереносимостью молочных продуктов, неустойчивым стулом. При частых поносах может наблюдаться дефицит массы тела, симптомы недостаточности пищеварения, признаки микроэлементной и витаминной недостаточности, анемия.
- Анемический синдром связан с нарушением всасывания витамина В12. Из-за нарушений микробиоты может развиваться фолиеводефицитная анемия. Возникает выраженная слабость, больной быстро утомляется. Часто беспокоит одышка при незначительной физической нагрузке
- Болевой синдром связан с растяжением желудка из-за нарушения эвакуации пищи. Боли, как правило, тупые, ноющие, распирающие, усиливающиеся после приёма пищи, разлитые, без чёткой локализации.
- Дистрофический синдром вызван гиповитаминозом (нехваткой витаминов Р, С, А, Д), а также белковой недостаточностью. Проявляется сухостью и бледностью кожи, ухудшением зрения, признаками поливитаминной недостаточности. Полигиповитаминоз значительно снижает иммунитет, из-за чего присоединяются различные инфекции [7] .
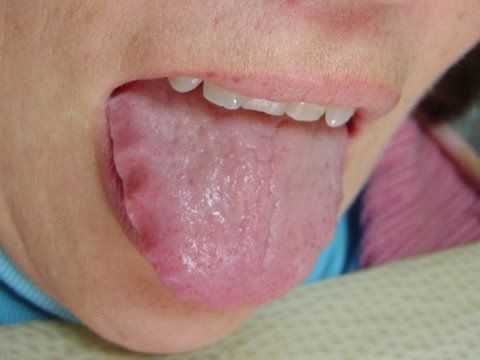
У людей с атрофическим гастритом отмечается «лакированный» язык, при обострениях язык увеличивается (видны отпечатки зубов), он обложен густым белым налётом. При пальпации (прощупывании) области желудка болезненность обычно отсутствует, но иногда возникает слабо выраженная разлитая болезненность в эпигастральной области.
Выработка соляной кислоты постепенно снижается, вплоть до полного её отсутствия. Часто присоединяется сопутствующая патология: панкреатит, холецистит , энтероколит. В компенсированной стадии, когда потеря париетальных клеток ещё не приводит к значительному снижению кислотности, диспепсические симптомы могут быть менее выражены, большинство функций желудка сохранены, при этом гистологическая оценка выявляет атрофию. Поэтому понятие атрофический гастрит (морфологический диагноз) и гастрит с пониженной кислотностью (функциональное состояние) неоднозначны.
У людей с аутоиммунным гастритом выявляются антитела к париетальным клеткам, сопутствует анемия, вызванная дефицитом витамина B12, и значительное снижение секреции соляной кислоты.
Симптомы общих расстройств:
- При астено-невротическом синдроме доминирует общая слабость, часто возникает потливость, раздражительность, беспокоят боли в сердце, аритмия , неустойчивость артериального давления со склонностью к гипотонии .
- При В12-дефицитной анемии на фоне хронического гастрита тела желудка у человека возникает жжение во рту, на языке, боли в сосочках и теле языка (глоссалгии), изменение чувствительности обеих рук или ног. Симптомы анемии также проявляются слабостью, утомляемостью, сонливостью. Часто у таких больных утрачен интерес к жизни и снижен жизненный тонус.
Клинические симптомы гастрита нельзя сопоставить с гистологическими изменениями. Атрофический гастрит развивается медленно, поражение при этом начинается со дна желудка, переходя на его тело, а затем и на остальную слизистую. Считается, что на первых этапах умеренно выраженного атрофического гастрита клиника малосимптомная, стёртая и не имеет специфических проявлений. Но на дальнейших стадиях появляются симптомы, связанные с моторной и секреторной недостаточность желудка.
Патогенез атрофического гастрита
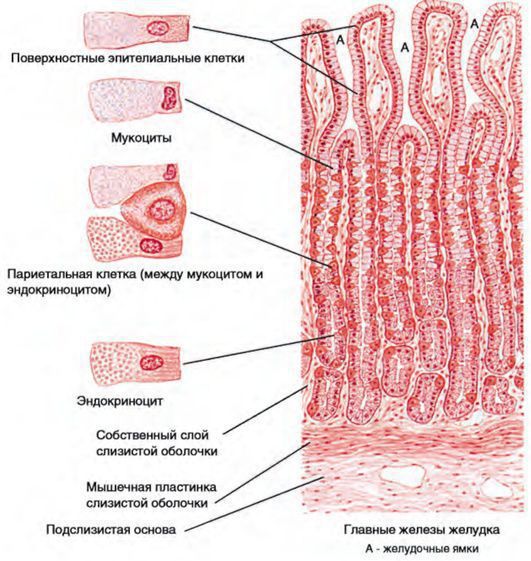
Эпителий слизистой оболочки желудка двухслойный:
- Поверхностный нежелезистый эпителий — обновляется каждые пять дней, покрывает стенку органа.
- Глубокий железистый слой — состоит из более стабильных длительно живущих клеток, выполняющих определённые функции:
- париетальные клетки — вырабатывают соляную кислоту;
- пилорокардиальные клетки — синтезируют слизь;
- главные клетки — продуцируют пепсин — основной пищеварительный фермент;
- G-клетки — железы эндокринной секреции, вырабатывают гастрин — гормон, регулирующий пищеварение.
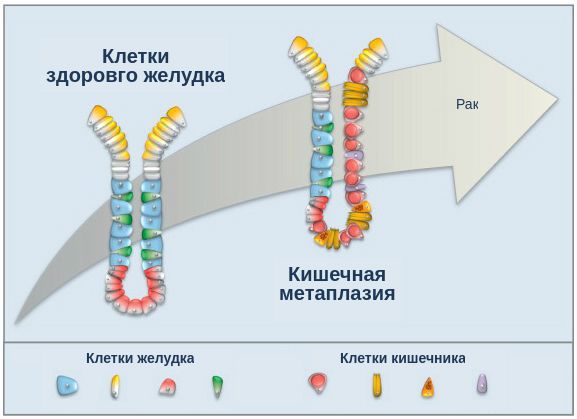
При гастрите оба слоя эпителия желудка вовлечены в патологический процесс. Заселение слизистой H. pylori вызывает хроническое повреждение клеток, ослабляет защитные свойства слизистой желудка, что ведёт к повреждению клеточных ядер свободными радикалами и токсинами. При этом изменяется клеточная структура, нарушается специализация клеток, появляются «гибридные» клетки, которые имеют свойства предраковых. Данный процесс называется кишечной метаплазией. В связи с этими изменениями слизистая желудка сначала приобретает вид тонкокишечного эпителия, затем — толстокишечного эпителия. Чем дальше заходит процесс метаплазии, тем больше вероятность развития аденокарциномы — железистого рака желудка.
Данный нарушенный процесс обновления клеток в слизистой желудка лежит в основе образования атрофии при гастрите. Прослеживается определённый патогенетический каскад, спровоцированный Н. pylori: от инфекционного гастрита через стадии атрофии, метаплазии и дисплазии к раку желудка. Особенно опасно появление неполной — толстокишечной — метаплазии.
Повреждение слизистой оболочки желудка при аутоиммунном гастрите реализуется через другой механизм: нарушение иммунитета приводит к образованию антител, повреждению ткани желудка иммунными комплексами. Чаще всего антитела вырабатываются к фактору Касла, который отвечает за всасывание витамина В12, и G-клеткам. Из-за этого постепенно снижается кислотность желудка, изменяется структура слизистой, снижается выработка соляной кислоты. В желудке нарушается всасывание железа и витаминов, развивается В12-дефицитная анемия. При этом заболевании в 90 % случаев выявляются антитела к париетальным клеткам, вырабатывающим соляную кислоту, и к Н + /К +- АТФазе, в 60 % случаев — антитела к фактору Касла.
При резко выраженной атрофии фундальных желёз возникает компенсаторная, рикошетная гиперпродукция гастрина, также увеличивается активность G-клеток. У людей после 50 лет более выражены явления атрофии с метаплазией железистого эпителия по кишечному типу. Риск появления рака желудка на фоне аутоиммунного гастрита в 3-10 раз выше, чем у других людей. Сочетание такого гастрита с инфекционным существенно ухудшает прогноз [5] .
Классификация и стадии развития атрофического гастрита
По принятой в Сиднее в 1990 году классификации, диагноз гастрита должен учитывать локализацию патологических изменений, гистологические характеристики, выявленные при исследовании биоптатов, эндоскопические находки и вероятные причины развития болезни [5] .
Сиднейская классификация гастритов
В последующем эта классификация дополнялась и уточнялась в связи с новыми научными данными. Сейчас для правильной формулировки диагноза «хронический гастрит» важно установить причину заболевания, распространённость поражения, степени активности и атрофии.
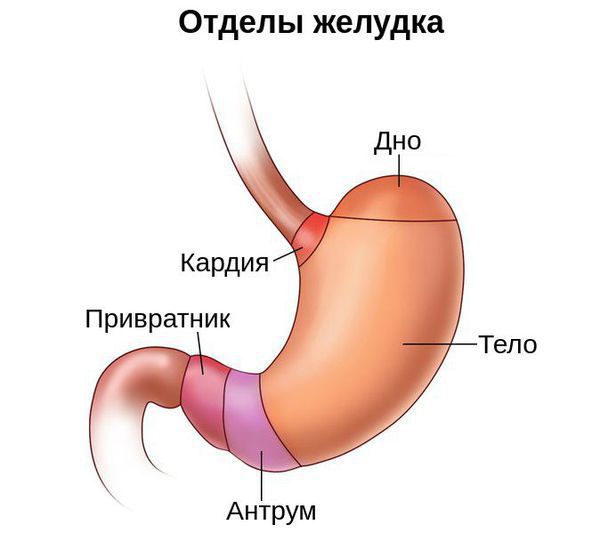
Условно желудок можно поделить на пять отделов: кардия, свод (дно, или фундальный отдел), тело, антрум и привратник. Атрофия может затронуть как один из этих отделов, так и весь желудок. В связи с этим выделяют диффузный атрофический гастрит (в фундальном, антральном или другом отделе) и мультифокальный атрофический гастрит (во всём желудке).
Морфологическая классификация гастрита широко применяется в практике, т. к. именно гистологические характеристики процесса помогают определить прогноз и тактику лечения пациента. Для этого используют визуально-аналоговую шкалу. Она позволяет оценить морфологическую картину слизистой желудка по:
- степени обсеменённости H. pylori (отсутствует, слабая, средняя, сильная);
- по выраженности воспалительного процесса и активности гастрита — лейкоцитарной инфильтрации [1] .
Степень атрофии также оценивается по визуально-аналоговой шкале, изображённой на схеме ниже. По выраженности атрофии и её виду выделяют три категории изменений слизистой оболочки желудка:
- Отсутствие атрофии — сохранена типичная клеточная структура слизистой, в препарате видны главные железы с достаточным количеством париетальных и главных клеток.
- Неподтверждённая атрофия — выражена воспалительная инфильтрация, относительно уменьшены главные железы, разрастания соединительной ткани нет.
- Подтверждённая атрофия :
- метапластическая — железы слизистой оболочки замещаются пилорическими или кишечными железами;
- неметапластическая — характерные для желудка железы сохранены, но количество их существенно уменьшено [1] .
При этом учитывается локализация и степень выраженности атрофических изменений (слабая, средняя, сильная), а также наличие и площадь очагов кишечной метаплазии.
Развитие болезни проходит определённые стадии:
- Поверхностный гастрит — повреждение слизистой желудка поверхностное, секреция соляной кислоты снижена незначительно, симптомы болезни пока не выражены.
- Очаговый атрофический гастрит — в стенке желудка формируются воспалительные очаги, при этом компенсаторно усиливаются функции сохранённых участков желудка.
- Диффузная форма гастрита — значительные нарушения секреторной активности, слизистая желудка истончается, образуются очаги тонкокишечной метаплазии, при эндоскопии слизистая приобретает мозаичный вид — зоны атрофии перемежаются с островками метаплазии и нормальной слизистой. Площадь изменённых участков и распространённость воспаления влияют на прогноз заболевания и риск ракового перерождения.
Осложнения атрофического гастрита
Выраженный атрофический гастрит всегда сопровождается В12-дефицитной анемией, при которой париетальные клетки, вырабатывающие соляную кислоту, практически отсутствуют. Витамин В12, поступающий с пищей, не всасывается, что приводит к хронической анемии с характерными проявлениями в виде быстрой утомляемости, нарушения зрения и вкусовых ощущений, мышечной слабости, головокружений, чувства покалывания и онемения в конечностях.
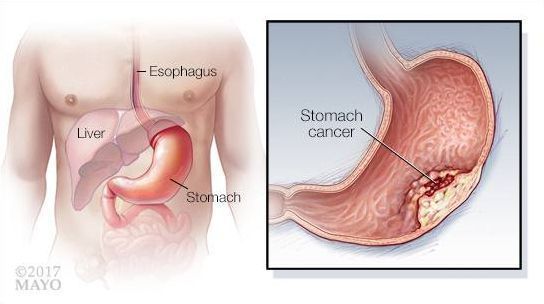
Самым серьёзным осложнением атрофического гастрита является рак желудка . Развитие злокачественной опухоли проходит несколько этапов на протяжении нескольких лет [5] . При этом железы желудка перестают вырабатывать соляную кислоту и гастрин, приобретают свойства тонко- или толстокишечных желёз. Такие изменённые железы в процессе зарождения рака становятся всё более незрелыми, метаплазия эпителия переходит от полного типа (тонкокишечного) к неполному (толстокишечному) типу. Такой процесс существенно повышает риск развития опухоли.
При ахлоргидрии — отсутствии соляной кислоты в желудочном соке — происходит к выраженное нарушение пищеварения, ухудшается переработка пищи, снижается всасывание отдельных микроэлементов и витаминов.
Диагностика атрофического гастрита
Гастрит — диагноз морфологический, т. е. он основан не на симптомах, а на изменениях строения слизистой желудка. Поэтому он может считаться объективным только после оценки слизистой желудка, взятой во время биопсии. Этим занимается патоморфолог. Только с помощью морфологического исследования можно достоверно выявить атрофию, воспаление и деструкцию слизистой желудка.
Клинический диагноз гастрита, т. е. диагноз без морфологического исследования, практически не имеет смысла. Симптомы диспепсии, которые заставляют больного обратиться к врачу, носят лишь функциональный характер и не всегда указывают на те морфологические изменения, которые составляют суть гастрита.
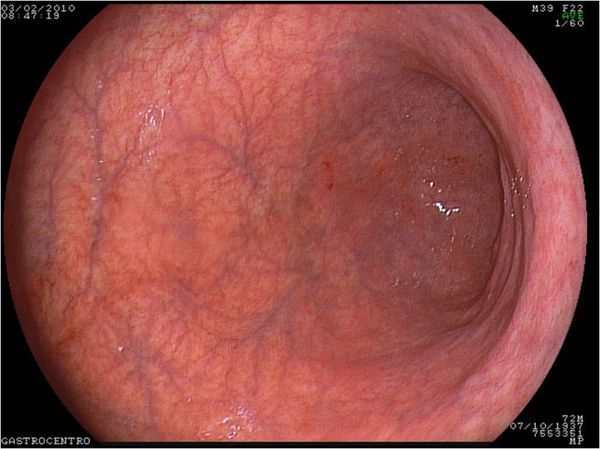
Изменения слизистой можно обнаружить при проведении эзофагогастродуоденоскопии (ЭГДС) — осмотре желудка и двенадцатиперстной кишки с помощью эндоскопа (через видео-трубку). Но результаты этого исследования являются субъективными и только косвенным образом могут указывать на наличие гастрита: они не позволяют оценить степень его прогрессирования.
Во время гастроскопии (ФГДС) выявляются истончение слизистой, уменьшение складок и усиление сосудистого рисунка. Чтобы обнаружить дисплазию или метаплазию, можно воспользоваться хромографией . Для этого слизистую желудка окрашивают специальным красителем: изменённые участки приобретают окраску, отличающую их от здоровой ткани. На УЗИ можно обнаружить сопутствующую патологию органов пищеварительной системы — печени, желчного пузыря, поджелудочной железы.
Способность париетальных клеток выделять соляную кислоту изучается при помощи рН-метрии . Это исследование проводится одномоментно с проведением ФГДС. От его результатов зависит та ктика лечения и прогноз заболевания. Также он помогает контролировать эффективность терапии. Так как при атрофическом гастрите кислотность снижена, pH может колебаться в пределах 3-6.
Лабораторными маркерами атрофического гастрита являются уровень пепсиогена I, пепсиогена II и гастрина-17 в крови. Определить его можно при помощи гемотеста . Снижение выработки пепсиногена I и II указывает на уменьшение функционирующих главных клеток.
Научно доказана возможность скрининга с помощью анализа крови для выявления атрофического гастрита и рака желудка [8] . Существенное значение имеет определение антител к фактору Кастла и антител к париетальным клеткам желудка в сыворотке крови. Тест значительно чувствителен — положителен у 95 % пациентов с В12-дефицитной анемией, хотя специфичность теста низкая: эти антитела могут присутствовать у небольшого процента людей с сахарным диабетом 1-го типа, тиреотоксикозом и аутоиммунным тиреоидитом .
Диагностика H. pylori необходима при любом варианте гастрита. Выяснив причину болезни, можно устранить инфекцию и прерывать патогенетический каскад заболевания и предупредить грозные осложнения, особенно на ранних стадиях [11] . Методы диагностики инфекции могут быть прямыми и косвенными. Настоятельно рекомендуется использовать несколько методов, чтобы исключить ложноположительные и ложноотрицательные результаты.
Оптимальным методом является морфологическое исследование биоптатов. Также в практике широко используется быстрый уреазный тест — определение H. pylori методом оценки количества аммиака в мочевине, образуемого этими бактериями. К другим способам относятся дыхательный тест и иммуноферментные анализы.
Крайне важно провести диагностику Н. pylori до лечения и после уничтожения бактерий, чтобы контролировать эффективность выбранной схемы терапии. Это связано с появлением штаммов бактерий, устойчивых к антибиотикам.
Дефекты пищеварения хорошо выявляет анализ кала (микроскопическое исследование) — достаточно простой метод, который позволяет обнаружить косвенные признаки снижения выработки соляной кислоты, а также изменения, характерные для патологии других органов пищеварительной системы. Так, при атрофическом гастрите в кале появляется большое количество неизменённых мышечных волокон, перевариваемой клетчатки соединительной ткани и внутриклеточного крахмала.
Важно также исследовать кровь по общим показателям . При атрофическом гастрите и В12-дефицитной анемии в анализе крови можно обнаружить снижение уровня гемоглобина.
Лечение атрофического гастрита
Современная терапия хронического гастрита предполагает воздействие на причины заболевания, в частности устранение H. pylori и лечение аутоиммунного гастрита.
Устранить аутоиммунные механизмы повреждения слизистой желудка можно только благодаря гормональной терапии. Назначение глюкокортикостероидов оправдано только при сопутствующей В12-дефицитной анемии.
Совершенно другой подход при обнаружении инфекции H. pylori и лабораторных подтверждений атрофических изменений. Он предполагает эрадикацию — уничтожение H. pylori. Терапия назначается после проведения суточной рН-метрии. При значении рН менее 6, несмотря на пониженную выработку соляной кислоты, назначаются ингибиторы протонной помпы (ИПП); при анацидном состоянии (рН ≥ 6) ИПП исключаются из схемы эрадикации и назначаются только антибиотики.
Согласно исследованиям американских учёных [6] , игнорирование наличия H. pylori при назначении антисекреторной терапии приводит к тому, что воспаление распространяется на всю слизистую оболочку желудка. В итоге через 10-15 лет хронический воспалительный процесс приводит к развитию атрофии главных желёз, повышая риск появления рака желудка. Поэтому при наличии показаний для длительного назначения ИПП необходимо предварительно пройти исследование для выявления H. pylori, а также курс эрадикационной терапии при положительном результате.
Первая линия терапии включает ИПП в полной суточной дозе (40 мг) и два антибиотика: кларитромицин + амоксициллин либо кларитромицин и фуразолидон . Пациентам с резко пониженной секреторной функцией вместо ингибиторов кислотной секреции показано назначение висмута субцитрата ( де-нол ). Если проводимая терапия не привела к полному уничтожению H. pylori, считается, что бактерия устойчива к проводимому лечению. В таком случае необходимо определить чувствительность бактерии к антибиотикам, применяемым в практике [2] .
Если первая линия терапии неэффективна, проводится вторая линия терапии: препарат висмута (висмута трикалия дицитрат), ИПП, тетрациклин и метронидазол . Длительность лечения составляет 7-14 дней.
В России широко используются препараты висмута в качестве терапии первой и второй линии (в комбинации трёх препаратов), чаще других назначается де-нол ( улькавис ). Назначение висмута при лечении хронического гастрита оправдано, т. к. нет необходимости быстро купировать боль, как при обострении язвенной болезни , когда применяются схемы с ИПП. Малосимптомное течение хронического гастрита позволяет провести эрадикацию на основе висмутсодержащих препаратов.
Через 4-6 недель после окончания антихеликобактерной терапии необходимо провести контрольное исследование — С13-уреазный дыхательный тест.
После устранения инфекции уже через месяц снижается активность гастрита. Если атрофия ещё не успела развиться, то можно говорить о полном излечении болезни. При атрофическом гастрите нормализуется клеточное обновление слизистой желудка, прерывается патогенетический каскад, что не даёт развиться раку желудка [9] .
Хронический химикоиндуцированный или желчный рефлюкс-гастрит объединяет большую группу больных, включая:
- людей с удалённой частью желудка;
- пациентов, получавших НПВС (нестероидные противовоспалительные средства);
- больных дуоденогастральным рефлюксом ;
- пациентов, страдающих алкоголизмом.
Цель лечения — нормализовать моторику желудочно-кишечного тракта и связывание желчных кислот.
Тактика лечения зависит от основной причины гастрита:
- ИПП . Поскольку желчные кислоты и лизолецитин повреждают слизистую желудка только при наличии соляной кислоты, ИПП можно использовать в зависимости от выраженности симптомов.
- Блокаторы дофаминовых рецепторов ( домперидон и другие) — показаны для предотвращения заброса в желудок содержимого двенадцатиперстной кишки.
- Урсодезоксихолевая кислота — применяется для нейтрализации желчных кислот, повреждающих слизистую желудка.
- Симптоматическая терапия :
- диета;
- приём прокинетиков ( ганатон , мотилиум , итомед ) — влияют на моторику желудка и двенадцатиперстной кишки;
- нормализация пассажа содержимого кишечника;
- восстановление баланса микрофлоры и нормализация стула при склонности к запору;
- приём препаратов, поглощающих газ (симетикон).
Также показано восполнение недостающих витаминов, назначение препаратов железа при анемии, заместительная терапия ферментами. Эффективна бальнеотерапия — приём минеральной воды с высоким содержанием солей для стимуляции секреции (в тёплом виде за 20-30 минут до еды), отвары трав (подорожника, полыни, фенхеля), кислые соки, растворы лимонной и янтарной кислот. Используются стимуляторы регенерации слизистой желудка (облепиховое масло, ребагит, метилурацил ), гастропротекторы ( мизопростол , вентер , де-нол), обволакивающие препараты — таблетки и суспензии на основе алюминия и висмута, препараты для улучшения сокращения органов желудочно-кишечного тракта. Активно применяется физиотерапия : электрофорез с лекарственными препаратами, хорошо снимают боли сеансы магнитотерапии, а также тепловые процедуры на область эпигастрия. Санаторно-курортное лечение показано вне периода обострения на бальнеологических курортах.
Прогноз. Профилактика
Прогноз заболевания серьёзнее у пациентов старше 50 лет, т. к. в этом возрасте метапластические процессы развиваются гораздо быстрее и чаще приводят к появлению рака. Эффективность лечения зависит от степени выраженности атрофии и площади поражения. Большое значение имеет ранее начало лечения и полное устранение H. pylori (иногда лечение помогает только времено подавить активность инфекции [13] ). При выявлении H. pylori после проведённой терапии необходимо повторное лечение.
Существенно влияет на прогноз заболевания площадь распространения метаплазии и атрофического процесса. Если метаплазия распространилась на 20 % слизистой, то риск ракового развития достигает почти 100 %. По статистике, хронический атрофический гастрит в 13 % случаев неизбежно заканчивается онкологией [10] . Большое значение для прогноза болезни имеет и снижение выработки соляной кислоты, т. к. при этом нарушаются механизмы противоопухолевой защиты.
Принципиально важно постоянное наблюдение пациентов с хроническим гастритом. Оно предполагает эндоскопию с биопсией и гистологическим исследованием, которое должно проводиться не реже двух раз в год. Чем больше степень воспалительных изменений, тем выше риск развития атрофии. Если атрофический гастрит уже развился, то необходимо установить его стадию. Это позволит определить, входит ли пациент в группу риска развития рака желудка [10] [12] .
Предраковые изменения на фоне атрофического гастрита (кишечная метаплазия и дисплазия) представляют наибольшую опасность. При этом своевременная диагностика и полное удаление H. pylori уже через пять лет восстанавливают слизистую желудка и значительно уменьшают площадь метаплазии.
Источник