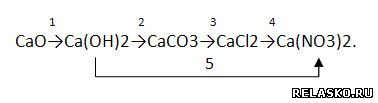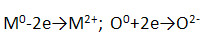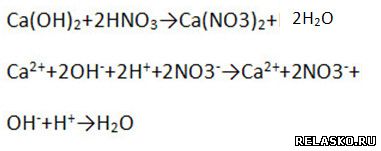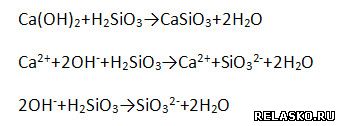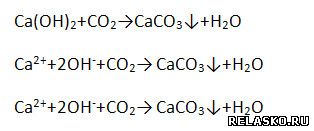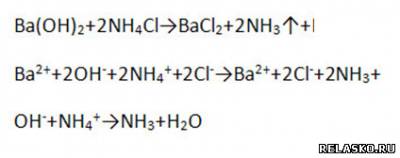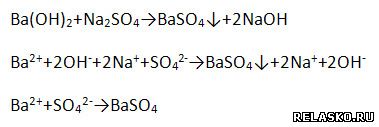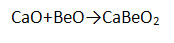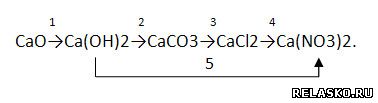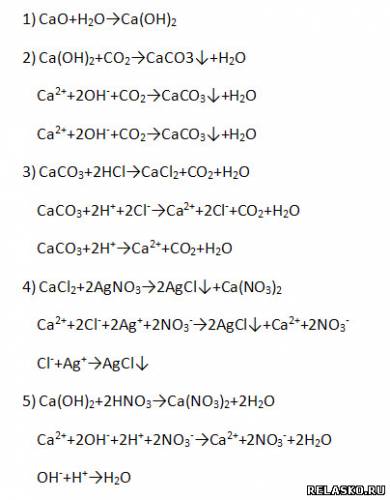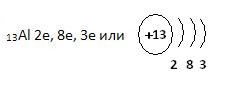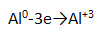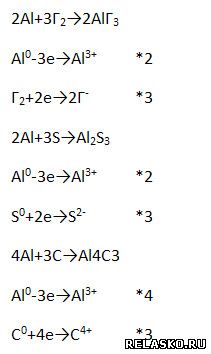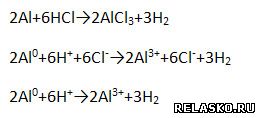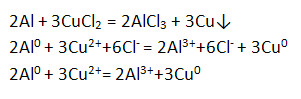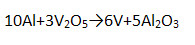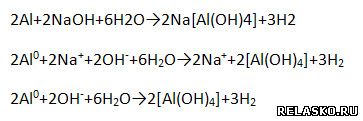Соотнесите газ собираемый способом вытеснения воздуха с расположением сосуда
Тема 20. Общая характеристика неметаллов.
Часть I
1. Положение неметаллов (НМ) в Периодической системе.
По диагонали B-At и над ней в 6 группах располагаются неметаллы. Всего из 114 элементов к НМ относят 22.
2. Особенности строения атомов НМ:
1) небольшой радиус атома
2) число электронов на внешнем уровне 4-8.
3. НМ обладают свойством аллотропии – явление существования одного хим. элемента в виде 2 или нескольких простых веществ.
4. Заполните таблицу «Причины аллотропии».
5. НМ – простые вещества и свободные атомы, проявляют и окислительные, и восстановительные свойства.
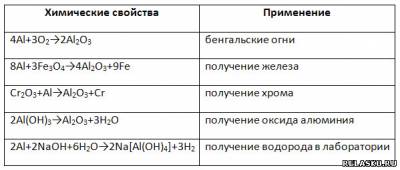
Заполните таблицу «Химические свойства неметаллов».
Запишите уравнения реакций, рассмотрите их в свете процессов окисления-восстановления.
6. Дополните таблицу «Состав воздуха».
Часть II
1. Запишите, в каком порядке «выкипают» из жидкого воздуха его основные составные части.
1) азот N2 (tк)=-196 ⁰С
2) аргон Ar (tк)=-186 ⁰С
3) кислород O2 (tк)=-183 ⁰С
2. Молярный объём воздуха имеет массу 29 г. Величина, показывающая, во сколько раз молярная масса любого газа тяжелее М воздуха, называется относительной плотностью этого газа по воздуху и обозначается Dвозд.
Найдите Dвозд для:
3. Какой объём каждого из трёх основных компонентов воздуха можно получить из 500 м3 воздуха?
4. Дополните схему «Роль воздуха в природе и жизни человека».
5. Соотнесите газ, собираемый способом вытеснения воздуха, с расположением сосуда.
6. Выберите явления, которые вызывает присутствие в воздухе его составных частей: 1) случайных; 2) переменных. Из букв, соответствующих правильным ответам, вы составите названия химических элементов – неметаллов:
1) азот; 2) сера.
а) смог – 1
б) парниковый эффект – 2
в) грипп – 1
г) озоновые дыры – 2
д) аллергия на цветение растений – 1
е) туман – 2
ж) кислотные дожди – 1
з) свежесть воздуха в сосновых лесах – 2
Источник
Соотнесите газ собираемый способом вытеснения воздуха с расположением сосуда

1. Как различить кристаллические сульфаты магния, кальция, бария?
При растворении в воде:
MgSO4 – растворится полностью;
CaSO4 – растворится частично;
BaSO4 – не растворится.
2. Запишите уравнения реакций, с помощью которых можно осуществить превращения по схеме:
Для всех реакций, кроме первой, запишите уравнения в молекулярной, полной и сокращённой ионной формах:
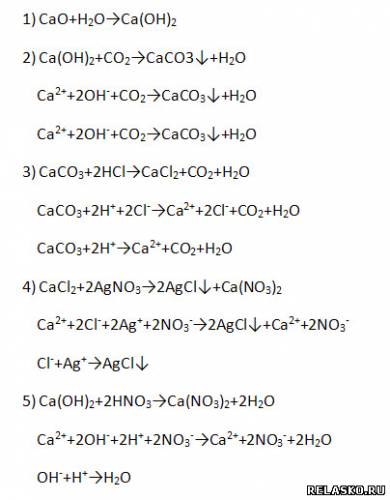
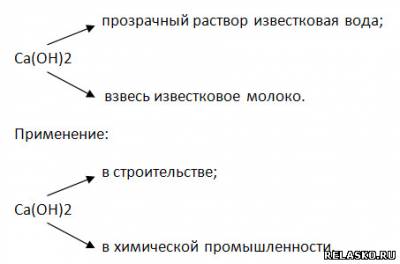
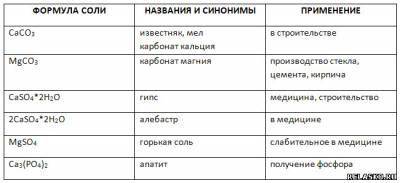
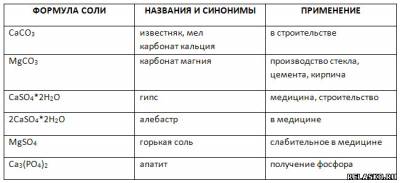
3. Заполните таблицу «Применение солей кальция и магния»
4. Фосфоры – это люминофоры
Область их применения: Шоу-техника, декорации, светящиеся диски.
5. Напишите синквейн о химическом элементе кальции или его соединении.
1. кальций
2. металлический и блестящий
3. химически активный
4. основа минералов
5. строительство.
6. Какую массу известняка, содержащего 20% примесей, подвергли обжигу, если получено 112 кг негашёной извести?

 |  |
| Родион | Дата: Четверг, 01.10.2015, 17:56 | Сообщение # 32 | |
| | Тема 15. Соединения щёлочноземельных металлов. 1) Имеют ионную кристаллическую решётку и образованы за счёт ионной химической связи, схема которой: Физические свойства данных соединений: белые гигроскопичные кристаллические вещества. 2) Характер оксидов – основный, что подтверждается химическими свойствами (напишите уравнения возможных реакций – молекулярные, полные и сокращённые ионные): 2. Гидроксиды M(OH)2. 1) Тип кристаллической решётки – ионная, состоит из катионов М2+ и анионов ОН-. Физические свойства: белые кристаллические вещества, хорошо растворяются в воде. Реакция с участием оксида кальция:
2) Химические свойства (составьте уравнения возможных реакций в молекулярной, полной и сокращённой ионной формах): б) взаимодействует с нерастворимой кислотой (составьте уравнения возможных реакций в молекулярной, полной и сокращённой ионной формах) в) взаимодействует с кислотными оксидами г) взаимодействует с солями, если образуется ↑
д) взаимодействует с солями, если образуется ↓ е) взаимодействует с амфотерными оксидами ж) взаимодействует с амфотерными основаниями | |
|
| Родион | Дата: Четверг, 01.10.2015, 17:59 | Сообщение # 33 | |
| | Часть II 1. Как различить кристаллические сульфаты магния, кальция, бария? При растворении в воде: 2. Запишите уравнения реакций, с помощью которых можно осуществить превращения по схеме: Для всех реакций, кроме первой, запишите уравнения в молекулярной, полной и сокращённой ионной формах:
3. Заполните таблицу «Применение солей кальция и магния»
4. Фосфоры – это люминофоры Область их применения: Шоу-техника, декорации, светящиеся диски. 5. Напишите синквейн о химическом элементе кальции или его соединении. 1. кальций 6. Какую массу известняка, содержащего 20% примесей, подвергли обжигу, если получено 112 кг негашёной извести?
| |
|
| Родион | Дата: Пятница, 02.10.2015, 09:24 | Сообщение # 34 | |
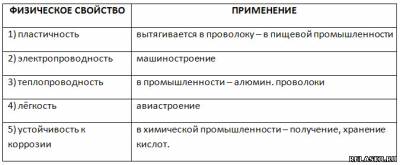
| | Тема 16. Алюминий. 1. Дополните схему строения атома алюминия. 13Al 2е, 8е, 3е или 2. Al проявляет сильные восстановительные свойства, получая при этом с.о. +3, по соответствующей схеме: 3. Эта же схема отражает образование в простом веществе металлической связи. Алюминий имеет металлическую кристаллическую решётку и характеризуется следующими физическими свойствами: серебристо-белый, электро-, термопроводен, пластичный. 4. Заполните таблицу «Применение алюминия на основе его физических свойств».
5. В ряду активности металлов алюминий следует за металлами IIA группы, т.е. очень активен, но с водой, как подсказывает бытовой опыт, не взаимодействует при обычных условиях (алюминиевые провода и посуда не разрушаются под действием воды). Почему? Есть защитная плёнка оксида алюминия. Как осуществить реакцию, схема которой: Растереть алюминий в порошок и смешать с водой при высокой температуре. 6. Химические свойства алюминия (запишите уравнения возможных реакций – молекулярные, полные и сокращённые ионные). 1) Сгорает при нагревании (рассмотрите с позиций окисления-восстановления). 2) Взаимодействует с неметаллами (рассмотрите ОВР). 3) Взаимодействует с растворами кислот. 4) Взаимодействует с растворами солей. 5) Взаимодействует с оксидами металлов – алюминотермия. 6) Взаимодействует с растворами щелочей. | |
|
| Родион | Дата: Пятница, 02.10.2015, 09:26 | Сообщение # 35 |
| | Часть II 1. Заполните таблицу «Применение алюминия на основе его химических свойств».
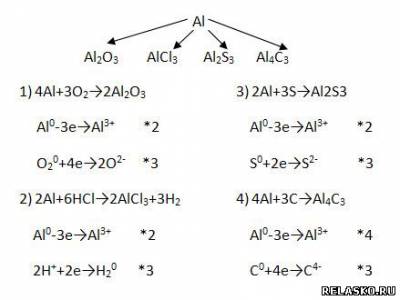
2. Запишите уравнения реакций, с помощью которых можно осуществить соответствующие переходы, в свете ОВР.
3. Амальгама – это соединение, в состав которого входит ртуть. 4. Подготовьте сообщение об амальгамах золота и их значении, используя различные источники информации(интернет). Запишите тезисы сообщения или составьте его план в особой тетради. Метод амальгамации основан на способности ртути образовывать сплавы — амальгамы с различными металлами, в том числе и с золотом. В этом методе увлажненная дробленая порода смешивалась со ртутью и подвергалась дополнительному измельчению в мельницах-чашах. Амальгаму золота (и сопутствующих металлов) извлекали промывкой, после чего ртуть отгонялась из собранной амальгамы и использовалась повторно. Метод амальгамации известен с I века до н. э., наибольшие масштабы приобрел в американских колониях Испании начиная с XVI века. Это стало возможным благодаря наличию в Испании огромного ртутного месторождения — Альмаден. В более позднее время использовался метод внешней амальгамации, когда дробленая золотоносная порода при промывке пропускалась через обогатительные шлюзы, выстланные медными листами, покрытыми тонким слоем ртути. Метод амальгамации применим только на месторождениях с высоким содержанием золота или уже при его обогащении. Сейчас он используется очень редко, главным образом старателями в Африке и Южной Америке. 5. Подготовьте с помощью Интернета презентацию (5-10 слайдов) на тему «История алюминия». Запишите план презентации. 1) Открытие алюминия 2) Нахождение в природе 3) Физические и химические свойства 6. Вычислите, какое количество граммов оксида хрома (III), содержащего 20% примесей, и моль алюминия необходимо для получения 4,5 моль хрома с помощью алюминотермии. Источник |