- комбинаторика — Раскраска шахматной доски n x n в n цветов
- 2 ответа
- комбинаторика — Сколько существует таких раскрасок?
- 1 ответ
- Решение №963 Найдите количество способов закрасить некоторые клетки «лесенки» …
- Подготовка к олимпиаде
- Мáркеры для клеток: как ученые «раскрашивают» клетки, чтобы отличить одну от другой
- Конкурс «био/мол/текст»-2017
- Естественные клеточные маркеры и способы их рассмотреть
- Раковые маркеры
- Искусственные маркеры: внедрить и распознать
- Как ВИЧ помогает ученым
комбинаторика — Раскраска шахматной доски n x n в n цветов
Сколькими способами можно раскрасить клетки шахматной доски n x n в n цветов так, чтобы клетки, имеющие общую сторону, были окрашены в разные цвета и чтобы в каждом горизантольном ряду встречались все n цветов
Встречал задачу для 6 и 8, поэтому написал 2n, хотя неуверен, что условие четности необходимо, но пусть будет так, чтоб наверняка.
задан 18 Окт ’15 21:43
sapere aude
1.9k ● 13 ● 76
63% принятых
так сколько цветов — n или «все 2n»?
из условий «в каждом ряду встречаются все цвета» и «число цветов равно длине ряда» уже следует, что соседние клетки окрашены в разные цвета.
2 ответа
В самом начале, видимо, опечатка: имеется в виду $%2n$% цветов.
Условие чётности здесь, по сути, не нужно. Задача решается в общем виде для любой доски $%m\times m$%.
Первую строку выбираем $%m!$% способами. Следующую — с учётом отсутствия неподвижных элементов подстановки. Если сверху идут $%1$%, $%2$%, . , $%m$%, а под ними $%i_1$%, $%i_2$%, . , $%i_m$%, то это приводит к известной задаче о подстановках без неподвижных элементов. Их количество вычисляется по формуле $%f(m)=m!(\frac1<2!>-\frac1<3!>+\frac1<4!>-\frac1<5!>-\cdots+(-1)^m\frac1
Каждая очередная строка раскрашивается тем же числом способов, и в итоге будет $%m!f(m)^
Источник
комбинаторика — Сколько существует таких раскрасок?
Каждую клетку доски $%3\times 3$% раскрашивают в один из трёх цветов, причём клетки, имеющие общую сторону, не должны быть одного цвета. К тому же, все три цвета использовать совсем не обязательно. Сколько существует таких раскрасок?
задан 3 Мар 15:32
В задачах на число способов раскраски указывается — считать ли раскраски, полученные при поворотах/симметриях, различными
@spades: здесь не было сказано, поэтому раскраски различны по умолчанию. Но при наличии ограничений получается своя задача, также представляющая интерес. Можно будет потом заодно прикинуть, какие там ответы.
1 ответ
Рассмотрим раскраску четырёх клеток, соседних с центральной. Там присутствует один цвет или два. Разбираем случаи.
1) Все рассмотренные клетки одного цвета. Его выбираем 3 способами. Каждую из оставшихся 5 клеток независимо раскрашиваем в один из двух цветов. Итого 3 * 2^5 = 96.
2) Три рассмотренные клетки одного цвета, одна — другого. Тут 3 способа выбрать цвет, повторяющийся трижды, и 2 способа выбрать оставшийся. Также 4 способа выбрать место для клетки одного цвета. Далее центр раскрашивается однозначно, две угловые клетки тоже, и две угловые — в 2 цвета каждая. Итого 3 * 2 * 4 * 2^2 = 96.
3) Две рассмотренные клетки одного цвета, две другого.
а) Одноцветные клетки идут напротив. Здесь 3 способа выбора горизонтальных, 2 для вертикальных. Остальное однозначно. Это 6 способов.
б) Одноцветные клетки идут по диагоналям. Тут 2 способа выбрать направление диагонали, 3 способа выбора цвета верхней диагонали, 2 для нижней. Два угла раскрашены однозначно, как и центр, два угла — 2 способами каждый. Итого 2 * 3 * 2 *2^2 = 48.
Источник
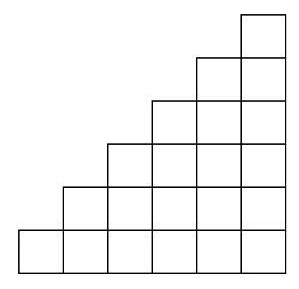
Решение №963 Найдите количество способов закрасить некоторые клетки «лесенки» …
Найдите количество способов закрасить некоторые клетки «лесенки» так, чтобы выполнялись следующие условия:
• Ниже каждой закрашенной клетки либо нет других клеток, либо они все закрашены.
• В одном столбце закрашено 5 клеток, в другом – 4 клетки, в третьем – 3 клетки, …, в последнем – 0 клеток.
Источник задания: ВсОШ sochisirius.ru
Ниже каждой закрашенной клетки либо нет других клеток, либо они все закрашены.
Это условие говорит о том, что нужно начинать закрашивать клетки с нижний и подряд, не пропуская клеток.
5 клеток можем закрасить, только в 2 столбцах на выбор.
4 клетки, учитывая что в одном уже закрашено 5 клеток, можем тоже закрасить в 2 столбцах на выбор.
3 клетки, учитывая, что есть столбец с 5 клетками и 4 клетками, тоже 2 способами. И так далее..
2 клетки – 2 способами.
1 клетку – 2 способами.
0 клеток – 1 способом (останется один столбец)
Тогда всего вариантов:
2·2·2·2·2·1 = 32
Ответ: 32.
Есть три секунды времени? Для меня важно твоё мнение!
Насколько понятно решение?
Средняя оценка: 4.8 / 5. Количество оценок: 6
Оценок пока нет. Поставь оценку первым.
Новости о решённых вариантах ЕГЭ и ОГЭ на сайте ↙️
Вступай в группу vk.com 😉
Расскажи, что не так? Я исправлю в ближайшее время
В отзыве оставляйте контакт для связи, если хотите, что бы я вам ответил.
Источник
Подготовка к олимпиаде
Раскраска дома
1. В каждой вершине правильного 100-угольника поставлены фишки: 76 красных и 24 синих. Доказать, что найдутся 4 красные фишки, образующие квадрат.
Решение. Фишки образуют 25 квадратов. Синие фишки являются вершинами не более чем в 24 квадратах, поэтому хотя бы один квадрат будет красным.
2. Клетки прямоугольника 5 × 41 окрашены в два цвета. Доказать, что можно выбрать 3 строки и 3 столбца так, чтобы их пересечения имели один цвет.
Решение. Будем считать, что в прямоугольнике 41 столбец, по пять клеток в каждом. В каждом столбце пометим 3 одноцветные клетки. Это можно сделать 10 способами. Значит, найдется
5 столбцов с одинаково помеченными клетками. Из них хотя бы в трех помечены клетки одного цвета.
3. Клетки таблицы 15 × 15 окрашены в три цвета. Доказать, что найдется 2 строки, в которых клеток одного цвета поровну.
Решение. Допустим противное. Тогда во всех строках клеток каждого цвета разное количество, а всего в таблице клеток одного цвета не менее
0 + 1 + . + 14 = 105; клеток всех трех цветов не менее 315, а в таблице 225 клеток — противоречие.
Найти раскраску
1. Таблицу 4 × 4 раскрасить в 4 цвета так, чтобы на любой горизонтали, вертикали и диагонали были бы все цвета.
Ответ: рис. 1.
2. Сколько клеток таблицы 8 × 8 можно закрасить так, чтобы никакие 3 центра закрашенных клеток не лежали на одной прямой?
Решение. Можно закрасить 16 клеток (рис. 2).

Раскрасить больше 16 клеток нельзя: тогда на какой-то горизонтали появится третья окрашенная клетка.
3. Найти все развертки куба, которыми можно покрыть плоскость без пропусков и перекрытий.
Ответ: плоскость можно покрыть паркетом из фигур, изображенных на рисунке 3.
Сколько способов?
1. Каждую грань кубика разбили на 4 одинаковых квадрата и раскрасили квадраты в несколько цветов так, чтобы квадраты, имеющие общую сторону, были разных цветов. Какое наибольшее количество квадратов одного цвета могло получиться?
Решение. Это количество будет наибольшим, когда боковая поверхность куба покрашена в шахматном порядке. Основание нельзя покрасить в тот цвет, который на боковой поверхности был использован 8 раз (рис. 4).
2. Сколькими способами можно покрасить в 6 цветов грани куба?
Решение. Любую грань можно покрасить в первый цвет (пусть это верхняя грань). Для нижней грани остается 5 вариантов. Любую грань боковой поверхности можно покрасить в третий цвет. Для остальных граней остается 3! = 6 вариантов. Итого: 5×6 = 30.
3. Сколькими способами можно окрасить в 6 цветов 6 равных секторов диска?
Решение. Любой сектор может быть окрашен в любой цвет. Для остальных секторов остается 5! = 120 вариантов.
Раскраска — метод решения
1. Можно ли таблицу 6 × 6 с вырезанными противоположными углами покрыть костями домино размером 1 × 2? Кости не должны перекрываться и выступать за края таблицы.
Решение. Раскрасим таблицу в шахматном порядке (рис. 5).
Получим 18 белых и 16 черных клеток. Кость домино покрывает одну белую и одну черную клетку, следовательно, на доске можно разместить 16 костей, и две белые клетки не будут покрыты доминошками.
2. Учитель попросил ученика вырезать из картонной шахматной доски (8 × 8) 8 квадратов размером 2 × 2 (с условием: не портить оставшиеся клетки). Потом учитель вспомнил, что ему нужно 9 квадратов. Может ли он из остатков доски вырезать девятый квадрат? А десятый?
Решение. Решающее свойство: при вырезании одного квадрата может быть испорчен только один закрашенный. Следовательно, вырезав 8 квадратов, ученик испортил не более 8 закрашенных. Если ученик вырезал 8 закрашенных квадратов, кроме одного углового, то из остатков доски еще один квадрат вырезать можно, а два — не вырезать (рис. 6).
3. Можно ли таблицу 6 × 6 с вырезанными противоположными углами обойти ходом шахматного коня (побывав в каждой клетке один раз)?
Решение. Нет. Клетка, откуда идет конь, и клетка, куда он идет, разного цвета (см. рис. 5).
Эти задачи предлагались школьникам на олимпиадах разных лет. Подобные задачи встречаются в заданиях международной математической олимпиады «Кенгуру».
Источник
Мáркеры для клеток: как ученые «раскрашивают» клетки, чтобы отличить одну от другой
Выделить все важное и отличить от других — вот задача клеточных мáркеров.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: В этой статье рассказывается о том, как ученые научились в широком смысле «раскрашивать» клетки — выделять из общей смеси только те, которые им интересны, а остальные отсеивать. Речь пойдет как о естественных поверхностных и внутриклеточных мáркерах и способах их выявления, так и о более изощренных генетических способах маркировать клетки. Читателя ждет открытие, что штрих-коды бывают не только в магазинах, но и в клетках, а вирус иммунодефицита человека превратился в послушный инструмент.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

Что первое приходит на ум неискушенному в науке человеку при слове «мáркер»? Бьюсь об заклад, что добрая половина представляет себе желтый широкий фломастер для выделения текста. Другая половина, наверняка, представляет себе черный нестираемый маркер, которым одно время были исписаны все трубы, заборы и веранды. Начертания «Маша + Саша = Любовь» скрепляли чувства подростков навечно, а менее романтичные, но выразительные фразы надолго свидетельствовали о личной неприязни. Встречались даже стихи. Однако предлагаю уважаемым читателям узнать еще одно значение этого слова — очень научное и так нужное всей современной биологии и биомедицине. В научном понимании и конкретно в клеточной биологии, слово «маркер» в широком смысле означает что-то, что отличает одну живую клетку (или группу клеток) от других. Это может быть молекула на поверхности клеточной мембраны, или какой-нибудь внутриклеточный белок, или вещество, которое синтезируется/накапливается только в этом конкретном виде клеток, или генетическая особенность, присущая только данному типу клеток. Условно все маркеры можно разделить на естественные, которые существуют сами по себе, и искусственные — введенные намеренно. Давайте разберемся с ними по порядку.
Естественные клеточные маркеры и способы их рассмотреть
В многоклеточных организмах существует клеточная специализация. Несмотря на то, что клетки содержат одинаковую ДНК, они отличаются друг от друга: клетки мышц умеют сокращаться, нейроны — проводить нервные импульсы, и так далее. Это происходит из-за того, что в каждом виде клеток работает только определенный набор генов из всего их разнообразия, содержащегося в ДНК. Именно поэтому маркером клеток может служить любой ген, который экспрессируется избирательно — только в каком-нибудь конкретном виде клеток. Особенно удобно, когда такой отличительный ген кодирует белок, располагающийся на поверхности клетки.
Раковые маркеры
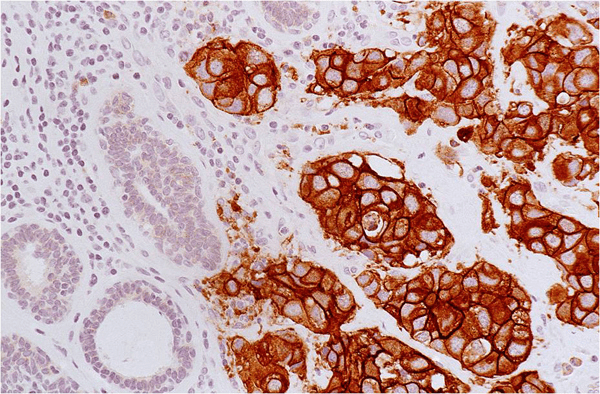
Часто можно слышать слово — «онкомáркер». Это классический пример клеточных маркеров: молекул на поверхности опухолевых клеток, которые или не встречается совсем, или присутствуют в гораздо меньшем количестве на поверхности здоровых клеток. Одним из ярких примеров онкомаркеров является HER2-антиген на поверхности клеток рака груди (рис. 1) [1]. HER2 — рецептор эпидермального ростового фактора. В результате аномального увеличения количества копий гена этого рецептора в опухолевых клетках нарушается регуляция клеточного цикла, и опухоль начинает быстро расти. HER2+-варианты рака груди — очень агрессивны [2].
В этом случае у ученых есть целый набор методов, как можно «увидеть» клетки, несущие такой маркер, отличить их от остальных клеток и даже отсортировать: в одну пробирку — клетки с поверхностным маркером (или с несколькими маркерами), в другую — остальные. Эти методы основаны на использовании антител.
Антитела — специальные белки, которые могут распознавать молекулы за счет пространственного взаимодействия. Именно антитела играют важную роль в нашем иммунитете — они связываются с белками или другими молекулами на поверхности бактерий и вирусов, что и запускает иммунную реакцию. Современная наука научилась делать антитела против практически любых белков — в том числе и против поверхностных клеточных маркеров. Чтобы использовать антитела для определения маркеров, ученые прибегают к еще одной хитрости. Они присоединяют к антителу еще один белок: или фермент, или флуоресцирующий (светящийся) белок. Тогда, если к исследуемым клеткам добавить антитела против поверхностного маркера, связанные с ферментом, потом отмыть лишние антитела и добавить субстрат для фермента, который при расщеплении приобретает какой-нибудь цвет, то клетки, несущие на своей поверхности нужный маркер, окажутся окрашенными, а остальные клетки — останутся бесцветными (рис. 1).
Рисунок 1. Пример выявления онкомаркера HER2 с помощью антител (иммуногистохимия). Коричневые клетки несут на своей поверхности HER2.
Такая модификация выявления маркера называется иммуногистохимией («иммуно» — из-за того, что используют иммунные антитела, «химия» — потому что в методе присутствует химическая реакция расщепления субстрата ферментом, «гисто» — потому что чаще всего такой метод применяют к гистологическим срезам — тонким слайсам исследуемой ткани, которые закреплены на стеклянной подложке).
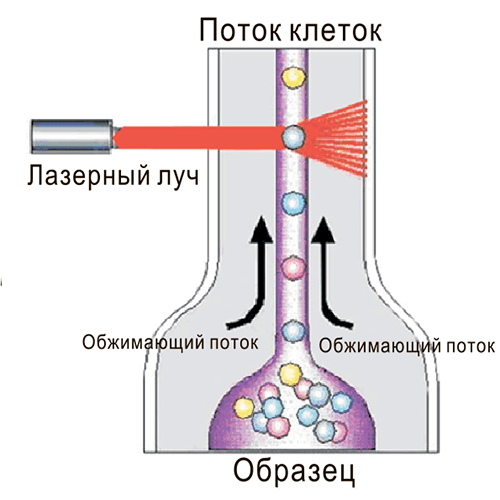
Другой метод, позволяющий выявлять поверхностные маркеры, называется проточной цитофлуориметрией (fluorescence-activated cell sorting, FACS) [3]. Здесь исследуемые клетки (в виде одноклеточной взвеси) смешивают с антителами, к которым присоединены флуоресцирующие белки. Антитела связываются со своими маркерами-мишенями, a не связавшиеся антитела удаляют. Далее клетки загружают в прибор. Он создает тонкую струю из клеточной суспензии, проходящую через свет лазера буквально по одной клетке. Если на поверхности клетки есть искомые маркеры, то вместе с клеткой в луч лазера попадают и антитела, связавшиеся с маркерами. Происходит возбуждение флуорофора на антителе, и он испускает на своей длине волны свет, который и регистрируется детектором (рис. 2).
Рисунок 2. Общий принцип проточной цитофлуориметрии.
После этого прибор может отклонить эту клетку из струи или в одну сторону, или в другую. Таким образом можно разделить клетки на две группы: с маркером и без. Получается, что прибор «знает», есть ли искомые маркеры на каждой из исследуемых клеток, сколько таких клеток, умеет сортировать нужные и ненужные клетки.
Описанные способы позволяют выявлять естественные маркеры — молекулы, которые и до начала исследования присутствовали на поверхности или внутри клеток. Эти методы сильно помогли ученым разобраться в том, чем опухолевые клетки отличаются от нормальных, стволовые клетки — от более зрелых и дифференцированных, и разные ткани — друг от друга.
Искусственные маркеры: внедрить и распознать
У описанных выше методов есть один существенный недостаток: они не позволяют установить родственные связи между клетками. Вот, предположим, у нас есть 100 клеток, и у 12 из них есть маркер А на поверхности. Все эти клетки А для нас будут на одно лицо, как близнецы (рис. 3).
Рисунок 3. Братья-близнецы из фильма «Приключения Электроника».
Мы не сможем сказать, произошли ли все эти 12 клеток от одной материнской и являются ли «близкими родственниками». Или, скажем, можно предположить, что они получились после деления нескольких клеток с исследуемым маркером и являются друг другу двоюродными, троюродными братьями и сестрами, а может быть и вовсе седьмой водой на киселе. Чтобы исследовать родственные связи в клеточной популяции (еще говорят — «исследовать клональный состав популяции» [4]) и следить за тем, как ведет себя потомство отдельных клеток, ученые научились вводить искусственные генетические маркеры в клетки. Делают это несколькими способами. Один из самых продвинутых способов на сегодняшний день — использование специальных вирусов.
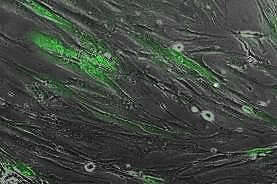
Рисунок 4. Мультипотентные мезенхимальные стромальные клетки (ММСК) человека, маркированные лентивирусом с зеленым флуоресцентным белком GFP.
собственные данные автора статьи, [4]
Современная генная инженерия достигла таких невиданных высот, что специалисты научились конструировать вирусы с заранее известными, тщательно отобранными для целей исследователей свойствами. Например, можно создать вирус, который способен заражать клетку — проникать через ее оболочку в ядро, — встраиваться в ДНК зараженной клетки, и больше ничего не делать: не создавать новые вирусные частицы, не копировать себя в геноме зараженной клетки, не экспрессировать ни один из вирусных генов. Вместо этого ученые смогли заставить вирус, который встроился в ДНК клетки, экспрессировать нужные белки (например, на этом принципе основана генотерапия). В частности, можно сделать так, что с ДНК вируса экспрессируется флуоресцентный белок [5], и зараженная клетка начинает светиться во флуоресцентном микроскопе (рис. 4).
Вирусы, которые способны направленно доставлять гены в ДНК клетки, стали называть вирусными векторами.
Как ВИЧ помогает ученым
Не все вирусы способны встраиваться в ДНК клетки-хозяина. Такой способностью обладают вирусы семейства Retroviridae, или ретровирусы. Представители этого семейства — РНК-содержащие вирусы, которые после проникновения в клетку используют ее транскрипционный аппарат и собственную обратную транскриптазу, чтобы получить вирусную ДНК, которая затем встраивается в ДНК клетки-хозяина. Семейство Retroviridae среди прочих содержит два рода, которых чаще всего используют в качестве векторов, — это Gammaretrovirus (гаммаретровирусы) и Lentivirus (лентивирусы). Преимущество последних заключается в том, что помимо делящихся клеток (когда отсутствует ядерная мембрана), они способны заражать и клетки, находящиеся в состоянии покоя!
На заметку: именно к этому семейству принадлежит вирус иммунодефицита человека (ВИЧ). На его основе придуманы многие генетические векторы. Так что, в руках ученых ВИЧ из возбудителя страшной болезни превратился в послушный инструмент исследования.
Введение вектора в клетки для исследования их клонального состава принято называть маркированием клеток. Вы здесь совершенно справедливо спросите: «Позвольте, а где же здесь маркирование? Ну, ввели мы ДНК вируса в ДНК клетки, но дальше-то что?». А я Вам отвечу, что здесь-то и начинается самое интересное! Введенная ДНК действительно может выступать в роли маркера. Здесь есть два варианта: 1) маркером может служить не сама вирусная ДНК, а то место, куда она встроилась; 2) маркер может содержаться в самой вирусной ДНК.
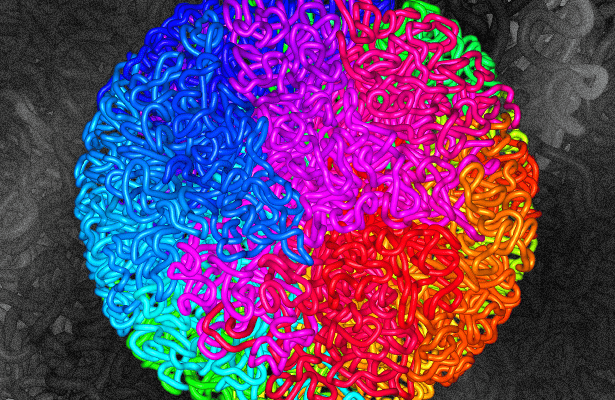
Разберем эти возможности по порядку. Итак, наш вирус проник в клетку, сумел добраться до ядра, с боем прорвался через ядерную мембрану и встроился в ДНК клетки-хозяина. Но вот вопрос: в какое именно место он встроился? Вы когда-нибудь видели, как выглядит ДНК в клетке? Ну, вот примерно так, как на рисунке 5 .
Про то, каким удивительным образом в одном клеточном ядре величиной в несколько микрометров упаковываются молекулы ДНК, длина которых измеряется в метрах, читайте увлекательную статью на «Биомолекуле»: «Организовать геном: запутанная история гипотез и экспериментов» [6].
Рисунок 5. Модель фрактально-глобулярной структуры ДНК. Цветом здесь условно обозначены разные хромосомы.
Соответственно, у одного маленького вируса много возможностей, куда встроиться. В идеале — их бесконечно много, и поэтому найти две клетки, в которых бы вирусы встроились в абсолютно одинаковом месте, — довольно сложно. Еще один важный момент заключается в том, что если зараженная клетка решит поделиться, то обе ее дочерние клетки будут содержать провирус (так называется вирус, который встроился в геномную ДНК) в одном и том же месте генома! Другими словами, генетический маркер — наследуемый признак. Если научиться определять, в какое же именно место генома попал вирус в разных клетках, то можно было бы отличать потомство одной зараженной клетки от другой! И ученые умеют это! Существует несколько методов, позволяющих это сделать, главные из которых — метод саузерн-блоттинга и полимеразная цепная реакция, опосредованная лигированием [7], [8].
Про принцип гибридизации по Саузерну я отсылаю тебя, дорогой читатель, к другой замечательной статье, посвященной описанию важнейших методов молекулярной биологии: «Важнейшие методы молекулярной биологии и генной инженерии» [9]. А о полимеразной цепной реакции расскажет статья «12 методов в картинках: полимеразная цепная реакция» [10].
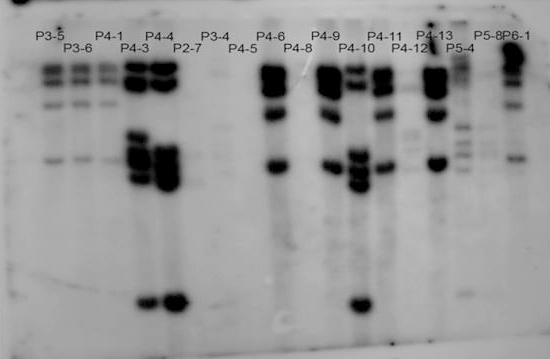
Оба метода основаны на том, что вследствие случайного характера интеграции вируса в геномную ДНК расстояние от провируса до ближайшего сайта рестрикции будет разным в двух независимо зараженных клетках. Соответственно, если из зараженных клеток выделить ДНК и разрезать ее одной из рестриктаз, то длина фрагмента, содержащего провирус, будет разной у потомства двух разных зараженных клеток, и будет одинаковой у всех клеток, которые произошли в результате деления одной зараженной клетки. Если после рестрикции разделить фрагменты гель-электрофорезом [11], перенести на нитроцеллюлозную мембрану и гибридизовать с короткой последовательностью дезоксирибонуклотидов, комплементарной провирусу (такие олигонуклеотиды принято называть зондами), то на фотобумаге проявится набор полос, который будет одинаковым для клеточного потомства одной клетки и разным — для клеточного потомства нескольких зараженных клеток (рис. 6).
Рисунок 6. Саузерн-блот клеточных клонов, полученных из популяции, зараженной лентивирусным вектором. Каждая дорожка — результат саузерн-блоттинга ДНК из клеточного клона (клеточного потомства одной зараженной клетки). Набор полос в каждой дорожке соответствует продукту гибридизации зонда, комплементарного провирусу, с фрагментами расщепленной ДНК, содержащими провирус. Фрагменты разделены по длине с помощью гель-электрофореза.
собственные данные автора статьи, [4]
Из картинки видно, что на первых трех (и некоторых других дорожках — предлагаю читателю размяться и подсчитать их!) паттерн полос идентичен. Это говорит о том, что ДНК, проанализированная в этих образцах, получена из клеток, произошедших от одной исходно зараженной материнской клетки. Легко также заметить, что дорожка с таинственным названием Р5-4 содержит совершенно другой набор полос. Это означает, что ДНК, использованная здесь, принадлежала другой зараженной клетке. Недостаток такого метода в том, что он не позволяет в явном виде идентифицировать сайт интеграции провируса. Метод позволяет только сравнивать между собой клеточные клоны и судить об их родстве.
Другой метод, который позволяет анализировать сайты интеграции провирусов, — полимеразная цепная реакция, опосредованная лигированием [8]. Это достаточно сложный и многостадийный метод, который включает в себя рестрикцию ДНК, присоединение (лигирование) адаптеров, использование магнитных микрочастиц, ПЦР, электрофорез и секвенирование и заслуживает отдельной статьи. Прошу тебя, мой читатель, поверить мне на слово — этот метод позволяет с точностью до нуклеотида определить место в ДНК, в которое произошла интеграция провируса. С помощью этой методики можно не только различить потомство зараженных клеток между собой, но также судить о том, сколько вирусов проникло в ДНК зараженной клетки, в какие гены произошла интеграция, и не произошло ли изменение их экспрессии в результате внедрения вируса [12], [13].
Ранее я упомянул о том, что в качестве маркера, кроме места интеграции, можно использовать и саму ДНК провируса. Давайте рассмотрим подробнее, как это можно сделать. Здесь нам поможет химический синтез олигонуклеотидов! Дело в том, что в ДНК вируса можно вводить любую информацию: например, ген, кодирующий флуоресцирующий белок или фермент. Правда, тогда все вирусные частицы ничем не будут отличаться одна от другой и приобретут смысл маркеров только тогда, когда попадут в клетку. А почему бы не сделать сами вирусные частицы уникальными? Для этого ученые конструируют лентивирусные векторы, несущие так называемые генетические штрих-коды [14]. Суть заключается в том, что с помощью химического синтеза получают смесь олигонуклеотидов, где в некоторых позициях случайным образом содержится любой из четырех известных дезоксирибонуклеотидов. Дизайн штрих-кода может быть, например, таким:
ATC NNN GGA NNN TAT NNN CGA NNN ATT NNN GTG NNN
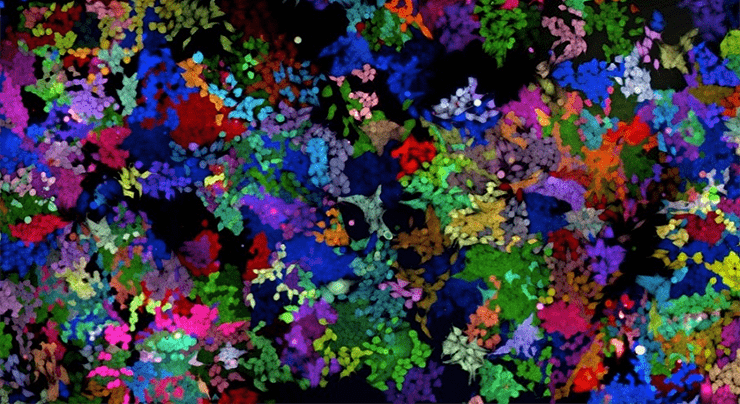
Здесь символы N обозначают любой из известных нуклеотидов (А, Т, C или G). Такой штрих-код ничего не кодирует, но он представляет собой смесь нуклеотидов с разными последовательностями. Приведенный штрих-код — на самом деле смесь из 4 18 (или приблизительно 10 11 после несложных, но утомительных математических преобразований) различных олигонуклеотидов! Такая смесь используется для сборки вирусов. На выходе получаются уже не обезличенные вирусы, похожие друг на друга как две капли воды, но целая библиотека вирусов, где каждая вирусная частица несет какой-то из возможных олигонуклеотидов-штрих-кодов. Клетки заражают такой вирусной библиотекой, и каждая зараженная клетка получает в свою ДНК уникальный стабильный наследуемый маркер в виде генетического штрих-кода. Все дочерние клетки будут нести тот же штрих-код (или набор штрих-кодов), который приобрела материнская клетка при заражении. Клеточное потомство двух разных зараженных материнских клеток будет иметь различные штрих-коды. Подобно тому, как штрих-коды на товарах в обычном продуктовом магазине позволяют однозначно идентифицировать и отличить один товар от другого, так генетические штрих-коды позволяют отличить потомство одной зараженной клетки от другой. Если затем из зараженной популяции клеток выделить ДНК и определить все присутствующие в ней штрих-коды с помощью новых методов секвенирования, то можно однозначно установить клональный состав клеточной популяции, проследить за динамикой клонов и выявить те клоны, которые преобладают над другими. После заражения библиотекой лентивирусов со штрих-кодами клеточная популяция становится как будто раскрашенной маркерами с очень-очень-очень разнообразной палитрой [15], примерно вот так (рис. 7):
Рисунок 7. Как выглядела бы клеточная популяция, если бы каждый генетический штрих-код имел свой цвет.
Рисунок 8. Канцелярские принадлежности.
Источник