- Получение алкадиенов
- Получение алкадиенов
- 1. Дегидрирование алканов
- 2. Синтез Лебедева
- 3. Дегидратация двухатомных спиртов
- 4. Дегидрогалогенирование дигалогеналканов
- Синтез бутадиена 1 3 по способу лебедева
- Реакция Лебедева: формула, механизм реакции. Получение бутадиена
- Принцип реакции
- Реагенты и продукты
- Механизм реакции
- Использование в промышленности
- Дальнейшее изучение
- Диеновый синтез
Получение алкадиенов
Алкадиены – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствуют две двойные связи между атомами углерода С=С.
Общая формула алкадиенов CnH2n-2 (как у алкинов, а также циклоалкенов), где n ≥ 3.
Наличие двух двойных связей между атомами углерода очень сильно влияет на свойства углеводородов. В этой статье мы подробно остановимся на свойствах, способах получения и особенностях строения алкадиенов.
Получение алкадиенов
1. Дегидрирование алканов
Отщепление водорода от бутана — это промышленный способ получения дивинила. Реакция протекает при нагревании в присутствии оксида хрома (III):

Изопрен получают каталитическим дегидрированием изопентана (2-метилбутана):
2. Синтез Лебедева
Н агревание этанола в присутствии катализатора (смесь оксидов Al2O3, MgO, ZnO) – это промышленный способ получения дивинила из этанола (синтез Лебедева).
При этом образуются бутадиен-1,3, вода и водород:
3. Дегидратация двухатомных спиртов
Под действием серной кислоты вода отщепляется от бутандиола-1,3. При этом образуется дивинил и вода:
4. Дегидрогалогенирование дигалогеналканов
Под действием спиртовых растворов щелочей протекает отщепление атомов галогена и водорода и образуются вода, соль и алкадиен.
При этом атомы галогенов в дигалогеналкане должны располагаться не у одного и не у соседних атомов углерода.
1,3-Дихлорбутан реагирует со спиртовым раствором гидроксида калия с образованием бутадиена-1,3:
Источник
Синтез бутадиена 1 3 по способу лебедева
Синтез бутадиена-1,3 (дивинила) по способу С. В. Лебедева и дегидрированием н-бутана
Производство бутадиена достигло большого развития в нашей стране, так как это позволило осуществить впервые в мире в крупном масштабе получение синтетического каучука и тем самым обеспечить резиновую промышленность отечественным сырьем. В результате многолетних исследований С. В. Лебедева к 1928 г. был разработан промышленный способ получения бутадиен а-1,3 из этилового спирта. Им был найден катализатор, позволяющий осуществить это превращение с хорошим выходом и в одну стадию. Известно, что в присутствии катализаторов, ускоряющих реакции дегидратации (А1208, ТЮ2 и др.), легко происходит отщепление воды от этилового спирта с образованием этилена: а над дегидрирующими катализаторами (ZnO, SnOa и др.) в результате отщепления водорода получается уксусный альдегид:
Лебедев нашел, что, применяя смешанный катализатор (из указанных двух групп), можно одновременно осуществить как дегидратацию, так и дегидрирование с получением бутадиена:
Производство бутадиена началось в 1932 г. на заводах в Ярославле и в Воронеже.
Указанная реакция, сопровождаемая многими побочными реакциями, осуществляется при 370—380° и давлении, близком к атмосферному, в так называемой контактной печи 3 (рис. 112); это — цилиндрическая печь высотой и диаметром по 6,5 м из огнеупорного кирпича с двойными стенками, внутри которой по окружности установлено 24 стальные реторты 4 прямоугольного сечения высотой 5 м, заполненные катализатором. Кольцевое пространство между двойными стенками представляет собой топку 5, в которой сгорает газообразное топливо; нагревание реторт происходит преимущественно за счет лучеиспускания раскаленной внутренней стенки; топочные газы поступают затем во внутреннее пространство печи и далее в боров. Спирт-сырец, синтетический, гидролизный, сульфитный или полученный брожением, смешивают с отходом производства — спиртом-регенератом. Полученная шихта (
80% спирт) испаряется в трубках спиртоиспарителя (на рис. 112 не указан), обогреваемых паром. Пары спирта, проходя через перегреватели / и 2, омываемые топочными газами, нагреваются
до 380° и поступают в контактную печь 3, где распределяются по всем ретортам. Выходящий из реторт так называемый контактный газ собирается в кольцевом трубопроводе 6 и охлаждается до 180° в котле-утилизаторе 7. Газ представляет собой смесь, содержащую более 30 веществ; помимо не прореагировавшего спирта и продуктов основной реакции — бутадиена, паров воды и водорода, — в ней содержатся в наибольшем количестве уксусный альдегид, диэтило-вый эфир, этилен, пропилен и псевдобутилен (бутен-2).
Бутадиен представляет собой газ с температурой кипения — 4,5°, хорошо растворимый на холоду в спирте и почти нерастворимый в воде и в разбавленном водой спирте. Для его выделения и очистки прежде всего удаляют из контактного газа вещества с относительно высокой температурой кипения. Газ охлаждается в холодильнике 8 водой, а затем в холодильнике 9 до 0° рассолом с холодильной установки. Образовавшийся в холодильниках конденсат представляет собой водный спирт, содержащий примеси — эфир, уксусный альдегид и др.; путем ректификации из него получают спирт-регенерат, который смешивают со свежим спиртом и вновь направляют на разложение.
Следующей стадией в процессе очистки является извлечение спиртом бутадиена из газа. Для повышения растворимости, а также и температуры кипения бутадиена газ предварительно сжимают до 7 am в компрессоре 10. После охлаждения нагревшегося при этом газа он поступает в три последовательно соединенные поглотительные башни (скруббера) с насадкой 12 (на рис. 112 изображен лишь один), где происходит абсорбция бутадиена холодным 80% спиртом, движущимся противоточно движению газа. Отходящий газ с высоким содержанием этилена, пропилена и водорода является ценным сырьем для различных производств органического синтеза. Отгонкой из раствора в отгонной ректификационной колонне 14 получается бутадиен-сырец, а спирт из этой колонны после охлаждения в теплообменнике 13 направляется вновь на абсорбцию.
Дальнейшая стадия очистки — удаление содержащихся в сырце этилового спирта, уксусного альдегида и эфира, для чего используется их хорошая растворимость в воде. Отмывка водой указанных примесей происходит в отмывной колонне с насадкой из керамических колец, при противоточном движении жидкостей. Выделяемый из конденсата и водного раствора уксусный альдегид добавляется к спиртовой шихте, а эфир путем присоединения воды при пропускании его смеси с водяным паром над А1203 превращается в спирт. Ректификацией отмытого сырца получают бутадиен-ректификат с содержанием 91—95% бутадиена; остальное — псевдобутилен, присутствие которого, однако, существенно не влияет на процесс полимеризации бутадиена. Выход бутадиена достигает 72% от теоретического количества, считая на прореагировавший спирт.
В настоящее время на заводах в Сумгаите (близ Баку) и в Стер-литамаке (Башкирская АССР) осуществлен новый способ получения бутадиена — каталитическим двухстадийным дегидрированием н-бутана. В этом способе сырьем служит бутановая фракция, выделяемая из попутного нефтяного газа, а также фракция н-бутана, получаемая в качестве отхода в производстве алкилата; сырье подвергается дополнительной ректификации для удаления примесей и высушиванию безводным хлористым кальцием. В первой стадии дегидрирования образуется смесь изомерных бутиленов — бутена-1 и бутена-2:
C4H105tC4H8+Ha-Q.
н-бутан бутен-1 и бутен-2
Для быстрого проведения процесса во избежание усиления побочных реакций крекинга применяется катализатор — Сг203 на носителе — А1аОэ, причем активатором служит КОН. При оптимальной температуре 580° и атмосферном давлении равновесие достигается за 2 сек с превращением 45% н-бутана в бутилены; при более высоких температурах усиливается крекинг углеводородов. Катализатор постепенно покрывается коксом и теряет свою активность. Применяется процесс с «кипящим» слоем пылевидного катализатора, который сходен с вышеописанным процессом каталитического крекинга нефтепродуктов (часть XII, § 5). Установка для дегидрирования также включает в себя трубчатую печь для нагревания бутана, реактор и регенератор — оба с «кипящим» слоем катализатора. Выходящий из реактора контактный газ после освобождения от пыли катализатора в циклоне охлаждается в котле-утилизаторе, затем в перегревателе и испарителе, где он отдает теплоту бутану, и, наконец, в скруббере, орошаемом водой.
Для того чтобы осуществить циркуляцию не прореагировавшего бутана, необходимо его отделить от образовавшихся бутиленов, водорода и продуктов побочных реакций. Газ сжимают до 13 am, охлаждают водой и извлекают из газа соляровым маслом С4-фрак-цию углеводородов (бутан и бутилены), которую выделяют отгонкой и конденсацией паров. Отделить бутан от бутиленов непосредственно ректификацией не удается вследствие близости температур кипения; однако при введении в смесь водного ацетона (80% ацетона + 20% воды) летучесть бутиленов уменьшается, вследствие их лучшей растворимости в ацетоне по отношению к летучести бутана и последний легко отделяется ректификацией под давлением 7 am; этот способ разделения веществ называется экстрактивной перегонкой. Раствор бутиленов в ацетоне из первой ректификационной колонны поступает во вторую отгонную колонну, в которой ректификацией пары бутиленов отделяются от ацетона. Выход бутиленов на прореагировавший бутан составляет 80% от теоретического количества.
Бутилены во второй стадии дегидрирования превращаются в бутадиен-1,3 в присутствии катализатора, содержащего Fe203, Сг203.
В этой обратимой реакции при 600—620° и атмосферном давлении превращению подвергается лишь 15% бутиленов; так как объем газа при протекании реакции возрастает, то уменьшение давления может повысить превращение до 25—30%. Понижение парциальных давлений углеводородов достигается введением в смесь больших количеств перегретого водяного пара (10 объемов и более на 1 объем бутиленов), который доставляет, кроме того, теплоту, необходимую для поддержания постоянной температуры. Парогазовая смесь пропускается через неподвижный слой катализатора в виде шариков и затем из нее выделяется, как указано выше, фракция С4-углеводородов, содержащая бутилены и бутадиен. Вследствие близости температур кипения разделить их ректификацией невозможно. Для их разделения используется способность холодного аммиачного раствора СН3СООСи извлекать из этой смеси бутадиен с образованием водорастворимого комплексного соединения (аналогично извлечению СО из газовой смеси, см. часть XII, § 14); при нагревании оно разлагается с выделением бутадиена; выделенные из смеси бутилены смешиваются со свежими и направляются повторно на дегидрирование. Выход бутадиена на прореагировавшие бутилены достигает 70%, а выход его на исходный бутан составляет 52—56% от теоретического количества. Несмотря на значительную сложность производственного процесса и более низкий выход бутадиена, чем по способу С. В. Лебедева, себестоимость его ниже на 25—30% бутадиена, полученного из синтетического спирта, вследствие дешевизны сырья. По этой причине и благодаря наличию громадных ресурсов н-бутана предполагается интенсивно развивать производство бутадиена из н-бутана.
Источник
Реакция Лебедева: формула, механизм реакции. Получение бутадиена
Реакция Лебедева Сергея Васильевича стала отправной точкой в исследованиях способов получения диеновых непредельных углеводородов, которые хорошо применяются до сих пор при создании синтетических каучуков. Данное открытие позволило использовать относительно дешевый и рентабельный метод синтеза искусственной резины для военного и технического назначения, что обеспечило в советские времена выпуск качественной и прочной замены натуральных каучуков.
Принцип реакции
По принципу протекания данный синтез относят к каталитическому пиролизу (термическому разложению), который проходит в присутствии алюмо-цинковых оксидных катализаторов при температуре около 450 °С.
В химии реакция Лебедева примечательна тем, что она проходит в одну стадию, но при этом внутри нее происходит сразу три изменения:
- отщепляется вода;
- отрывается водород;
- происходит присоединение между алкильными остатками.
Синтез неоднократно совершенствовался, применялись новые алюминиевые катализаторы с добавлением солей марганца и других металлов, а также варьировались условия проведения, что позволило снизить энергозатратность при поддержании температуры (360–370 °С) и увеличить степень превращения спирта в ходе реакции (до 50%, выход бутадиена–1,3 составляет 42%).
Реагенты и продукты
В ранних исследованиях С. В. Лебедев прибегал к созданию бутадиена из нефтяных фракций. Однако впоследствии он стал получать данный диен из этилового спирта, полученного путем брожения картофеля. Для получения одной лишь автомобильной шины требовалось переработать до 500 кг картофеля, что, естественно, было экономически невыгодно.
Позже, в период 1926-928 гг., С.В. Лебедев вместе со своей командой из учеников и вольных слушателей усовершенствовал способ получения бутадиена из этилового спирта. Выход диена на момент демонстрации результатов был 22%. Благодаря стараниям, ученые одержали победу на конкурсе, организованном И.В. Сталиным среди сейчас уже бывших стран Советского Союза, по предложениям способов производства синтетического каучука.
Так, теперь в конечном варианте синтеза, в основных продуктах получают бутадиен‒1,3 CH2=CH‒CH=CH2, воду H2O и свободный водород H2. Дополнительно могут образоваться некоторые ароматические соединения, этилен, пропилен, бутилены, высшие спирты и ацетальдегид, но в основном уравнении реакции Лебедева формулы этих веществ не указываются. Поскольку этот диен является газообразным веществом, нерастворимым в воде, его от всех других углеводородов отделяют конденсацией, адсорбцией спиртом, отмывкой H2O или же ректификацией.
Механизм реакции
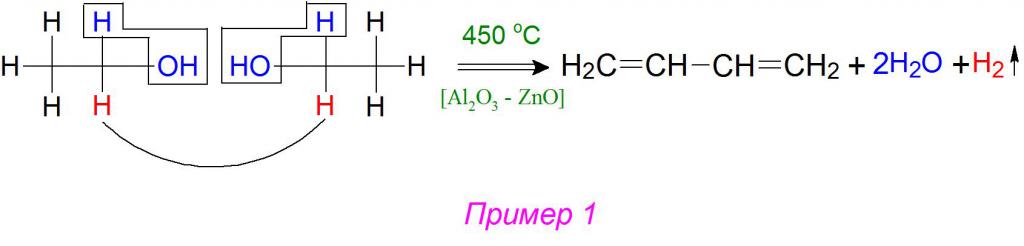
В синтезе при расщеплении (разложении) 2 молекул этилового спирта, благодаря дегидратирующе-дегидрирующим катализаторам, от них отрываются 2 молекулы воды и 1 молекула газообразного водорода. Согласно механизму реакции Лебедева, алкильные остатки присоединяются друг другу, образуя две непредельные сопряженные двойные связи в 1,3–положениях (пример 1).
Использование в промышленности
После триумфальной победы на международном конкурсе ученому дали возможность осуществить производство синтетического каучука в промышленном масштабе. Так как получение бутадиена по реакции Лебедева было признано очень ценным, его профинансировали, и в 1930 году в Ленинграде был построен опытный завод «Литер «Б»», который вплоть до 1990 года занимал первое место в мире по производству искусственного каучука. На базе этого предприятия впоследствии был создан Всесоюзный научно-исследовательский институт синтетического каучука, который продолжает заниматься изучением полимерных соединений.
Дальнейшее изучение
Открытия С. В. Лебедева послужили началом изучения свойств диеновых углеводородов, благодаря которым был открыт так называемый «диеновый синтез». Существуют три версии, по которым он в ходе научной деятельности изучил реакцию димеризации диенов. Первая предполагает, что в результате синтеза ученый получил димер циклопентадиена. Вторая версия говорит о димеризации изопрена с получением дипентена. А третья описывает получение винилциклогексена из двух молекул бутадиена‒1,3. Во всяком случае этот синтез лег в основу дальнейшего изучения свойств сопряженных диенов, которые развивали Отто Дильс и Курт Адлер, удостоенные Нобелевской премии в 1950 году.
Диеновый синтез
Реакция Дильса-Адлера позволила получать циклосоединения по довольно простым механизмам, не прибегая к сложным многостадийным реакциям. Суть реакции сводится к взаимодействию сопряженного диена и диенофила, который может быть представлен алкенами и алкинами с электроакцепторными заместителями, а также соединениями, содержащими двойные связи с гетероатомом, например –C=O, ‒C=N и др. В результате образуется циклический углеводород, поэтому эту реакцию еще называют «циклоприсоединением».
Синтез по Дильсу-Адлеру может проходить в присутствии кислот Льюиса, которые значительно ускоряют ход реакции и чаще всего способствуют хорошему выходу основного продукта, а также влияет на образование энантиомеров и цис-/транс- изомерии.
Примером такой реакции без катализатора может служить присоединение бутадиена–1,3 к пара-бензохинону в среде бензола при температуре 35 °С, в результате которого выход продукта достигает 100%. Синтез проходит с переходом протонов водорода между углеродными атомами для образования второго цикла и создания прочного соединения. В конце реакции образуется производное 1,4–нафтохинона, который может дальше реагировать с бутадиеном‒1,3 при 100 °С с образованием цикла на противоположной стороне. Из конечного продукта реакции путем дегидрирования можно получить антрахинон, производные которого используются в качестве красителей, например ализарин.
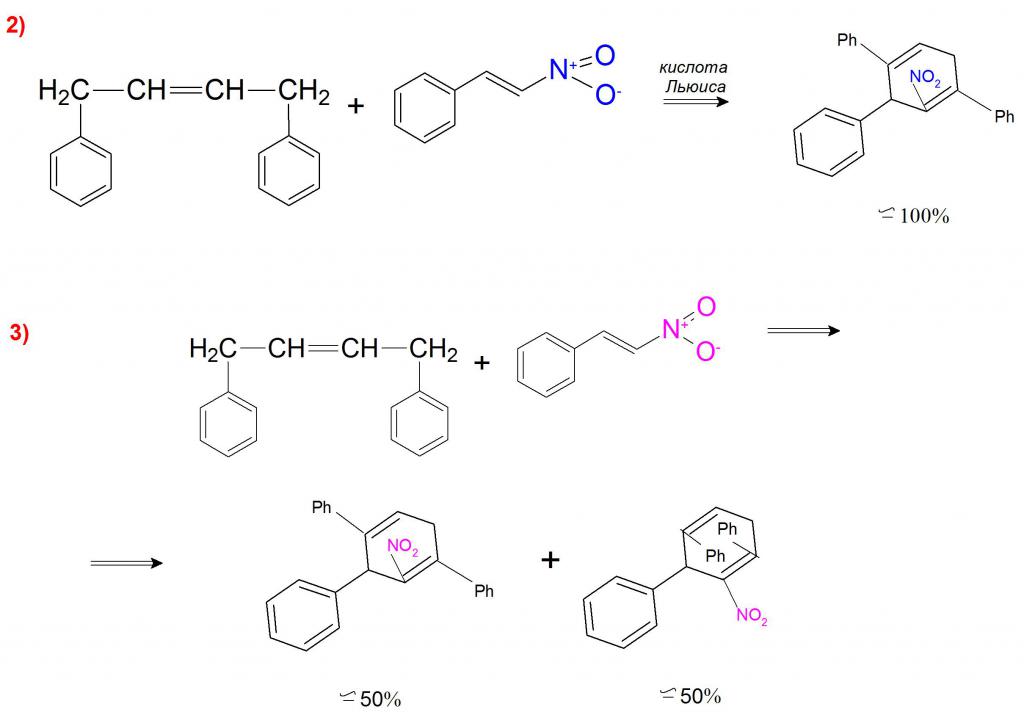
А примером каталитического синтеза может являться реакция 1,4–дифенилбутадиена с β-нитростиролом, где в присутствии кислоты Льюиса образуется только эндо-нитроаддукт (пример 2). Без участия катализатора эта реакция проходит с образованием эндо-нитросоединения и эндо-дифениловых продуктов в соотношении 1:1 (пример 3).
Такие реакции подтверждают целесообразность использования каталитически активных веществ в диеновом синтезе, так как они существенно ускоряют процесс и значительно влияют на регио- (орто-, пара- и мета-положения) и стереоселективность (оптические и эндо-/экзо-положения заместителей).
Источник