Рецепторный способ проникновения вирусов
После адсорбции вируса следует стадия проникновения его в клетку. Вирионы могут проникать в клетку одним из двух главных путей: опосредованным рецепторами эндоцитозом или слиянием.
Большинство клеток млекопитающих непрерывно осуществляют рецепторопосредованный эндоцитоз при поглощении макромолекул посредством специфических рецепторов. Многие оболочечные и безоболочечные вирусы используют эту ценную клеточную функцию для начала инфицирования. Вирионы прикрепляются к рецепторам, которые находятся в покрытых клатрином углублениях и вследствие эндоцитоза оказываются в покрытых клатрином вакуолях. Вакуоли проникают в цитоплазму и после удаления клатринового покрытия сливаются с эндосомами (кислые прелизосомальные вакуоли). Ацидофикация внутри везикул вызывает изменения в вирионных белках и поверхностных структурах. Изменения конфигурации капсидного белка VP4 пикорнавирусов, например, ведет к освобождению вирусной РНК из вириона в цитозоль. Подобным образом в кислой среде эндосом молекулы гемагглютинина (ГА) вируса гриппа претерпевают конформационные изменения, создавая возможность слияния между вирусной оболочкой и эндосомальной мембраной, ведущего к освобождению вирусного нуклеокапсида в цитоплазму. Многие другие оболочечные и безоболочечные вирусы претерпевают подобные изменения.
Вирусы с двойным капсидом (реовирусы) проникают в клетку путем фагоцитоза и в лизосомах превращаются в активные субвирусные частицы.
В основе проникновения в клетку оболочечных вирусов (пара- и ортомиксовирусы, ретровирусы и, возможно, рабдовирусы и герпесвирусы) лежит процесс сплавления (слияния) липопротеиновой оболочки вируса с плазматической мембраной клетки, в результате чего внутрь клетки проникает только нуклеопротеин вириона.
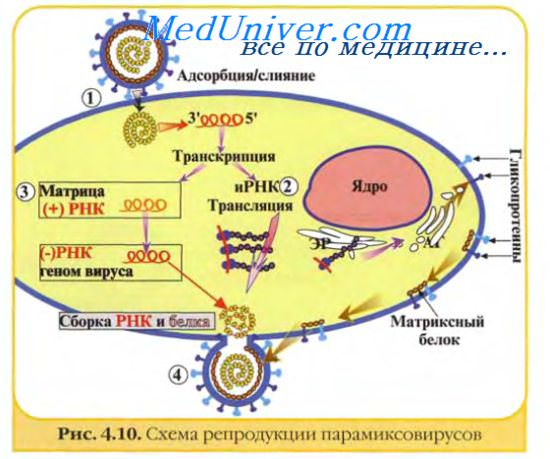
Гликопротеин F, расположенный на поверхности вирионов парамиксовирусов, принимает участие в проникновении вируса в клетку, причем активностью обладает только расщепленный полипептид. Расщепление гликопротеина НА ортомиксовирусов на большую и малую субъединицы необходимо для проникновения вирионов внутрь клетки.
Другие оболочечные вирусы также способны сливаться с цитоплазматической мембраной, благодаря собственной оболочке, обеспечивая вхождение нуклеиновой кислоты в клетку.
При данном способе проникновения функционально активный вирусный нуклеопротеин освобождается из вириона в период прохождения его внутрь клетки через мембрану, т.е. одновременно происходит проникновение и «раздевание» вириона. В составе вирусного нуклеопротеина некоторых вирусов внутрь клетки проникает и вирионная полимераза, которая обеспечивает синтез мРНК.
Раздевание вирионов (обнажение вирусного генома)
Для того чтобы вирусные гены стали доступными для транскрипции, необходимо, чтобы вирионы были хотя бы частично раздеты. В случаях с оболочечными вирусами РНК, у которых оболочка целиком сливается с цитоплазматической мембраной или эндоплазматической мембраной, нуклеокапсид освобождается прямо в цитоплазму и транскрипция вирусной нуклеиновой кислоты начинается, когда она все еще связана с этой структурой. У безоболочечных реовирусов после проникновения вирионов в клетку происходит разрушение наружного капсида клеточными ферментами. Однако сердцевина вириона не разрушается на протяжении всего инфекционного процесса, и двуспиральная геномная РНК консервируется внутри субвирусной частицы.
Для большинства других вирусов, однако, процедура раздевания завершается полным обнажением вирусного генома. Для некоторых вирусов, размножающихся в ядре, последняя стадия раздевания происходит быстрее, чем в цитоплазме.
— Вернуться в оглавление раздела «Микробиология.»
Источник
Механизмы вирусного заражения
Вирусы не относят к живым существам — это всего лишь кочевой генетический материал, несколько белков и иногда оболочка. Но это не мешает им проникать в клетки всех групп живых существ, вызывать серьезные заболевания и оставаться в организме своего хозяина годами.
О том, как устроены вирусы, как они проникают в клетку и всегда ли они опасны, в рамках гида «Полезные вирусы» ПостНауке рассказывает вирусолог Леонид Марголис.
Типы вирусов
Вирусы различаются по размеру, строению, структуре генома и наличию или отсутствию оболочки. Большинство изученных вирусов имеют диаметр от 20 до 300 нанометров. Например, размеры вириона коронавируса SARS-CoV-2 или вируса иммунодефицита человека составляют примерно 100–150 нанометров. Они относятся к песчинке так же, как песчинка относится к пятиэтажному дому. Но бывают вирусы еще меньше. Так, размер парвовируса (вызывает у человека в том числе инфекционную эритему) составляет порядка 22–24 нанометра. Существуют и значительно более крупные вирусы: мамавирус и вирус табачной мозаики сопоставимы по размерам с бактерией.
Вирусы разделяют на ДНК-содержащие и РНК-содержащие, их геном представлен ДНК и РНК соответственно. Большинство самых опасных вирусов, которые заражают человека, относятся к РНК-группе: ВИЧ, SARS-CoV-2, бешенство, грипп, гепатит C и другие.
Кроме того, некоторые исследователи выделяют вирусоподобные частицы (прионы), которые вовсе не содержат генома. В существование последних долго никто не верил, потому что это противоречит представлениям о строении подобных структур. В 1997 году за открытие прионов американский врач и профессор неврологии и биохимии Университета Калифорнии в Сан-Франциско Стенли Прузинер получил Нобелевскую премию. По сути прион — это белок с аномальной структурой, который превращает схожий с ним нормальный белок клетки в себе подобный. Прионы вызывают серьезные заболевания у человека, животных и даже некоторых грибов, но их вирусная природа не подтверждена.
Вирусы могут значительно различаться по строению и объему генетического материала. Например, у герпес-вирусов в тысячу раз больше закодированного материала, чем у более примитивного вируса иммунодефицита человека. Герпес-вирус несет с собой множество структурных белков, необходимых ему для репликации. В то же время вирус иммунодефицита состоит всего из нескольких генов и использует для воспроизведения белки инфицированной клетки.
Также вирусы можно поделить на безоболочечные и оболочечные, то есть покрытые только белковым капсидом или имеющие дополнительный билипидный (двойной) суперкапсид. И те и другие довольно успешно существуют, так как оба этих типа сохранились в ходе эволюции. При этом у каждого вируса есть свой уникальный механизм попадания в клетку и ее заражения.
Однако и такое деление может быть вскоре признано неверным, поскольку некоторые безоболочечные вирусы в определенных ситуациях могут обретать оболочку. Недавно обнаружилось, что вирус гепатита A, который ранее считали безоболочечным, может находиться в так называемых экстраклеточных везикулах — крошечных пузырьках, которые выделяет клетка. Считается, что эти структуры являются либо примитивными вирусами, которые утратили специфичность, либо эволюционно предшествуют современным вирусам. Сейчас подобные везикулы много изучают, потому что они играют важную роль в передаче генов и белков от одних клеток к другим.
Механизм проникновения вируса в клетку
Большинство вирусов видоспецифичны и могут поражать только определенные виды хозяев и конкретные клетки-мишени. Вирусные белки в капсиде вируса могут иметь сродство к белкам на поверхности клетки. Для проникновения в клетку белки слияния вируса используют соответствующие белки оболочки клетки — рецепторы. Если вирус не находит подобный рецептор, заражения не случится. Именно поэтому коронавирусы не заражают через кожу: у ее клеток нет необходимых рецепторов.
Рецепторами могут выступать любые белки клеточной оболочки. Конечно, они созданы не для того, чтобы вирус мог за них зацепиться, а для решения других задач. Например, белок ACE2, который отвечает за регулирование давления крови у человека, оказался рецептором для коронавируса SARS-CoV-2. А несколько других важных для иммунного ответа организма белков стали рецепторами для ВИЧ.
После того как вирус зацепился за рецептор на клеточной оболочке, ему нужно попасть внутрь клетки. Это может происходить по двум основным сценариям: через эндоцитоз или напрямую через клеточную мембрану.
Рассмотрим первый случай на примере вируса гриппа. Когда вирус попадает на клетку, она «чувствует», что что-то находится на ее оболочке, и поглощает это с помощью обычного эндоцитоза, то есть окружает частицу и «поедает», захватывая внутрь. Затем вирус попадает в лизосому — специальный пузырек с агрессивной кислотной средой, в котором происходит дефрагментация внешних частиц на будущий строительный материал для клетки.
Но вирус гриппа оказался хитрым. Он не разрушается в этих пузырьках благодаря белку, который умеет сливать его мембрану с мембраной лизосомы, и активируется именно в кислой среде. Получается, что мембраны вируса и лизосомы сливаются как два воздушных пузыря, после чего генетический материал вируса выбрасывается в клетку.
Во втором случае оболочка вируса сливается сразу с клеточной мембраной по тому же принципу, как это происходит с лизосомой, после чего его генетический материал и белки мигрируют непосредственно внутрь клетки. Так действует ВИЧ. Этот процесс очень отдаленно похож на слияние жировых пятен в супе. Обычно клеточные мембраны не сливаются, иначе жизнь на Земле была бы невозможна, поэтому вирус создал специальный механизм. Он очень близко подводит свою липидную мембрану к липидной мембране клетки и за счет специальных белков немного раздвигает липиды оболочки. Так вирусный геном попадает в клетку.
Когда генетический материал вируса оказывается в клетке, он ведет себя по-разному в зависимости от его структуры. Репликация генома у большинства ДНК-содержащих вирусов происходит в клеточном ядре. РНК-вирусы, как правило, реплицируются в цитоплазме. Но есть исключение — РНК-содержащие ретровирусы, способные к обратной транскрипции. Для репликации такие вирусы используют промежуточную стадию в виде ДНК-молекулы. На вирусной РНК строится одиночная цепочка ДНК, а затем дополняется комплементарной цепочкой и встраивается прямо в хромосомы хозяина, ничем не отличаясь от генов, которые мы унаследовали от родителей. После этого новые вирионы (вирусные частицы) появляются благодаря работе этого нового «гена».
Например, SARS-CoV-2 никак не взаимодействует с генетическим материалом клетки и находится только в цитоплазме, где происходит репликация его РНК и строятся необходимые вирусу белки. Там же происходит сборка новых вирионов, которые затем выходят из клетки. Вирус иммунодефицита человека тоже содержит РНК, но относится к ретровирусам, то есть его геном встраивается в клеточную хромосому.
«Спящие агенты» и латентный резервуар
Вирусы могут иметь разную степень патогенности (возможность вызывать инфекционный процесс), и это не всегда связано с их способностью взаимодействовать с геномом пораженной клетки. Герпес-вирусы не внедряются в клеточную ДНК, однако могут долго существовать в организме, и избавиться от них очень трудно, от некоторых и вовсе невозможно. И даже самые безобидные из герпес-вирусов время от времени могут начать снова реплицироваться в организме.
С другой стороны, РНК-вирус иммунодефицита человека встраивается в ДНК лимфоцитов, но опасен он не поэтому. Он может годами не реплицироваться, а находиться в состоянии «спящего агента» из детективных романов. Его засылают в другую страну, он тридцать лет ведет там нормальную жизнь, работает, женится, заводит детей. И активизируется только по специальному сигналу.
Существует множество лекарств, которые уничтожают этот вирус, не позволяют ему реплицироваться и передаваться из одной клетки в другую. Но у него всегда остается так называемый латентный резервуар, который мешает полностью его уничтожить: ВИЧ переходит в латентную форму, сохраняясь внутри лимфоцитов. Что же делать с вирусом, когда его невозможно обнаружить? На сегодняшний день наука не знает, как избавиться от вируса, который встроился в геном и никак себя не проявляет.
Вирус может долгое время оставаться в организме, даже когда симптомы заболевания уже не проявляются. Особенно актуальна эта проблема в связи с COVID-19. На текущий момент (июнь 2020 года) принято считать выздоровевшим и незаразным человека, который две недели не демонстрирует симптомов этого заболевания. Между тем, по последним данным, у некоторых пациентов тест на вирусную РНК оказывается положительным даже 45 дней спустя. Это не является стопроцентным маркером заболевания, потому что вирусная РНК сама по себе без капсида не может проникать в клетку и может являться просто остатками вируса, которые долго выходят из организма.
Как отмечает руководитель гематологического отделения Национального института здоровья США и специалист по парвовирусам Нил Янг, недавно обнаружилось, что парвовирусы могут десятилетиями оставаться в организме людей, которые однажды им переболели. Пока неизвестно, в каком виде он сохраняется в клетке. Аналогично происходит и с вирусом ветрянки, которой многие болели в детстве и которая относится к семейству герпес-вирусов. Это не очень опасная болезнь, но очень заразная. У многих переболевших вирус не исчезает бесследно и остается в нервных окончаниях, проявляясь спустя десятилетия в виде опоясывающего лишая.
Насколько вирусы заразны?
Заразность, инфекционность вируса, то есть способность передаваться другому организму, зависит от степени восприимчивости организма, от механизма передачи вируса, а также от того, насколько крепко он связывается со своим рецептором. SARS-CoV-2 отличает от других коронавирусов высокое сродство к рецептору — способность образовывать с ним сильную связь. Поэтому, по-видимому, так высока его инфекционность.
У ВИЧ инфекционность значительно ниже, но у него имеется удивительный механизм, который увеличивает шансы вируса поразить нужную клетку-мишень. Вирус иммунодефицита человека родственен специальным белковым нитям — амилоидным тельцам, которые находятся в сперме и, в свою очередь, привязываются к сперматозоидам. Так вирус не только получает доступ к клеткам-мишеням в организме хозяина, но и добывает себе транспорт в другой организм.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Источник
Рецепторный способ проникновения вирусов
В журнале Nature опубликован очень подробный обзор, характеризующих особенности строения и жизненный цикл SARS-CoV2, механизмы инфицирования и избегания своевременного иммунного ответа, обозначены потенциальные мишени для создания противовирусных препаратов. Также представлены результаты компьютерного моделирования строения вируса и механизмов проникновения в клетку.
Особенностью данного вируса является наличие очень большого количества гликанов на поверхности спайк-протеина, маскирующих его от иммунной системы человека. Поэтому на первом этапе заболевания вирус подобен «волку в овечьей шкуре» и остается невидим для иммунной системы. В дальнейшем, когда вирус уже размножился, иммунный ответ может развиться даже избыточно, что, по-видимому, лежит в основе тяжелого течения заболевания.
В S2- субъединице спайк-протеина есть три участка, делающих «ножку» спайк-протеина гибкой, что позволяет ей «искать» рецепторы на клетках хозяина более эффективно. Такая структура довольно редка для вирусов, обычно аналогичные «шипики» на поверхности вириона ригидны (такова, например, ситуация у вируса гриппа).
Важной частью спайк-протеина является RBD-домен, функцией которого является связь с рецептором ACE2 на поверхности клетки-хозяина. У SARS-CoV2 эта связь в 2-4 раза сильнее, чем у вируса SARS. Во время взаимодействия с рецептором этот домен «выдвигается» из-за двух маскирующих его молекул гликанов. Исследования in vitro показали, что мутации в этих двух гликанах могут полностью нарушать процессы проникновения вируса в клетку. Для эффективного взаимодействия RDB и ACE2 предпочтительна более «высокая» позиция этого домена на остальными структурами. У альфа варианта вируса найдено 10 дополнительных мутаций, приводящих RBD – домен в более «высокое» положение, а у дельта вируса – еще 3 мутации.
Для того, чтобы вирус проник в клетку, помимо связи с рецептором АСЕ2, необходимо еще одно взаимодействие с трансмембранной протеазой, которая частично расщепила бы фрагмент спайк-протеина с высвобождением гидрофобных аминокислот, которые стремились бы с скорейшему слиянию с рядом расположенной мембраной клетки-хозяина. SARS-CoV2 использует с этой целью две протеазы — TMPRSS2 (преимущественно) и катепсин. Преимущественное использование TMPRSS2 и прямое проникновение вируса в клетку минуя механизм образования эндосом с участием катепсина и является объяснением неэффективности гидроксихлорохина, который воздействует исключительно на катепсин-зависимый механизм проникновения вируса.
Попав в клетку, вирус подавляет экспрессию генов клетки-хозяина, в том числе – образование интерферонов, сигнализирующих о вирусной инфекции. Для ковидной инфекции типична очень низкая концентрация интерферонов в крови.
В дальнейшем может происходить формирование синцитиев из клеток легочной ткани. Считается, что синцитии позволяют дольше и эффективнее вырабатывать вирусные белки. Такой тип агрессии типичен для персистирующих вирусов – например, ВИЧ. SARS-CoV2 индуцирует даже формирование синцитиев клеток респираторного эпителия с лимфоцитами, что мешает нормальному иммунному ответу. Такой тип «маскировки» от иммунитета типичен для опухолей, а не вирусов.
В дальнейшем перестраивается эндоплазматический ретикулум с формированием шарообразных двухмембранных структур, в которых происходит активный синтез белков вируса. Выход вирионов наружу осуществляется в лизосомах, формирующихся в комлексе Гольджи, путем экзоцитоза. Считается, что молекулярные механизмы, ответственные за описанные процессы, могут быть мишенями для противовирусной терапии.
В месте соединения S1 и S2 субъединиц спайк-протеина есть зона, которая способна связывать и быть расщепленной фурином – протеазой клетки-хозяина, содержащейся в лизосомах. Такое предварительное расщепление значительно упрощает в дальнейшем взаимодействие с трансмембранной протеазой TMPRSS2 и значительно увеличивает проникновение вирусной частицы в следующую клетку. Для вируса SARS показано, что порядка 10% вирусных частиц на выходе из клетки – хозяина связано с фурином. У вируса SARS-CoV2 в соответствующем локусе, отвечающем за связь с фурином, идентифицированы мутации. Как следствие, до 50% вирионов альфа-разновидности SARS-CoV2, выходящих из клетки-хозяина, связаны с фурином, а в случае дельта-вируса – до 90%, что, по-видимому, и объясняет более агрессивное распространение этого варианта вируса. Есть данные, что у пациентов с дельта-формой в тканях легких и носоглотки содержание вирионов достоверно выше, чем у носителей альфа-формы.
По материалам: Megan Scudellari. How the coronavirus infects cells — and why Delta is so dangerous. Nature 595, 640-644 (2021). doi:
Источник