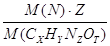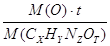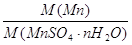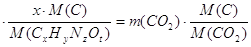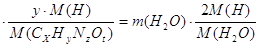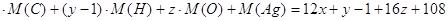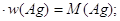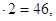Решение расчетных задач по химии алгебраическим способом.
консультация по химии по теме
Презентация полезна. как начинающим учителям химии, так и учащимся. В ней приводится примеры решения расчетных задач по химии несколькими математическими приемами. Здесь можно узнать (вспомнить) способы решения задач на смеси (способ введения двух неизвестных, одного неизвестного и «квадрат Пирса»), так же приведены примеры решения задач на нахождение молекудярных формул.
Скачать:
| Вложение | Размер |
|---|---|
| reshenie_raschetnykh_zadach_po_khimii.pptx | 668.38 КБ |
Предварительный просмотр:
Подписи к слайдам:
Решение расчетных задач по химии алгебраическим способом Автор: Крысь Н. С. Учитель химии МБОУ «СОШ №14 пос. Подъяпольский , Шкотовского района»
Задача № 1. В каком объемном соотношении необходимо смешать водород и углекислый газ , чтобы получить газовую смесь по плотности равную воздуху. Расчетные задачи на смеси
x – H 2 , y – CO 2 . n = ; M см = помня, что m см =m(H 2 )+m(CO 2 ), а n c м =n(H 2 )+n(CO 2 ), получим 29= => 27x=15y => 27 : 15 Ответ: для приготовления смеси нужно взять в молярном (объемном) отношении 27( CO 2 ) и 15(H 2 ) Способ № 1. Количество вещества. Введение двух неизвестных. ( x и y)
ПРИМЕМ КОЛИЧЕСТВО ВОДОРОДА ЗА 1 МОЛЬ , УГЛЕКИСЛОГО ГАЗА ЗА X МОЛЬ . M см = m см =m(H 2 )+m(CO 2 ), n c м =n(H 2 )+n(CO 2 ), 29= => 29+29х=2+44х=> 27=15х Ответ: 15 частей H 2 и 27 частей CO 2 Способ № 2. К оличество вещества (одно неизвестное)
H 2 2 15 воздух 29 С O 2 44 27 Ответ: CO 2 – 27 частей H 2 – 15 частей Способ №3. Квадрат Пирса (правили креста)
96% 30 :2=15массовых частей 40% 10% 56 :2=28 массовых частей на 15 массовых частей 96% серной кислоты нужно взять 28 частей 10% кислоты. Т.е. 15 x + 28 x =400 43 x =400, x =9,3. Масса 96% серной кислоты равна 15 x 9,3=139,5 г ; Масса 10% серной кислоты равна: 28 x 9,3=260,5г. Какие массы 96% и 10% серной кислоты необходимо взять для получения 400 г 40% серной кислоты?
Разновидности задач на нахождение молекулярной формулы вещества
При мононитровании 20,3 г . алкана выделилось 6,3 г . воды . Какой объем воздуха, измеренный при н.у ., потребуется для сгорания той же массы этого алкана ? Объемная доля кислорода в воздухе равна 21 % . Задача № 1
20 ,3 г 6,3 г C n H 2n+2 + HNO 3 = C n H 2n+1 NO 2 + H 2 O 1 моль 1 моль 14 n +2 г/моль 18 г/моль 1. Запишем уравнение реакции нитрования, используя общую формулу алканов .
n (H 2 O)= = = 0,35 моль 2. Найдем количество вещества выделившийся при нитровании воды.
n(C n H 2n+2 ) = n(H 2 O) = 0,35 моль 3. По уравнению реакции найдем количество вещества прореагировавшего алкана .
M(C n H 2n+2 ) = = = 58 г/моль 5. Вычислим число атомов углерода в алкане : 14 n + 2 = 58 n = 4 = C 4 H 10 4 . Найдем молекулярную массу прореагированного алкана .
0 ,35 моль x моль 2C 4 H 10 + 13O 2 = 8CO 2 + 10H 2 O 2 моль 13 моль n(O 2 ) = 2, 275 моль. 6 . Запишем уравнение реакции горения бутана.
V(O 2 ) = n(O 2 ) V M = 2,275( моль) 22,4 (л/моль) = 50,96 л. 7 . Вычисляем объем затраченного на горение кислорода.
V( воздуха ) = V (воздуха) = 100% = 242,7 л. 8. Найдем объем воздуха, содержащего необходимое количество кислорода.
Спасибо за внимание.
По теме: методические разработки, презентации и конспекты
Решение расчетных задач по химии с детьми с повышенной мотивацией к обучению.
Программа предназначена для учащихся 8-9 классов, имеющих базовую подготовку по теоретическим основам химии и желающих повысить уровень знаний в области неорганической химии и совершенствоваться в реш.
Статья «Решение расчетных задач по химии, как способ совершенствования химической компетентности»
Решение расчётных задач по химии — статья.
Рабочая программа элективного курса по химии, 10 класс «Решение расчетных задач по химии»
Представленный материал содержит рабочую программу элективного курса по химии, 10 класс «Решение расчетных задач по химии».
Рабочая программа по элективному курсу по химии в 11 классе » Решение расчетных задач по химии»
Рабочая программа элективного курса по химии расчитана для 11 класса и составляет 34 часа.
Элективный курс в 11 классе «Способы решения расчетных задач по химии»
Данный образовательный курс расширяет и углубляет компонент химического образования. Представленная программа включает новые знания для учащихся, не содержащиеся в базовых программах. Эти знания вызыв.
Рабочая программа элективного курса по химии «Способы решения расчетных задач по химии» в 10 классе
Программа рассчитана на 18 часов. Курс разделен на три блока: расчеты по химическим формулам, количественные характеристики растворов, вычисления по химическим уравнениям.
Источник
АЛГЕБРАИЧЕСКИЕ СПОСОБЫ РЕШЕНИЯ ХИМИЧЕСКИХ ЗАДАЧ
4. АЛГЕБРАИЧЕСКИЕ СПОСОБЫ РЕШЕНИЯ ХИМИЧЕСКИХ ЗАДАЧ
Алгебраические способы решения задач незаменимы, если задача сложна и ее нельзя решить одной — двумя пропорциями. Именно в этом случае удобно воспользоваться другими методами алгебры, чаще всего линейными уравнениями и неравенствами. Решение задач можно свести к двум этапам: составлению уравнения (системы уравнений) по условию задачи и решению полученного уравнения.
1) Вычисление состава соединений, смесей, выведение формул соединений.
При решении химических задач часто возникает потребность проводить вычисления для нахождения соотношений составных частей в различных объектах. В качестве последних можно рассматривать химические соединения, смеси веществ, сплавы. Задачи этого типа приходиться решать не только химикам, но и представителям самых разнообразных профессий – агрономам, врачам, металлургам, геологам и т. д.
В задачах обычно рассматриваются объекты, которые состоят из компонентов. Количественный состав объектов удобно выражать в долях, которые составляют компоненты по отношению к целому объекту. Употребляют массовую, объемную и молярную доли. Массовая доля w (X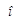
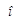
W ( 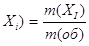
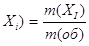
Массу компонента в объекте вычисляют, умножив массу объекта на массовую долю компонента в нем: m(x ) = m ( об ) ∙ w ( x )
Так, зная химический состав соединений, т. е. их формулы и молярные массы, можно вычислять массовые доли элементов в этих соединениях. И наоборот, зная массовые доли элементов в соединениях, можно находить молекулярную формулу соединения.
Ниже приведены примеры решения отдельных задач. Все они принадлежат к одному типу, поэтому алгоритмы их решения идентичны. В преобладающем большинстве случаев ход решения строится так: обозначаем буквами неизвестные величины и формулируем их физический смысл; словесно формулируем смысл уравнений и неравенств, которые затем записываем с помощью символов; подставляем числовые значения; решаем систему уравнений и неравенств и даем ответ.
Задача № 1 . Вывести формулу вещества с молярной массой 123 г/моль, если состав его , выраженный в массовых долях , следующий : углерод 58,5 %, водород 4,1 %, азот 11,4 %, кислород 26,0 %
Решение: Формулу соединения условно можно записать CxH y Nz Ot .
Искомые величины – числа атомов в молекуле ( индексы в данной формуле- x, y, z, t).
Массовые доли химических элементов в данном веществе можно выразить:
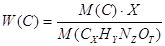
W (H) = 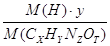
Составим уравнения, учитывая, что произведение молярной массы соединения на массовую долю данного элемента, входящего в его состав, равно молярной массе элемента, умноженной на его индекс в формуле соединения.
Решим каждое уравнение :
М ( CxHy NzOt) ∙ w ( C ) = x∙ M ( C ) 123∙0,585 = 12 х , х = 6
М ( Cx HyNzOt) ∙w ( H ) = y ∙ M ( H ) 123 ∙ 0. 041 = уу = 5
М ( CxHyNz Ot) ∙ w (N ) = z ∙ M ( N ) 123 ∙ 0, 114 = 14 z z = 1
M ( Cx Hy Nz Ot ) ∙ w ( O ) = t∙ M (O) 123∙ 0,26 = 16t, t=2
Ответ: формула соединения 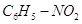
Задача № 2 . В кристаллогидрате сульфата марганца (II) массовая доля марганца равна
0, 268. Определить количество вещества воды, приходящееся на 1 моль кристаллогидрата. Написать формулу соли.
Решение: Рассматриваемым объектом является 1 моль кристаллогидрата сульфата марганца (II). Его формулу условно запишем 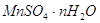
Составим уравнение, учитывая, что массовая доля марганца в кристаллогидрате равна отношению молярных масс марганца и данного кристаллогидрата:
W (Mn) =
Подставляя в уравнение вместо символов их числовые значения, получим: 0,268 = 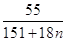
Ответ: 1 моль кристаллогидрата сульфата марганца ( II ) содержит 3 моль воды. Формула соли — 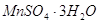
Задача № 3 . При полном сгорании 3,1 г органического вещества (М= 93 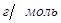
Решение: В общем виде соединение можно представить формулой 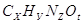
Составим уравнения, учитывая следующее:
1) масса углерода в сгоревшем веществе и в образовавшемся оксиде углерода
m ( CxHy NzOt )
или 3,1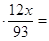
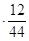
1) массы водорода в сгоревшем веществе и в образовавшейся воде равны:
m (CxHyNzOt)
или 3,1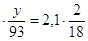
2) масса азота в 3,1 г соединения равна 0,47 г:
m (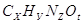
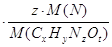
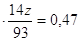
3) молярная масса соединения равна сумме молярных масс каждого элемента, умноженных на соответствующие индексы в формуле:
М (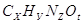
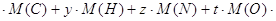
93=6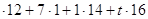
Ответ: формула соединения 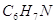
Задача № 4 . Массовая доля серебра в соли предельной одноосновной органической кислоты составляет 70,59 %. Написать молекулярную формулу этой кислоты, если известно , что она состоит из углерода , водорода и кислорода .
Решение: Запишем химические формулы кислот и её соли в условном виде: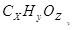
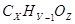
Выражая молярную массу соли серебра через молярные массы составляющих её атомов, получим:
М (Аg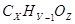
х
Составим уравнение, учитывая, что произведение молярной массы соли на массовую долю в ней серебра равно молярной массе серебра:
М (Аg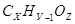
(107+12х+у+16z)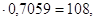
По условию задачи одноосновная предельная органическая кислота имеет общую формулу 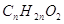
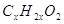
Искомые числа х и у одновременно удовлетворяют двум уравнениям:
12х +у +16
Решая систему уравнений, получим х = 1, у = 2. Следовательно, формула кислоты — 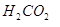
Ответ: Формула кислоты — НСООН.
Задача № 5 . После полного термического разложения 2,0 г смеси карбонатов кальция и стронция получили 1,23 г смеси оксидов этих металлов. Оксид углерода (IV) улетучился. Вычислить массу карбоната стронция в исходной смеси.
Решение: Запишем уравнение реакции:
SrC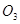
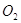
Источник