- Энтропия. Энергия Гиббса
- Понятие энтропии
- Абсолютная энтропия веществ и изменение энтропии в процессах
- Стандартная энтропия
- Стандартная энтропия образования
- Энергия Гиббса
- Стандартная энергия Гиббса образования
- Энтальпийный, энтропийный фактор и направление процесса
- Примеры решения задач
- Задачи для самостоятельного решения
- Энергию Гиббса химической реакции можно рассчитать двумя способами
Энтропия. Энергия Гиббса
Понятие энтропии
Абсолютная энтропия веществ и изменение энтропии в процессах
Стандартная энтропия
Стандартная энтропия образования
Энергия Гиббса
Стандартная энергия Гиббса образования
Энтальпийный, энтропийный фактор и направление процесса
Примеры решения задач
Задачи для самостоятельного решения
Понятие энтропии
Энтропия S – функция состояния системы. Энтропия характеризует меру неупорядоченности (хаотичности) состояния системы. Единицами измерения энтропии являются Дж/(моль·К).
Абсолютная энтропия веществ и изменение энтропии в процессах
При абсолютном нуле температур (Т = 0 К) энтропия идеального кристалла любого чистого простого вещества или соединения равна нулю. Равенство нулю S при 0 К позволяет вычислить абсолютные величины энтропий веществ на основе экспериментальных данных о температурной зависимости теплоемкости.
Изменение энтропии в процессе выражается уравнением:
где S(прод.) и S(исх.) – соответственно абсолютные энтропии продуктов реакции и исходных веществ.
На качественном уровне знак S реакции можно оценить по изменению объема системы ΔV в результате процесса. Знак ΔV определяется по изменению количества вещества газообразных реагентов Δnг. Так, для реакции
(Δnг = 1) ΔV > 0, значит, ΔS > 0.
Стандартная энтропия
Величины энтропии принято относить к стандартному состоянию. Чаще всего значения S рассматриваются при Р = 101,325 кПа (1 атм) и температуре Т = 298,15 К (25 о С). Энтропия в этом случае обозначается S о 298 и называется стандартной энтропией при Т = 298,15 К. Следует подчеркнуть, что энтропия вещества S (S о ) увеличивается при повышении температуры.
Стандартная энтропия образования
Стандартная энтропия образования ΔS о f,298 (или ΔS о обр,298) – это изменение энтропии в процессе образования данного вещества (обычно 1 моль), находящегося в стандартном состоянии, из простых веществ, также находящихся в стандартном состоянии.
Энергия Гиббса
Энергия Гиббса G – функция состояния системы. Энергия Гиббса равна:
Абсолютное значение энергии Гиббса определить невозможно, однако можно вычислить изменение δG в результате протекания процесса.
Критерий самопроизвольного протекания процесса: в системах, находящихся при Р, Т = const, самопроизвольно могут протекать только процессы, сопровождающиеся уменьшением энергии Гиббса (ΔG
Стандартная энергия Гиббса образования
Стандартная энергия Гиббса образования δG о f,298 (или δG о обр,298) – это изменение энергии Гиббса в процессе образования данного вещества (обычно 1 моль), находящегося в стандартном состоянии, из простых веществ, также находящихся в стандартном состоянии, причем простые вещества пристутствуют в наиболее термодинамически устойчивых состояниях при данной температуре.
Для простых веществ, находящихся в термодинамически наиболее устойчивой форме, δG о f,298 = 0.
Энтальпийный, энтропийный фактор и направление процесса
Проанализируем уравнение ΔG о Т = ΔН о Т — ΔТS о Т. При низких температурах ТΔS о Т мало. Поэтому знак ΔG о Т определяется в основном значением ΔН о Т (энтальпийный фактор). При высоких температурах ТΔS о Т – большая величина, знак Δ G о Т определяется и энтропийным фактором. В зависимости от соотношения энтальпийного (ΔН о Т) и энтропийного (ТΔS о Т) факторов существует четыре варианта процессов.
-
-
- Если ΔН о Т о Т > 0, то ΔG о Т
- Если ΔН о Т > 0, ΔS о Т о Т > 0 всегда (процесс не протекает ни при какой температуре).
- Если ΔН о Т о Т о Т о /ΔS о (процесс идет при низкой температуре за счет энтальпийного фактора).
- Если ΔН о Т > 0, ΔS о Т > 0, то ΔG о Т ΔН о / ΔS о (процесс идет при высокой температуре за счет энтропийного фактора).
-
Примеры решения задач
Задача 1. Используя термодинамические справочные данные, вычислить при 298,15 К изменение энтропии в реакции:
Объяснить знак и величину ΔS о .
Решение. Значения стандартных энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | NH3(г) | O2(г) | NО(г) | H2O(ж) |
| S о 298, Дж/(моль·К) | 192,66 | 205,04 | 210,64 | 69,95 |
В данной реакции ΔV o х.р.,298
Задача 2. Используя справочные термодинамические данные, рассчитать стандартную энтропию образования NH4NO3(к). Отличается ли стандартная энтропия образования NH4NO3(к) от стандартной энтропии этого соединения?
Решение. Стандартной энтропии образования NH4NO3 отвечает изменение энтропии в процессе:
Значения стандартных энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | N2(г) | H2(г) | O2(г) | NH4NO3(к) |
| S о 298, Дж/(моль·К) | 191,50 | 130,52 | 205,04 | 151,04 |
Стандартная энтропия образования NH4NO3(к), равная — 609,06 Дж/(моль·К), отличается от стандартной энтропии нитрата аммония S о 298(NH4NO3(к)) = +151,04 Дж/(моль·К) и по величине, и по знаку. Следует помнить, что стандартные энтропии веществ S о 298 всегда больше нуля, в то время как величины ΔS 0 f,298, как правило, знакопеременны.
Задача 3. Изменение энергии Гиббса реакции:
равно δG о 298= –474,46 кДж. Не проводя термодинамические расчеты, определить, за счет какого фактора (энтальпийного или энтропийного) протекает эта реакция при 298 К и как будет влиять повышение температуры на протекание этой реакции.
Решение. Поскольку протекание рассматриваемой реакции сопровождается существенным уменьшением объема (из 67,2 л (н.у.) исходных веществ образуется 36 мл жидкой воды), изменение энтропии реакции ΔS о о 298 реакции меньше нуля, то она может протекать при температуре 298 К только за счет энтальпийного фактора. Повышение температуры уменьшает равновесный выход воды, поскольку ТΔS о
Задача 4. Используя справочные термодинамические данные, определить может ли при 298,15 К самопроизвольно протекать реакция:
Если реакция не будет самопроизвольно протекать при 298,15 К, оценить возможность ее протекания при более высоких температурах.
Решение. Значения стандартных энергий Гиббса и энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | С4Н10(г) | С2Н4(г) | Н2(г) |
| ΔG о f,298× , кДж/моль | — 17,19 | 68,14 | 0 |
| S о 298, Дж/(моль·К) | 310,12 | 219,45 | 130,52 |
ΔG о х.р.,298 > 0, следовательно, при Т = 298,15 К реакция самопроизвольно протекать не будет.
Поскольку ΔS о х.р.,298 > 0, то при температуре Т>ΔН о /ΔS о величина ΔG о х.р.,298 станет величиной отрицательной и процесс сможет протекать самопроизвольно.
Задача 5. Пользуясь справочными данными по ΔG о f,298 и S о 298, определите ΔH о 298 реакции:
Решение. Значения стандартных энергий Гиббса и энтропий исходных веществ и продуктов реакции приведены ниже:
| Вещество | N2O(г) | H2(г) | N2H4(г) | H2O(ж) |
| ΔG о f,298, кДж/моль | 104,12 | 0 | 159,10 | -237,23 |
| S о 298, Дж/(моль·К) | 219,83 | 130,52 | 238,50 | 69,95 |
ΔG о 298 = ΔН о 298 – ТΔS о 298. Подставляя в это уравнение величины ΔН о 298 и ТΔS о 298, получаем:
ΔН о 298 = –182,25× 10 3 + 298·(–302,94) = –272526,12 Дж = – 272,53 кДж.
Следует подчеркнуть, что поскольку ΔS о 298 выражена в Дж/(моль× К), то при проведении расчетов ΔG 0 298 необходимо также выразить в Дж или величину ΔS 0 298 представить в кДж/(мольK).
Задачи для самостоятельного решения
1. Используя справочные данные, определите стандартную энтропию образования ΔS о f,298 NaHCO3(к).
2. Выберите процесс, изменение энергии Гиббса которого соответствует стандартной энергии Гиббса образования NO2(г):
Источник
Энергию Гиббса химической реакции можно рассчитать двумя способами
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
Система – совокупность тел, мысленно или фактически обособляемых из окружающей среды
Состояние системы характеризуется набором термодинамических параметров состояния: Т, р ,V, С …
Процесс перехода из одного состояния в другое (Т = const– изотермический, p = const— изобарический, V = const— изохорический )
ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СОСТОЯНИЯ СИСТЕМЫ:
U-внутренняя энергия, H – энтальпия , S — энтропия, G – свободная энергия Гиббса,
F – энергия Гельмгольца
Функции состояния системы (характеристические ф-ции) свойства системы, значения которых однозначно определяются параметрами состояния. Изменение функций состояния не зависит от пути перехода системы из одного состояния в другое, а определяется лишь разностью значений функции в конечном и начальном состоянии. Величина функции зависит от количества или массы вещества.
U-внутренняя энергия— включает в себя все виды энергии системы (движения и взаимодействия молекул, атомов, ядер, электронов и др. частиц), кроме потенциальной и кинетической энергии движения всей системы как целого объекта. Абсолютное значение U определить невозможно, можно определить изменение ΔU= U2 – U1 с помощью работы (W) и теплоты (Q).
Работа (W) – количественная мера направленного движения частиц
Теплота (Q) – количественная мера хаотического движения частиц
Н=U+p·V — энтальпия, функция состояния системы, абсолютное значение определить невозможно, можно определить ΔH
Термохимия– часть термодинамики, изучающая тепловые эффекты процессов
Термохимические уравнения (указаны агрегатные состояния веществ и тепловой эффект
реакции, допустимы дробные стехиометрические коэффициенты)
Эндотермическая реакция-реакция с поглощением теплоты,ΔrH > 0 .
Экзотермическая реакция-реакция с выделением теплоты,ΔrH 5 Па
∆fH º i – стандартная энтальпия (теплота) образования
i –го вещества равна тепловому эффекту образования одного моля этого вещества из соответствующих простых веществ, если все участники реакции находятся в стандартных состояниях При этом энтальпии образования простых веществ, устойчивых в данных условиях, принимают равными нулю.
Тогда стандартная энтальпия реакции равна:
Стандартные энтальпии образования табулированы, как правило, при 298 К (Δf Hº298)
Зависимость энтальпии реакции (в данном случае стандартной) от температуры в области 298 ÷Т, в которой нет фазовых переходов, в интегральномвиде выражается уравнением Кирхгофа:
Δr HºT= Δr Hº298+ 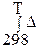
Где ∆rcºp – изменение стандартной теплоемкости системы в ходе реакции, равное разности суммарной стандартной теплоемкости продуктов реакции и суммарной стандартной теплоемкости исходных веществ с учетом стехиометрических коэффициентов
Энтропия S –функция состояния системы мера неупорядоченности состояния системы
S=R·lnW (W-термодинамическая вероятность системы, число возможных микросостояний, которыми можно реализовать данное макросотояние) [дж/моль·К]. Можно определить абсолютное значение (3-ий закон термодинамики- энтропия идеального кристалла при Т= 0 К равна 0). Энтропия увеличивается с ↑Т ; Sг>Sж>Sт
Стандартную энтропию реакции при 298К, ∆rSº298 рассчитывают по формуле
Зависимость энтропии реакции от температуры в области 298 ÷Т, в которой нет фазовых переходов, в интегральном виде выражается уравнением:
∆rSºТ = ∆rSº298+ 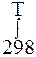
Функциями состояния системы: энергия Гиббса: G=Н-T·S, и энергия Гельмгольца: F=U-T∙S
Критерий возможности самопроизвольного протекания реакции в прямом направлении в изобарно-изотермических условиях:∆rGТ=∆rНТ — Т∙∆rSТ º
Энергию Гиббса химической реакции можно рассчитать двумя способами
Если исходные вещества и продукты реакции находятся в стандартных состояниях, то по этим формулам рассчитывают стандартную энергию Гиббса реакции ∆rGºT. Связь между ∆rGT (при нестандартных состояниях веществ) и∆rGºT (при стандартных)
выражается уравнением изотермы Вант-Гоффа
где pi – относительное парциальное давлениесоответствующих газообразных компонентов реакции
Источник




