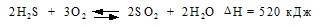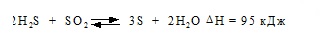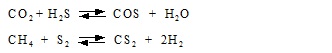- Производство серы из сероводородсодержащих и нефтезаводских газов методом Клауса
- Установка производства серы – процесс Клауса
- Назначение
- Применение серы
- Химизм процесса
- Основные реакции
- Побочные реакции
- Технологическая схема
- Термическая стадия
- Сепарация
- Реакционная печь
- Котел-утилизатор
- Конденсация серы
- Каталитическая стадия
- Нагрев газа
- Первый каталитический реактор
- Второй и третий каталитические реакторы
- Очистка хвостовых газов
- Дегазация серы
- Грануляция серы
- Материальный баланс
- Достоинства и недостатки
- Достоинства
- Недостатки
- Существующие установки
- Процесс Клауса — Claus process
- СОДЕРЖАНИЕ
- История
- Описание процесса
- Тепловой шаг
- Побочные реакции
- Каталитическая стадия
- Процесс Клауса ниже точки росы
- Производительность процесса
Производство серы из сероводородсодержащих и нефтезаводских газов методом Клауса
Различают 4 основных технологии Клауса
Смесь кислых газов в природном газе по объему состоит из сероводорода более чем на 50%.
Основной объем остальной части составляет углекислый газ, и есть небольшое количество серооксида углерода и углеводородов (метан, этан).
Эту смесь кислых газов обычно выделяют на промысле, в процессе очистки и подготовки газа для транспортировки.
Сера является побочным продуктом этого процесса.
Сначала из смеси кислых газов выделяется сероводород.
Затем его перерабатывают осноdнsм на сегодняшний день методом Клауса в элементную серу.
Английский химик К. Клаус, запатентовал в 1883 г основанный на окислении способ получения серы из сероводорода.
Различают 4 основных технологии Клауса:
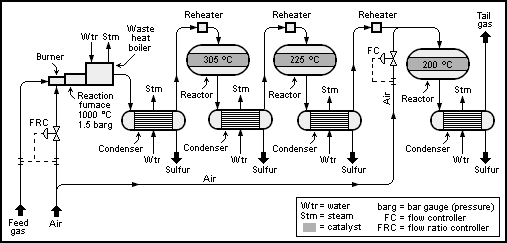
Прямоточный процесс Клауса (пламенный способ) применяют при объемных долях сероводорода в кислых газах выше 50% и углеводородов менее 2%.
При этом весь кислый газ подается на сжигание в печь-реактор термической ступени установки Клауса, выполненный в одном корпусе с котлом-утилизатором.
В топке печи-реактора температура достигает 1100-1300°С и выход серы до 70%.
Дальнейшее превращение сероводорода в серу осуществляется в 2-3 ступени на катализаторах при температуре 220-260°С.
После каждой ступени пары образовавшейся серы конденсируются в поверхностных конденсаторах.
Тепло, выделяющееся при горении сероводорода и конденсации паров серы, используется для получения пара высокого и низкого давления.
Выход серы — 96-97%.
Разветвленный процесс (1/3 — 2/3) применяют при низкой объемной доле сероводорода в кислых газах (30-50%) и углеводородов менее 2% .
1/3 кислого газа подвергается сжиганию с получением сернистого ангидрида, а 2/3 — поступают на каталитическую ступень, миную печь-реактор.
Серу получают, подавая серный ангидрид в каталитические ступени для взаимодействия с находящимся в 2/3 кислого газа сероводородом.
Выход серы — 94-95%.
Разветвленный процесс с предварительным подогревом кислого газа и воздуха применяют при объемной доле сероводорода в кислом газе 15-30%, когда при использовании обычной разветвленной схемы не достигается минимально допустимая температура 930°С в топке печи-реактора.
Дело в том, что при содержании сероводорода менее 45% стабильность горения кислого газа снижается, и подогрев газа и воздуха стабилизирует горение.
Выход серы — 94-95%.
Процесс прямого окисления применяют при объемной доле сероводорода в кислом газе 10-15%.
При этом, высокотемпературная стадия окисления (сжигания) газа не применяется.
Кислый газ, смешивается с расчетным количеством воздуха, вернее, говоря простым химическим языком, стехиометрическим количеством, и подается сразу на каталитическую ступень конверсии.
Содержание углеводородов в кислом газе обычно составляет до 5%.
Чем больше содержание углеводородов, тем больше расход воздуха для горения, объем газов после горения и необходимые для процесса размеры оборудования.
Качество серы снижает углеводород, образующийся при горении углеводородов образуется углерод.
За счет реакций с сероводородом углерод образует CS2 и COS, которые уменьшают выход серы.
Для повышения степени извлечения серы до 99,0-99,7% используют 3 процесса доочистки отходящих газов метода Клауса:
— продолжение реакции Клауса, для превращения H2S и SO2 в серу на твердом или жидком катализаторе,
— восстановление всех сернистых соединений в сероводород с последующим его извлечением,
— окисление всех сернистых соединений до SO2 или до элементарной серы с последующим их извлечением.
Степень конверсии сероводорода в процессе Клауса является очень важным параметром, поскольку определяет выход серы и содержание вредных примесей в хвостовом газе.
Наиболее высокая конверсия сероводорода в процессе Клауса до 99,8% (содержание серы в газе на выходе — 0,05-0,15 г/м 3 , основная часть — в твердом виде) достигается при 110-120 о С.
Источник
Установка производства серы – процесс Клауса
Назначение
Установки производства серы преобразуют H2S, содержащийся в потоках кислых газов из установок регенерации аминов и установок нейтрализации сернисто-щелочных стоков, в жидкую серу. Обычно двух или трехступенчатый процесс Клауса восстанавливает более 92% H2S в виде элементарной серы.
Большинство нефтеперерабатывающих заводов требуют извлечения серы более чем на 98,5%, поэтому третья ступень Клауса работает ниже точки росы серы. Третья ступень может содержать катализатор селективного окисления, иначе в состав установки производства серы необходимо предусматривать установку дожигания хвостовых газов. Становится все более популярным дегазировать полученную расплавленную серу. Крупные компании предлагают запатентованные процессы, которые дегазируют расплавленную серу до 10-20 мас. ppm H2S.
Применение серы
- производство крупных резинотехнических изделий (покрышек и т.п.):
- производство модифицированных асфальтовых покрытий и бетонов с особыми характеристиками
- в качестве фумигатора: горящая сера выделяет сернистый газ, которым окуривают оборудование и собранный для переработки виноград.
- использование тонкоизмельчённой серы в качестве универсального инсектицида и акарицида.
- производство спичечных головок, чёрного пороха и различных пиротехнических составов.
Химизм процесса
Основные реакции
Процесс состоит из многостадийного каталитического окисления сероводорода по следующей общей реакции:
Процесс Клауса включает сжигание одной трети H2S с воздухом в реакторной печи с образованием диоксида серы (SO2) в соответствии со следующей реакцией:
2H2S+3O2 → 2SO2+2H2O
Оставшиеся несгоревшие две трети сероводорода подвергаются реакции Клауса (реакция с SO2) с образованием элементарной серы следующим образом:
2H2S + SO2 ←→ 3S + 2H2O
Побочные реакции
Образование газообразного водорода:
Технологическая схема
Технологию Клауса можно разделить на две стадии процесса:
- термическая
- каталитическая
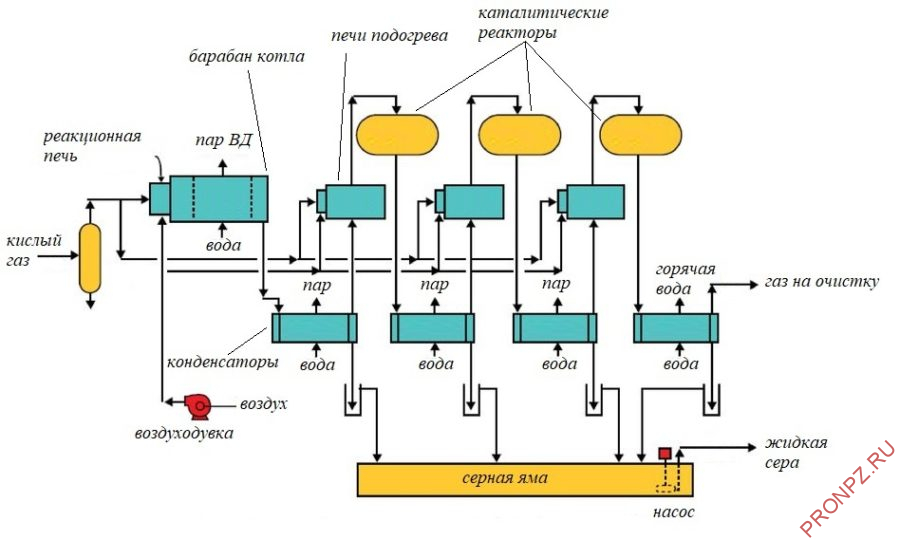
Термическая стадия
Сепарация
Кислый газ поступает в сепаратор для отделения увлеченных примесей, таких, как вода и монотаноламин с установок аминовой очистки, после чего поступает в реакционную печь.
Реакционная печь
Процесс термического окисления протекает в основной реакционной печи, смонтированной в одном агрегате с котлом-утилизатором.
Реакционная печь является важнейшим элементом оборудования в процессе Клауса. Минимальная температура для эффективной работы реакционной печи на “чистом” кислом газе должна контролироваться на уровне выше 925°C.
Котел-утилизатор
Продукты сгорания охлаждаются в котле-утилизаторе и конденсаторе серы. Пар поднимается на паровой барабан, связанный с котлом-утилизатором. Как правило, от 60 и более процентов серы извлекается в термической секции установки Клауса.
Конденсация серы
Основная часть горячего газа из камеры сгорания проходит через трубу охладителя технологического газа и охлаждается таким образом, что образующаяся на стадии реакции сера конденсируется. Тепло, выделяемое технологическим газом, и выделяющееся тепло конденсации используются для получения пара среднего или низкого давления. Полученная жидкая сера удаляется в секции конденсатора и самотеком поступает в резервуар для хранения серы. Здесь она поддерживается в расплавленном состоянии при температуре около 140 °C паровыми змеевиками. Сера, накопленная в этом резервуаре, перекачивается на грузовые или железнодорожные вагоны для отправки.
Каталитическая стадия
Каталитическое восстановление серы состоит из трех технологических операций:
- нагрев,
- каталитическая реакция
- охлаждение и конденсация.
Эти три шага обычно повторяются максимум три раза. Там, где после установки Клауса добавляется установка сжигания или очистки хвостового газа (ТГТУ), обычно устанавливаются только две каталитические ступени.
Нагрев газа
Первая технологическая стадия в каталитической стадии – это процесс нагрева газа. Необходимо предотвратить конденсацию серы в слое катализатора, что может привести к загрязнению катализатора. Требуемая рабочая температура слоя в отдельных каталитических стадиях достигается нагреванием технологического газа в печах подогрева до достижения желаемой рабочей температуры слоя.
Первый каталитический реактор
Каталитические реакторы работают при более низких температурах – от 200 до 315°C. В качестве катализатора иногда используют глинозем или бокситы. Каждая каталитическая ступень может восстановить от половины до двух третей поступающей серы. Количество каталитических стадий зависит от желаемого уровня конверсии. По оценкам, общее восстановление серы может составить от 95 до 97 процентов.
Каталитическая конверсия максимизируется при более низких температурах, но необходимо позаботиться о том, чтобы каждый слой работал выше точки росы серы.

Второй и третий каталитические реакторы
Рабочие температуры последующих каталитических ступеней обычно составляют 240 °C для второй ступени и 200 °C для третьей ступени (температура нижнего слоя).
Очистка хвостовых газов
Хвостовой газ из процесса Клауса, все еще содержащий горючие компоненты и соединения серы (H2S, H2 и CO), либо сжигается в установке для сжигания, либо подвергается дальнейшей очистке в последующей установке для очистки хвостового газа.
Дегазация серы
Получаемая на установках Клауса сера содержит растворенный сероводород (до 200–300 ppm по массе) в виде свободного сероводорода и химически связанного полисульфида водорода. При перемешивании и понижении температуры полисульфиды, содержащиеся в жидкой сере, разлагаются с выделением сероводорода.
В настоящее время в производстве газовой серы все более широко используется процесс дегазации жидкой серы путем ее продувки воздухом.
Грануляция серы
Основным условием потребителей элементарной серы является поставка ее в виде прочных малопористых гранул. Удобство обращения с гранулированной серой связано с тем, что она не слеживается, сохраняет сыпучесть и не образует пыли при хранении и перевозках, легко транспортируется и дозируется.
Сущность известных способов получения гранулированной серы сводится к истечению расплава серы через отверстие в виде отдельных капель, которые в процессе свободного падения охлаждаются воздухом, сырым водяным паром или струями воды.
Материальный баланс
| Сырье | % масс. | кг/ч |
| Сероводород | 100,0 | 291,92 |
| Всего: | 100,0 | 291,92 |
| Продукты | ||
| Сера элементарная | 97,0 | 283,18 |
| Потери | 3,0 | 8,73 |
| Всего: | 100,0 | 291,92 |
Достоинства и недостатки
Достоинства
- Простота технологического оформления установки.
- Удаление H2S из газов сжигания, что позволяет соблюдать экологические стандарты предприятия.

Недостатки
- Непреднамеренная конденсация и накопление серы может привести к таким проблемам, как затруднение прохода потока технологического газа, закупорка твердой серой, пожар и повреждение оборудования.
- Превышение предложения серы на рынке над ее спросом.
- Коррозия и загрязнение оборудования вследствие присутствия аммиака, H2S, CO2 возможного образования серной кислоты.
Существующие установки
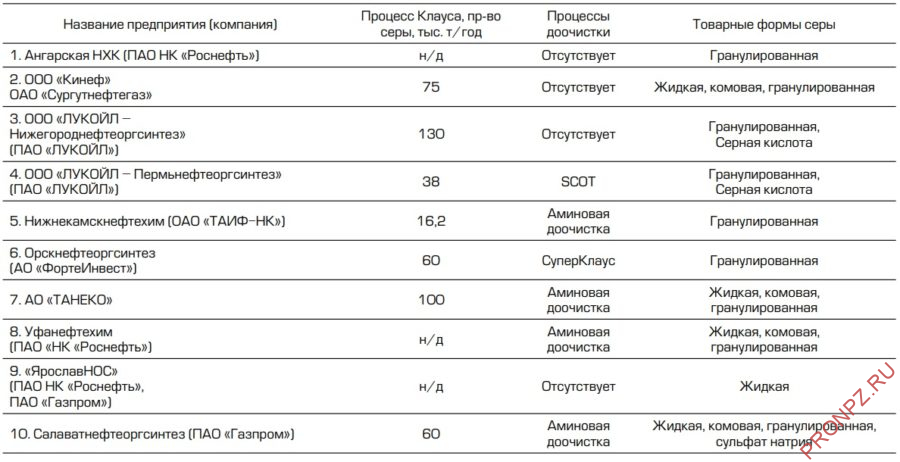
В настоящее время основными производителями серы являются газоперерабатывающие заводы (ГПЗ), нефтеперерабатывающие заводы (НПЗ) и нефтегазохимические комплексы (НГХК). Сера на этих предприятиях производится из кислых газов, образующихся при аминовой очистке высокосернистого углеводородного сырья. Подавляющее количество газовой серы выпускается по известному методу Клауса.
Из данных, представленных в табл.1–3, видно, какие виды товарной серы выпускают сегодня российские предприятия, производящие серу.
Таблица 1 – Нефтеперерабатывающие заводы России, производящие серу
Таблица 2 – Нефтегазохимические комплексы России, производящие серу
Таблица 3 – Газоперерабатывающие заводы России, производящие серу
Источник
Процесс Клауса — Claus process
Процесс Клауса — наиболее важный процесс обессеривания газа , извлекающий элементарную серу из газообразного сероводорода . Впервые запатентованный в 1883 году химиком Карлом Фридрихом Клаусом , процесс Клауса стал отраслевым стандартом.
Многоступенчатый процесс Клауса извлекает серу из газообразного сероводорода, содержащегося в неочищенном природном газе, и из побочных продуктов, содержащих сероводород, получаемых при переработке сырой нефти и других промышленных процессах. Побочные газы в основном поступают из установок физической и химической очистки газа ( Selexol , Rectisol , Purisol и аминовые скрубберы ) на нефтеперерабатывающих заводах , заводах по переработке природного газа и установках газификации или синтез-газа . Эти побочные газы могут также содержать цианистый водород , углеводороды , диоксид серы или аммиак .
Газы с содержанием H 2 S более 25% подходят для извлечения серы в прямоточных установках Клауса, в то время как альтернативные конфигурации, такие как установка с разделенным потоком или предварительный подогрев сырья и воздуха, могут использоваться для обработки более бедного сырья.
Сероводород получают, например, в гидро-обессеривания нефтеперерабатывающих нафты и других нефтяных масел, превращают в серу в Клауса растений. Реакция проходит в два этапа:
Подавляющее большинство из 64 000 000 тонн серы, произведенной во всем мире в 2005 году, составляла сера из побочных продуктов нефтеперерабатывающих и других заводов по переработке углеводородов. Сера используется для производства серной кислоты , лекарств, косметики, удобрений и резинотехнических изделий. Элементарная сера используется как удобрение и пестицид.
СОДЕРЖАНИЕ
История
Этот процесс был изобретен Карлом Фридрихом Клаусом , немецким химиком, работающим в Англии. В 1883 году ему был выдан британский патент. Позже IG Farben значительно изменил этот процесс .
Клаус родился в Касселе в немецкой земле Гессен в 1827 году, изучал химию в Марбурге, прежде чем эмигрировать в Англию в 1852 году. Он умер в Лондоне в 1900 году.
Описание процесса
Принципиальная технологическая схема базовой установки SuperClaus с 2 + 1 реакторами (преобразователем) показана ниже:
Технологию Клауса можно разделить на два этапа: термический и каталитический .
Тепловой шаг
На термической стадии газ, содержащий сероводород, вступает в реакцию субстехиометрического горения при температурах выше 850 ° C, так что элементарная сера осаждается в охладителе технологического газа, расположенном ниже по потоку.
Содержание H 2 S и концентрация других горючих компонентов ( углеводородов или аммиака ) определяют место сжигания исходного газа. Газы Клауса (кислый газ), не содержащие других горючих веществ, кроме H 2 S, сжигаются в фурмах, окружающих центральный муфель , в результате следующей химической реакции:
2 H 2 S + 3 O 2 → 2 SO 2 + 2 H 2 O (Δ H = -518 кДж моль -1 )
Это сильно экзотермическое полное окисление сероводорода в свободном пламени с образованием диоксида серы, который вступает в реакцию в последующих реакциях. Самая важная из них — реакция Клауса:
Температура внутри печи Клауса часто поддерживается выше 1050 ° C. Это обеспечивает разрушение БТЭК (бензол, толуол, этилбензол и ксилол), которые в противном случае засорили бы последующий катализатор Клауса.
Газы, содержащие аммиак, такие как газ из отпарной колонны кислой воды (SWS) нефтеперерабатывающего завода, или углеводороды преобразуются в муфеле горелки. В муфель нагнетается достаточно воздуха для полного сгорания всех углеводородов и аммиака. Отношение воздуха к кислому газу регулируется таким образом, что в целом 1/3 всего сероводорода (H 2 S) превращается в SO 2 . Это обеспечивает стехиометрическую реакцию реакции Клауса на второй каталитической стадии (см. Следующий раздел ниже).
Разделение процессов горения обеспечивает точную дозировку необходимого объема воздуха, необходимого в зависимости от состава подаваемого газа. Для уменьшения объема технологического газа или получения более высоких температур сгорания потребность в воздухе также может быть покрыта путем впрыска чистого кислорода. В промышленности доступно несколько технологий, использующих высоко- и низкоуровневое обогащение кислородом, что требует использования специальной горелки в реакционной печи для этого варианта процесса.
Обычно от 60 до 70% от общего количества элементарной серы, полученной в процессе, получают на стадии термического процесса.
Основная часть горячего газа из камеры сгорания проходит через трубу охладителя технологического газа и охлаждается, так что сера, образующаяся на стадии реакции, конденсируется . Тепло, выделяемое технологическим газом, и выделяемое при конденсации тепло используются для производства пара среднего или низкого давления . Конденсированная сера удаляется на выходе жидкости из охладителя технологического газа.
Сера образуется в термической фазе в виде высокореакционных бирадикалов S 2, которые соединяются исключительно с аллотропом S 8 :
Побочные реакции
Другие химические процессы, происходящие на термической стадии реакции Клауса:
Каталитическая стадия
Реакция Клауса продолжается на каталитической стадии с активированным оксидом алюминия (III) или титана (IV) и служит для увеличения выхода серы. Больше сероводорода ( H 2 S ) вступает в реакцию с SO 2, образовавшимся при сгорании в реакционной печи в реакции Клауса, и приводит к образованию газообразной элементарной серы.
2 H 2 S + SO 2 → 3 S + 2 H 2 O (Δ H = -1165,6 кДж моль -1 )
Один из предполагаемых механизмов состоит в том, что S 6 и S 8 десорбируются с активных центров катализатора с одновременным образованием стабильной циклической элементарной серы.
Каталитическое восстановление серы состоит из трех подэтапов: нагревание, каталитическая реакция и охлаждение плюс конденсация. Эти три шага обычно повторяются не более трех раз. Если установка для сжигания или очистки отходящих газов (TGTU) добавляется после установки Клауса, обычно устанавливаются только две каталитические ступени.
Первым технологическим этапом каталитической стадии является процесс нагрева газа. Это необходимо для предотвращения конденсации серы в слое катализатора, которая может привести к его засорению. Требуемая рабочая температура слоя на отдельных каталитических ступенях достигается путем нагревания технологического газа в подогревателе до тех пор, пока не будет достигнута желаемая температура рабочего слоя.
В промышленности используются несколько методов подогрева:
- Байпас горячего газа: включает смешивание двух потоков технологического газа из охладителя технологического газа (холодный газ) и байпаса (горячий газ) из первого прохода котла-утилизатора.
- Непрямые пароперегреватели: газ также можно нагреть паром высокого давления в теплообменнике.
- Обменники газ / газ: при этом охлажденный газ из охладителя технологического газа косвенно нагревается от горячего газа, выходящего из расположенного выше по потоку каталитического реактора в теплообменнике газ-газ.
- Нагреватели прямого нагрева: подогреватели с подогревом, использующие кислый газ или топливный газ, который сжигается субстехиометрически, чтобы избежать прорыва кислорода, который может повредить катализатор Клауса.
Обычно рекомендуемая рабочая температура первой стадии катализатора составляет от 315 ° C до 330 ° C (температура нижнего слоя). Высокая температура на первой стадии также помогает гидролизу COS и CS 2 , которые образуются в печи и в противном случае не были бы преобразованы в модифицированном процессе Клауса.
Каталитическая конверсия максимальна при более низких температурах, но необходимо следить за тем, чтобы каждый слой работал выше точки росы серы. Рабочие температуры последующих каталитических ступеней обычно составляют 240 ° C для второй ступени и 200 ° C для третьей ступени (температуры нижнего слоя).
В конденсаторе серы технологический газ, поступающий из каталитического реактора, охлаждается до температуры от 150 до 130 ° C. Тепло конденсации используется для генерации пара на межтрубном пространстве конденсатора.
Перед хранением потоки жидкой серы из охладителя технологического газа, конденсаторов серы и из конечного сепаратора серы направляются в установку дегазации, где удаляются растворенные в сере газы (в основном H 2 S).
Остаточный газ процесса Клауса, все еще содержащий горючие компоненты и соединения серы (H 2 S, H 2 и CO), либо сжигается в установке для сжигания, либо дополнительно обессеривается в последующей установке для обработки хвостового газа.
Процесс Клауса ниже точки росы
Обычный процесс Клауса, описанный выше, имеет ограниченную конверсию из-за достижения реакционного равновесия. Подобно всем экзотермическим реакциям, большая конверсия может быть достигнута при более низких температурах, однако, как упоминалось, реактор Клауса должен работать при температуре выше точки росы по сере (120–150 ° C), чтобы избежать физической дезактивации жидкой серы катализатора. Чтобы решить эту проблему, реакторы Клаусса с пониженной точкой росы ориентированы параллельно, с одним рабочим и одним запасным. Когда один реактор насыщается адсорбированной серой, технологический поток перенаправляется в резервный реактор. Затем реактор регенерируют, направляя технологический газ, нагретый до 300–350 ° C, для испарения серы. Этот поток направляется в конденсатор для извлечения серы.
Производительность процесса
На каждую тонну выхода серы будет производиться более 2,6 тонны пара.
Эти физические свойства элементарной серы , полученной в процессе Клауса могут отличаться от полученного других процессов. Сера обычно транспортируется в жидком виде ( точка плавления 115 ° C). В элементарной сере вязкость быстро увеличивается при температурах выше 160 ° C из-за образования цепей полимерной серы. Другая аномалия обнаружена в растворимости остаточного H 2 S в жидкой сере в зависимости от температуры. Обычно растворимость газа уменьшается с повышением температуры, но с H 2 S все наоборот. Это означает, что токсичный и взрывоопасный газ H 2 S может накапливаться в свободном пространстве любого резервуара охлаждающей жидкой серы. Объяснение этой аномалии заключается в эндотермической реакции серы с H 2 S с образованием полисульфанов H 2 S x .
Источник