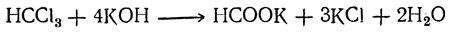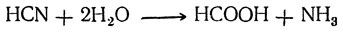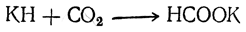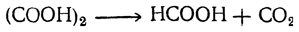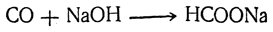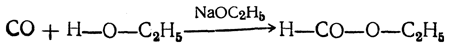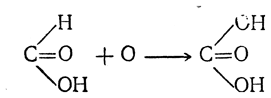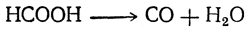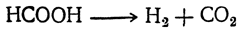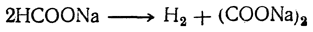- Муравьиная кислота
- Муравьиная кислота: общая характеристика и применение
- История появления муравьиной кислоты
- Открытие
- Получение
- Физические и химические свойства муравьиной кислоты
- Применение
- Безопасность и допустимость использования
- Муравьиная кислота
- Содержание
- Физические и химические свойства
- Получение
- Безопасность
- Нахождение в природе
- Применение
- Производные муравьиной кислоты
Муравьиная кислота
Муравьиная кислота НСООН была открыта еще в XVII столетии в едких выделениях муравьев. Она содержится также в жгучей крапиве.
Муравьиная кислота может быть получена всевозможными способами (аналогичными описанным выше общим способам) из различных простейших соединений углерода. Так, например, она получается из хлороформа действием разбавленной щелочи
В настоящее время единственным промышленным способом получения муравьиной кислоты является пропускание окиси углерода через нагретый едкий натр:
Пропусканием окиси углерода через нагретые спиртовые растворы алкоголятов получаются эфиры муравьиной кислоты по уравнению
Муравьиную кислоту в виде водного раствора можно получить из муравьинокислых солей перегонкой с разбавленной серной кислотой. Безводную кислоту не удается получить дробной перегонкой водных растворов, так как муравьиная кислота дает с водой постояннокипящую (при 107° С) смесь, содержащую 77,5% кислоты. Безводная кислота может быть получена или разложением сероводородом муравьинокислого свинца, или обезвоживанием водной кислоты при помощи безводной щавелевой кислоты.
Безводная муравьиная кислота — жидкость, обладающая крайне острым запахом.
Муравьиная кислота отличается от всех остальных жирных кислот тем, что карбоксильный углерод в ней соединен не с алкилом, а с атомом водорода. Поэтому ее можно рассматривать и как альдегид, в котором группа СНО соединена с гидроксилом. Подобно альдегидам муравьиная кислота может окисляться, образуя угольную кислоту
т. е. представляет собой как бы альдегид, соответствующий угольной кислоте.
Муравьиная кислота, как и альдегиды, является сильным восстановителем. Она может восстанавливать при нагревании соли окиси ртути до солей закиси и даже до металлической ртути, а также окись серебра до металлического серебра, вследствие чего серебряная соль муравьиной кислоты легко разлагается с выделением серебра.
При нагревании с концентрированной серной кислотой муравьиная кислота распадается на окись углерода и воду:
Эта реакция может быть использована для получения чистой окиси углерода.
В присутствии порошкообразного иридия или родия муравьиная кислота распадается на водород и двуокись углерода:
При быстром нагревании муравьинокислого натрия до 400° С выделяется водород и образуется щавелевокислый натрий:
Муравьиная кислота находит довольно значительное применение как восстановитель, а также используется при крашении тканей; 1,25%-ный водный раствор ее употребляется в медицине («муравьиный спирт», или spiritus formicarum).
Источник
Муравьиная кислота: общая характеристика и применение
HCOOH – рациональная формула муравьиной кислоты, насыщенной односоставной карбоновой кислоты, входящая в так называемую карбоксильную группу. В настоящее время муравьиная кислота имеет систематическое название метановой, является органическим соединением, зарегистрированным в качестве пищевой добавки Е236.
История появления муравьиной кислоты
Открытие
В 1670 году натуралист, член Лондонского королевского общества Джон Рей провел эксперимент, результатом которого стало появление нового водного раствора химического соединения, проявляющего типичные свойства кислот. Рей путем кипячения воды в сосуде с помещенными в него рыжими лесными муравьями, произвел процесс перегонки паром.
Сейчас процесс заменен синтезом муравьиной кислоты из угарного газа и воды. Позже энтомологи подтвердят, что в теле муравьев в брюшной полости находятся ядовитые железы, которые вырабатывают кислоту как средство защиты от нападения.
Рыжие лесные муравьи оказались не единственными носителями кислоты данного вида. Муравьиная кислота, хоть и в меньших объемах, обнаружена в пчелином яде, гусеницах шелкопряда, сосновой хвое, крапиве, фруктах, а также выделениях животных и даже человека. Соли и эфиры кислоты, формиаты, также получили название от латинского formica — муравей.
Получение
С XIX века муравьиную кислоту получают химическим путем в виде натриевой соли. Большее количество муравьиной кислоты получается как побочный продукт при жидкофазном окислении бутана и бензиновой фракции при производстве другой кислоты – уксусной.
Около 35% мирового производства получают гидролизом формамида. Основным промышленным способом получения муравьиной кислоты является реакция монооксида углерода с гидроксидом натрия: NaOH + CO → HCOONa → (+H2SO4, −Na2SO4) HCOOH. Процесс разделен на две стадии:
- 1 стадия. Монооксид углерода пропускают под давлением 0.6 – 0.8 МПа через 120 – 130 °C гидроксид натрия.
- 2 стадия. Обработка формиата натрия серной кислотой и перегонка продукта вакуумом.
Еще одним способом является разложение глицериновых эфиров щавелевой кислоты. При нагревании щавелевой кислоты и безводного глицерина путем отгона воды образуют щавелевые эфиры. Разлагая щавелевые эфиры методом нагревания, получают углекислый газ и образования муравьиных эфиров. Последние методом разложения водой образуют глицерин и муравьиную кислоту.
Физические и химические свойства муравьиной кислоты
Одна из самых простых карбоновых кислот, муравьиная одновременно является самой сильной. При попадании на кожу вызывает ожог, жжение, растворение. Растворяет капрон, нейлон и прочие полимеры.
Муравьиная кислота представляет собой бесцветную жидкость с едким и резким запахом. Смешивается с водой, этанолом, диэтиловым эфиром. Растворяется в ацетоне, бензоле, глицерине и толуоле. Обладает свойствами кислот и альдегида, в молекулярной формуле есть кислотная часть (CO-OH) и атом углерода (H-CO). Такая особенность привела к особенной реакции восстанавливать серебро, что характерно для альдегидов, но не для кислот.
Важная особенность муравьиной кислоты является изготовление «тяжелых» жидкостей. Применяемые геологами, минеролагами, геммологами, помогают при идентификации и разделении минералов по свойствам их плотности.
При растворении металлического таллия в 90% растворе муравьиной кислоты, получают формиат таллия. При растворении таких веществ и их солей получают раствор в котором плавают тяжелый шпат, корунд, малахит.
Муравьиная кислота известна своими бактерицидными свойствами. Используется при дезинфекции продовольственной тары. Кислота используется как пищевой концентрат. Слабые растворы применяют в медицине.
Применение
Основное применение муравьиной кислота – консервант, это обусловлено высоким бактерицидными и антисептическими свойствами. Останавливающая свойства гнилостности муравьиная кислота (пищевой вариант E236) широко применяется во многих областях, среди которых:
- пищевая:
- консервация соков, овощей
- очистка от примесей сахаров при производстве меда, маринадов
- дезинфекция винных и пивных емкостей
- медицинская:
- анальгетическое и противовоспалительное средство
- лечение грибковых заболеваний, ушибов, растяжений, варикозного расширения вен
- противотуберкулерных растворах
- анестетиков
- косметологическая:
- очищающие средства при лечении угревой сыпи
- стимуляция роста волос
- средства для соляриев и загара
- бытовая:
- чистящие средства против ржавчины и известкового налета
- сельское хозяйство:
- заготовка зимних кормов
- борьба с клещами при пчеловодстве
Более подробно о сферах применения муравьиной кислоты можно узнать в публикации «Применение муравьиной кислоты в различных отраслях».
Безопасность и допустимость использования
Следует обратить внимание на то, что применение муравьиной кислоты в продуктах питания разрешено России, Беларуси, а также странах ЕАЭС. В странах Евросоюза разрешено применять Е236 в косметических средствах, а в США в составе синтетических ароматизаторов для продуктов питания.
Неразбавленная муравьиная кислота вызывает сильные химические ожоги, 10% и более обладает разъедающим эффектом, менее 10% — раздражающим.
Основная отличительная особенность метановой кислоты — это отсутствие производств в России. Тем не менее, муравьиную кислоту всегда можно купить в ООО «Эверест». Узнать подробнее можно здесь.
Источник
Муравьиная кислота
| Муравьиная кислота | |
|---|---|
 | |
 | |
| Систематическое наименование | Метановая кислота |
| Традиционные названия | Муравьиная кислота |
| Хим. формула | CH₂O₂ |
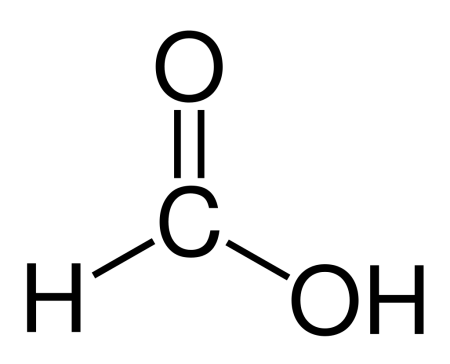
| Рац. формула | HCOOH |
| Состояние | Жидкость |
| Молярная масса | 46,025380 г/моль |
| Плотность | 1,2196 г/см³ |
| Динамическая вязкость | 0,16 Па·с |
| Энергия ионизации | 11,05 ± 0,01 эВ |
| Т. плав. | 8,25 °C |
| Т. кип. | 100,7 °C |
| Т. всп. | 60 °C |
| Т. свспл. | 520 °C |
| Пр. взрв. | 18 ± 1 об.% |
| Тройная точка | 281,40 K (8,25 °C), 2,2 кПа |
| Кр. точка | 588 K (315 °C), 5,81 МПа |
| Мол. теплоёмк. | 98,74 Дж/(моль·К) |
| Энтальпия образования | −409,19 кДж/моль |
| Давление пара | 120 мм. рт. ст. (16 кПа) при 50 °C |
| pKa | 3,75 |
| Показатель преломления | 1,3714 |
| Дипольный момент | 1,41 (газ) Д |
| ГОСТ | ГОСТ 5848-73 ГОСТ 1706-78 |
| Рег. номер CAS | 64-18-6 |
| PubChem | 284 |
| Рег. номер EINECS | 200-579-1 |
| SMILES | |
| Рег. номер EC | 200-579-1 |
| Кодекс Алиментариус | E236 |
| RTECS | LQ4900000 |
| ChEBI | 30751 |
| ChemSpider | 278 |
| Токсичность | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Муравьиная кислота (систематическое наименование: метановая кислота) HCOOH — органическое соединение, первый представитель в ряду насыщенных одноосновных карбоновых кислот. Зарегистрирована в качестве пищевой добавки под обозначением E236. Своё название муравьиная кислота получила потому, что впервые она была выделена в 1670 году английским натуралистом Джоном Рэйем из рыжих лесных муравьёв. В природе также обнаружена у пчёл, в крапиве, хвое. Соли и анионы муравьиной кислоты называются формиатами.
Содержание
Физические и химические свойства
При стандартных условиях муравьиная кислота представляет собой резко пахнущую бесцветную жидкость. Растворима в ацетоне, бензоле, глицерине, толуоле. Смешивается с водой, диэтиловым эфиром, этанолом.
Константа диссоциации: 1,772⋅10 −4 .
Муравьиная кислота, кроме кислотных свойств, проявляет также некоторые свойства альдегидов, в частности, восстановительные. При этом она окисляется до углекислого газа. Например:
При нагревании с сильными водоотнимающими средствами (H2SO4 (конц.) или P4O10) разлагается на воду и моноксид углерода:
Муравьиная кислота реагирует с аммиачным раствором оксида серебра:
Взаимодействие муравьиной кислоты с гидроксидом меди:
Проявляет все свойства одноосновных карбоновых кислот:
Образует формиаты с металлами:
Со спиртами образует сложные эфиры:
HCOOH + CH3OH → HCOOCH3 + H2O 
Получение
- Побочный продукт в производстве уксусной кислоты жидкофазным окислением бутана.
- Окисление метанола:
CH3OH → HCHO → HCOOH - Реакцией монооксида углерода с гидроксидом натрия:
NaOH + CO → HCOONa → (+H2SO4, −Na2SO4) HCOOH
Это основной промышленный метод, который осуществляют в две стадии: на первой стадии монооксид углерода под давлением 0,6—0,8 МПа пропускают через нагретый до 120—130 °C гидроксид натрия; на второй стадии проводят обработку формиата натрия серной кислотой и вакуумную перегонку продукта. - Разложением глицериновых эфиров щавелевой кислоты. Для этого нагревают безводный глицерин со щавелевой кислотой, при этом отгоняется вода и образуются щавелевые эфиры. При дальнейшем нагревании эфиры разлагаются, выделяя углекислый газ, при этом образуются муравьиные эфиры, которые после разложения водой дают муравьиную кислоту и глицерин.
Безопасность
Опасность муравьиной кислоты зависит от концентрации. Согласно классификации Европейского союза, концентрация до 10 % обладает раздражающим эффектом, больше 10 % — разъедающим.
При контакте с кожей 100%-я жидкая муравьиная кислота вызывает сильные химические ожоги. Попадание даже небольшого её количества на кожу причиняет сильную боль, поражённый участок сначала белеет, как бы покрываясь инеем, потом становится похожим на воск, вокруг него появляется красная кайма. Кислота легко проникает через жировой слой кожи, поэтому промывание поражённого участка раствором соды необходимо произвести немедленно. Контакт с концентрированными парами муравьиной кислоты может привести к повреждению глаз и дыхательных путей. Случайное попадание внутрь даже разбавленных растворов вызывает явления тяжёлого некротического гастроэнтерита.
Муравьиная кислота быстро метаболизируется и выводится организмом. Тем не менее, муравьиная кислота и формальдегид, образующиеся при отравлении метанолом, вызывают повреждение зрительного нерва и ведут к слепоте.
По данным ПДК в воздухе рабочей зоны равна 1 мг/м 3 (максимально-разовая). Может попадать в организм при вдыхании. Порог восприятия запаха может достигать, например, 453 мг/м 3 . можно ожидать, что использование широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками СИЗОД) приведёт к чрезмерному воздействию муравьиной кислоты на, по крайней мере, часть работников — из-за запоздалой замены противогазных фильтров. Для защиты от неё следует использовать более эффективные изменение технологии и средства коллективной защиты.
Нахождение в природе
В природе муравьиная кислота обнаружена в хвое, крапиве, фруктах, едких выделениях медуз, пчёл и муравьёв. Муравьиная кислота впервые была выделена в 1670 году английским натуралистом Джоном Рэйем из рыжих лесных муравьёв, чем и объясняется её название.
В больших количествах муравьиная кислота образуется в качестве побочного продукта при жидкофазном окислении бутана и лёгкой бензиновой фракции в производстве уксусной кислоты. Муравьиную кислоту получают также гидролизом формамида (
35 % от общего мирового производства); процесс состоит из нескольких стадий: карбонилирование метанола, взаимодействие метилформиата с безводным NH3 и последующий гидролиз образовавшегося формамида 75%-ной H2SO4. Иногда используют прямой гидролиз метилформиата (реакцию проводят в избытке воды или в присутствии третичного амина), гидратацию СО в присутствии щёлочи (кислоту выделяют из соли действием H2SO4), дегидрогенизацию CH3OH в паровой фазе в присутствии катализаторов, содержащих Cu, а также Zr, Zn, Cr, Mn, Mg и др. (метод не имеет промышленного значения).
Применение
В основном, муравьиную кислоту используют как консервирующий и антибактериальный агент при заготовке корма. Муравьиная кислота замедляет процессы гниения и распада, поэтому сено и силос, обработанные муравьиной кислотой, дольше сохраняются. Муравьиная кислота также используется в протравном крашении шерсти, для борьбы с паразитами в пчеловодстве, как растворитель в некоторых химических реакциях.
В лабораториях используют разложение жидкой муравьиной кислоты под действием горячей концентрированной серной кислоты, либо пропуская муравьиную кислоту над оксидом фосфора P2O5, для получения монооксида углерода.
В медицине используется для приготовления растворов пермуравьиной кислоты («первомур», или рецептура «С-4» (смесь перекиси водорода и муравьиной кислоты)). Первомур используют в хирургии в качестве предоперационного антисептического средства, в фармацевтической промышленности для дезинфекции оборудования.
Производные муравьиной кислоты
Соли и эфиры муравьиной кислоты называют формиатами.
Источник