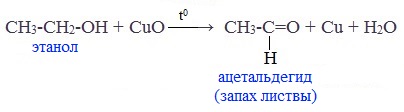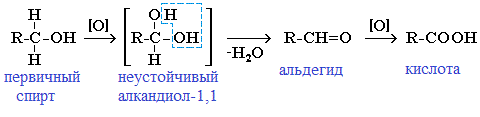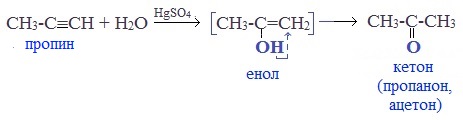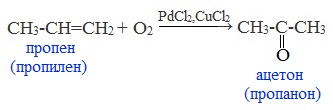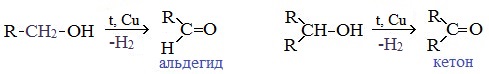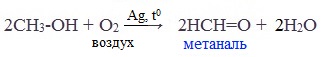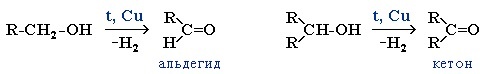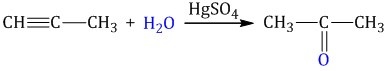- Промышленный способ получения кетонов
- Получение формальдегида
- Как из кислоты или спирта получить кетон
- Получение кетонов — зачем это нужно
- Какими реакциями это возможно
- Получение кетонов каталитическим дегидрированием спиртов
- Как получить кетоны при помощи пиролиза карбоновых кислот и их солей
- Получение кетонов с помощью гидролиза
- Получение кетонов восстановлением нитросоединений
- Получение кетонов расщеплением гидропероксидов
- Получение кетонов гидратацией алкинов
- Получение кетонов ацилированием металлоорганических соединений
Промышленный способ получения кетонов
1. Окисление спиртов
В лаборатории карбонильные соединения получают окислением спиртов в жестких условиях в присутствии сильных окислителей (дихромата калия К2Cr2O7 или перманганата калия КМnО4) в серной кислоте Н2SO4. В качестве окислителя можно использовать оксид меди (II) при нагревании.
При окислении первичных спиртов образуются альдегиды:
Видеоопыт «Окисление этилового спирта оксидом меди (II)»
Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот:
Чтобы предотвратить превращение альдегида в кислоту, его отгоняют в ходе реакции (tкип альдегида, не образующего межмолекулярные водородные связи, ниже tкип спирта и кислоты).
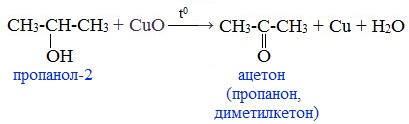
При окислении вторичных спиртов образуются кетоны:
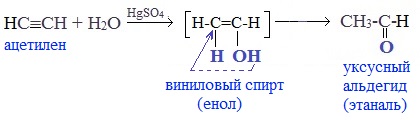
Присоединение воды к ацетилену происходит в присутствии катализатора соли ртути (II) и идет через образование неустойчивого непредельного спирта (енола), который изомеризуется в уксусный альдегид (в случае ацетилена):
Кетоны получают при гидратации других гомологов ряда алкинов:
Раньше это был промышленный способ получения карбонильных соединений. В настоящее время этот способ находит ограниченное применение из-за загрязнения получаемых продуктов токсичными солями ртути и относительной дороговизны.
3. Каталитическое окисление алкенов кислородом воздуха
Этим способом в промышленности получают уксусный альдегид — окислением этилена кислородом воздуха (Вакер-процесс).
Эта реакция протекает в присутствии катализатора – смеси PdCl2 и CuCl2 и температуре 100 0 С:
Этим экономичным способом получают низшие альдегиды и кетоны.
Этот промышленный способ более перспективен, чем гидратация алкинов, при которой используются токсичные ртутные катализаторы.
4. Каталитическое дегидрирование спиртов
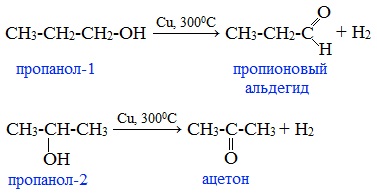
В промышленности альдегиды и кетоны получают дегидрированием спиртов, пропуская пары спирта над нагретым катализатором (Cu, соединения Ag, Cr или Zn).
Первичные спирты окисляются до альдегидов, а вторичные – до кетонов.
Этот способ получения объясняет суть названия «альдегид» (от лат. alconol dehydrogenatum – спирт, от которого «отняли» водород).
Этот способ позволяет получать карбонильные соединения, в особенности альдегиды, без побочных продуктов окисления.
В 1835 г. немецкий химик Ю. Либих выделил индивидуальное вещество, молекула которого содержала на два атома водорода меньше, чем этанол. Ученый установил состав этого соединения – С2Н4О и назвал его альдегидом (от лат. al conol dehyd rogenatum — т.е. дегидрированный спирт, «спирт, лишенный водорода»).
В 1867 г. немецкий химик-органик А. Гофман, пропуская пары метилового спирта над раскаленной платиновой спиралью, получил газообразное вещество состава СН2О, молекула которого отличается от открытого Либихом альдегида на группу -СН2— . Именно это соединение (муравьиный альдегид) открывает гомологический ряд альдегидов.
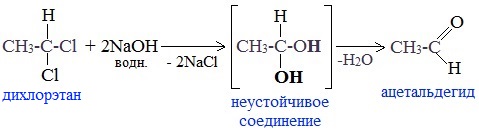
5. Щелочной гидролиз дигалогеналканов
Реакция протекает при действии водных растворов щелочей на дигалогензамещенные углеводороды, содержащие два атома галогена у одного и того же атома углерода.
При щелочном гидролизе дигалогеналканов образуются двухатомные спирты, в которых две группы ОН соединены с одним атомом углерода. Эти вещества неустойчивы и при отщеплении воды, превращаются в карбонильные соединения.
Если два атома галогена связаны с первичным атомом углерода, то образуются альдегиды:
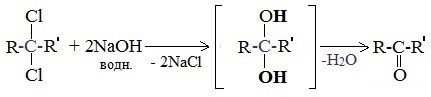
При гидролизе дигалогеналканов, содержащих атомы галогена у вторичного атома углерода, образуются кетоны:
Это лабораторный способ получения карбонильных соединений.
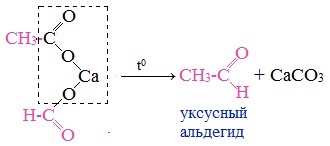
6. Пиролиз солей карбоновых кислот
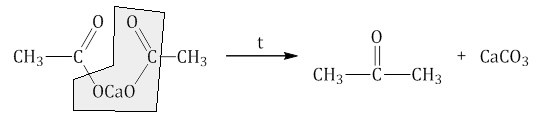
При пиролизе (термическое разложение) кальциевых, бариевых солей карбоновых кислот образуются соответствующие карбонильные соединения. Из смешанной соли муравьиной и другой карбоновой кислоты получают альдегиды, а в остальных случаях образуются кетоны.
Это лабораторный способ получения карбонильных соединений.
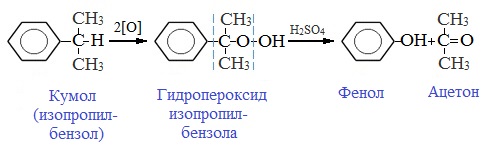
7. Кумольный способ получения ацетона (наряду с фенолом)
Простейший кетон – ацетон – получают кумольным методом вместе с фенолом:
Это промышленный способ получения ацетона.
Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
Получение формальдегида
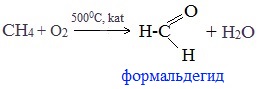
1. Окисление метана
Формальдегид в промышленности можно получить окислением метана кислородом воздуха при высоких температурах с использованием катализатора:
2. Окисление метанола
Основной промышленный способ получения формальдегида – окисление метанола с использованием серебряного катализатора при температуре 650 0 С и атмосферном давлении:
Реакция происходит на раскаленной серебряной сетке, через которую проходят пары ментола, смешанные с воздухом. Реакция настолько экзотермична, что выделяющейся в ходе ее теплоты достаточно для того, чтобы поддерживать сетку в раскаленном состоянии.
В настоящее время разработан перспективный способ высокотемпературного окисления метанола с использованием железомолибденовых катализаторов:
Источник
Как из кислоты или спирта получить кетон
Получение кетонов — зачем это нужно
Представить понятие данных химических веществ возможно, рассмотрев для начала характеристику карбонильных соединений. К данной категории относят материалы органического происхождения, молекулы которых содержат карбонильную группу.
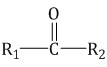
Карбонильные соединения классифицируют на альдегиды и кетоны. Общая химическая формула карбонильных соединений имеет следующий вид:
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Кетоны представляют собой соединения, в молекуле которых наблюдается связь карбонильной группы с двумя углеводородными радикалами.
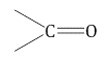
Структурная формула кетонов имеет следующий вид:
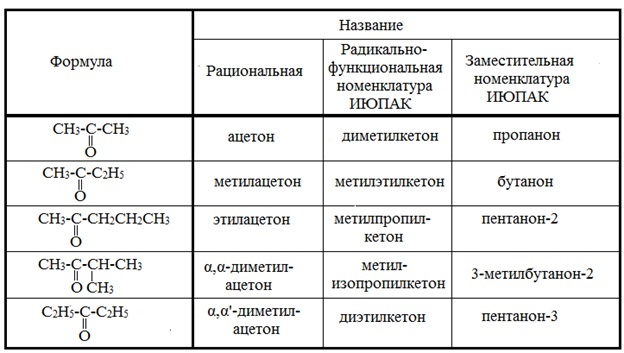
Гомологический ряд кетонов отличается сложной структурой из-за изомерии. Данную характеристику можно представить в виде таблицы:
К простейшему типу кетонов относится популярное растворяющее вещество – ацетон. Летучая жидкость не имеет окраса и обладает специфическим запахом. Сферы применения ацетона:
- синтез таких материалов, как поликарбонат и полиуретан;
- изготовление эпоксидной смолы;
- производство лаков;
- создание взрывчатых компонентов;
- медицинская промышленность;
- экстракция растительных материалов.
Какими реакциями это возможно
Существует несколько способов получения кетонов. К таким методикам можно отнести:
- каталитическое дегидрирование спиртов;
- пиролиз карбоновых кислот и их солей;
- гидролиз;
- восстановление нитросоединений;
- расщепление гидропероксидов;
- гидратация алкинов;
- ацилирование металлоорганических соединений.
Получение кетонов каталитическим дегидрированием спиртов
С помощью данной химической реакции получают необходимые соединения. Для образования кетонов используют вторичные спирты. В качестве катализаторов применяют следующие материалы:
- медь;
- серебро;
- хромиты меди;
- оксид цинка и другие.
В отличие от медных катализаторов оксид цинка характеризуется высокой стойкостью, что способствуют сохранению активности в процессе реакции. Но в этом случае процесс может сопровождаться дегидратацией.
Как получить кетоны при помощи пиролиза карбоновых кислот и их солей
Данный способ основан на древнем методе Пириа. Процесс представляют собой сухую перегонку кальциевой соли кислоты или смеси кислот. Некоторое время пиролиз карбоновых кислот и их солей был главным способом получения ацетона в промышленных масштабах. Исходя из особенностей строения солей, существует возможность получения симметричных кетонов. Таким примером является использование одинаковых кислотных остатков в кальциевых солях. Также с помощью пиролиза получают несимметричные кетоны. В данном случае необходимо наличие разных кислотных остатков в кальциевых солях. В качестве материалов для химических реакций можно применять любые кислые соединения, за исключением муравьиной кислоты. Процесс заключается в следующем:
- смесь кислот необходимо пропустить над катализатором, к примеру ThО;
- в условиях высокотемпературной среды образуется соль;
- затем протекает реакция пиролиза;
- происходит разложение карбоната тория на ThO и CO2.
Примеры получения кетонов с помощью пиролиза карбоновых кислот и их солей:
Получение кетонов с помощью гидролиза
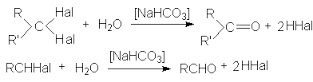
С помощью гидролиза вицинальных галогеналканов образуются гликоли. Кетоны являются результатом химической реакции в виде гидролиза геминальных галогенпроизводных УВ. Процесс выглядит следующим образом:
Получение кетонов восстановлением нитросоединений
Данная реакция Дж.У. Нефа открыта в 1894 году. При восстановлении нитросоединений используют разведенные минеральные кислоты. Во время воздействия этих веществ на соли аци-форм вторичных нитросоединений происходит реакция гидролиза, и образуются кетоны.
Получение кетонов расщеплением гидропероксидов
Окисляясь, углеводороды, согласно принципу радикально-цепного механизма, преобразуются в гидропероксиды. Реакция окисления сопровождается высокими температурами и давлением. В таких условиях гидропероксиды распадаются на свободные радикалы. Процесс может несколько отличаться в зависимости от разветвленности гидропероксида. Природа конечного продукта реакции определяется строением гидроперекиси. В результате цепного процесса окисления образуются кетоны.
Получение кетонов гидратацией алкинов
Карбонильные соединения образуются в результате химической реакции с участием солей ртути (II). В этой среде вода присоединяется к алкинам. К примеру, получение ацетона сопровождается гидратацией пропина.
Получение кетонов ацилированием металлоорганических соединений
Получение необходимых химических веществ данного типа может происходить несколькими способами. Наиболее распространенными методами получения кетонов с помощью ацилирования являются:
- Извлечение кетонов с применением металлоорганических соединений из эфиров и хлорангидридов карбоновых кислот. В результате образуются третичные кетоны.
- Получение кетонов, используя металлоорганические соединения из амидов. При этом полученные кетоны не могут в дальнейшем преобразоваться в спирты.
- Образование кетонов с применением металлоорганических соединений из нитрилов. В процессе получаются нестабильные кетимины, которые путем гидролиза переходят в кетоны.
- Вырабатывание кетонов из карбоновых кислот.
Источник