- Этиленгликоль: химические свойства и получение
- Строение этиленгликоля
- Водородные связи и физические свойства спиртов
- Химические свойства этиленгликоля
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- 2. Реакции замещения группы ОН
- 2.1. Взаимодействие с галогеноводородами
- 2.2. Этерификация (образование сложных эфиров)
- 2.4. Взаимодействие с кислотами-гидроксидами
- 3. Дегидратация
- 4. Окисление этиленгликоля
- 4.1. Окисление оксидом меди (II)
- 4.2. Окисление кислородом в присутствии катализатора
- 4.3. Жесткое окисление
- 4.4. Горение этиленгликоля
- 5. Дегидрирование этаниленгликоля
- Получение этиленгликоля
- 1. Щелочной гидролиз дигалогеналканов
- 2. Гидрирование карбонильных соединений
- 3. Гидролиз сложных эфиров
- 4. Мягкое окисление алкенов
- Промышленный способ получения этиленгликоля
- Свойства продукта и технические характеристики
- Промышленные методы производства этиленгликоля
- Области применения этиленгликоля
Этиленгликоль: химические свойства и получение
Этиленгликоль C2H4(OH)2 или CH2(OH)CH2OH, этандиол-1,2 – это органическое вещество, предельный двухатомный спирт .
Общая формула предельных нециклических двухатомных спиртов: CnH2n+2O2 или CnH2n(OН)2
Строение этиленгликоля
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому этиленгликоль – жидкость с относительно высокой температурой кипения.
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Химические свойства этиленгликоля
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
1. Кислотные свойства
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
При взаимодействии этиленгликоля с растворами щелочей реакция практически не идет, т. к. образующийся алкоголят почти полностью гидролизуется водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому этиленгликоль не взаимодействует с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Этиленгликоль взаимодействует с активными металлами (щелочными и щелочноземельными).
| Например, этиленгликоль взаимодействует с калием с образованием гликолята калия и водорода . |
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии этиленгликоля с галогеноводородами группы ОН замещаются на галоген и образуются дигалогеналкан.
| Например, этиленгликоль реагирует с бромоводородом. |
2.2. Этерификация (образование сложных эфиров)
Многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, этиленгликоль реагирует с уксусной кислотой с образованием эфира: |
2.4. Взаимодействие с кислотами-гидроксидами
Этиленгликоль взаимодействует и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии этиленгликоля с азотной кислотой образуется нитроэтиленгликоль : |
3. Дегидратация
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. При высокой температуре (180 о С) протекает внутримолекулярная дегидратация этиленгликоля и образуется соответствующий ацетальдегид.
4. Окисление этиленгликоля
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
4.1. Окисление оксидом меди (II)
Этиленгликоль можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества.
4.2. Окисление кислородом в присутствии катализатора
Этиленгликоль можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.).
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) этиленгликоль окисляется до щавелевой кислоты.
| Например, при взаимодействии этиленгликоля с перманганатом калия в серной кислоте образуется щавелевая кислота |
4.4. Горение этиленгликоля
При сгорании этиленгликоля образуется углекислый газ и вода и выделяется большое количество теплоты.
5. Дегидрирование этаниленгликоля
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования.
| Например, при дегидрировании этиленгликоля образуется этандиаль |
Получение этиленгликоля
1. Щелочной гидролиз дигалогеналканов
При взаимодействии дигалогеналканов с водным раствором щелочей образуются двухатомные спирты. Атомы галогенов в дигалогеналканах замещаются на гидроксогруппы.
| Например, при нагревании 1,2-дихлорэтана с водным раствором гидроксида натрия образуется этиленгликоль |
2. Гидрирование карбонильных соединений
| Например, при гидрировании этандиаля образуется этиленгликоль |
О=CН-CH=O + 2H2 → CH2(OH)-CH2OH
3. Гидролиз сложных эфиров
При гидролизе сложных эфиров этиленгликоля и карбоновых кислот образуются этиленгликоль и карбоновая кислота.
4. Мягкое окисление алкенов
Мягкое окисление протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкена разрывается только π-связь и окисляется каждый атом углерода при двойной связи.
При этом образуются двухатомные спирты (диолы).
Источник
Промышленный способ получения этиленгликоля
В промышленности этиленгликоль получают гидратацией окиси этилена. Свойство вступать в реакцию поликонденсации обеспечивает ему стабильно растущий спрос в секторе производства полиэфиров, а уникальная возможность не замерзать при пониженных температурах делает его незаменимым в производстве антифризов.
Свойства продукта и технические характеристики
Этиленгликоль представляет собой бесцветную вязкую гигроскопичную жидкость без запаха, сладковатого вкуса. Температура кипения 197,6 °С, температура плавления –12,7 °С, плотность – 1,1132 г/см 3 . Хорошо растворим в воде, спиртах, кетонах и др., умеренно — в бензоле, толуоле, диэтиловом эфире. Водные растворы этиленгликоля замерзают при низких температурах (до -70 °С).
Этиленгликоль ядовит. При попадании внутрь действует на центральную нервную систему и почки, смертельная доза — 1,4 г/кг. Предельно допустимая концентрация в воздухе рабочей зоны — 5 мг/м 3 . Относится к третьему классу опасности. Из-за низкой упругости паров этиленгликоль не вызывает острых отравлений при вдыхании.
При транспортировке этиленгликоль должен быть расфасован только в алюминиевые бочки или бочки из коррозионно-стойкой стали. Этиленгликоль, упакованный в бочки, транспортируют в крытых транспортных средствах всеми видами транспорта, а также в железнодорожных цистернах. Хранят в бочках в закрытых не отапливаемых складах.
В нижеследующей таблице кратко представлены технические требования к моноэтиленгликолю высшего и первого сорта согласно ГОСТ 19710-83 .
Технические характеристики этиленгликоля (согласно ГОСТ 19710-83 )
Показатель
Значение
Высший Сорт
Сорт 1
Массовая доля этиленгликоля. %. не менее
Массовая доля диэтиленгликоля. %. не более
Цвет в единицах Хазена, не более:
в обычном состоянии
после кипячения с соляной кислотой
Массовая доля остатка после прокаливания, %, не более
Массовая доля железа. %. не более
Массовая доля воды, %, не более
Массовая доля кислот в пересчете на уксусную, %, не более
Показатель преломления при 20° С
Пропускание в ультрафиолетовой области спектра,%, не менее, при длинах волн, нм:
Этиленгликоль был впервые получен в 1859 году французским химиком Шарлем Адольфом Вудсом. Первое промышленное производство этиленгликоля основывалось на гидролизе дихлорэтана водным раствором соды при 200 °С и давлении 10 МПа. Он использовался в небольших масштабах в период Первой мировой войны в качестве теплоносителя и компонента взрывчатых веществ. Широкое промышленное производство началось в 1937 году, когда был разработан процесс прямого окисления этилена в этиленоксид, что обеспечило доступным сырьем производство этиленгликоля. В настоящее время мировое производство этиленгликоля основано на гидратации окиси этилена.
В период Второй мировой войны этиленгликоль получил широкое распространение в авиации, где он стал использоваться в качестве охладителя радиатора и антиобледенителя стекол. В последующие годы сферы использования этиленгликоля расширялись, появлялись новые продукты на его основе. На сегодняшний день производство этиленгликоля является важной составляющей химической промышленности. Потребность в этом продукте в мире с каждым годом увеличивается.
Промышленные методы производства этиленгликоля
В настоящее время основным промышленным способом получения этиленгликоля является гидратации окиси этилена. Реакция включает раскрытие эпоксидного цикла и образование гидроксильных групп. Она проходит в воде при небольшом нагревании и несколько повышенном давлении в присутствии кислотного катализатора.
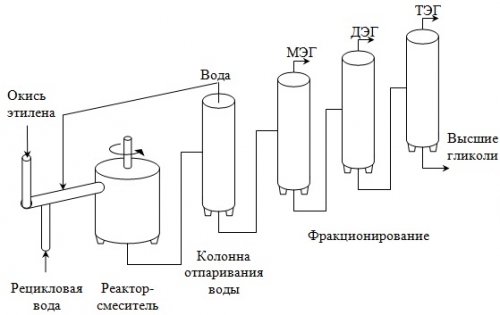
Процесс проводят в нейтральной среде под давлением 10≈12 кгс/см2 при 160≈180 °С в непрерывно действующем автоклаве, который представляет собой стальную колонну высотой 10 м и диаметром 1 м. Раствор, выходящий из автоклава, упаривают в двух- или трехкорпусном выпарном агрегате и фракционируют. В процессе производства моноэтиленгликоля получаются также ди- и триэтиленгликоли.
С установки выходит достаточно чистый этиленгликоль, который удовлетворяет жестким требованиям, предъявляемым производителями полиэтилентерефталата и полиэфирных волокон. Ниже представлена схема установки по получению этиленгликоля и ориентировочный материальный баланс процесса.
Материальный баланс процесса синтеза этиленгликоля
Сырье
Масса, кг
Продукты
Масса, кг
* Ди-, три- и тетраэтиленгликоли
Этиленгликоль также может быть получен взаимодействием этиленоксида с СО2 при температуре 80-120°С и давлении 2-5 МПа в присутствии галогенидов щелочных металлов, аммония или аминов с последующей гидратацией образующегося этиленкарбоната.
Этиленгликоль образуется также при ацетоксилировании этилена с последующим гидролизом моно- и диацетатов этиленгликоля (катализаторами служат хлориды Pd, Li, нитраты Fe, Ni). Недостаток метода — высокая коррозионность среды, трудность отделения солей и продуктов реакции, необходимость регенерации катализатора.
При уменьшении добычи нефти и резком увеличении стоимости этилена представляют интерес методы синтеза этиленгликоля из альтернативного сырья: синтез-газа, метанола, СО и воды при т-ре 200°С и давлении 70 МПа либо в жидкой фазе при 40 МПа в присутствии оксидных медно-магниевых или родиевых катализаторов; из СО и Н2 — через диэфиры щавелевой кислоты.
Так, компания IPCI ( International Polyol Chemicals Inc., США), работающая в области создания новых, «зеленых» химических технологий, разработала новый способ производства многоатомных спиртов (этиленгликоля, пропиленгликоля, бутандиолов и глицерина) из сахаров любого происхождения. По этой технологии с 2004 года уже работает завод в Changchun (Китай) мощностью 10 тыс. тонн в год.
Области применения этиленгликоля
Этиленгликоль применяют в химической, текстильной, автомобильной, авиационной, электротехнической промышленности, в производстве гидравлических и закалочных жидкостей, полиуретанов, алкидных смол и др.
Два основных пути использования этиленгликоля абсолютно различны. С одной стороны, он применяется как потребительский продукт, а с другой – как сырье для более сложных химических процессов. Вследствие низкой температуры замерзания этиленгликоль является основным ингредиентом автомобильного антифриза. В зависимости от концентрации этиленгликоля в водном растворе можно получить основу охлаждающей жидкости с температурой замерзания от 0°С до 70°С. Водные растворы этиленгликоля не расширяются при замерзании и не образуют сплошной твердой массы, а превращаются в кашицеобразную рыхлую массу, объем которой больше первоначального только на 0,25-0,30%.
Из-за высокой химической активности он используется как мономер в производстве полиэфиров и полиэтилентерефталата, пластмассы для изготовления широко распространенных пластиковых бутылок для воды и напитков. Широкое распространение получили синтетические полиэфирные волокна на основе ПЭТФ.
На указанные области применения – в качестве антифриза, в производстве ПЭТФ и полиэфиров — приходится до 98% общего количества этиленгликоля, производимого в мире. Кроме того, этиленгликоль иногда используется в авиации в качестве антиобледенителя для ветровых стекол. Две гидроксильных группы в молекуле этиленгликоля делают его пригодным также для производства поверхностно-активных веществ и латексных красок. Смесь моноацетата и диацетата этиленгликоля представляет собой отвердитель, используемый в литейном производстве при изготовлении самоотверждающихся формовочных и стержневых смесей с жидким стеклом.
Низкомолекулярные и высокомолекулярные полиэфиры (ПЭГ) используются в качестве мягких лекарственных форм; гидрофильной основа для кремов, зубных паст, компонент лосьонов, дезодорантов, шампуней; эмульгаторов, диспергаторов, антистатиков в текстильной и кожевенной промышленности; пластификаторов в целлюлозно-бумажной промышленности; компонентов смазочно-охлаждающих жидкостей; в производстве полиуретанов; растворителей и добавок в лаках и красках; в производстве вискозы.
На основе насыщенных сложных эфиров, получаемых взаимодействием этиленгликоля с себационовой, ортофталевой кислотами, изготавливают полиэфирные клеи. Этиловый эфир этиленгликоля (этилцеллозольв) используется в качестве растворителя (нитро- и ацетилцеллюлозы, смол, лаков и др.), некоррозивных антифризов, антикристаллизационных присадок к моторным топливам и т.д. Гигроскопичность обуславливает применение этиленгликоля в качестве увлажнителя для текстильных волокон, бумаги, кожи и клеев.
Этиленгликоль также используют для ускорения сушки и улучшения эластичности покрытий алкидных красок на масляной основе, в качестве осушающего агента природного газа и моторных масел, для получения чернил, пестицидов, морилок, протрав и многих других продуктов.
C текущей ситуацией и прогнозом развития российского рынка моноэтиленгликоля можно познакомиться в отчете Академии Конъюнктуры Промышленных Рынков « Рынок моноэтиленгликоля в России ».
Источник