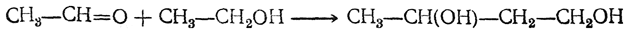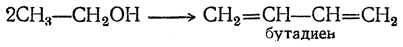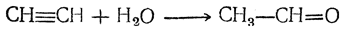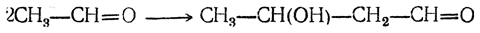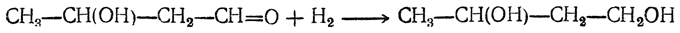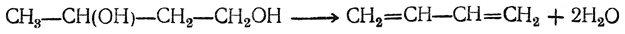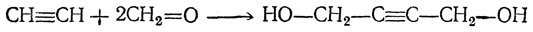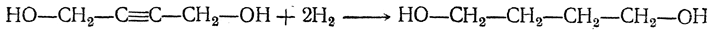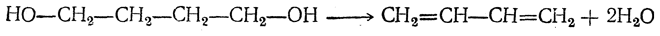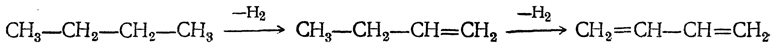- Добыча нефти и газа
- Изучаем тонкости нефтегазового дела ВМЕСТЕ!
- Производство Бутадиена-1,3
- Исторический очерк промышленного производства бутадиена в СССР и России
- Добыча нефти и газа
- Изучаем тонкости нефтегазового дела ВМЕСТЕ!
- Производство Бутадиена-1,3
- Исторический очерк промышленного производства бутадиена в СССР и России
- Бутадиен-1,3, или дивинил
Добыча нефти и газа
Изучаем тонкости нефтегазового дела ВМЕСТЕ!
Производство Бутадиена-1,3
Бутадиен-1,3 (дивинил) — ненасыщенный углеводород, простейший представитель сопряжённых диеновых углеводородов
БД — бесцветный газ с характерным запахом, температура кипения минус 4,5 °C, температура плавления минус 108,9 °C, температура вспышки минус 40°C, плотность 0,650 г/см3 при минус 6 °C. Плохо растворим в воде, хорошо растворим в спирте, керосине.
Исторический очерк промышленного производства бутадиена в СССР и России
После блестящих работ С.В. Лебедева, выполненных в первые десятилетия 20 века, посвященных полимеризации «двуэтиленовых» углеводородов и повторенных затем крупнейшими химиками мира (Б.А. Догадкин, Ю.Б. Монаков, В.А. Кормер) стало ясно, что каучукоподобный материал можно получать не только из изопрена, являющегося мономерным звеном натурального каучука, но и из другого диенового мономера — бутадиена-1,3 (СН2=СН-СН=СН2). Это послужило стимулом к проведению многочисленных исследований по разработке методов получения БД.
В России разработкой способов получения БД занимались два ученых исследователя: С.В.Лебедев, заведовавший кафедрой химии в Военно-медицинской академии, и Б.В. Бызов. Оба ученых работали в Ленинграде.
Профессор Б.В. Бызов разрабатывал свой метод получения БД — вакуумным пиролизом керосина при температуре 600 °С. Это была первая в мире работа по получению мономера из нефтяного сырья. Лаборатория Б.В. Бызова размещалась на территории завода «Красный треугольник». Она была оснащена большой пиролизной печью, аппаратами для химического выделения БД и автоклавами для синтеза каучука.
С.В. Лебедев собрал группу энтузиастов из 6 человек, которые в невероятно трудных условиях на укрупненной лабораторной установке испытали созданный им бифункциональный катализатор дегидрирования и дегидратации этилового спирта в БД. По современным представлениям одновременно протекает цепь реакций:
Дегидрирование этилового спирта в ацетальдегид:
СН3СН2ОН ® СНзСНО + H2
Конденсация альдегида в альдоль с отщеплением воды и образованием кротонового альдегида:
2СН3СНО ® СНзСН(ОН)СН2-СНО ® СНзСН=СН-СНО + Н2О
Восстановление карбонильной группы кротонового альдегида водородом, отщепляемым от этилового спирта, с образованием кротилового спирта и ацетальдегида:
СНзСН=СН-СНО + СН3СН2ОН ® СНзСН=СН-СН2ОН + СНзСНО
Дегидратация кротилового спирта в БД:
СНзСН=СН-СН2ОН ® СН2=СН-СН=СН2 + Н2О.
На выход БД влияют несколько факторов: температура, время контактирования, природа и активность катализатора. Оптимальная температура процесса колеблется в пределах от 400 до 450 °С. При превышении данного температурного режима начинается пиролитическая деструкция БД. Благоприятно действует на выход снижение давления на 0,25 атм и время контакта от 2 до 10 сек.
В первые годы эксплуатации метода выход БД не превышал 20 % (масс.) от прореагировавшего спирта (з4 % от теоретического). Упорные работы в направлении совершенствования каталитической системы позволили значительно повысить эти показатели (до 71,5 % от теории).
Основным недостатком процесса являлась низкая селективность. Достоинство способа — сравнительная простота аппаратурного оформления технологического процесса.
Разработанный С.В. Лебедевым способ получения БД из спирта позволил Советскому Союзу в чрезвычайно короткие сроки (с 19з1 по 19зб гг.) осуществить строительство и пуск 4 заводов по производству СК из БД. Эта технология стала лучшим из известных на тот момент миру способов синтетического получения БД.
Однако впоследствии этот процесс С.В. Лебедева утратил промышленное значение.
В годы Второй мировой войны в условиях изоляции от рынка натурального каучука в фашистской Германии исключительное значение приобрели работы великого химика В.Ю. Реппе, впервые в мире пересмотревшего промышленную химию ацетилена. В Германии эта химия имела прочную сырьевую основу в виде богатых залежей каменного угля, который превращается в карбид кальция и ацетилен.
Синтезы многих органических продуктов, разработанные В.Ю. Реппе, как правило, ярки, оригинальны, основаны на использовании специально разработанных индивидуальных катализаторов. В основе реализованного в промышленности метода синтеза БД лежат следующие реакции:
СН=СН + 2 СН20 ® НОСН2- С=С-СН2ОН
Реакция протекает при температуре 100 °С, давлении 0,5 МПа в присутствии меди нанесенной на диоксид кремния. Выход бутиндиола по ацетилену 89 %, по ФА 90 %.
Н0СН2- СН=СН-СН20Н + 2Н2 ® Н0СН2- СН2-СН2-СН20Н
Гидрирование бутиндиола до бутандиола осуществляется при 150 °С, давлении 30 МПа в присутствии медь-никель-хромового катализатора. Выход бутандиола составляет 98 %.
Н0СН2- СН2-СН2-СН20Н ® (СН2)40 + Н20
Дегидратация — циклизация бутандиола в тетрагидрофуран протекает при 60 °С, давлении 7,0 МПа в присутствии фосфорной кислоты. Выход тетрагидрофурана количественный.
(СН2)04 ® СН2=СН-СН=СН2 + Н2O
Превращение тетрагидрофурана в БД осуществляется при 270 °С, давлении 0,1 МПа в присутствии дизамещенного фосфата натрия. Выход БД составляет 97 %.
Несмотря на множество оригинальных технологических решений (использование катализаторов высокой селективности) после войны процесс был остановлен из-за очень сложной технологии.
Источник
Добыча нефти и газа
Изучаем тонкости нефтегазового дела ВМЕСТЕ!
Производство Бутадиена-1,3
Бутадиен-1,3 (дивинил) — ненасыщенный углеводород, простейший представитель сопряжённых диеновых углеводородов
БД — бесцветный газ с характерным запахом, температура кипения минус 4,5 °C, температура плавления минус 108,9 °C, температура вспышки минус 40°C, плотность 0,650 г/см3 при минус 6 °C. Плохо растворим в воде, хорошо растворим в спирте, керосине.
Исторический очерк промышленного производства бутадиена в СССР и России
После блестящих работ С.В. Лебедева, выполненных в первые десятилетия 20 века, посвященных полимеризации «двуэтиленовых» углеводородов и повторенных затем крупнейшими химиками мира (Б.А. Догадкин, Ю.Б. Монаков, В.А. Кормер) стало ясно, что каучукоподобный материал можно получать не только из изопрена, являющегося мономерным звеном натурального каучука, но и из другого диенового мономера — бутадиена-1,3 (СН2=СН-СН=СН2). Это послужило стимулом к проведению многочисленных исследований по разработке методов получения БД.
В России разработкой способов получения БД занимались два ученых исследователя: С.В.Лебедев, заведовавший кафедрой химии в Военно-медицинской академии, и Б.В. Бызов. Оба ученых работали в Ленинграде.
Профессор Б.В. Бызов разрабатывал свой метод получения БД — вакуумным пиролизом керосина при температуре 600 °С. Это была первая в мире работа по получению мономера из нефтяного сырья. Лаборатория Б.В. Бызова размещалась на территории завода «Красный треугольник». Она была оснащена большой пиролизной печью, аппаратами для химического выделения БД и автоклавами для синтеза каучука.
С.В. Лебедев собрал группу энтузиастов из 6 человек, которые в невероятно трудных условиях на укрупненной лабораторной установке испытали созданный им бифункциональный катализатор дегидрирования и дегидратации этилового спирта в БД. По современным представлениям одновременно протекает цепь реакций:
Дегидрирование этилового спирта в ацетальдегид:
СН3СН2ОН ® СНзСНО + H2
Конденсация альдегида в альдоль с отщеплением воды и образованием кротонового альдегида:
2СН3СНО ® СНзСН(ОН)СН2-СНО ® СНзСН=СН-СНО + Н2О
Восстановление карбонильной группы кротонового альдегида водородом, отщепляемым от этилового спирта, с образованием кротилового спирта и ацетальдегида:
СНзСН=СН-СНО + СН3СН2ОН ® СНзСН=СН-СН2ОН + СНзСНО
Дегидратация кротилового спирта в БД:
СНзСН=СН-СН2ОН ® СН2=СН-СН=СН2 + Н2О.
На выход БД влияют несколько факторов: температура, время контактирования, природа и активность катализатора. Оптимальная температура процесса колеблется в пределах от 400 до 450 °С. При превышении данного температурного режима начинается пиролитическая деструкция БД. Благоприятно действует на выход снижение давления на 0,25 атм и время контакта от 2 до 10 сек.
В первые годы эксплуатации метода выход БД не превышал 20 % (масс.) от прореагировавшего спирта (з4 % от теоретического). Упорные работы в направлении совершенствования каталитической системы позволили значительно повысить эти показатели (до 71,5 % от теории).
Основным недостатком процесса являлась низкая селективность. Достоинство способа — сравнительная простота аппаратурного оформления технологического процесса.
Разработанный С.В. Лебедевым способ получения БД из спирта позволил Советскому Союзу в чрезвычайно короткие сроки (с 19з1 по 19зб гг.) осуществить строительство и пуск 4 заводов по производству СК из БД. Эта технология стала лучшим из известных на тот момент миру способов синтетического получения БД.
Однако впоследствии этот процесс С.В. Лебедева утратил промышленное значение.
В годы Второй мировой войны в условиях изоляции от рынка натурального каучука в фашистской Германии исключительное значение приобрели работы великого химика В.Ю. Реппе, впервые в мире пересмотревшего промышленную химию ацетилена. В Германии эта химия имела прочную сырьевую основу в виде богатых залежей каменного угля, который превращается в карбид кальция и ацетилен.
Синтезы многих органических продуктов, разработанные В.Ю. Реппе, как правило, ярки, оригинальны, основаны на использовании специально разработанных индивидуальных катализаторов. В основе реализованного в промышленности метода синтеза БД лежат следующие реакции:
СН=СН + 2 СН20 ® НОСН2- С=С-СН2ОН
Реакция протекает при температуре 100 °С, давлении 0,5 МПа в присутствии меди нанесенной на диоксид кремния. Выход бутиндиола по ацетилену 89 %, по ФА 90 %.
Н0СН2- СН=СН-СН20Н + 2Н2 ® Н0СН2- СН2-СН2-СН20Н
Гидрирование бутиндиола до бутандиола осуществляется при 150 °С, давлении 30 МПа в присутствии медь-никель-хромового катализатора. Выход бутандиола составляет 98 %.
Н0СН2- СН2-СН2-СН20Н ® (СН2)40 + Н20
Дегидратация — циклизация бутандиола в тетрагидрофуран протекает при 60 °С, давлении 7,0 МПа в присутствии фосфорной кислоты. Выход тетрагидрофурана количественный.
(СН2)04 ® СН2=СН-СН=СН2 + Н2O
Превращение тетрагидрофурана в БД осуществляется при 270 °С, давлении 0,1 МПа в присутствии дизамещенного фосфата натрия. Выход БД составляет 97 %.
Несмотря на множество оригинальных технологических решений (использование катализаторов высокой селективности) после войны процесс был остановлен из-за очень сложной технологии.
Источник
Бутадиен-1,3, или дивинил
Бутадиен-1,3, или дивинил, СН2=СН—СН=СН2 представляет собой газ, конденсирующийся при —4,5° С. Вследствие громадного технического значения бутадиена-1,3 как одного из важнейших исходных мономеров для производства синтетических каучуков было разработано много способов его получения, в том числе и промышленных.
Бутадиен образуется при термическом разложении различных органических веществ; в небольших количествах содержится в газах, получаемых пиролизом нефтепродуктов и каменного угля. Он может быть получен пиролизом циклогексана и других углеводородов нефти, пиролизом циклогексанола, дегидратацией 1,3-бутиленгликоля, а также конденсацией альдегида и спирта в присутствии глинозема как катализатора (И. И. Остромысленский). В последнем случае, вероятно, промежуточно образуется 1,3-бутиленгликоль
который сразу же дегидратируется. Другой способ получения бутадиена из спирта состоит в окислении этанола в ацегальдегид, который конденсируют в альдоль; восстановление альдоля дает 1,3-бутиленгликоль.
Первым технически целесообразным путем получения бутадиена из спирта является способ С. В. Лебедева, впервые осуществленный в промышленных масштабах в СССР в 1932 г. и в дальнейшем получивший широкое распространение. По С. В. Лебедеву спирт непосредственно превращается в бутадиен при пропускании его паров при 400—500° С над катализатором, обладающим одновременно дегидрирующим и дегидратирующим действием. Суммарно процесс выражается уравнением
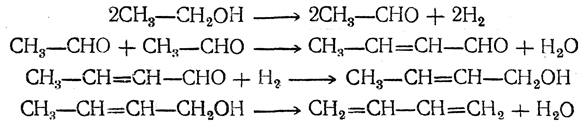
Вероятно, механизм этой реакции (М. Я. Каган, Ю. Д. Горин) таков:
Можно получать дивинил, в том числе и в промышленном масштабе, на основе ацетилена. Более старый метод синтеза из ацетилена может быть представлен следующей схемой:
Позднее был предложен следующий путь: 1. Получение 1,4-бутиндиола конденсацией ацетилена и формальдегида (с Сu2Сl2 в качестве катализатора):
2. Гидрирование 1,4-бутиндиола в 1,4-бутандиол:
3. Дегидратация 1,4-бутандиола в дивинил либо непосредственно
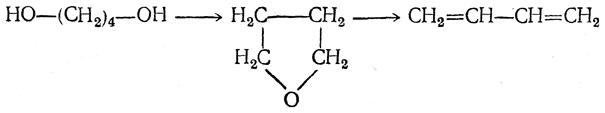
либо с промежуточным выделением тетрагидрофурана
В настоящее время самым эффективным методом получения дивинила является каталитическое дегидрирование природного бутана, а также бутиленов, содержащихся в газах термической переработки нефти. Реакция проводится над различными алюмо-хромовыми катализаторами при 500—650° С. В зависимости от применяемых катализаторов бутан может быть превращен в бутадиен либо сразу, либо в две стадии
причем для каждой стадии требуются свои катализаторы и условия реакции. Эти методы, разрабатывавшиеся одновременно в СССР и в США, в настоящее время осуществляются как промышленные.
Хлорпроизводное дивинила — 2-хлорбутадиен-1,3, или хлоропрен, СН2—СН—ССl=СН2 может быть получен присоединением молекулы хлористого водорода к винилацетилену, получаемому при пропускании ацетилена через солянокислые растворы медных солей. Хлоропрен — жидкость с характерным эфирным запахом, несколько напоминающим запах бромистого этила; т. кип. 59,4°С, относительная плотность 0,9533 (при 20°С). Подобно дивинилу, но значительно легче, хлоропрен полимеризуется в каучукоподобные вещества — синтетические каучуки, выпускаемые в СССР под названием наирит, а в США — под названием неопрен.
Полихлоропреновые каучуки обладают рядом ценных физико-химических свойств — стойкостью к атмосферным воздействиям, к солнечному свету, к различным маслам и химическим агентам, а также негорючестью, благодаря чему они нашли очень широкое применение.
Источник