Азотная кислота: получение и химические свойства
Строение молекулы и физические свойства
Азотная кислота HNO3 – это сильная одноосновная кислота-гидроксид. При обычных условиях бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C ( при нормальном атмосферном давлении). Азотная кислота смешивается с водой во всех соотношениях. На свету частично разлагается.
Валентность азота в азотной кислоте равна IV, так как валентность V у азота отсутствует. При этом степень окисления атома азота равна +5. Так происходит потому, что атом азота образует 3 обменные связи и одну донорно-акцепторную, является донором электронной пары.
Поэтому строение молекулы азотной кислоты можно описать резонансными структурами:
Обозначим дополнительные связи между азотом и кислородом пунктиром. Этот пунктир по сути обозначает делокализованные электроны. Получается формула:
Способы получения
В лаборатории азотную кислоту можно получить разными способами:
1. Азотная кислота образуется при действии концентрированной серной кислоты на твердые нитраты металлов. При этом менее летучая серная кислота вытесняет более летучую азотную.
Например , концентрированная серная кислота вытесняет азотную из кристаллического нитрата калия:
2. В промышленности азотную кислоту получают из аммиака . Процесс осуществляется постадийно.
1 стадия. Каталитическое окисление аммиака.
2 стадия. Окисление оксида азота (II) до оксида азота (IV) кислородом воздуха.
3 стадия. Поглощение оксида азота (IV) водой в присутствии избытка кислорода.
Химические свойства
Азотная кислота – это сильная кислота . За счет азота со степенью окисления +5 азотная кислота проявляет сильные окислительные свойства .
1. Азотная кислота практически полностью диссоциирует в водном растворе.
2. Азотная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , азотная кислота взаимодействует с оксидом меди (II):
Еще пример : азотная кислота реагирует с гидроксидом натрия:
3. Азотная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов, сульфитов).
Например , азотная кислота взаимодействует с карбонатом натрия:
4. Азотная кислота частично разлагается при кипении или под действием света:
5. Азотная кислота активно взаимодействует с металлами. При этом никогда не выделяется водород! При взаимодействии азотной кислоты с металлами окислителем всегда выступает азот +5. Азот в степени окисления +5 может восстанавливаться до степеней окисления -3, 0, +1, +2 или +4 в зависимости от концентрации кислоты и активности металла.
металл + HNO3 → нитрат металла + вода + газ (или соль аммония)
С алюминием, хромом и железом на холоду концентрированная HNO3 не реагирует – кислота «пассивирует» металлы, т.к. на их поверхности образуется пленка оксидов, непроницаемая для концентрированной азотной кислоты. При нагревании реакция идет. При этом азот восстанавливается до степени окисления +4:
Золото и платина не реагируют с азотной кислотой, но растворяются в «царской водке» – смеси концентрированных азотной и соляной кислот в соотношении 1 : 3 (по объему):
HNO3 + 3HCl + Au → AuCl3 + NO + 2H2O
Концентрированная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (IV), азот восстанавливается минимально:
С активными металлами (щелочными и щелочноземельными) концентрированная азотная кислота реагирует с образованием оксида азота (I):
Разбавленная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (II).
С активными металлами (щелочными и щелочноземельными), а также оловом и железом разбавленная азотная кислота реагирует с образованием молекулярного азота:
При взаимодействии кальция и магния с азотной кислотой любой концентрации (кроме очень разбавленной) образуется оксид азота (I):
Очень разбавленная азотная кислота реагирует с металлами с образованием нитрата аммония:
Таблица . Взаимодействие азотной кислоты с металлами.
| Азотная кислота | ||||
| Концентрированная | Разбавленная | |||
| с Fe, Al, Cr | с неактивными металлами и металлами средней активности (после Al) | с щелочными и щелочноземельными металлами | с неактивными металлами и металлами средней активности (после Al) | с металлами до Al в ряду активности, Sn, Fe |
| пассивация при низкой Т | образуется NO2 | образуется N2O | образуется NO | образуется N2 |
6. Азотная кислота окисляет и неметаллы (кроме кислорода, водорода, хлора, фтора и некоторых других). При взаимодействии с неметаллами HNO3 обычно восстанавливается до NO или NO2, неметаллы окисляются до соответствующих кислот, либо оксидов (если кислота неустойчива).
Например , азотная кислота окисляет серу, фосфор, углерод, йод:
Безводная азотная кислота – сильный окислитель. Поэтому она легко взаимодействует с красным и белым фосфором . Реакция с белым фосфором протекает очень бурно. Иногда она сопровождается взрывом.
Видеоопыт взаимодействия фосфора с безводной азотной кислотой можно посмотреть здесь.
Видеоопыт взаимодействия угля с безводной азотной кислотой можно посмотреть здесь.
7. Концентрированная а зотная кислота окисляет сложные вещества (в которых есть элементы в отрицательной, либо промежуточной степени окисления): сульфиды металлов, сероводород, фосфиды, йодиды, соединения железа (II) и др. При этом азот восстанавливается до NO2, неметаллы окисляются до соответствующих кислот (или оксидов), а металлы окисляются до устойчивых степеней окисления.
Например , азотная кислота окисляет оксид серы (IV):
Еще пример : азотная кислота окисляет иодоводород:
Сера в степени окисления -2 окисляется без нагревания до простого вещества, при нагревании до серной кислоты.
Например , сероводород окисляется азотной кислотой без нагревания до молекулярной серы:
При нагревании до серной кислоты:
Соединения железа (II) азотная кислота окисляет до соединений железа (III):
8. Азотная кислота окрашивает белки в оранжево-желтый цвет («ксантопротеиновая реакция«).
Ксантопротеиновую реакцию проводят для обнаружения белков, содержащих в своем составе ароматические аминокислоты. К раствору белка прибавляем концентрированную азотную кислоту. Белок свертывается. При нагревании белок желтеет. При добавлении избытка аммиака окраска переходит в оранжевую.
Видеоопыт обнаружения белков с помощью азотной кислоты можно посмотреть здесь.
Источник
Теоретические основы производства азотной кислоты



Принципиальная схема производства разбавленной азотной кислоты
Химическая схема получения азотной кислоты
– получение разбавленной кислоты последующим концентрированием ее в случае необходимости;
– непосредственное получение концентрированной азотной кислоты.
Наиболее распространен первый способ, что связано с использованием в народном хозяйстве как концентрированной, так и разбавленной кислоты. Методы различаются физико-химическими закономерностями протекающих процессов и технологическими схемами. Однако независимо от схемы, синтез азотной кислоты из аммиака описывается общей химической схемой:
Производство азотной кислоты из аммиака складывается из трех стадий:
Первая стадия – каталитическое окисление аммиака в оксид азота (II):
Вторая стадия – окисление оксида азота (II) (необходимо ↓температуры, ↑ давления) в оксид азота (IV) и дальнейшая димеризация оксида азота (IV) в N2O4:
а) 2NO + O2 = 2NO2 + Qа’) 2NO ↔ (NO)2 + Q
Реакция а’) обратимая, повышение температуры вызывает смещение равновесия этой реакции в левую сторону. Таким образом, уменьшение скорости окисления оксида азота (II) в NO2 объясняется снижением концентрации димера.
Третья стадия – абсорбция оксида азота (IV) водой с образованием разбавленной азотной кислоты:
3NO2 + H2O = 2HNO3 + NO + Q
Выделяющийся при этом оксид азота (II) окисляется до диоксида (IV) и снова абсорбируется.
Независимо от конкретной технологической схемы принципиальная схема производства разбавленной азотной кислоты включает 3 стадии и пять основных операций:
Первая стадия — окисление аммиака до оксида азота (II):
1-я операция: очистка аммиака и воздуха и получение аммиачновоздушной смеси;
2-я операция: окисление аммиака на катализаторе.
Вторая стадия — окисление оксида азота (II) в оксид азота (IV):
3-я операция: охлаждение нитрозных газов;
4-я операция: частичное окисление оксида азота (II) в оксид азота (IV).
Третья стадия — абсорбция оксида азота (IV) водой с образованием разбавленной азотной кислоты:
5-я операция: дальнейшее доокисление оксида азота (II) до оксида азота (IV) и одновременное образование азотной кислоты в процессе абсорбции оксид азота (IV) водой.
ПЕРВАЯ СТАДИЯ — окисление аммиака кислородом воздуха.
При окислении аммиака возможно протекание следующих процессов:
4NH3 + 4 O2 ® 2N2O + 6 H2O + Q (горение в отсутствии катализаторов)
На поверхности платиновых катализаторов протекает следующая реакция:
Протекание первых трех реакций приводит к непроизводительному расходу аммиака. Установлено, что уже при 750 °С превращение аммиака в конечные продукты достигает 100 %. В азотнокислом производстве процесс окисления производят на катализаторах, обладающих избирательностью действия, т.е. на катализаторах, обладающих избирательностью действия, — резко ускоряющих реакцию получения NO по сравнению с прочими реакциями окисления аммиака.
В азотнокислой промышленности в основном применяют платиновые катализаторы. Процесс окисления аммиака на платиновом катализаторе относится к числу наиболее быстрых каталитических реакций, известных в настоящее время (10 -4 сек).
Реакция (**) – гетерогенная, необратимая, экзотермическая.
Выход оксида азота (II) составляет 98% при соблюдении следующих оптимальных условий:
а) температура на поверхности катализатора – 800ºС.
Повышение температуры способствует увеличению не только скорости химической реакции, но и коэффициента диффузии аммиака в смеси. Поэтому повышение температуры – эффективное средство увеличения скорости процесса окисления, протекающего как в кинетической, так и в диффузионной области. Однако повышение температуры катализа выше 800 – 850 °С быстро снижает выход NO и повышает выход элементарного азота, в том числе и за счет термической диссоциации NH3. На платиновом катализаторе поддерживают температуру от 800 °С при атмосферном давлении и до 900 °С при повышенном давлении, при котором время контакта сильно уменьшается и побочные реакции практически не успевают протекать. На низкоактивных неплатиновых катализаторах время соприкосновения необходимо увеличивать в десятки раз по сравнению с платиновым, при этом температура снижается до 700 – 750 °С.

б) Состав газовой смеси. Состав газовой смеси влияет на температурный режим и общую скорость процесса. По уравнению реакции (**) на 1 моль NH3 расходуется 1,25 моль О2, НО при таком соотношении компонентов выход оксида азота (II) не превышает 65%, т.е. очень мал.
Поэтому реакция проводится в избытке кислорода, соотношение O2:NH3 = 1.8 – 2.0; газ, поступающий на катализатор, содержит:
O2 – (9.5 – 10.5 %) 20%;
Окисление протекает автотермично, если содержание аммиака в газовой смеси достигает 11%.
Следует учитывать, что при обычной температуре смесь аммиака с воздухом взрывоопасна в интервале 16-27 % NH3. При повышении температуры границы взрывоопасности расширяются.
в) Давление. Повышение давления ускоряет процесс окисления NH3, так как увеличиваются концентрации реагирующих компонентов в объеме. Кроме того,при повышенном давлении увеличивается производительность катализатора вследствие уменьшения объема газовой смеси, который обратно пропорционален давлению. НО: при повышенном давлении существенно возрастает унос мельчайших частичек платины с газом, что удорожает товарную кислоту. При повышении давления необходимо увеличивать толщину стенок аппаратуры, в результате чего возрастает ее стоимость. Поэтому применяют давления 0.2 – 1 МПа.
г) Основной промышленный катализатор окисления аммиака – платина и её сплавы с родием (Rh 4 %) или палладием (3 % Pd). Платиновый катализатор применяют в виде пакетов сеток, сплетенных из тончайших проволок (диаметр 0,06 мм), сетки имеют 1024 отверстия в 1 см 2 . Сетки эти для создания определенного времени контактирования скрепляются в виде пакета, устанавливаемого в контактном аппарате. На 1 м 2 активной поверхности контактной сетки под атмосферным давлением можно окислить до 600 кг, а при давлении 0.8 МПа – до 3000 кг аммиака в сутки. Однако при работе под давлением 0.8 МПа и выше платиновый катализатор разрушается быстрее (унос платины составляет 0.3 – 0.4 г, часть платины улавливается и регенерируется, но расходы на платину составляют значительную часть себестоимости азотной кислоты.)
Сейчас наряду с платиновыми катализаторами используют катализаторы из смеси оксидов железа и хрома. Контактные массы изготавливаются в виде таблеток диаметром 5 мм. Однако неплатиновые катализаторы значительно менее активны.
Окисление аммиака на платиновых катализаторах является одной из самых кратковременных каталитических реакций, известных в настоящее время (время протекания реакции 1·10 -4 сек). Скорость каталитического окисления аммиака зависит от технологического режима процесса и конструкции контактного аппарата. На высокоактивных платиноидных катализаторах процесс протекает в диффузной области. На менее активных (оксидных) катализаторах при пониженных температурах и хорошем перемешивании газовой смеси окисление аммиака определяется скоростью каталитических актов, т.е. протекает в кинетической области.
С целью экономии платины применяют двухстадийное контактирование, при котором аммиак частично окисляется на платиноидных сетках, а затем доокисляется в слое неплатинового зернистого катализатора (оксиды Fe, Cr, соли Со). Если использовать двухступенчатый катализатор, состоящий из одной сетки и слоя таблеток, выход оксида азота (II) составляет 97%.
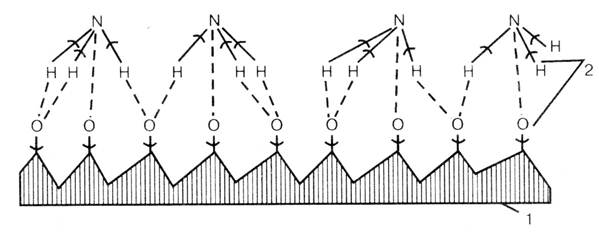
Механизм реакции, протекающей на катализаторе (Рис 4.1):
Оксида азота (II) образуется только на поверхности катализатора.
Рис. 5.1. Схема окисления аммиака на катализаторе: сплошные линии — ранее возникшие связи; пунктирные — вновь образующиеся связи.
1 — катализатор; 2 — места разрыва связей
а) Сначала атомы платины адсорбируют на себе молекулы кислорода, которые диссоциируют при этом на атомы.
б) Далее, благодаря высокому сродству кислорода к водороду, молекулы аммиака при приближении к поверхности катализатора ориентируются своими атомами водорода к атомам кислорода.
в) В результате происходит образование молекул воды и оксида азота (II), которые вытесняются новыми молекулами кислорода
Активность катализаторов может сильно понижаться вследствие отравления некоторыми примесями, имеющимися в газовой смеси, или в результате экранирующего действия механических взвесей. К наиболее сильным контактным ядам процесса окисления аммиака принадлежат соединения серы и фосфора.
В промышленности применяется несколько типов контактных аппаратов для окисления аммиака. Однако все они имеют приблизительно одинаковый принцип действия.
При работе под атмосферным давлением на платиноидном катализаторе в аппарате устанавливают пакет из 3–4 сеток. При повышенном давлении устанавливают до 18 сеток. При двухстадийном контактировании число платиноидных сеток может быть снижено до 1-3 (при повышенном давлении.)
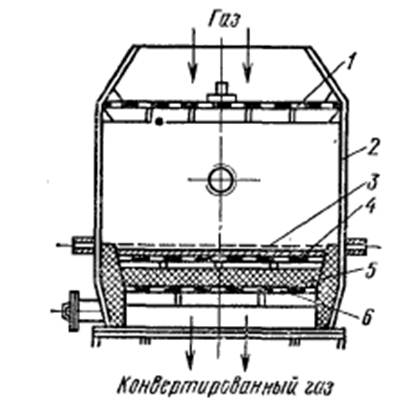 | Рисунок 5.2. – контактный аппарат: 1 – распределительная решетка; 2 – корпус аппарата; 3 – платиноидная сетка; 4 – слой неплатинового катализатора; 5 – насадка; 6 – опорная решетка |
ВТОРАЯ СТАДИЯ процесса – окисление оксида азота (II) до оксида азота (IV) и дальнейшая частичная димеризация оксида азота (IV) до тетраоксида азота (N2O4).
Нитрозные газы, полученные при окислении аммиака, содержат около 20 об. % NO, кислород, азот и пары воды. Для получения азотной кислоты оксид азота (II) необходимо окислить до диоксида.
Это гомогенная, некаталитическая, экзотермическая реакция, протекающая с уменьшением объёма:
2NO + O2 = 2NO2. + Q
В соответствии с принципом Ле-Шателье снижение температуры и повышение давления будет сдвигать равновесие этой реакции вправо.
Было показано, что при снижении температуры ниже 100ºС, равновесие реакции было полностью сдвинуто в сторону образования оксида азота (IV) и с понижением температуры скорость реакции возрастала, т. е. для этой реакции наблюдается аномальная зависимость скорости от температуры. При 0 °С реакция протекает в 12 раз, а при 300°С – в 30 раз медленнее, чем при – 130°С.
При температуре выше 700 °С образования диоксида азота практически не происходит. Следовательно, в горячих нитрозных газах, выходящих из контактного аппарата, NO2 отсутствует, и для его получения готовую смесь необходимо охладить ниже 100 °С. Для увеличения скорости превращения NO в NO2 реакционную смесь энергично охлаждают.
. Известно, что для всех одностадийных химических реакций повышение температуры вызывает повышение их скорости.
Предполагают, что окисление оксида азота (II) до оксида азота (IV) идёт с образованием промежуточного продукта – димера оксида азота (N2O2), т. е. реакция протекает в две стадии:
Поскольку реакция образования димера идёт с выделением теплоты, то с повышением температуры равновесие смещается в сторону образования оксида азота (II), а концентрация димера N2O2 уменьшается.
Понижение скорости реакции превращения оксида азота (II) до оксида азота (IV) с повышением температуры реакции можно объяснить уменьшением концентрации димера оксида азота (II).
Степень окисления NO возрастает при повышении давления. В установках, работающих под атмосферным давлением, окисление оксида азота с последующей абсорбцией NO2 водой проводят лишь на 92 – 93%, а при повышенном давлении окисляют NO и абсорбируют водой уже 98 – 99 % исходного оксида азота. Поэтому в азотнокислых цехах, работающих при атмосферном давлении, приходится устанавливать дополнительную громоздкую аппаратуру для частичного окисления и абсорбции смеси NO и NO2 щелочами. В цехах, работающих под давлением, можно ограничиться водной абсорбцией.
Одновременно в системе протекает реакция димеризации оксида азота (IV) в тетраоксид:
Скорость этой реакции очень велика.
Так как эта реакция, как и две предыдущие реакции, протекает с выделением тепла и уменьшением объёма, то повышение давления и понижение температуры способствует окислению оксида азота (II) до оксида азота (IV) и димеризации оксида азота (IV).
Таким образом, в нитрозных газах поступающих на абсорбцию, содержатся NO2, N2O3, N2O4, O2, N2O, NO, N2, пары воды и др.
(Двуокись азота может взаимодействовать окись азота NO + NO2 = N2O3 + 40,2 кДж. Правда, содержание этого оксида ничтожно.)
ТРЕТЬЯ СТАДИЯ. Поглощение оксида азота (IV) и его димера водой протекает по двум следующим реакциям:
2NO2 + H2O = HNO3 + НNO2 + Q
Получаемая при этом азотистая кислота неустойчива и разлагается:
Суммарно взаимодействие NO2 с водой можно представить уравнением реакции:
3NO2 + H2O = 2HNO3 + NO + Q
3N2O4 + 2H2O = 4HNO3 + 2NO + Q
Поглощение диоксида азота водой – типичный хемосорбционный процесс в системе газ-жидкость.
Так как реакции идут с выделением тепла и уменьшением объёма, то при понижении температуры и повышении давления равновесие сдвигается в сторону образования кислоты.
В производстве необходимо получать кислоту возможно большей концентрации. При этом увеличивается давление паров оксидов азота над раствором кислоты, что снижает движущую силу процесса, и, следовательно, общую скорость процесса. Для сдвига равновесия в сторону образования HNO3 необходимо снижать температуру и повышать давление. При абсорбции оксидов азота используется принцип противотока: наиболее концентрированный газ встречается с концентрированной кислотой, а в конце абсорбции остатки NO2 поглощаются наиболее слабой кислотой.
Вследствие экзотермичности процесса абсорбции температура вытекающей продукционной кислоты обычно составляет не менее 50 °С, поэтому в установках, работающих под атмосферным давлением получается кислота, содержащая лишь 50 % HNO3. В установках, работающих под давлением 0.6 – 0.8 МПа, можно получить 58 – 60 % -ную кислоту. Поднимая давление до 5 МПа, в установках прямого синтеза HNO3 из оксидов азота и кислорода получают кислоту концентрацией 98 % HNO3.
Кроме температуры и давления равновесное состояние в этой реакции зависит от концентрации образующейся азотной кислоты.
Чемменьше концентрация образующейся азотной кислоты, тем больше степень превращения оксида азота (IV) и его димера в азотную кислоту.
Наоборот, с повышением концентрации кислоты степень превращения оксида азота (IV) уменьшается.
. Следовательно, при нормальных условиях можно получить только разбавленную азотную кислоту с концентрацией до 47 – 50%.
Для увеличения концентрации кислоты необходимо повысить давление, понизить температуру и увеличить содержание оксида азота (IV).
Источник