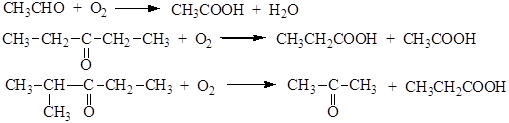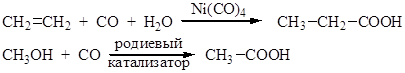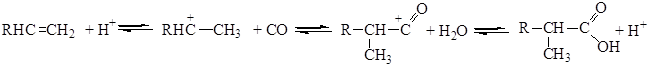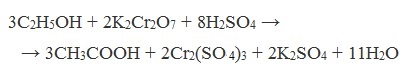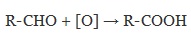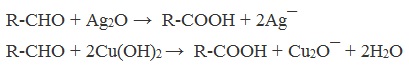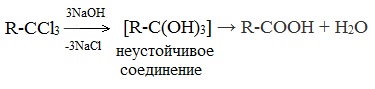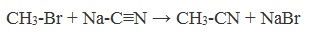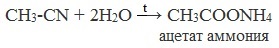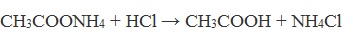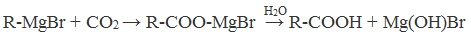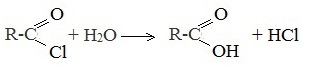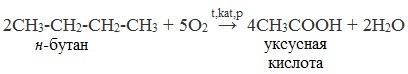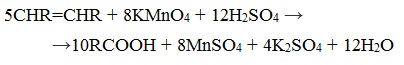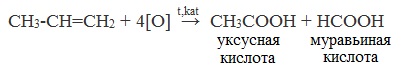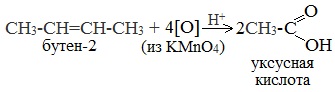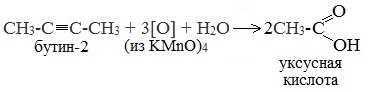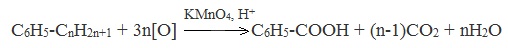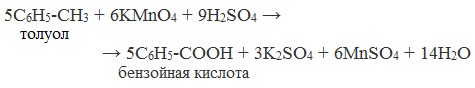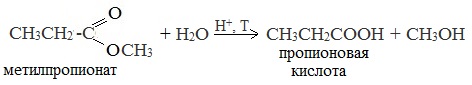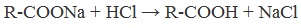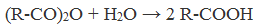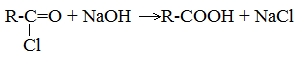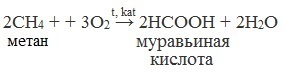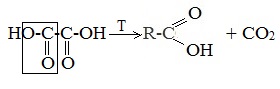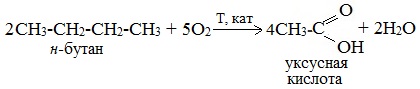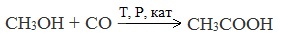Промышленные способы получения карбоновых кислот
13.1.1. Окисление углеводородов. Существует два способа: окисление низших алканов C4-C8 преимущественно до уксусной кислоты и окисление твердого парафина с образованием синтетических жирных кислот (СЖК) с прямой цепью углеродных атомов С10-С20, являющихся сырьем для синтеза ПАВ (поверхностно-активных веществ).
Процесс протекает в жидкой фазе при нагревании или в присутствии катализаторов. При окислении алканов происходит деструкция по связям между вторичными углеродными атомами, поэтому из н-бутана образуется главным образом уксусная кислота, а в качестве побочных продуктов – метилэтилкетон и этилацетат.
13.1.2.Синтезы на основе оксида углерода (II). Карбоновые кислоты получают на основе оксида углерода реакцией карбонилирования:
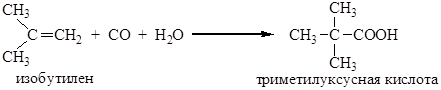
Присоединение по двойной связи при кислотном катализе всегда протекает по правилу Марковникова, вследствие этого только из этилена получается неразветвленная кислота, а из его гомологов — α-метилзамещенные кислоты. Особый интерес данный метод представляет для синтеза кислот с третичным радикалом (неокислот) из разветвленных олефинов (реакция Коха):
Механизм реакции состоит в предварительном протонировании алкена кислотой с образованием иона карбения, его взаимодействия с СО с получением ацилий – катиона и реакции последнего с водой с образованием карбоновой кислоты:
Неокислоты и их соли обладают очень высокой растворимостью и вязкостью, а их сложные эфиры — стабильностью к гидролизу, что обеспечивает им широкое применение в ряде отраслей.
Карбонилирование спиртов катализируется комплексами металлов (Ni, Со, Fe, Pd). Процесс реализован в промышленности для синтеза уксусной кислоты из метанола и характеризуется высокими экономическими показателями.
Кислоты также получают окислением альдегидов (продукт оксосинтеза).
Лабораторные способы получения карбоновых кислот
Окисление алканов.
Окисление алкенов.
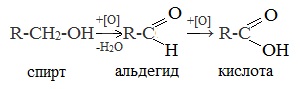
13.2.3. Окисление первичных спиртов.
13.2.4. Окисление альдегидов и кетонов. Альдегиды окисляются значительно легче, чем кетоны. Кроме того, окисление альдегидов приводит к образованию кислот с тем же числом углеродных атомов, в то время как окисление кетонов протекает с разрывом углерод – углеродных связей (образуются две кислоты или кислота и кетон):
Окислителями служат перманганат или бихромат калия. Окисление кетонов требует более жестких условий, чем альдегидов.
13.2.5. Гидролиз нитрилов. Нитрилы получают взаимодействием галогеналканов с цианистым калием, проводят гидролиз водными растворами кислот или щелочей. В кислой среде азот выделяется в виде соли аммония:
в щелочной — в виде гидроксида аммония, который разлагается с выделением аммиака, кислота же получается в виде соли:
13.2.6. Синтез Гриньяра. При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:
Под действием сильной кислоты (обычно НСl) соль превращается в кислоту:
Гидролиз жиров
Жиры — сложные эфиры карбоновых кислот и глицерина (триглицериды). Карбоновые кислоты, входящие в состав жиров имеют углеродную цепь от 3 до 18 углеродных атомов.
Кипячение жиров или масел с водными растворами щелочей (NaOH, КОН) приводит к получению солей карбоновых кислот и глицерина.
Эта операция называется омылением, так как соли карбоновых кислот используют для изготовления мыла.
Гидролиз производных карбоновых кислот.
Физические свойства
Низшие кислоты с числом атомов углерода до 3 – легколетучие бесцветные жидкости с характерным острым запахом, смешиваются с водой в любых соотношениях. Большинство кислот С4 – С9 – маслянистые жидкости с неприятным запахом. Растворимость в воде сильно уменьшается с ростом молярной массы. Кислоты от С10 и выше – твердые вещества, нерастворимые в воде. Плотности муравьиной и уксусной кислот больше единицы, остальных – меньше единицы. Температура кипения возрастает с увеличением молярной массы, при одном и том же числе углеродных атомов кислоты нормального строения кипят выше, чем кислоты с разветвленным углеродным скелетом. Сравнение температур кипения кислот и спиртов с одинаковым числом углеродных атомов показало, что кислоты кипят при значительно более высоких температурах, чем спирты. Это свидетельствует о более высокой ассоциации молекул кислот по сравнению со спиртами за счет образования водородных связей.
Карбоновые кислоты, как и спирты, способны образовывать водородные связи. Если акцептором является достаточно сильное основание, образование водородной связи предшествует полному переносу протона к основанию. По Бренстеду, соединение, являющееся донором водорода, считают «кислотой». Будет ли данное соединение «донором водорода» («кислотой»), зависит от природы «акцептора водорода» («основания»). Чем сильнее основание, тем больше вероятность того, что данное соединение будет вести себя по отношению к нему как кислота:
Межмолекулярные водородные связи, возникающие между молекулами карбоновых кислот, настолько прочны, что даже в газообразном состоянии значительная часть молекул существует в виде димеров:
С ростом углеводородной цепи способность кислот к образованию водородных связей уменьшается.
Источник
Промышленные способы получения карбоновых кислот
1. Окисление углеводородов. Существует два способа: окисление низших алканов C4-C8 преимущественно в уксусную кислоту и окисление твердого парафина в так называемые синтетические жирные кислоты (СЖК) с прямой цепью углеродных атомов С10-С20, являющихся сырьем для синтеза ПАВ (поверхностно-активных веществ).
Процесс протекает в жидкой фазе при нагревании или в присутствии катализаторов. При окислении алканов происходит деструкция по связям между вторичными углеродными атомами, поэтому из н-бутана образуется главным образом уксусная кислота, а в качестве побочных продуктов – метилэтилкетон и этилацетат.
2.Синтезы на основе оксида углерода (II). Карбоновые кислоты получают на основе оксида углерода по реакции карбонилирования:
Присоединение по двойной связи при кислотном катализе всегда протекает по правилу Марковникова, вследствие этого только из этилена получается неразветвленная кислота, а из его гомологов — α-метилзамещенные кислоты. Особый интерес данный метод представляет для синтеза кислот с третичным радикалом (неокислот) из изоолефинов (реакция Коха):
Механизм реакции состоит в предварительном протонировании алкена кислотой с образованием иона карбения, его взаимодействия с СО с получением ацилий – катиона и реакции последнего с водой с образованием карбоновой кислоты:
Неокислоты и их соли обладают очень высокой растворимостью и вязкостью, а их сложные эфиры — стабильностью к гидролизу, что обеспечивает им широкое применение в ряде отраслей.
Карбонилирование спиртов катализируется комплексами металлов (Ni, Со, Fe, Pd). Процесс реализован в промышленности для синтеза уксусной кислоты из метанола и характеризуется высокими экономическими показателями.
Кислоты также получают окислением альдегидов (продукт оксосинтеза).
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Промышленные способы получения карбоновых кислота
Некоторые карбоновые кислоты встречаются в природе в свободном состоянии (муравьиная, уксусная, масляная, валериановая и др.). Однако, основным источником карбоновых кислот является органический синтез. Рассмотрим основные способы получения карбоновых кислот
Общие способы получения карбоновых кислот
1. Окисление первичных спиртов и альдегидов под действием различных окислителей
В качестве окислителей применяют KMnO4 и K2Cr2O7.
Например:
Для окисления альдегидов используются те же реагенты, что и для спиртов.
При окислении перманганатом калия происходит обесцвечивание фиолетово-розового раствора.
При окислении дихроматом калия — цвет меняется с оранжевого на зеленый.
А также для них характерны реакции «серебряного зеркала» и окисление гидроксидом меди (II) – качественные реакции альдегидов:
2. Гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода
В результате реакции образуются спирты, содержащие три группы ОН у одного атома углерода. Такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
3. Получение карбоновых кислот из цианидов (нитрилов)
Этот способ позволяет наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия:
Образующийся нитрил уксусной кислоты CH3-CN (ацетонитрил, метилцианид) при нагревании гидролизуется с образованием ацетата аммония:
При подкислении раствора выделяется кислота:
4. Использование реактива Гриньяра (по схеме)
5. Гидролиз галогенангидридов кислот
С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту:
В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов кислородом воздуха ( в присутствии катализаторов – солей марганца или при нагревании под давлением)
Обычно образуется смесь кислот. При окислении бутана единственным продуктом является уксусная кислота:
3. Окисление алкенов и алкинов
При жестком окислении алкенов кипящим раствором KMnO4 в кислой среде происходит полный разрыв двойной связи:
При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты:
4. Окисление гомологов бензола (получение бензойной кислоты)
Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия:
В лаборатории
1. Гидролиз сложных эфиров
При кислотном гидролизе получают карбоновые кислоты и спирты (реакция обратная этерификации):
2. Из солей карбоновых кислот
3. Гидролиз ангидридов кислот
При легком нагревании с водой ангидриды образуют соответствующие карбоновые кислоты:
4. Щелочной гидролиз галоген производных карбоновых кислот
Специфические способы получения важнейших кислот
Способы получения НСООН
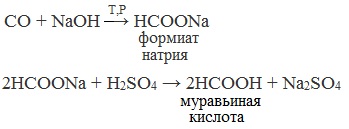
1. Взаимодействие оксида углерода (II) с гидроксидом натрия
Муравьиную кислоту получают нагреванием под давлением гидроксида натрия и оксида углерода (II) под давлением и обработкой полученного формиата натрия серной кислотой:
2. Каталитическое окисление метана
3. Декарбоксилирование щавелевой кислоты
Муравьиную кислоту можно получить при нагревании щавелевой кислоты:
Способы получения СН3СООН
Получение уксусной кислоты для химических целей
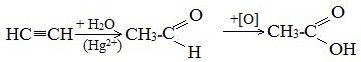
1. Синтез из ацетилена
Данный способ получения уксусной кислоты основан на окислении уксусного альдегида, который в свою очередь получают из ацетилена по реакции Кучерова (ацетилен получают из очень доступного сырья — метана):
2. Каталитическое окисление бутана
Большое значение имеет способ получения уксусной кислоты, основанный на окислении бутана кислородом воздуха:
Процесс получения уксусной кислоты из метана является многостадийным (метан – ацетилен – уксусный альдегид – уксусная кислота). Ее получение окислениям будана сокращает число стадий, что дает большой экономический эффект.
3. Каталитическое карбонилирование метанола
Получение уксусной кислоты для пищевых целей
4. Уксуснокислое брожение этанола
Уксусную кислоту для пищевых целей получают уксуснокислым брожением жидкостей, содержащих спирт (вино. пиво):
Источник