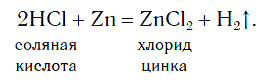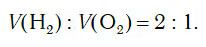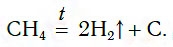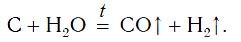- Урок 26. Получение водорода и его применение
- Получение водорода в лаборатории
- Получение водорода в промышленности
- Применение водорода
- Получение водорода
- Получение водорода в лаборатории
- Получение водорода в промышленности
- Водород и его свойства
- Что такое водород
- Нахождение в природе, изучение его свойств
- Химические и физические свойства
- Получение водорода, как добыть вытеснением из воды
- Получение и собирание водорода в домашних условиях, техника безопасности
- Особенности применения водорода
Урок 26. Получение водорода и его применение
В уроке 26 «Получение водорода и его применение» из курса «Химия для чайников» узнаем о получении водорода в лабораториях и в промышленности, а также выясним в каких отраслях промышленности его применяют.
Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:
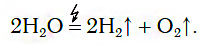
Из уравнения процесса разложения следует, что из 2 моль воды образуются 2 моль водорода и 1 моль кислорода. Следовательно, и соотношение объемов этих газов также равно:
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
Существуют и другие промышленные способы получения водорода.
Применение водорода
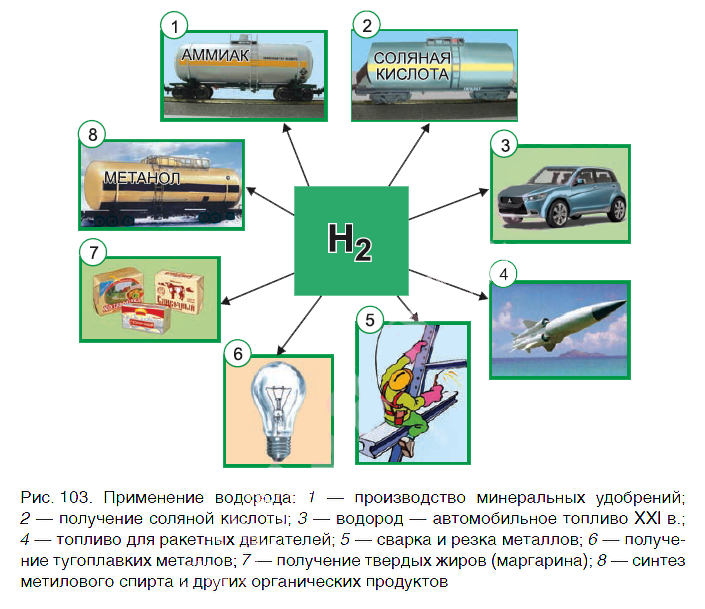
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 о С. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.
В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
- В лаборатории водород получают действием кислот на металлы.
- В промышленности для получения водорода используют доступное и дешевое сырье — природный газ, воду.
- Водород — это перспективный источник энергии XXI в.
Надеюсь урок 26 «Получение водорода и его применение» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Источник
Получение водорода
История открытия водорода История водорода начинается с XVI века, когда было замечено, что при действии кислот на железо и другие металлы выделяется некий неизвестный газ. Первоначально его назвали «горючим воздухом». Такое название газ получил из-за способности гореть. Во второй половине XVIII века английский ученый Генри Кавендиш получил водород при действии соляной кислоты HCl на цинк:
Zn + 2HCl = ZnCl2 + H2
Что же такое кислота с точки зрения химии? Кислота – это сложное вещество, в состав которого всегда входят атомы водорода. В формулах кислот атомы водорода принято писать на первом месте. Атомы, следующие в формуле за водородом, называют кислотным остатком. Так, в соляной кислоте HCl кислотный остаток – Cl.
Например, в серной кислоте H2SO4, кислотный остаток – SO4. Кислота – сложное вещество, в состав которого входят атомы водорода и кислотный остаток Генри Кавендиш изучил свойства «горючего воздуха». Он установил, что этот газ намного легче воздуха, а при сгорании на воздухе образует прозрачные капли жидкости. Этой жидкостью оказалась вода.
Генри Кавендиша считают первооткрывателем водорода. Вывод о том, что «горючий воздух» представляет собой простое вещество, был сделан в 1784 году французским химиком Антуаном Лораном Лавуазье. Антуан Лоран Лавуазье дал этому веществу латинское название (Hydrogenium), которое происходило от греческих слов «хюдор» – вода и «геннао» – рождаю. В те годы под элементами подразумевали простые вещества, которые нельзя далее разложить на составные части. Поэтому у химического элемента водорода такое же название, как и у просто вещества H2. Русское слово водород – это точный перевод латинского названия Hydrogenium.
Получение водорода в лаборатории
Современный лабораторный способ получения водорода не отличается от того, которым его получал Генри Кавендиш. Это реакции металлов с кислотами. В лаборатории водород получают в аппарате Киппа (рисунок 152).
Аппарат Киппа изготовляется из стекла и состоит из нескольких частей:
- реакционная колба с резервуаром;
- воронка с длинной трубкой;
- газоотводная трубка.
Реакционная колба имеет верхнюю шарообразную часть с отверстием, в которое вставляется газоотводная трубка, снабженная краном или зажимом, и нижний резервуар в виде полусферы. Нижний резервуар и реакционная колба разделены резиновой или пластиковой прокладкой с отверстием, через которое проходит в нижний резервуар длинная трубка воронки, доходящая почти до дна. На прокладку через боковое отверстие шпателем насыпают твёрдые вещества (мрамор, цинк). Отверстие закрывается пробкой с газоотводной трубкой. Затем при открытом кране или зажиме в верхнюю воронку заливается раствор кислоты. Когда уровень жидкости достигает вещества на прокладке, начинается химическая реакция с выделением газа. При закрытии крана давление выделяющегося газа выдавливает жидкость из реактора в верхнюю часть воронки. Реакция прекращается. Открытие крана приводит к возобновлению реакции. Поместим в реакционную колбу кусочки цинка. В качестве кислоты воспользуемся серной кислотой. При контакте цинка и серной кислоты протекает реакция:
Zn + H2SO4 = ZnSO4 + H2
Водородом можно заполнить мыльный пузырь.
Для этого необходимо опустить газоотводную трубку в мыльный раствор. На конце трубки начнется формирование мыльного пузыря, заполненного водородом; со временем пузырь отрывается и улетает вверх, что доказывает легкость водорода. Соберем выделяющийся водород. С учетом того, что водород намного легче воздуха, для сбора водорода сосуд, в котором собирается газ, необходимо располагать вверх дном, или производить собирание методом вытеснения воды. Как обнаружить водород? Заполним пробирку водородом, держа ее вверх дном, по отношению к газоотводной трубке. Поднесем пробирку отверстием к пламени спиртовки – слышится характерный хлопок.
Хлопок – это признак того, что в пробирке содержится водород. При поднесении пробирки к пламени водород вступает в реакцию с кислородом, содержащимся в воздухе. При малых количествах реакция кислорода и водорода сопровождается хлопком. Более подробно об этой реакции будет рассказано в следующем параграфе.
Получение водорода в промышленности
Одним из промышленных способов получения водорода является реакция разложения воды под действием электрического тока:
2H2O эл.ток → 2H2 + O2.
Данный метод позволяет получить чистый водород и кислород. Процесс превращения химических веществ в другие вещества под действием электричества называется электролизом.
Электролиз – химическая реакция, протекающая под действием электрического тока Проведем электролиз воды. В стакан наполненный водой, опустим металлические электроды. Поверх электродов опустим в стакан пробирки, заполненные водой. Подсоединим электроды к источнику тока – батарейке. В пробирках наблюдается выделение газов – водорода и кислорода, которые вытесняют воду. Наблюдая за процессом электролиза, можно заметить, что в одной из пробирок газа собирается в два раза больше, чем в другой. Проанализировав уравнение реакции электролиза воды, можно сделать вывод, в какой пробирке выделяется водород, а в какой – кислород. Попробуйте это сделать самостоятельно.
Существуют и другие способы получения водорода. Железо-паровой метод долгое время широко применялся в промышленности. Через электрическую трубчатую печь проходит трубка из нержавеющей стали, заполненная железными стружками. Через трубку с железными стружками пропускают водяной пар. При температуре около 800°С пары воды взаимодействуют с железом, образуя оксид Fe3O4 (железную окалину) и газообразный водород:
3Fe + 4Н2О = 4Н2 + Fe3O4.
Можно получить Н2, пропуская Н2О через слой раскаленного угля. При этом образуется смесь двух газов – СО и Н2 (водяной газ):
Н2О + С = CO + Н2
В настоящее время водород получают взаимодействием углеводородов (в основном метана, СН4) с водяным паром или неполным окислением метана кислородом:
2СН4 + О2 = 2СО + 4Н2
Итог статьи:
- В лаборатории водород получают в аппарате Киппа
- Исходными веществами для получения водорода в лаборатории являются некоторые металлы и кислоты
- Собирать водород нужно методом вытеснения воды, или методом вытеснения воздуха, расположив пробирку вверх дном по отношению к газоотводной трубке
- Кислота – сложное вещество, в состав которого входят атомы водорода и кислотный остаток
- Обнаружить водород можно по характерному хлопку при поднесении пробирки с водородом к пламени
- Одним из промышленных способов получения водорода является электролиз воды
- Электролиз – химическая реакция, протекающая под действием электрического тока
Источник
Водород и его свойства
Что такое водород
Водород — самый легкий химический элемент, занимающий в периодической таблице Менделеева начальное место.
Его атомный номер — единица. На одноатомную форму водорода приходится около 75% барионной массы, она считается самым распространенным веществом во всей Вселенной. Водородная плазма — основное вещество звезд, за исключением компактных.
У водорода три изотопа:
К общим характеристикам относятся следующие свойства: не имеет цвета запаха, вкуса. Двухатомная форма ( Н 2 ) нетоксична, однако в соединении с воздухом (или О 2 ) пожароопасна и склонна к взрывам. Взрывоопасность также проявляется в присутствии прочих газов-окислителей, например, фтора, хлора.
На Земле водород присутствует в составе молекулярных соединений, например, вода. Его роль в кислотно-основных реакциях трудно переоценить.
Нахождение в природе, изучение его свойств
Звездная температура позволяет существовать водороду в виде плазмы. Это примерно 6000оС. Однако пространство между звездами заполнено отдельными молекулами, атомами и ионами, которые зачастую образовывают молекулярные скопления различных размеров и форм — облака. Плотность вещества при этом не является постоянной величиной, как и его температура.
В коре Земли водород считается десятым по распространенности элементом. Его массовая доля равна 1%. В то же время по числу атомов он достигает 17%. Это второе место после кислорода, доля которого равна 52%. Отсюда и значительная роль водорода в природе, особенно в химических превращениях.
Водород, в отличие от кислорода, не может существовать в свободном состоянии, только в связанном. Исключение составляет атмосфера, в сухом остатке которой 0,00005% простого вещества — водорода.
Все органические вещества включают в свой состав водород. Велика его доля в живых клетках (по количеству атомов его удельный вес достигает 63%).
В составе воды водород имеет большое значение в протекании геохимических процессов. Так, вулканические газы вызывают истечение определенных количестве водорода вдоль разломов (причина — рифтогенез). По этой же причине часто обнаруживают водород в районе угольных месторождений.
Натуральные минералы могут содержать Н2 в виде ионов аммония, гидроксил-ионов и воды.
Причина появления молекул Н2 в атмосфере — разложение формальдегида — участника окисления метана и прочих органических соединений. Кроме того, причина его образования — неполное сгорание топлива и биомассы, фиксация азота некоторыми микроорганизмами, содержащимися в воздухе.
Молекулы водорода легкие, поэтому имеют высокую тепловую скорость. При попадании в верхние слои атмосферы такие молекулы часто улетают в космос, при этом их потери могут достигать 3 кг каждую секунду.
Химические и физические свойства
Начиная говорить о химических свойствах водорода, нужно отметить чрезвычайную прочность его двухатомной молекулы. Для того, чтобы она распалась и атомы могли провзаимодействовать с другими участниками химической реакции, необходима энергия:
1 2 H 2 → 2 H — 432 к Д Ж
Обычные температурные условия обеспечивают протекание реакций только с металлами высокой активности, к примеру, с кальцием:
1 2 C a + H 2 → C a H 2
Исключение составляет реакция с фтором, продуктом которой является фтороводород:
1 2 F 2 + H 2 → 2 H F
Если имеется возможность повышения температуры (либо при другом воздействии, к примеру, освещении), водород может вступать в реакцию с большинством металлов и неметаллов:
1 2 O 2 + 2 H 2 → 2 H 2 O
В реакциях с галогенами образуются галогеноводороды:
1 2 H 2 + F 2 → 2 H F (в темноте происходит взрыв)
1 2 H 2 + C l 2 → 2 H C l (на свету происходит взрыв)
В реакции с оксидами водород проявляет восстановительные свойства:
1 2 C u O + H 2 → H 2 O + C u
Высокая температура делает возможной реакцию с сажей:
1 2 C + 2 H 2 → C H 4
Когда активные металлы соединяются с водородом, образуются гидриды, например гидрид натрия (NaH), гидрид кальция (CaH2), гидрид магния (MgH2). Эти солеобразные твердые, легко гидролизирующиеся вещества:
1 2 C a H 2 + 2 H 2 → C a ( O H ) 2 + 2 H 2
Оксиды металлов, реагируя с водородом, восстанавливаются с выделением воды:
1 2 F e 2 O 3 + 3 H 2 → 2 F e + 3 H 2 O
Благодаря свойствам водорода, он нашел применение для восстановления органических веществ. Протекают реакции с участием катализатора, а также при высоких параметрах давления и температуры. К примеру, насыщенные алканы образуются в результате гидрирования ненасыщенных алкенов и алкинов.
Физические свойства водорода:
- В 14,5 раз легче воздуха. Поэтому молекулы движутся быстрее других молекул газов, передавая тепло.
- Имеет высокую теплопроводность (в 7 раз выше, чем у воздуха).
- Двухатомная молекула.
- Плотность — 0,08987 г/л, температура кипения-252,76оС, удельная теплота сгорания — 120,9*106Дж/кг, растворимость в воде — 18,8 мл/л
Хорошо растворяется в металлах, поэтому способен диффундировать в них. В серебре не растворим.
Получение водорода, как добыть вытеснением из воды
Потребление в мире водорода составляет порядка 75 млн т. Основная масса приходится на нефтепереработку и производство аммиака. Получение водорода для таких промышленных нужд происходит в основном из природного газа (его расход составляет 205 млрд м3). Оставшуюся часть берут из угля. Примерно 100 тыс т вырабатывают с помощью реакции электролиза.
Получение водорода сопровождается поступлением в атмосферу 830 млн т углекислого газа. Стоимость получения водорода из газа составляет от полутора до трех долларов за каждый кг.
Получение водорода методом электролиза в химии выглядит так:
1 2 2 N a C l + 2 H 2 O → 2 N a O H + C l 2 + H 2
Метод конверсии метана при температуре 1000оС с водяными парами:
1 2 C H 4 + H 2 O ↔ C O + 3 H 2
Следующий способ получения — пропускание водяных паров над горящим коксом (температура не менее 1000оС):
1 2 H 2 O + С ↔ С O + H 2
Свободный водород выделяется в результате реакции катализа окислением кислородом:
1 2 2 C H 4 + O 2 ↔ 2 C O + 4 H 2
В промышленности H2 часто получают путем электролиза водных растворов активных металлов:
1 2 2 H 2 O → 4 e — 2 H 2 ↑ + O 2 ↑
а также путем крекинга и риформинга углеводородов при переработке нефти.
Существуют способы получения Н2 лабораторными способами:
- Металл + разбавленная кислота: 1 2 Z n + H 2 S O 4 → Z n S O 4 + H 2 ↑
- Реакция кальция с водой: 1 2 C a + 2 H 2 O → C a ( O H ) 2 + H 2 ↑
- Гидролиз гидридов металлов: 1 2 N a H + H 2 O → N a O H + H 2 ↑
- Взаимодействие щелочи с цинком (алюминием): 1 2 2 A l + 2 N a O H + 6 H 2 O → 2 N a ( A l ( O H ) 4 ) + 3 H 2
- В результате электролиза водных растворов щелочей либо кислот: 1 2 2 H 3 O + + 2 e — → 2 H 2 O + H 2 ↑
В промышленности используется очистка водорода из сырья, которое содержит углерод (в частности — водородсодержащий газ ВСГ). Методы следующие:
- ВСГ придают температуру конденсации метана и этана -158оС и давление 4МПа. При концентрации в сырье 40% процент очищенного водорода доходит до 93-94%. Такой метод называется низкотемпературной конденсацией.
- Адсорбционное выделение на цеолитах.
- Абсорбционное выделение жидкими растворителями.
- Мембранное концентрирование.
- Селективное поглощение металлами.
Получение и собирание водорода в домашних условиях, техника безопасности
Реальным способом получения водорода в домашних условиях является реакция щелочи с алюминием. Газ получается гораздо чище, чем в реакции с кислотой. Схема следующая. В качестве алюминия используют фольгу, щелочного раствора — средство «Крот».
Берем стеклянную емкость, засыпаем в нее немного средства против засора «Крот» и наливаем 100 г воды обычной температуры. Перемешиваем до полного растворения и помещаем сюда же фольгу, скатанную в небольшие шарики. Выделение тепла свидетельствует о начале реакции, после чего ее скорость активируется. Через 20-60 секунд можно добавить новую порцию фольги.
Чтобы образовавшийся водород собрать, можно закрыть банку крышкой, сделав в ней отверстие, в которое вставить трубку. Второй конец трубки закрепить в воздушном шарике.
Поскольку водород является взрывоопасным веществом, делать это нужно крайне осторожно, начиная от момента возможного вытеснения крышки до конца процесса. Попадание водорода в воду приведет к образованию вещества, способного вызвать обморожение.
Особенности применения водорода
Водород используется во многих производственных сферах, что отражено в таблице:
| Применение | Доля |
| Производство аммиака | 54 % |
| Нефтепереработка и химическая промышленность | 35 % |
| Производство электроники | 6 % |
| Металлургия и стекольная промышленность | 3 % |
| Пищевая промышленность | 2 % |
В химической промышленности активный водород идет на производство аммиака (50%), метанола (8%). В нефтеперерабатывающей — для гидрокрекинга и гидроочистки. На эти цели расходуется около 37% всего водорода, что производится.
Пищевая и косметическая промышленность «пользуется» водородом для производства пищевых добавок, а также саломаса, маргарина, мыла, косметических продуктов.
Для химических лабораторий водород — газ-носитель для газовой хроматографии, а для метеорологии — наполнитель оболочек метеозондов.
Водород — ценное ракетное топливо, однако, ввиду незначительного диапазона температур, используется смесь жидкой и твердой фаз.
В электроэнергетике водород применяют для охлаждения электрогенераторов. Его высокая теплопроводность позволяет использовать газ для заполнения сфер гирокомпасов и колб LED-лампочек.
Источник