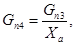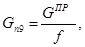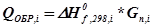- Получение уксусной кислоты
- 14. Получение уксусной кислоты биотехнологическим способом.
- 15. Получение и использование аминокислот.
- Биотехнологические процессы получения органических кислот.
- Дипломная работа: Микробиологический синтез уксусной кислоты
- Список использованной литературы
- Для промышленного производства уксусной кислоты в качестве субстрата применяют этиловый спирт – получаемый сбраживанием углеводов дрожжами, либо используется технический спирт. В нашем случае мы используем спирт полученный сбраживанием углеводов.
- Сырьем для современных способов быстрого уксусного брожения служит в настоящее время почти исключительно дешевый спирт, который обычно поступает из спиртовой промышленности (картофельный или зерновой), однако может применяться и синтетический этиловый спирт. Он применяется в виде водного раствора с концентрацией 4—11% об. Так как уксуснокислые бактерии не могут размножаться в чистом водно-спиртовом растворе, добавляются в качестве органических углеводных источников мелассы тростниковый сахар или глюкоза, в качестве неорганических питательных солей — фосфат аммония и калия, сульфат магния, а в качестве микроэлементов— ионы марганца. В качестве биологически активного вещества служит солодовый или дрожжевой экстракт [3, 5].
- 1.6.2. Быстрый способ уксусного брожения
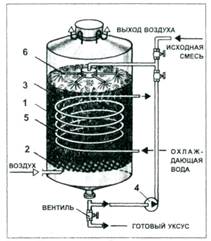
- Рис. 2. Аппарат Фрингса: 1 – корпус; 2 – ложное перфорированное днище; 3 – слой буковых стружек; 4 – циркуляционный насос; 5 – змеевик системы термостатирования; 6 – распределительное устройство.
- Генераторы Фрингса, также могут быть изготовлены из древесины (рис. 3.). Как правило, это древесина лиственницы или дуба. Они работают с выходом этилового спирта до 80—95% от теоретически возможного. Из затора с 11% об. спирта и 8 г уксусной кислоты на 1 л образуется уксус со 107 г уксусной кислоты и 0,3% спирта. Уксус из сборной емкости у днища генератора отводится в танк и выдерживается [2, 5].
- Но и у этого метода есть существенные недостатки, главным из которых размер аппарата. В начале шестидесятых годов 20 века появилась технология, при которой уксуснокислые бактерии стали культивировать в специальных аппаратах – ферментерах в жидкости, — так называемый метод периодического глубинного культивирования [7].
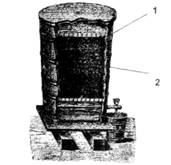
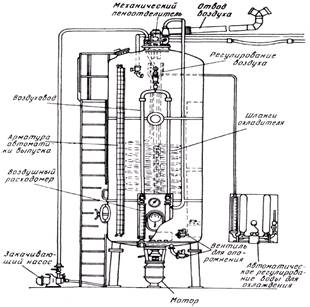
- 1.6.3 Глубинный способ с использованием ацетатора
- Краткое описание свойств уксусной кислоты и ее констант.
Получение уксусной кислоты
Биотехнология получение органических кислот.
В настоящее время биотехнологическими (микро-) способами в промышленных масштабах синтезируют ряд органических кислот, лимонная, итаконовая, глюконовая, 2-кетоглюконовая, уксусная, молочная. Из них лимонную, глюконовую, кетоглюконовую и итаконовые кислоты получают лишь микробиологическ5им способом, молочную салициловую и уксусную – как химическим, так и микробиологическим способами, а яблочную – химическим и энзиматическим.
Органические кислоты используют в пищевой, химической, фармацевтической, легкой промышленности, в быту.
Микробиологические процессы получения органических кислот можно разделить на две группы: анаэробные (молочная, пропионовая) и аэробные (уксусная, лимонная, итаконовая, глюконовая). Все органические кислоты являются промежуточными или конечными продуктами катаболизма углеводов.
Получение лимонной кислоты. Производство лимонной кислоты принадлежит к числу старейших промышленных микробиологических процессов – было организовано в 1893 г. Из всех органических кислот по объему производства лимонная кислота занимает 1-е место в мире- составляет около 400 тыс.т в год.
В настоящее время в качестве продуцента лимонной кислоты применяются различные мутантные штаммы A.niger. Используемые в производстве штаммы отличаются большой скоростью роста, легкостью культивирования и высоким выходом ЛК (98-99% в расчете на потребленную сахарозу).
В процессе ферментации можно выделить 2 фазы: 1) активного роста гриба и 2) интенсивного кислотообразования, рост мицелия в этот период становится незначительным. Лимонная кислота накапливается вначале в клетках, а затем выделяется в среду.
Сверхсинтез лимонной кислоты происходит при лимитировании роста грибов минеральными компонентами среды и одновременно избыточном содержании источника углерода. Основным сырьем для производства лимонной кислоты является меласса. Известны два способа ферментации Asp.niger – поверхностный и глубинный.
Для промышленного получения уксуса используют штаммы Acetobacter aceti, A.pasterianus или A.peroxidans, A.xylinum, а также G.oxydans и несколько подвидов этого вида. В качестве сырья для получения пищевого уксуса используют вино, пивное сусло, мед, соки различных фруктов и ягод после спиртового брожения или водный раствор этилового спирта.
Самой старой технологией получения столового уксуса лучшего качества был так называемый медленный, или орлеанский (французкий) процесс, в котором исходным сырьем было легкое виноградное вино, которым на 3/5 заполняли плоские деревянные чаны и туда же наливали столовый уксус, заполняя оставшиеся 2/5 объема. На поверхности смеси развивалась пленка ацетобактерий. После завершения окисления этанола отбирали из чана 10% жидкости, а взамен добавляли столько же вина.
В настоящее время почти везде пищевой уксус согласно так называемому «генераторному», или немецкому (быстрому) процессу, впервые реализованному в 1832 г. Особенность его – создание максимальной поверхности для снабжения воздухом уксуснокислые бактерий и как следствие, быстрое окисление спирта в уксусную кислоту. Процесс ведут в специальных чанах – струйных генераторах.
Более прогрессивным методом считается погруженная ферментация, которую на Западе проводят в ацетаторах Фрингса, в них возможно осуществление хорошей контролируемой аэрации.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
14. Получение уксусной кислоты биотехнологическим способом.
Продуцентами уксусной кислоты являются уксуснокислые бактерии рода Acetobacter. Эти бактерии приспособлены к сахаристым и спиртовым субстратам, растут при сильно кислых условиях (рН = 4,0). К быстроокисляющим бактериям относят высокопроизводственный штамм Acetobacter curvum (курвум).
В качестве сырья для получения пищевого уксуса используют виноградное вино, пивное сусло, мед, соки различных фруктов и ягод после спиртового брожения или водный раствор этилового спирта для получения белого уксуса. Кроме спирта среда содержит уксусную кислоту и минеральные соли N, P, S, Mn, K. Иногда добавляют источники витаминов в виде различных экстрактов. Уксусная кислота служит источником углерода и энергии для бактерий.
Этот способ может быть непрерывным и периодическим. В течение длительного времени применяется адсорбирование уксуснокислых бактерий на древесной стружке, древесном угле, коксе и других субстратах. Пропуская раствор этанола через генераторы с иммобилизованными бактериями, получают 10-15 %-ный раствор уксусной кислоты. Из 100 л безводного спирта теоретически должно быть получено 103 л уксусной кислоты. На практике выход уксуса из 100 л этанола редко превышает 90 л, что связано с переокислением и неполным окислением этанола бактериями, а также с его испарением.
В столовом уксусе содержится 5-9 % уксусной кислоты. Уксус с концентрацией кислоты 20-30 % получают путем вымораживания исходного раствора. Путем перегонки получают 70-80 %-ную уксусную кислоту, называемую уксусной эссенцией. Ледяная уксусная кислота содержит 98,0-99,8 % кислоты.
Уксусную кислоту или уксус широко используют в пищевой промышленности. Уксус, полученный микробиологическим путем (пищевая уксусная кислота, столовый уксус), различается по сортам в зависимости от характера сбраживаемого субстрата. Известен яблочный, виноградный, грушевый и другие сорта уксуса.
15. Получение и использование аминокислот.
Существует несколько способов получения аминокислот. При производстве аминокислот могут быть использованы отходы мясоперерабатывающей промышленности (отходы обработки животного сырья, кровь и т.д.), яичный белок, казеин молока, клейковина пшеницы, соевый шрот и т.д. При переработке этого сырья все аминокислоты переходят в гидролизат, и для выделения отдельных аминокислот необходима сложная многостадийная очистка. Кроме того, само сырье считается дефицитным и дорогим, поэтому аминокислоты имеют высокую себестоимость.
Химический синтез аминокислот достаточно эффективен, однако его недостатком является то, что в процессе синтеза образуется смесь из биологически активной L-формы и D-изомера аминокислоты. D-форма является балластом, так как не усваивается животными и человеком, а некоторые D-формы аминокислот обладают токсическими свойствами. Разделение изомеров – дорогая и трудоемкая процедура. Синтетически производится незаменимая аминокислота метионин.
В настоящее время большую часть аминокислот производят с помощью микробного синтеза, причем микроорганизмы синтезируют только L-форму. Это значительно облегчает выделение и очистку аминокислот и позволяет получать препараты с низкой себестоимостью. Микроорганизмы, образующие аминокислоты, не накапливают их в клетке, а постоянно выделяют в питательную среду. Поэтому аминокислоты выделяют из фильтрата культуральной жидкости.
Глутаминовая кислота – первая аминокислота, полученная микробным синтезом. В промышленном производстве используют бактерии Corinebacterium glutamicum и Brevibacterium flavum и др. Условия сверхсинтеза глутамата натрия следующие.
Лизин образуют многие микроорганизмы: бактерии, актиномицеты, сине-зеленые водоросли, некоторые виды микроскопических грибов.
Триптофан образуют микроорганизмы бактериального и грибного происхождения: Aerobacter, Bacillus, Escherichia (E. coli), Sacсharomyces (S. сerevisiae), Candida и другие.
Некоторые аминокислоты используют в качестве приправ, так как они обладают определенными вкусовыми свойствами и могут сообщать продукту приятные аромат и вкус. Большое распространение имеет глутаминовая кислота и ее натриевая соль (глутамат натрия), которая является эффективным усилителем вкуса мясных и овощных блюд. Данную аминокислоту добавляют во многие продукты при консервировании, замораживании и длительном хранении. Растет спрос на глицин и аланин, которые также применяют в качестве приправ.
Источник
Биотехнологические процессы получения органических кислот.
Органические кислоты и их соли широко используются в пищевой, фармацевтической, кожевенной, текстильной, химической, металлургической и других отраслях промышленности. Большинство кислот, используемых для технических нужд, производится химическим путем на основе нефтехимического сырья и продуктов сухой перегонки древесины. В тех случаях, когда химический синтез кислот является сложным и экономически невыгодным, или если они имеют пищевое или медицинское назначение, кислоты производят микробиологическим путем. С помощью микроорганизмов может быть получено более 50 различных органических кислот, методы получения их разработаны достаточно подробно. В настоящее время только 6 органических кислот производится биотехнологическим путем в промышленном масштабе. Причем лимонную, глюконовую, кетоглюконовую и итаконовую кислоты производят только микробиологическим путем, а молочную и уксусную — как химическим, так и микробиологическим методами.
Уксусная кислота имеет наибольшее значение среди органических кислот. Ее используют при выработке многих химических веществ, включая каучук, пластмассы, волокна, инсектициды. Микробиологический способ производства уксусной кислоты состоит в превращении этанола в уксусную кислоту при участии бактерий Acetobacter иGluconobacter.Процесс идет в анаэробных условиях в режиме непрерывного культивирования продуцента.
Лимонную кислотушироко используют в пищевой (приготовление соков, кондитерских изделий), фармацевтической и косметической промышленности. Ею заменяют фосфаты в составе детергентов, так как она полностью метаболизируется живыми организмами и не загрязняет окружающую среду. Лимонная кислота образует хелаты с металлами, поэтому ее применяют для их очистки. Производят лимонную кислоту из сахара или из отходов его производства – мелассы, из содержащих глюкозу гидролизатов древесины и зерна. Мировое производство лимонной кислоты составляет более 300 тыс.т в год. Для промышленного производства лимонной кислоты используют, главным образом, культуру грибаAspergillus nigerиA. wentii.
Глюконовая, кетоглюконовая, итаконовая и молочная кислоты используются в пищевой промышленности в качестве подкислителей. Глюконат натрия, в виде которого обычно выделяют глюконовую кислоту, используют для извлечения металлов из руд, борьбы с коррозией, как моющее средство, в качестве медицинского препарата. Итаконовая кислота применяется при производстве пластмасс и красителей. Молочную кислоту используют при выделке кож и как сырье для производства биоразлагаемого полимера полилактата.
Получение продуктов брожения. Интенсивные технологии получения этанола.
Для производства спирта используют любое крахмалсодержащее сырье (все виды зерновых культур, картофель). Также используют сахаросодержащее сырье: свеклосахарную, тростниковую, сырцовую мелассу, сахар-сырец и др.
Технология производства этилового спирта состоит из ряда последовательных стадий: подготовка крахмалсодержащего сырья, разваривание крахмалсодержащего сырья, осахаривание разваренной массы, приготовление дрожжей, сбраживание осахаренного сусла, выделение спирта из бражки и его ректификация.
Подготовка крахмалсодержащего сырья включает его очистку от примесей, измельчение зерна на молотковых или вальцовых дробилках до частиц размером менее 3 мм. Очистка картофеля происходит на гидравлическом транспортере, затем его моют в картофелемоечных машинах и измельчают на молотковых дробилках или картофелетерках.
Измельченное сырье смешивается с теплой водой в соотношении 1 : 2,5–3,5. После перемешивания зерновой замес (или картофельная кашица) поступает в аппарат для разваривания, цель которого заключается в разрушении клеточной структуры сырья и растворении крахмала. Разваривание проводят в цилиндроконических аппаратах при нагревании острым паром под давлением не менее 0,4–0,6 МПа.
Процесс разваривания может проводиться периодическим, полунепрерывным или непрерывным способами. Наиболее распространено непрерывное разваривание. Измельченное сырье подогревается сначала вторичным, затем острым паром до температуры разваривания и выдерживается при этой температуре, продвигаясь по варочным аппаратам.
После 1 ч пропаривания при 90 °С в результате открытия нижнего клапана и резкого падения давления происходит как бы взрыв пропаренного сырья, и оно продавливается в аппарат (затиратель).
Разваренную массу охлаждают до температуры +57…61 °С (в зависимости от вида осахаривающего материала и способа осахаривания). Осахаривание охлажденной разваренной массы осахаривающими материалами (солодовым молоком или ферментными препаратами) проводят периодическим или непрерывным способом.
В результате получают продукт – сусло спиртового производства. Оно имеет массовую долю сухого вещества 16-18%, в том числе 13-15% сбраживаемых Сахаров. Оса харенное сусло (затор) охлаждают до температуры +18…22 °С в теплообменниках или с помощью вакуума.
Дата добавления: 2020-04-08 ; просмотров: 554 ; Мы поможем в написании вашей работы!
Источник
Дипломная работа: Микробиологический синтез уксусной кислоты
| Название: Микробиологический синтез уксусной кислоты Раздел: Рефераты по биологии Тип: дипломная работа Добавлен 15:50:50 08 декабря 2010 Похожие работы Просмотров: 1609 Комментариев: 13 Оценило: 3 человек Средний балл: 4.7 Оценка: неизвестно Скачать | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Р, мас.% | 3,0 | 5,9 | 8,0 | 9,3 | 10,0 |
| S, об.% | 2,6 | 1,8 | 1,6 | 0,9 | 0,2 – 0,15 |
Ферментацию проводят в батарее, состоящей из пяти последовательно соединенных ферментаторов. Каждый аппарат снабжен мешалкой, барботером и змеевиковым теплообменником. В первый ферментатор загружается посевной материал, и непрерывно подаются питательная среда, в которой суммарная концентрация этилового спирта и уксусной кислоты составляет 6,4—6,7%, а также стерильный воздух. При этом создаются оптимальные условия для быстрого размножения уксуснокислых бактерий. Первый ферментатор является генератором уксуснокислых бактерий для всех последующих аппаратов; в нем также происходит окисление этилового спирта в уксусную кислоту.
Культуральная жидкость передается из ферментатора в ферментатор за счет давления, создаваемого воздухом. В каждом ферментаторе обеспечиваются условия, способствующие интенсивному окислению этилового спирта в уксусную кислоту. Для поддержания нужной концентрации спирта во второй, третий и четвертый аппараты добавляют 40%-ный этиловый спирт. Содержание спирта и уксусной кислоты в каждом ферментаторе в течение процесса указано в таблице 1. Температура и интенсивность аэрации от ферментатора к ферментатору снижаются: если в первом аппарате температура равна 28 °С, а интенсивность аэрации 0,35—0,40 м3/(м3•мин), то в последнем аппарате соответственно 25 °С и 0,1—0,15 м3/(м3•мин). Культуральная жидкость выводится из пятого ферментатора с концентрацией уксусной кислоты не ниже 9% и не выше 9,3%. Из 100 л безводного этилового спирта получают 75—90 кг уксусной кислоты [2, 4, 6, 7].
Данный метод достаточно быстро был внедрен в производство на нескольких заводах. Сейчас по этой технологии работают Экспериментальный пищекомбинат в Балашихе, уксусные цеха в городах Горловка и Днепродзержинск на Украине, завод в Словакии [7].
Из всех рассмотренных способов один уже не применяется, второй скоро полностью покинет производственный процесс, а оставшиеся три последних метода являются применяемыми и развиваемыми методами производства.
Для своей работы я выбираю последний метод получения уксусной кислоты, проточное культивирование. Этот метод наиболее выгоден, так как выход продукта составляет 90% и более; процесс идет с более полной степенью превращения исходного сырья; существует возможность увеличения объема получаемого продукта, добавлением этилового спирта непосредственно во время процесса, во второй, в третий, четвертый и пятый аппараты установки; снижаются затраты на производство, так как основная часть уксуснокислых бактерий получается в первом аппарате, а в остальных идет, по большей части, окисление этилового спирта в уксусную кислоту и поддержание процессов жизнедеятельности уксуснокислых бактерий. Также, данный метод был выбран и потому, что он разработан сравнительно не давно и является достаточно перспективным.
1.7 Принципиальная технологическая схема получения уксусной кислоты
После рассмотрения методов получения уксусной кислоты, и после того как был определен основной метод. Можно представить принципиальную технологическую схему получения уксусной кислоты применяемую, непосредственно в процессе получения.
Как, уже было сказано раннее, ферментацию проводят в батарее, состоящей из пяти последовательно соединенных ферментаторов. Каждый аппарат снабжен мешалкой, барботером и змеевиковым теплообменником. Но, при этом нужно учитывать, что процесс начинается не в ферментаторах, а в лаборатории, где получают посевной материал, выращивая уксуснокислые бактерии на жидкой питательной среде в колбах на качалках. А затем в лабораторном ферментаторе вместимостью 30 л [4, 6].
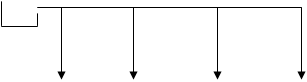
Из выше сказанного можно сделать соответствующие выводы о виде принципиальной схемы.
 |

 |
 |
 |


 |  |  |  |
 | |||
 |

Схема 1. 1 – колба, 2 – лабораторный ферментатор (30 л.), 3 – батарея: 3.1 – напорный бак для исходной питательной среды, 3.2 – бак напорный для этанола, 3.3 , 3.4, 3.5, 3.6 – ферментаторы, 4 – сборник готового уксуса.
Можно сказать, что данная схема не ограничивается тем, что на ней изображено, это связано с различными применяемыми стадиями очистки и стадиями доведения продукта до товарных форм.
1.8 Очистка и подготовка полученного продукта к применению
1.8.1 Обработка сырого уксуса
При стоянии качества уксуса улучшаются (это не относится к «белому» уксусу). Улучшение качества может быть обусловлено образованием эфиров с этанолом, который остается после ферментации. При стоянии преципитирующий материал осаждается, что облегчает последующие операции [2].
Для осветления в раствор уксусной кислоты добавляют бентонит и небольшое количество лимонной кислоты. После перемешивания осветленный раствор уксусной кислоты подают на фильтр-пресс. Фильтрацию осуществляют через фильтры с диатомовой землей. Можно применять ультрафильтрацию, которая удобна для проточного культивирования. Фильтрат, представляющий собой 9%-ную уксусную кислоту (столовый уксус), подают в сборник готового продукта, из которого осуществляют розлив [2, 4].
1.8.3 Концентрирование уксусной кислоты
В столовом уксусе содержится 5—9% кислоты (в СССР) или 4% (США), получаемой из 10—13%-го уксуса. Уксус с концентрацией 20—30% кислоты получают путем вымораживания исходного раствора. Лед, который образуется в этом процессе, отбрасывается. Процесс концентрирования довольно дорог. Путем перегонки получают 70—80%-ю уксусную кислоту, называемую уксусной эссенцией. Ледяная уксусная кислота содержит 98—99,8% кислоты [2].
Чтобы обеспечить длительную стойкость, уксус пастеризуется до или после розлива. Для этого достаточно короткого нагревания до 60 – 65 ºС. Иногда применяют химическое консервирование, например ионами серебра [5].
Уксус применяют в значительном количестве в домашнем хозяйстве и в промышленности пищевых продуктов для заквашивания и в качестве приправы к кушаньям, особенно салатам, а также для консервирования овощей, таких, как цветная капуста и огурцы (маринованные овощи), а также грибов и рыбных продуктов, для изготовления горчицы и майонеза. Уксус, полученный с помощью уксуснокислых бактерий, называется спиртовым уксусом, однако для пищевых целей применяют и уксус, полученный синтетическим путем. Также уксус (уксусную кислоту) используют для растворения органических красителей, при получении медикаментов, пластмасс, синтетических волокон [2, 5].
1.10 Вредители уксуса
1.10.1 Микробные поражения
Микробные поражения вызываются, прежде всего, вследствие образования слизистых веществ и расщепления уксусной кислоты. Хотя различные виды уксусных бактерий могут образовывать слизистые вещества, наибольшие трудности вызываются, по-видимому, только видом Acetobacter . В чанах для окисления, например в генераторе Frings, из-за слизи может нарушаться аэрация и сильно сокращаться образование уксуса.
Многие микроорганизмы и среди них гифомицеты, мицелиальные дрожжи и сами уксуснокислые бактерии могут расщеплять разведенную уксусную кислоту на углекислый газ и воду:
СН3СООН + 2О2 → СО2 + 2Н2О
Во время изготовления уксуса расщепление уксусной кислоты наступает тогда, когда недостает спирта или имеется избыток воздуха [2, 5].
1.10.2 Немикробные вредители
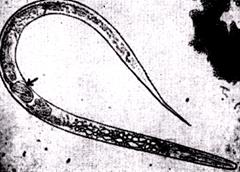
На уксусных предприятиях и в округе встречаются в массовом количестве различные виды клещей и дрозофилы обыкновенной (Drosophila ). С ними можно относительно легко бороться, применяя инсектициды. Уксусная угрица (Anguillula aceti ) (рис. 6)
Рис. 6. — Женская особь с приплодом в различных стадиях развития (увеличено в 120 раз).
Может проникать в уксусные чаны, исключая глубинные установки, размножаться в них и вызывать существенные трудности и потери. Живородящие нематодыдлиной 2 мм и толщиной 0,04 мм для человека безвредны, однако вызывают помутнение, а также вкусовой брак и неприятный запах уксуса. Их можно уничтожить нагреванием до 54°С или обработкой сернистым газом, а затем относительно легко отфильтровать [2, 5].
В литературном обзоре было проведено исследование основных способов микробиологического синтеза уксусной кислоты, выбран метод получения, который рассматривается как основной.
В ходе исследования синтеза было рассмотрено несколько методов получения, из которых один уже не используется это «Орлеанский метод», так как он морально устарел. Следующий метод, который был рассмотрен это «быстрый способ уксусного брожения», этот метод достаточно производителен в особенности по непрерывной схеме, но он также вытесняется более современными методами. На данный момент широкое распространение имеют «глубинные методы». «Глубинный метод с использованием ацетатора», «двустадийный глубинный полупроточный процесс» и «проточное культивирование» эти три метода имеют свои преимущества и недостатки, но все они сейчас используются в промышленном синтезе уксусной кислоты, как наиболее современные методы. Метод «проточного культивирования» был выбран как основной метод получения уксусной кислоты в данной работе.
Так же в литературном обзоре были рассмотрены продуценты уксусной кислоты, стадии подготовки исходного сырья, подготовки питательной среды, получения посевного материала, очистки полученного продукта и подготовки к применению, применение уксуса и вредители уксуса. Была рассмотрена химия получения уксусной кислоты.
2. Технологическая схема микробиологического синтеза уксусной кислоты
На рис. 7 изображена технологическая схема микробиологического синтеза уксусной кислоты. Римскими цифрами обозначены основные материальные потоки, арабскими цифрами обозначено технологическое оборудование.
1. – инокулятор для получения посевного материала; 2. – реактор для приготовления питательной среды; 3. – напорный бак для питательной среды; 4. – напорный бак для этанола; 5. – вихревой насос; 6. – паровая колона для подогрева питательной среды до температуры стерилизации; 7. – выдерживатель питательных сред при температуре стерилизации; 8. – теплообменник для охлаждения стерильных питательных сред; 9. – ферментатор; 10. – компрессор; 11. – осветлитель; 12. – фильтр пресс; 13. – сборник готового очищенного продукта; 14. – фасовочный аппарат.
Ферментацию проводят в батарее, состоящей из пяти последовательно соединенных ферментаторов. Каждый аппарат снабжен мешалкой, барботером и змеевиковым теплообменником. В первый ферментатор загружается посевной материал, и непрерывно подаются питательная среда, а также стерильный воздух. При этом создаются оптимальные условия для быстрого размножения уксуснокислых бактерий. Первый ферментатор является генератором уксуснокислых бактерий для всех последующих аппаратов; в нем также происходит окисление этилового спирта в уксусную кислоту.
Культуральная жидкость передается из ферментатора в ферментатор за счет давления, создаваемого воздухом. В каждом ферментаторе обеспечиваются условия, способствующие интенсивному окислению этилового спирта в уксусную кислоту. Для поддержания нужной концентрации спирта во второй, третий, четвертый и пятый аппараты добавляют 40%-ный этиловый спирт. Температура и интенсивность аэрации от ферментатора к ферментатору снижаются. Но при всем этом для процесса окисления требуется достаточно большие количества кислорода, который поступает с помощью компрессора, вместе с атмосферным воздухом, в каждый аппарат батареи, через барботер.
Посевную культуру уксуснокислых бактерий выращивают в лаборатории, в колбах на качалках, а затем в инокуляторе на жидкой питательной среде, после чего полученный посевной материал подают в первый ферментатор, где происходит генерация уксуснокислых бактерий.
Так же, в первый ферментатор подается питательная среда, которая проходит стадию стерилизации, данная стадия заключается в том, что питательную среду нагревают в паровой колоне до температуры стерилизации, затем подают в выдерживатель, где питательная среда находится заданное время при температуре стерилизации, после чего ее подают в теплообменник, где происходит охлаждение уже стерильной питательной среды, затем в напорный бак и после этого среда подается в ферментатор.
После того как культуральная жидкость пройдет через все пять аппаратов, она выходит из последнего с концентрацией уксусной кислоты не ниже 9 % и не выше 9,2 – 9,3 %. Воздух, который также выводиться из последнего аппарата уходит в атмосферу, не нуждаясь в какой – либо очистке, а культуральная жидкость попадает на стадию осветления. Ее осветляют бентонитом с добавлением небольшого количества лимонной кислоты. После перемешивания раствор уксуса подают на фильтр пресс, где из него отдельно выводятся отходы – это биомасса и бентонит, а так же отфильтрованный раствор уксуса, который поступает в сборник готового продукта, а затем на фасовочный аппарат (розлив).
Рис. 7. Технологическая схема микробиологического синтеза уксусной кислоты.
3. Расчет модели реактора на ЭВМ
Для расчета был выбран ферментатор, действующий по схеме реактора идеального смешения. Ферментатор выполнен из нержавеющей стали и снабжен мешалкой, барботером и змеевиковым теплообменником. Ферментатор используется для проведения процесса уксуснокислого брожения при глубинном культивировании. Исходным реагентом является смесь этилового спирта и затравки уксусной кислоты. Процесс идет при постоянной аэрации, т.к. уксуснокислые бактерии – строгие аэробы. Так как в ферментаторе протекает экзотермический процесс, и температура реакционной массы быстро поднимается, тепло нужно отводить (уксуснокислое брожение протекает при температуре 28 – 30 ºС), для этого используются специальные устройства, такие как теплообменники. В данном случае применяется встроенный внутрь реактора змеевиковый теплообменник (расчет на ЭВМ ведется для реактора с рубашечным теплообменником). В целях перемешивания реакционной массы и равномерного ее распределению по всему объему реактора, применяются устройства, которые называются мешалки. Мешалки бывают разнообразных видов: якорные, рамные, листовые, пропеллерные и т.д.
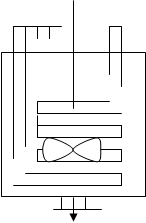 |
Рис. 8. Реактора со встроенным змеевиковым теплообменником
Механическое перемешивание (наиболее распространенное в промышленности) осуществляется при помощи мешалок различного типа. Каждая мешалка представляет собой ту или иную комбинацию лопастей, насажанных на вал.
Различают следующие типы мешалок:
Лопастные мешалки разделяются на:
1. собственно лопастные (для высоковязких сред)
2. листовые (для маловязких сред)
4. якорные (для высоковязких, способных налипать, сред)
5. Z– образные (применяются в резиновой промышленности для перемешивания клеев).
Пропеллерные мешалки в качестве рабочего органа имеют устройство, напоминающее гребной винт, лопасти которого укреплены на втулке, насажанной на вал. Диаметр лопастей dне должен превышать 0,2 – 0,33 диаметра корпуса D.
Окружная скорость вращения до 15 м/с.
Пропеллерные мешалки применяются для создания эмульсий, тонких суспензий и аэрозолей путем диспергирования газа в диспер


Для перемешивания и вязкопластичных сред используются шнековые и ленточные мешалки.
Теплообменные аппараты предназначены для передачи теплоты между различными средами. Теплообменные аппараты по назначению подразделяются на теплообменники, холодильники, конденсаторы и испарители. В теплообменниках теплота регенерируется жидкой или газообразной средами.
По роду теплоносителей в зависимости от их состояния теплообменные аппараты различаются на парожидкостные, жидкостно-жидкостные, газожидкостные, газо-газовые и парогазовые. Теплообменные аппараты по конфигурации поверхности теплообмена разделяют на трубчатые с прямыми трубками, змеевиковые, ребристые, спиральные, пластинчатые, а по компоновке ее – на кожухотрубчатые, типа «труба в трубе», оросительные и т.д. Наиболее распространены кожухотрубчатые теплообменные аппараты.
Реактор – это устройство, предназначенное для проведения химического процесса.
Существует несколько классификаций реакторов, приведем, только две основные:
1. По способу отвода и подвода исходного сырья и продукта реакции:
· Реактор периодического действия,
· Реактор непрерывного действия,
· Реактор полупереодического действия,
· Реактор полунепрерывного действия.
2. По гидродинамическому режиму:
Реактор идеального смешения периодического действия (РИСП).
Происходит мгновенное перемешивание исходных реагентов таким образом, что их концентрации во всех точках объема одинаковы.
Реактор идеального смешения непрерывного действия (РИСН).
Исходные реагенты загружаются в реактор непрерывно, продукты отводятся так же непрерывно.
Реактор идеального вытеснения (РИВ).
В РИВ реакционная масса движется в одном направлении с постоянной скоростью, без продольного и поперечного перемешивания. В виду схожести такого движения с движением поршня в цилиндре, его также называют поршневым.
Краткое описание свойств уксусной кислоты и ее констант.
Уксусная кислота СН3СООН – является типичным представителем органических кислород содержащих кислот. Она является бесцветной прозрачной жидкостью, более вязкой, чем вода (1,22 мПа*С) с характерным резким запахом. Данная кислота имеет плотность 1,05 г/см3 при 20 0С, поверхностное натяжение 27,8*103 Н/м, теплоемкость 0,49 ккал/кг*0С. СН3СООН смешивается в любых соотношениях с водой, эфиром благодаря своей природе и способности диссоциировать на ионы. Она хорошо растворяет серу, фосфор, галлоидоводороды. Безводная уксусная кислота (ледяная) является хорошим растворителем для многих органических соединений, но может вступать с ними в химическое взаимодействие и соответственно изменять их свойства.
СН3СООН является устойчивым к действию температур соединением: в газообразном состоянии она не разлагается при температуре около 400 0С. Имеет теплоту сгорания 3490 ккал/кг.
Уксусная кислота с химической точки зрения является типичной органической кислотой с соответствующими свойствами. Она реагирует с основаниями, спиртами, аминами. Вступает в реакции замещения атома водорода в СН3-группе на галоген, может образовывать ангидриды как внутри, так и межмолекулярные.
При попадании на кожу, как и все кислоты, вызывает ожоги. Ее пары оказывают раздражающее действие на слизистые оболочки дыхательных путей, глаз и могут повредить их.
СН3СООН широко используется при производстве ацетатов, полимерных материалов и композиций, эфиров и т.д. Данная кислота нашла свое применение и в пищевой, текстильной промышленности. Большое значение имеют производные данного соединения.
3.1 Алгоритм расчета
1. Конечная концентрация реагирующего компонента А.
Са к = Са 0 (1 – Ха к)
2. Численное дифференцирование интегральной и кинетической кривой.
3. Среднее время пребывания в реакторе идеального смешения.
τсм = (Са 0 — Са к) / Vrк
4. Объем реакционной массы.
6. Тепловая мощность реактора.
Q= qv[qtСа 0 Ха к – Cpρ (tk– tн)] / 3600
6. Расход хладагента
Gw= 3600 * Q/ [Gw(twk– tw)]
7. Диаметр реактора
8. Высота стенки
9. Площадь смоченной стенки.
10. Площадь элиптического днища.
11. Общая смоченная поверхность.
12. Средняя движущая сила.
Δtc= (twk– twн) / ln[(tk- twн) / (tk- twk)]
13. Средняя температура хладагента в режиме вытеснения.
14. Вязкость реакционной массы при средней температуре.
15. Вязкость хладагента.
16. Коэффициент Ренольдса в аппарате с мешалкой.
Re= ρwDм , где Dм = d0t* Dа
17. Коэффициент Прандтля в аппарате с мешалкой.
Pr= 1000 Ср μ / λ
18. Объемный расход воды.
19. Средняя скорость воды.
20. Коэффициент Ренольдса для хладагента в рубашке.
21. Коэффициент Прандтля для хладагента в рубашке.
Prх = 1000Cwμw/ λw
22. Коэффициент Нуссельта для аппарата с мешалкой.
Nu = 0.36 Re0.67 Pr0.33 (Pr/ Pr ст)0,14(Dм/ Da)
23. Коэффициент теплоотдачи
24. Удельная тепловая мощность реакционной массы.
25. Температура ржавчины со стороны воды.
tw= х — qг(rc+ δc/λc)
26. Коэффициент Нуссельта для хладагента в рубашке.
Nuх = 0,037 Reх0,8 Prх0,4 (Pr/ Prст)0,25, если Re> 5*105
27. Коэффициент теплоотдачи воды.
αх = Nuхλх / Dэ, где Dэ = 2δр
28. Удельная тепловая мощность от стенки к воде.
29. Средняя удельная тепловая мощность.
30. Необходимая поверхность теплопередачи.
31. Необходимая высота рубашки, если F 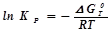
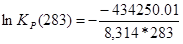
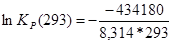
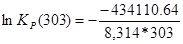
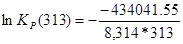
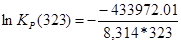
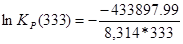
6) Построение таблицы по результатам расчета:
Таблица 6. Результатам расчета
| Т, К | 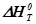 , Дж/моль , Дж/моль | 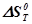 , Дж/К , Дж/К | 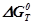 ,Дж ,Дж | lnKP | KP |
| 283 | — 439077,993 | — 17,06 | — 434250,01 | 184,56 | 1,42*1080 |
| 293 | — 439026,14 | — 16,54 | — 434180 | 178,24 | 2,56*1077 |
| 303 | — 438973,79 | — 16,05 | — 434110,64 | 172,33 | 6,95*1074 |
| 313 | — 438921,22 | — 15,59 | — 434041,55 | 166,79 | 2,73*1072 |
| 323 | — 438868,69 | — 15,16 | — 433972,01 | 161,60 | 1,52*1070 |
| 333 | — 438816,4 | — 14,77 | — 433897,99 | 156,72 | 1,16*1068 |
7) Выводы сделанные на основании термодинамического расчета.
Реакция экзотермическая, так как значение энтальпии на всем отрезке температур отрицательно. Поэтому в соответствии с принципом Ле Шателье, повышение температуры сдвигает равновесие в сторону образования исходных веществ.
Так же, в соответствии с принципом Ле Шателье, изменение давления сдвигает равновесие реакции в сторону образования продуктов реакции.
Равновесие реакции можно сдвинуть, вправо применив избыток спирта (увеличив подачу кислорода), или же постоянно удалять один из продуктов реакции – воду или уксусную кислоту.
Так как тепловой эффект реакции значительный, то необходимо выбрать реактор с каким-либо охлаждением. Таким образом, можно выбрать реактор, используемый в последнем, рассмотренном, в литературном обзоре, методе получение уксусной кислоты — проточное культивирование. В данном методе используется реактор с внутренним теплообменном, т.е. реактор со встроенным змеевиковым теплообменником.
Так же нужно указать, что данный термодинамический расчет выполнен для реакции описывающей приблизительно процесс синтеза уксусной кислоты, так как сам микробиологический процесс на много сложнее и его описание представляет довольно большие трудности, связанные с большим количеством стадий проходящих биологических процессов. Отсюда можно сказать, что данный расчет не имеет особого практического интереса для данной работы.
5. Материальный баланс стадии синтеза
5.1 Исходные данные
СН3CH2ОН + О2 → СН3СООН + Н2О
Таблица 7. – Исходные данные
| Производительность реактора, G | 16,620 т/год |
| Число дней в году, n | 330 |
| Технологический выход продукта, f | 90% |
| Молярные соотношения исх. реагентов, A : B | 1:2,58 |
| Степень превращения, хА | 83% |
| Селективность реакций, Ф | 85% |
| Mr(СН3CH2ОН) | 46 г/моль |
| Mr(О2) | 32 г/моль |
| Mr(СН3СООН) | 60 г/моль |
| Mr(Н2О) | 18 г/моль |
1) Практическая производительность реактора:

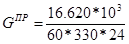
2) Состав исходной смеси: этанол и кислород.
Количество подаваемого этанола:
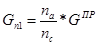
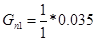
— с учетом технологического выхода:
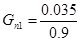
— с учетом селективности:
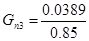
— с учетом степени превращения:
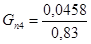
Количество непрореагировавшего этанола:
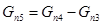
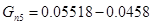
Количество подаваемого кислорода:
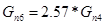
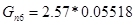
Количество кислорода пошедшего на реакцию:
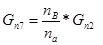
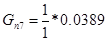
Количество кислорода непрореагировавшего:
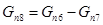
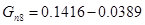
3) Конечная смесь имеет состав: этанол, кислород, уксусная кислота, вода.
Количество этанола и кислорода считать здесь не имеет смысла, так как они были посчитаны, как непрореагировавшие, выше.
Количество образовавшейся уксусной кислоты:
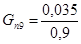
Количество образовавшейся воды:
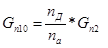
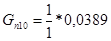
Таблица 8. — Результаты расчета материального баланса.
| Приход | ||||||
| Вещество | Gm | Gn | Gv | |||
| кг | % | кмоль/ч | % | м3/ч | % | |
| С2Н5ОН | 2,538 | 35,9 | 0,0552 | 28,05 | 1,236 | 27,9 |
| О2 | 4,531 | 64,1 | 0,1416 | 71,95 | 3,172 | 72,09 |
| Итого: | 7,069 | 100 | 0,1968 | 100 | 4,40 | 100 |
| Расход | ||||||
| Вещество | Gm | Gn | Gv | |||
| кг | % | кмоль/ч | % | м3/ч | % | |
| С2Н5ОН | 0,5315 | 7,54 | 0,0098 | 4,98 | 0,2195 | 4,99 |
| О2 | 3,386 | 48,02 | 0,109 | 55,44 | 2,442 | 55,54 |
| СН3СООН | 2,434 | 34,52 | 0,0389 | 19,79 | 0,8714 | 19,80 |
| Н2О | 0,7 | 9,92 | 0,0389 | 19,79 | 0,8714 | 19,80 |
| Итого: | 7,052 | 100 | 0,1966 | 100 | 4,40 | 100 |
5) Выводы расчетов материального баланса.
· практическая производительность реактора – 0,0389 кмоль/ч;
· технологические потери продукта – 0,0039 кмоль/ч;
· материальные потоки исходных веществ и продуктов реакции сведены в табл. 8.
· В данной работе материальный баланс не имеет никакого практического интереса по причине, того, что расчет произведен для основной реакции микробиологического синтеза уксусной кислоты, которая имеет очень сложный вид, связанный с прохождением биологических процессов.
6. Тепловой баланс стадии синтеза
6.1. Исходные данные
Таблица 9. — Исходные данные
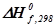
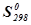
Температура исходных реагентов…………….10ºC= 283 К
Температура конечных продуктов……………30ºC= 303 К
Тепловые потери от прихода тепла…………..….4%
1) Теплоемкость исходных веществ:
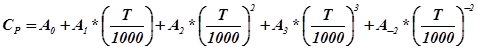
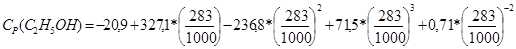
= 63,19 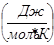
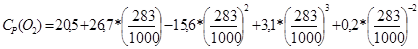
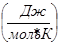
Средняя мольная теплоемкость исходных реагентов:
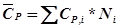
где Ni- процентное содержание i- го компонента в мольном потоке (в приходе)
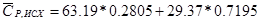
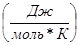
2) Количество теплоты, вносимое с исходными реагентами:
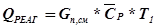
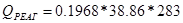
3) Расчет теплоты химической реакции:
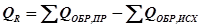
Исх.: 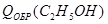
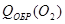
Пр.: 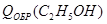
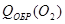
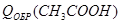
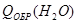
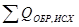
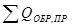
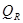
4) Теплоемкость продуктов реакции
5) 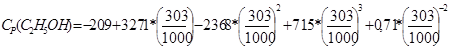
= 66,19 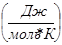
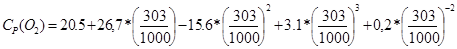
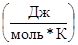
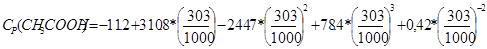
= 67,26 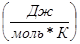
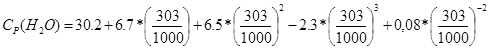
= 33,63 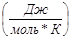
Средняя мольная теплоемкость продуктов реакции:
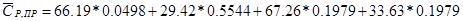
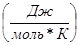
6) Количество тепла, выносимого с продуктами реакции:
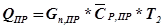
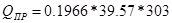
7) Количество тепла, расходуемого на нагревание смеси:
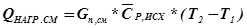
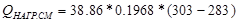
8) Количество тепла, выделяющегося или поглощающегося при фазовых передах веществ:
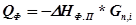
Так как в интервале температур 10…30ºCвещества не изменяют своего фазового состояния , то 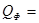
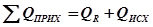
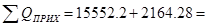
10) Потери тепла:
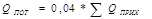
11) Расход тепла:
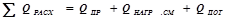
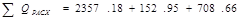
12) Тепловая нагрузка на реактор:
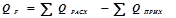
12) Построение таблицы по результатам расчета материального баланса.
Таблица 10. — Результаты
| Приход | Расход | ||||
| Qi | кДж/ч | % | Qi | кДж/ч | % |
| QРЕАГ | 2164.28 | 12.22 | QПР | 2357.18 | 13.31 |
| QR | 15552.2 | 87.78 | QНАГР.СМ | 152.95 | 0.86 |
| QПОТ | 708.66 | 4.00 | |||
| QF | 14497.7 | 81.83 | |||
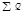 | 17716.48 | 100.00 | 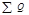 | 17716.48 | 100.00 |
13) Выводы расчетов теплового баланса.
·тепловые потоки на входе в реактор (ПРИХОД тепла) – 17716,48кДж/ч;
·тепловые потоки на выходе из реактора (РАСХОД тепла) – 3218,79кДж/ч;
·тепловые потери – 708,66 кДж/ч;
·тепловая нагрузка на реактор – 14497,7 кДж/ч;
·основные тепловые потоки сведены в табл. 10.
· В данной работе тепловой баланс не имеет никакого практического интереса по причине, того, что расчет произведен для основной реакции микробиологического синтеза уксусной кислоты, которая имеет очень сложный вид, связанный с прохождением биологических процессов.
Данная работа содержит несколько разделов, основным из которых является литературный обзор. В нем описываются основные методы получения уксусной кислоты микробиологическим синтезом. Так же в этом разделе представлено: химизм процесса микробиологического синтеза уксусной кислоты, стадии подготовки исходного сырья, стадии очистки готового продукта, продуценты уксусной кислоты, применение и вредители уксуса. В ходе описания основных методов получения уксусной кислоты, был выбран один метод, который рассматривается как основной для данной работы. Это метод «проточного культивирования». Он наиболее выгоден, так как выход продукта составляет 90% и более; процесс идет с более полной степенью превращения исходного сырья; существует возможность увеличения объема получаемого продукта, добавлением этилового спирта непосредственно во время процесса, во второй, в третий, четвертый и пятый аппараты установки; снижаются затраты на производство, так как основная часть уксуснокислых бактерий получается в первом аппарате, а в остальных идет, по большей части, окисление этилового спирта в уксусную кислоту и поддержание процессов жизнедеятельности уксуснокислых бактерий. Также, данный метод был выбран и потому, что он разработан сравнительно не давно и является достаточно перспективным.
Следующий раздел работы это «технологическая схема микробиологического синтеза уксусной кислоты». Соответственно в нем имеется описание технологической схемы, сама схема на которой указаны все материальные потоки и обозначены все аппараты, участвующие в процессе синтеза.
Затем идут такие разделы работы, как «расчет модели реактора на ЭВМ», в котором представлен расчет ферментера на ЭВМ, здесь рассчитаны основные параметры аппарата; «термодинамический расчет основной реакции», «материальный баланс стадии синтеза» и «тепловой баланс стадии синтеза».
Последние три раздела данной работы не представляют особого интереса, так как они связаны с химизмом процесса, а в данном случае химизм процесса микробиологического синтеза уксусной кислоты достаточно сложен из-за того, что это биологический процесс и имеет многостадийность. В данной же работе расчет в последних трех разделах проводился по упрощенной реакции, не учитывая промежуточных стадий.
Список использованной литературы
1. Биотехнология: Принципы и применение: учеб. пособ./ Г. Бич, Д. Бест, К. Брайерли [и др.]; Под ред. И. Хиггинса и др.; Перевод с англ. А.С. Антонова; Под ред. А.А. Баева. – М.: Мир, 1988. – 479 с.
2. Воробьева, Л.И. Промышленная микробиология: учебник/ Л.И. Воробьева. — М.: Знание, 1985. – 64 с.
3. Уэбб, Ф. Биохимическая технология и микробиологический синтез: учебник/ Ф. Уэбб. — перевод с англ. П.Е. Швалева. — М.: Медицина, 1969.
4. Яковлев, В.И. Технология микробиологического синтеза: [Учеб. Пособие для сред. ПТУ]/ В.И. Яковлев. – Л.: Химия. Ленинград. отд – ние, 1987. – 271 с.
5. Мюллер, Г. Микробиология пищевых продуктов растительного происхождения: учебник/ Г. Мюллер, П. Литц, Г.Д. Мюнх. — Перевод с нем. А.М. Калашниковой; Под ред. И.М. Грачевой. – М.: Пищевая пром – сть, 1977.
6. Мосичев, М.С. Общая технология микробиологических производств: учебник /М.С. Мосичев, А.А. Складнеев, В.Б. Котов. – М.: Легкая и пищевая промышленность, 1982. – 264с.
7. Кустова, Н. Уксус. Что это такое и как его делают/ Н. Кустова// Наука и жизнь. – 2002. — № 7. – С. 108 – 111.
8. Промышленная микробиология.
9. Справочник нефтехимика/ Под ред. С. К. Огородникова. Том 1. — Л.: Химия, 1978.
10. Содержание и порядок оформления самостоятельной (курсовой) работы.// Ю. В. Попов, Г. М. Бутов, Т. К. Корчагин, К. Ф. Красильникова. — ВолгГТУ, Волгоград, 1996.
11. Сборник задач к практическим занятиям по курсу «Основы инженерной химии»: Учеб. Пособие / Г. М. Бутов, К. Ф. Красильникова, Т. К. Корчагин и др. — ВолгГТУ, Волгоград, 2000
12. А.Г. Касаткин. Основные процессы и аппараты химической технологии. М.: Химия, 1971. –784с.
13. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии. Учебное пособие для вузов / Под редакцией П.Г.Романкова. Л.: Химия, 1976. – 576с.
14. Рабинович, В.А. Краткий химический справочник. Изд. 2-е испр. и доп./ В.А. Рабинович, З.Я. Хавин. – Л.: Химия, 1978. – 392с.
15. Петров, А.А. Органическая химия: Учебник для вузов./ А.А. Петров, Х.В. Бальян, А.Т. Трощенко; Под ред. Стадничука М.Д. – 5-е изд., перераб. и доп. – СПб.: Иван Федоров, 2002. – 624с.
Источник

 5 – 6 дней, после чего повторяется.
5 – 6 дней, после чего повторяется.
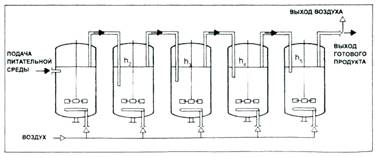 Исследованиями Ю. Л. Игнатова было показано, что накапливаемая в процессе уксусная кислота снижает окислительную активность бактерий и уменьшает удельную скорость роста клеток. Этот факт позволил П. И. Николаеву с сотрудниками организовать процесс получения уксусной кислоты в батарее из нескольких аппаратов глубинным способом в непрерывном режиме. В результате получилась оригинальная схема, в которой процесс получения 9%-ной уксусной кислоты ведут в четырех-пяти последовательно соединенных ферментерах (рис. 5).
Исследованиями Ю. Л. Игнатова было показано, что накапливаемая в процессе уксусная кислота снижает окислительную активность бактерий и уменьшает удельную скорость роста клеток. Этот факт позволил П. И. Николаеву с сотрудниками организовать процесс получения уксусной кислоты в батарее из нескольких аппаратов глубинным способом в непрерывном режиме. В результате получилась оригинальная схема, в которой процесс получения 9%-ной уксусной кислоты ведут в четырех-пяти последовательно соединенных ферментерах (рис. 5).