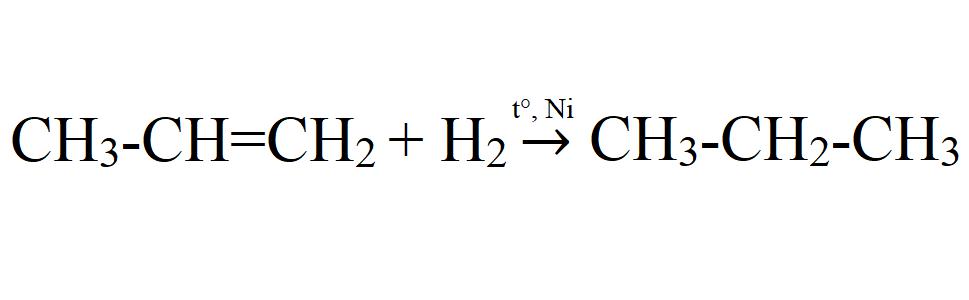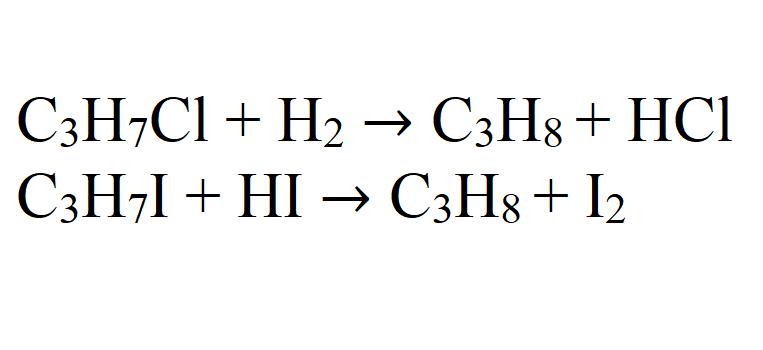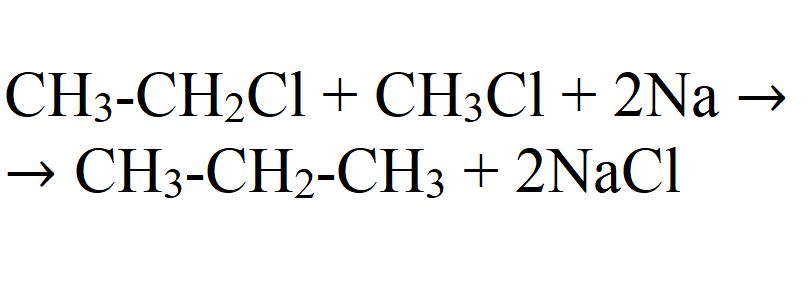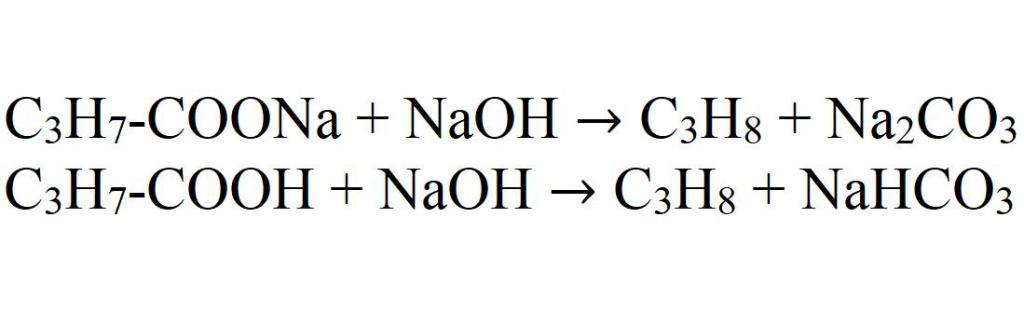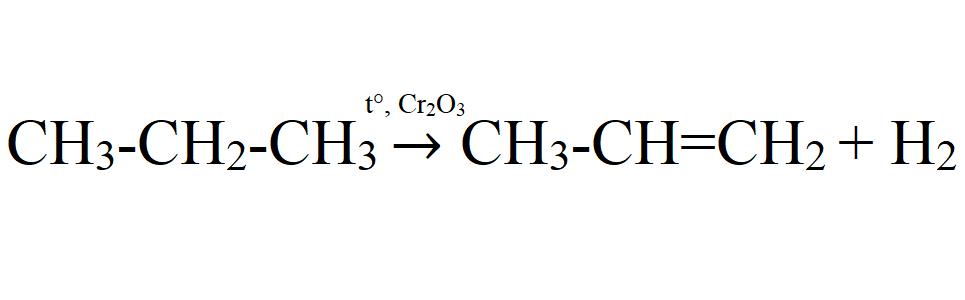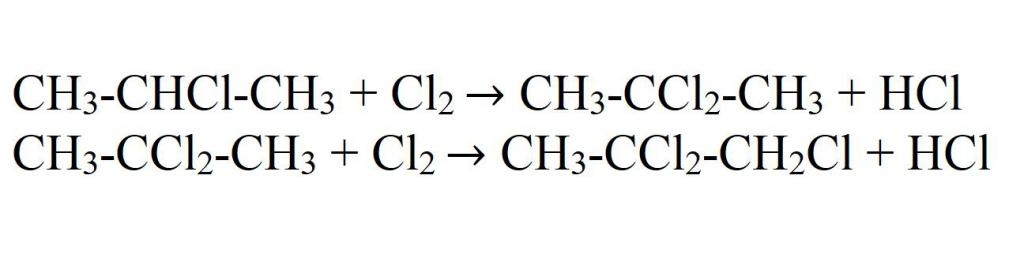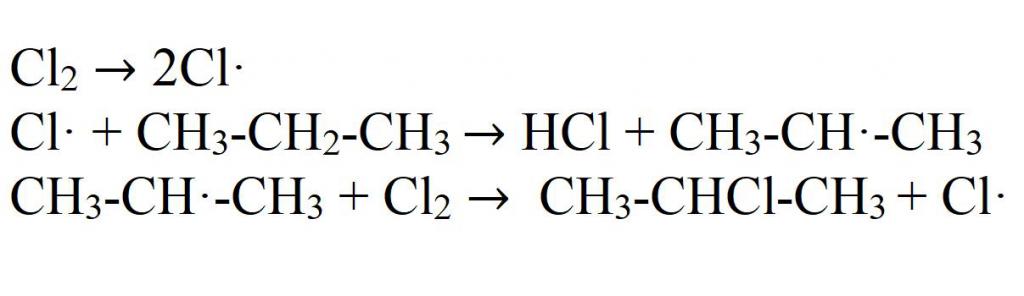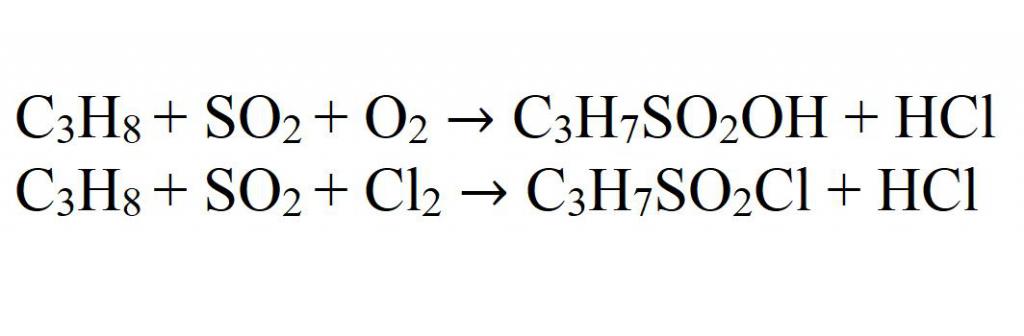- Пропан: химические свойства, строение, получение, применение
- Строение
- Способы получения
- Физические свойства пропана
- Химические свойства пропана
- Применение
- Пропан
- Характеристики и физические свойства пропана
- Получение пропана
- Химические свойства пропана
- Пропан: способы получения и химические свойства
- Гомологический ряд пропана
- Строение пропана
- Изомерия пропана
- Химические свойства пропана
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование пропана
- 2. Дегидрирование пропана
- 3. Окисление пропана
- 3.1. Полное окисление – горение
- Получение пропана
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 3. Гидрирование алкенов и алкинов
- 4. Синтез Фишера-Тропша
- 5. Получение пропана в промышленности
Пропан: химические свойства, строение, получение, применение
Пропан — это органическое соединение, третий представитель алканов в гомологическом ряду. При комнатной температуре он представляет собой газ без цвета и запаха. Химическая формула пропана — C3H8. Пожаро- и взрывоопасен. Обладает небольшой токсичностью. Он оказывает слабое воздействие на нервную систему и обладает наркотическими свойствами.
Строение
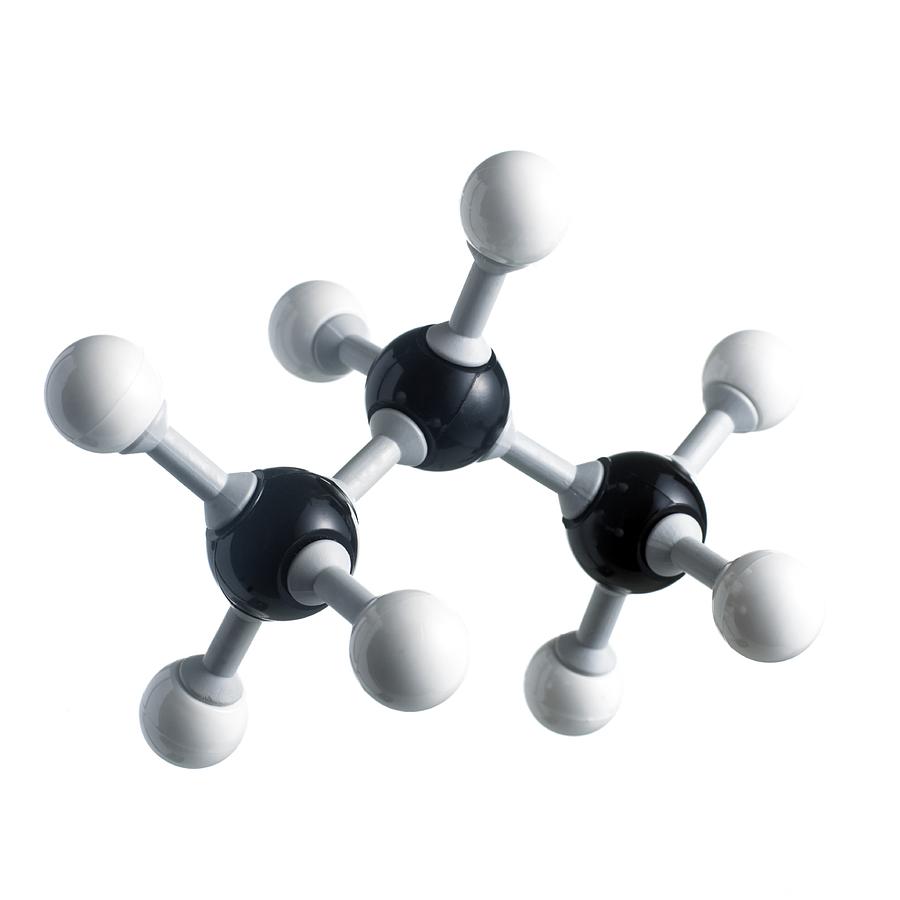
Пропан — это предельный углеводород, состоящий из трех атомов углерода. По этой причине он имеет изогнутую форму, но из-за постоянного вращения вокруг осей связей существует несколько молекулярных конформаций. Связи в молекуле ковалентные: С-С неполярные, C-H слабополярные. Из-за этого их сложно разорвать, а вещество довольно трудно вступает в химические реакции. Это и задает все химические свойства пропана. Изомеров у него нет. Молярная масса пропана — 44,1 г/моль.
Способы получения
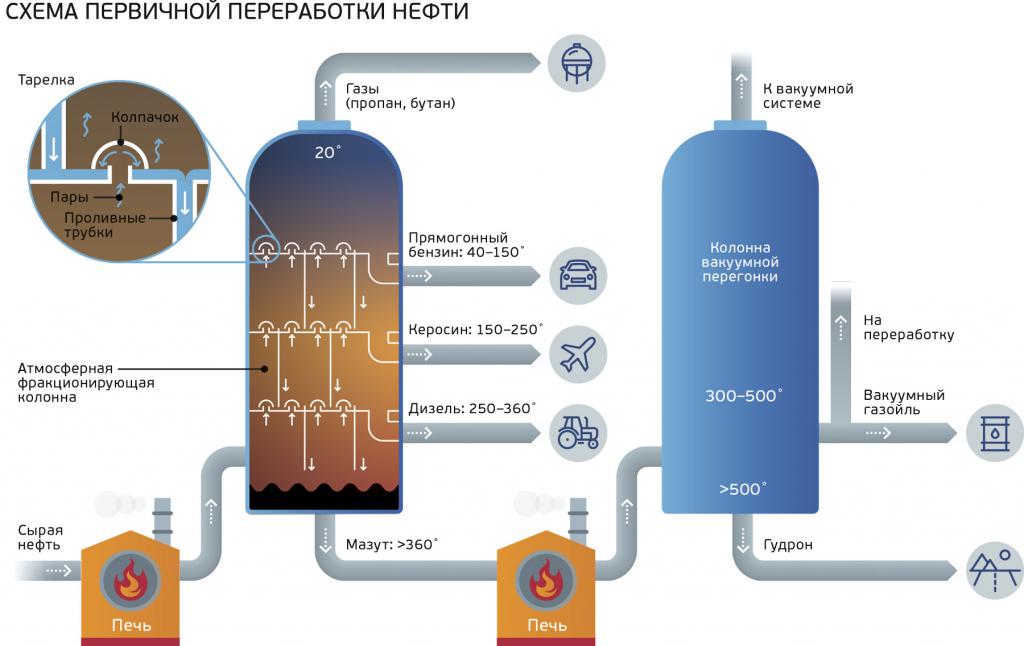
В промышленности пропан почти не синтезируют искусственно. Его выделяют из природного газа и нефти с помощью перегонки. Для этого существуют специальные производственные установки.
В лаборатории пропан можно получить следующими химическими реакциями:
- Гидрирование пропена. Данная реакция идет только при повышении температуры и при наличии катализатора (Ni, Pt, Pd).
Физические свойства пропана
Как уже упоминалось, пропан — это газ без цвета и запаха. Он не растворяется в воде и других полярных растворителях. Зато растворяется в некоторых органических веществах (метанол, ацетон и другие). При — 42,1 °C сжижается, а при − 188 °C становится твердым. Огнеопасен, так как образует с воздухом легковоспламеняющиеся и взрывоопасные смеси.
Химические свойства пропана
Они представляют собой типичные свойства алканов.
- Каталитическое дегидрирование. Осуществляется при 575 °C с использованием катализатора оксида хрома (III) или оксида алюминия.
Механизм реакций галогенирования — цепной. Под действием света или высокой температуры молекула галогена распадается на радикалы. Они вступают во взаимодействие с пропаном, отнимая у него атом водорода. В результате этого образуется свободный пропил. Он взаимодействует с молекулой галогена, вновь разбивая ее на радикалы.
Бромирование происходит по такому же механизму. Йодирование можно осуществлять только специальными йодсодержащими реагентами, так как пропан не взаимодействует с чистым йодом. При взаимодействии с фтором происходит взрыв, образуется полизамещенное производное пропана.
Нитрование может осуществятся разбавленной азотной кислотой (реакция Коновалова) или оксидом азота (IV) при повышенной температуре (130-150 °C).
Сульфоокисление и сульфохлорирование осуществляется при УФ-свете.
Можно провести и более мягкое окисление, используя определенные катализаторы. Реакция горения пропана будет другой. В этом случае получают пропанол, пропаналь или пропионовую кислоту. В качестве окислителей, кроме кислорода, могут использоваться перекиси (чаще всего перекись водорода), оксиды переходных металлов, соединения хрома (VI) и марганца (VII).
Пропан реагирует с серой с образованием изопропилсульфида. Для этого в качестве катализаторов используется тетрабромэтан и бромид алюминия. Реакция идет при 20 °C в течение двух часов. Выход реакции составляет 60 %.
С теми же катализаторами может реагировать с оксидом углерода (I) с образованием изопропилового эфира 2-метилпропановой кислоты. Реакционная смесь после реакции должна быть обработана изопропанолом. Итак, мы рассмотрели химические свойства пропана.
Применение
Из-за хорошей горючести пропан находит применение в быту и промышленности как топливо. Он может быть использован также в качестве горючего для автомобилей. Пропан горит с температурой почти 2000° C, поэтому его используют для сварки и резки металла. Пропановыми горелками разогревают битум и асфальт в дорожном строительстве. Но зачастую на рынке используется не чистый пропан, а его смесь с бутаном (пропан-бутан).
Как ни странно, но нашел он применение и в пищевой промышленности как добавка Е944. Благодаря своим химическим свойствам пропан используется там в качестве растворителя ароматизаторов, а также для обработки масел.
Смесь пропана и изобутана используется как хладагент R-290a. Он более эффективен, чем старые хладагенты, и также является экологически чистым, так как не разрушает озоновый слой.
Большое применение пропан нашел в органическом синтезе. Его используют для получения полипропилена и различного рода растворителей. В нефтепереработке его используют для деасфальтизации, то есть уменьшения доли тяжелых молекул в битумной смеси. Это необходимо для вторичного использования старого асфальта.
Источник
Пропан
Характеристики и физические свойства пропана
Пропан практически не растворим в воде, так как его молекулы малополярны и не взаимодействуют с молекулами воды. Он хорошо растворяется в неполярных органических растворителях, таких как бензол, тетрахлорметан, диэтиловый эфир и др.
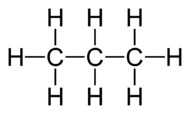
Рис. 1. Строение молекулы пропана.
Таблица 1. Физические свойства пропана.
Плотность (20 o С), кг/м 3
Температура плавления, o С
Температура кипения, o С
Получение пропана
Основными источниками пропана являются нефть и природный газ. Его можно выделить фракционной перегонкой природного газа или бензиновой фракции нефти.
В лабораторных условиях пропан получают следующими способами:
— гидрированием непредельных углеводородов
— по реакции щелочного плавления солей одноосновных органических кислот
— взаимодействием галогеналканов с металлическим натрием (реакция Вюрца)
Химические свойства пропана
В обычных условиях пропан не реагирует с концентрированными кислотами, расплавленными и концентрированными щелочами, щелочными металлами, галогенами (кроме фтора), перманганатом калия и дихроматом калия в кислой среде.
Для пропана наиболее характерны реакции, протекающие по радикальному механизму. Энергетически более выгоден гомолитический разрыв связей C-H и C-C, чем их гетеролитический разрыв.
Все химические превращения пропана протекают с расщеплением:
Источник
Пропан: способы получения и химические свойства
Пропан C3H8 – это предельный углеводород, содержащий три атома углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, нерастворим в воде и не смешивается с ней.
Гомологический ряд пропана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение пропана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :

При образовании связи С–С происходит перекрывание sp 3 -гибридных орбиталей атомов углерода:

При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:

Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:

Это соответствует тетраэдрическому строению.
| Например, в молекуле пропана C3H8 атомы водорода располагаются в пространстве в вершинах тетраэдров, центрами которых являются атомы углерода. При этом углеродный скелет образует угол, т.е. геометрия молекулы — уголковая или V-образная. |
Изомерия пропана
Для пропана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Химические свойства пропана
Пропан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для пропана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для пропана характерны радикальные реакции.
Пропан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Пропан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании пропана образуется смесь хлорпроизводных.
| Например, при хлорировании пропана образуются 1-хлорпропан и 2-хлопропан: Бромирование протекает более медленно и избирательно.
|