- Оксид меди (II)
- Оксид меди (II)
- Способы получения оксида меди (II)
- Химические свойства оксида меди (II)
- Оксид меди (I)
- Оксид меди (I)
- Способы получения оксида меди (I)
- Химические свойства оксида меди (I)
- Получение меди
- Способы получения меди
- Получение меди электролизом
- Получение оксида меди
- Получение сульфата меди
- Получение хлорида меди
- Получение глицерата меди
- Получение нитрата меди
- Получение сульфида меди
- Оксид меди (II), свойства, получение, химические реакции
- Оксид меди (II), свойства, получение, химические реакции.
- Краткая характеристика оксида меди (II):
- Физические свойства оксида меди (II):
- Получение оксида меди (II):
- Химические свойства оксида меди (II). Химические реакции оксида меди (II):
- Применение и использование оксида меди (II):
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
Оксид меди (II)
Оксид меди (II)
Оксид меди (II) CuO – твердое кристаллическое вещество черного цвета.
Способы получения оксида меди (II)
Оксид меди (II) можно получить различными методами :
1. Термическим разложением гидроксида меди (II) при 200°С :
2. В лаборатории оксид меди (II) получают окислением меди при нагревании на воздухе при 400–500°С:
2Cu + O2 → 2CuO
3. В лаборатории оксид меди (II) также получают прокаливанием солей (CuOH)2CO3, Cu(NO3)2:
Химические свойства оксида меди (II)
Оксид меди (II) – основный оксид (при этом у него есть слабо выраженные амфотерные свойства) . При этом он является довольно сильным окислителем.
1. При взаимодействии оксида меди (II) с сильными и растворимыми кислотами образуются соли.
Например , оксид меди (II) взаимодействует с соляной кислотой:
СuO + 2HBr = CuBr2 + H2O
CuO + 2HCl = CuCl2 + H2O
2. Оксид меди (II) вступает в реакцию с кислотными оксидами.
Например , оксид меди (II) взаимодействует с оксидом серы (VI) с образованием сульфата меди (II):
3. Оксид меди (II) не взаимодействует с водой.
4. В окислительно-восстановительных реакциях соединения меди (II) проявляют окислительные свойства:
Например , оксид меди (II) окисляет аммиак :
3CuO + 2NH3 → 3Cu + N2 + 3H2O
Оксид меди (II) можно восстановить углеродом, водородом или угарным газом при нагревании:
СuO + C → Cu + CO
Более активные металлы вытесняют медь из оксида.
Например , алюминий восстанавливает оксид меди (II):
3CuO + 2Al = 3Cu + Al2O3
Источник
Оксид меди (I)
Оксид меди (I)
Оксид меди (I) Cu2O – твердое кристаллическое вещество коричнево-красного цвета.
Способы получения оксида меди (I)
В лаборатории оксид меди (I) получают восстановлением свежеосажденного гидроксида меди (II), например , альдегидами или глюкозой:
Химические свойства оксида меди (I)
1. Оксид меди (I) обладает основными свойствами.
При действии на оксид меди (I) галогеноводородных кислот получают галогениды меди (I) и воду:
Например , соляная кислота с оксидом меди (I) образует хлорид меди (I):
Cu2O + 2HCl = 2CuCl↓ + H2O
2. При растворении Cu2O в концентрированной серной, азотной кислотах образуются только соли меди (II):
3. Устойчивыми соединениями меди (I) являются нерастворимые соединения (CuCl, Cu2S) или комплексные соединения [Cu(NH3)2] + . Последние получают растворением в концентрированном растворе аммиака оксида меди (I), хлорида меди (I):
Аммиачные растворы солей меди (I) взаимодействуют с ацетиленом :
СH ≡ CH + 2[Cu(NH3)2]Cl → СuC ≡ CCu + 2NH4Cl
4. В окислительно-восстановительных реакциях соединения меди (I) проявляют окислительно-восстановительную двойственность:
Например , при взаимодействии с угарным газом, более активными металлами или водородом оксид меди (II) проявляет свойства окислителя :
Cu2O + CO = 2Cu + CO2
А под действием окислителей, например, кислорода — свойства восстановителя :
Источник
Получение меди
Медь или купрум, названа так в честь острова Кипр, где нашли крупное ее месторождение. Это один из первых металлов, освоенных человеком. Медный век – удивительная эпоха, в которую обиход человека был наполнен медными орудиями и предметами быта, он продолжался с IV до III тысячелетия до н. э.
Способы получения меди
Для извлечения меди из минералов и руд, в которых она находится, на сегодняшний день используют три метода:
- гидрометаллургический
- пирометаллургичекий
- электролиз.
Получение меди пирометаллургическим методом является наиболее распространенным. Сырьем для этого процесса выступает халькопирит. Чтобы получить из халькопирита чистую медь, необходимо осуществить ряд операций. Первая, из которых, заключается в обогащении медной руды, методом окислительного обжига или флотации.
В основе флотации лежит тот факт, что пустая порода и ее медесодержащие части, смачиваются по-разному. Если поместить всю массу породы в емкость с жидким составом, в котором имеются воздушные пузырьки, то часть с минеральными элементами, перемещается при помощи этих пузырьков на поверхность, и прилипает к ним. В результате на поверхности ванны наблюдается наличие концентрата или черновой меди. В этом составе присутствует от 10 до 35% чистой меди. Этот порошкообразный концентрат является сырьем для дальнейшего получения чистой меди.
Совсем по-другому протекают реакции получения меди методом окислительного обжига. Этим методом обогащают медные руды, в составе которых имеется существенное количество серы. Для реализации этой технологии необходимо нагреть руду до температуры 700–8000 градусов. Под действием таких высоких температур происходит окисление сульфидов, и объем серы в медной руде снижается почти в два раза. Следующим этапом является расплавление обогащенной руды в отражательных или шахтных печах при температуре 14500. Результатом этого расплава является образование штейна – сплава, который состоит из сульфидов меди и железа.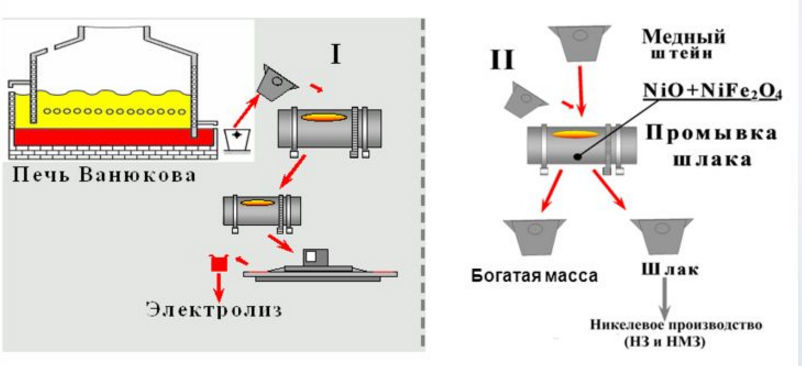
Черновая медь, полученная таким способом, имеет в своем составе около 91% меди. Для дополнительной очистки металла выполняется рафинирование меди, то есть удаление посторонних примесей. Это осуществляется благодаря технологии огневого рафинирования в присутствии подкисленного раствора медного купороса. Это рафинирование меди носит электролитический характер, и дает возможность получить металл с чистотой 99,9%.
Гидрометаллургический метод обогащения меди основан на процессе выщелачивания металла с помощью серной кислоты. Результатом такого процесса является получение раствора, из которого в дальнейшем выделяют чистую медь. Также этот метод подходит для выделения драгоценных металлов. Эту технологию применяют для обогащения руд, в которых присутствует крайне малое количество меди.
Получение меди электролизом
Электролиз меди является одним этапов химико-физических процессов, которому подвергают руду, чтобы получить медь. Примечательно, что для получения 1 тонны чистой меди, потребуется переработать как минимум 200 тонн медной руды.
Сама процедура обработки медной руды – это многоступенчатый и очень сложный процесс, который состоит из 7 стадий. Самой последней и является электролиз меди.
Руду после добычи необходимо измельчить в особых машинах. Далее происходит процесс флотации, в результате которого, как мы знаем, формируется концентрат с сохранением минералов меди. После этого происходит обжиг при высоких температурах в специальных печах. Шихту, полученную в процессе обжига, помещают в печь для плавки, где она становится штейном, который в свою очередь оправляют на конвертирование. Продукт, полученный после этих процессов, называют черновой медью, где 2-3% объема занимают примеси. В качестве примесей выступают цинк, железо, или сера. Их удаляют реакцией окисления. На этом этапе образуется «красная» медь, в которой присутствует 99,7-99,9% Cu. Последним этапом является непосредственно электролиз меди, который позволяет добиться получения максимально чистой меди.
Чтобы осуществить процесс электролиза меди понадобится специальное оборудование, а именно емкости, которые заполняют водным раствором сульфата меди с содержанием свободной серной кислоты. В результате проведения электролиза, мы получим осадок чистой меди на катодах. А все, что окажется на дне ванны, принято называть шламом. Он является сырьем для получения благородных металлов.
Получение оксида меди
Оксид меди (II) CuO представляет собой кристаллы черного цвета, которые подвергаются кристаллизации в моноклинной сингонии. Плотность соединения составляет 6,51 г/см3, а плавится он при температуре 1447°С в условиях высокого давления. В результате нагревания до 1100°С является выделение оксида меди (I):
В воде оксид меди не растворяется и не вступает в реакции с ней. Обладает слабыми амфотерными свойствами с преобладанием основных.
С водными растворами аммиака реагирует с образованием гидроксида тетраамминмеди (II):
Также легко вступает в реакции с разбавленными кислотами с выделением соли и воды:
Результатом сплавления оксида меди со щелочами является образование купратов:
Чистую медь из оксида можно получить методом восстановления водородом, угарным газом и активными металлами:
Реакция получения оксида меди методом прокаливания гидроксида меди (II) при температуре 200°С:
Также получить оксид меди можно в процессе окисления металлической меди на воздухе при температуре 400–500°С:
Получение сульфата меди
Получить сульфат меди можно тремя реакциями:
растворить CuO в H2SO4
в присутствии концентрированной серной кислоты с медью, обязательно при нагревании
методом взаимодействия Cu2O с разбавленной серной кислотой
Получение хлорида меди
В природе хлорид меди находится в составе очень редкого минерала эрнохальцита CuCl₂•2H₂O, который представляет собой кристаллы синего цвета.
Двухвалентный хлорид меди обладает важным практическим значением, и добычи его только лишь из природного минерала очень мало. Поэтому ученые придумали несколько способов искусственного получения данного соединения.
Главной реакцией промышленного синтеза CuCl₂ можно назвать реакцию хлорирования сульфида меди в условиях высокой температуры от 300 до 400 градусов °С. Выглядит реакция так
Еще одним вариантом синтеза хлорида двухвалентной меди является хлорирующий обжиг, который осуществляется при температуре более 500 С:
- CuS + 2NaCl + 2O₂ ―› CuCl₂ + Na₂SO₄
Обе реакции нуждаются в использовании специализированного оборудования и соблюдении повышенных мер безопасности, по этой причине данные реакции можно проводить только в условиях промышленного производства. В лабораторных условиях также можно получить хлорид меди следующими реакциями
- Cu + Cl₂ ―› CuCl₂
- CuO + 2HCl ―› CuCl₂ +H₂O
- Cu(OH)₂ + 2HCl ―› CuCl₂ + 2H₂O. Реакция нейтрализации
- CuCO₃ + 2HCL ―› CuCl₂ + H₂O + CO₂. В результате этой реакции более сильная кислота вытеснит кислотный остаток более слабой кислоты. Протекает реакция замещения
- 3Сu + 2HNO₃ + 6HCl ―› 3CuCl₂ + 2NO +4H₂0. Эта реакция является наиболее оригинальной. Она протекает только в присутствии смеси двух сильных кислот.
Получение глицерата меди
Качественная реакция для выявления присутствия глицерина в растворах осуществляется в присутствии сульфата меди (II) и раствора гидроксида натрия. В результате реакции образуется глицерат меди – комплексное соединение сине-василькового оттенка.
Химическую реакцию проводят следующим образом:
- к раствору сульфата меди (II) приливают раствор гидроксида натрия, в результате чего происходит окрашивание раствора в синий цвет. Таким образом, наблюдаем выпадения осадка гидроксида меди (II)
- после этого добавляем несколько мл глицерина и перемешиваем раствор. Образовавшийся осадок растворяется с образованием комплексного соединения оттенка индиго. Это и есть глицерат меди.
Получение нитрата меди
Получение нитрата меди Cu(NO3)2 довольно увлекательное занятие. А также очень полезное, поскольку он является довольно популярным красителем. Нитрат меди (II) можно получить в процессе растворения чистой меди, ее оксида или гидроксида в азотной кислоте. Уравнения выглядят следующим образом:
Получение сульфида меди
Сульфид меди(II) или моносульфид меди — CuS, является неорганическим бинарным соединением двухвалентной меди с серой. Он верного цвета, в воде не растворяется , также как и в разбавленных растворах кисло. В природе его можно встретить в виде редкого минерала ковеллина.
Получение сульфида меди осуществляется при помощи прямого взаимодействия элементов, а также в результате обменной реакции солей двухвалентной меди с водорастворимыми сульфидами.
- Na2S+CuSO4=CuS+Na2SO4
- CuCl2 + H2S —> CuS + 2HCl
- 2CuS + H2 —>Cu2S + H2S. Эта реакция протекает в условиях высокой температуры от 600 до 700 oC
Получение сухим методом дает сульфиду меди возможность проводить электрический ток. Когда отметка термометра достигает 400 °C, наблюдается заметное разложение сульфида.
Источник
Оксид меди (II), свойства, получение, химические реакции
Оксид меди (II), свойства, получение, химические реакции.
Оксид меди (II) – неорганическое вещество, имеет химическую формулу CuO.
Химические свойства оксида меди (II)
Краткая характеристика оксида меди (II):
Оксид меди (II) – неорганическое вещество черного цвета.
Так как валентность меди меняется и равна одному, двум или трем, то оксид меди содержит соответственно два атома меди и один атом кислорода, один атом меди и один атом кислорода, два атома меди и три атома кислорода.
Оксид двухвалентной меди содержит соответственно один атом меди и один атом кислорода.
Химическая формула оксида меди (II) CuO.
Порошок. Не растворяется в воде.
Физические свойства оксида меди (II):
| Наименование параметра: | Значение: |
| Химическая формула | CuO |
| Синонимы и названия иностранном языке | меди окись (устар. рус.) |
сopper (II) oxide (англ.)
тенорит (рус.)
Получение оксида меди (II):
Оксид меди (II) получается в результате следующих химических реакций:
1. окисления меди:
2. термического разложения гидроксида меди (II), нитрата меди (II), карбоната меди (II):
3. нагревания малахита:
Химические свойства оксида меди (II). Химические реакции оксида меди (II):
Оксид меди (II) относится к основным оксидам.
Химические свойства оксида меди (II) аналогичны свойствам основных оксидов других металлов . Поэтому для него характерны следующие химические реакции:
1. реакция оксида меди (II) с водородом:
CuО + H2 → Cu + H2О (t = 300 o C).
В результате реакции образуется медь и вода .
2. реакция оксида меди (II) с углеродом:
CuО + С → Cu + СО (t = 1200 o C).
В результате реакции образуется медь и оксид углерода .
3. реакция оксида меди (II) с серой:
CuО + 2S → Cu + S2О (t = 150-200 o C).
Реакция протекает в вакууме. В результате реакции образуется медь и оксид серы .
4. реакция оксида меди (II) с алюминием:
3CuО + 2Al → 3Cu + Al2О3 (t = 1000-1100 o C).
В результате реакции образуется медь и оксид алюминия .
5. реакция оксида меди (II) с медью:
CuО + Cu → Cu2О (t = 1000-1200 o C).
В результате реакции образуется оксид меди (I).
6. реакция оксида меди (II) с оксидом лития :
Реакция протекает в токе кислорода. В результате реакции образуется купрат лития.
7. реакция оксида меди (II) с оксидом натрия :
Реакция протекает в токе кислорода. В результате реакции образуется купрат натрия.
8. реакция оксида меди (II) с оксидом углерода :
CuО + СО → Cu + СО2.
В результате реакции образуется медь и оксид углерода (углекислый газ).
9. реакция оксида меди (II) с оксидом железа :
В результате реакции образуется соль – феррит меди. Реакция протекает при прокаливании реакционной смеси.
10. реакция оксида меди (II) с плавиковой кислотой:
В результате химической реакции получается соль – фторид меди и вода.
11. реакция оксида меди (II) с азотной кислотой:
В результате химической реакции получается соль – нитрат меди и вода .
Аналогично проходят реакции оксида меди (II) и с другими кислотами.
12. реакция оксида меди (II) с бромистым водородом (бромоводородом):
В результате химической реакции получается соль – бромид меди и вода .
13. реакция оксида меди (II) с йодоводородом:
В результате химической реакции получается соль – йодид меди и вода .
14. реакция оксида меди (II) с гидроксидом натрия :
В результате химической реакции получается соль – купрат натрия и вода .
15. реакция оксида меди (II) с гидроксидом калия :
В результате химической реакции получается соль – купрат калия и вода .
16. реакция оксида меди (II) с гидроксидом натрия и водой:
Гидрокосид натрия растворен в воде. Раствор гидроксида натрия в воде 20-30 %. Реакция протекает при киппении. В результате химической реакции получается тетрагидроксокупрат натрия.
17. реакция оксида меди (II) с надпероксидом калия:
В результате химической реакции получается соль – купрат (III) калия и кислород .
18. реакция оксида меди (II) с пероксидом калия:
В результате химической реакции получается соль – купрат (III) калия.
19. реакция оксида меди (II) с пероксидом натрия:
В результате химической реакции получается соль – купрат (III) натрия.
20. реакция оксида меди (II) с аммиаком:
3CuO + 2NH3 → N2 + 3Cu + 3H2O (t = 500-550 o C).
Аммиак пропускают через нагретый оксид меди (II). В результате химической реакции получается азот, медь и вода.
В результате химической реакции получается нитрид меди, азот и вода.
21. реакция оксида меди (II) и йодида алюминия:
В результате химической реакции получаются соль – йодид меди, оксид алюминия и йод.
Применение и использование оксида меди (II):
Оксид меди используется для производства стекла и эмалей для придания им соответствующей окраски (зеленой, синей, медно-рубиновой).
Примечание: © Фото //www.pexels.com, //pixabay.com

оксид меди реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие оксида меди
реакции с оксидом меди
Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 545)
- Экономика Второй индустриализации России (102 552)
- Программа искусственного интеллекта ЭЛИС (27 771)
- Метан, получение, свойства, химические реакции (24 220)
- Этилен (этен), получение, свойства, химические реакции (24 020)
- Природный газ, свойства, химический состав, добыча и применение (21 588)
- Крахмал, свойства, получение и применение (20 906)
- Пропилен (пропен), получение, свойства, химические реакции (20 040)
- Целлюлоза, свойства, получение и применение (19 754)
- Прямоугольный треугольник, свойства, признаки и формулы (19 010)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник













