- Азотная кислота: получение и химические свойства
- Строение молекулы и физические свойства
- Способы получения
- Химические свойства
- Азотная кислота
- Основные свойства и описание способов получения азотной кислоты
- Описание основных характеристик
- Химические признаки
- Варианты получения HNO3
- Вытеснение из солей
- Дуговой способ
- Аммиачный метод
- Меры безопасности
Азотная кислота: получение и химические свойства
Строение молекулы и физические свойства
Азотная кислота HNO3 – это сильная одноосновная кислота-гидроксид. При обычных условиях бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C ( при нормальном атмосферном давлении). Азотная кислота смешивается с водой во всех соотношениях. На свету частично разлагается.
Валентность азота в азотной кислоте равна IV, так как валентность V у азота отсутствует. При этом степень окисления атома азота равна +5. Так происходит потому, что атом азота образует 3 обменные связи и одну донорно-акцепторную, является донором электронной пары.
Поэтому строение молекулы азотной кислоты можно описать резонансными структурами:
Обозначим дополнительные связи между азотом и кислородом пунктиром. Этот пунктир по сути обозначает делокализованные электроны. Получается формула:
Способы получения
В лаборатории азотную кислоту можно получить разными способами:
1. Азотная кислота образуется при действии концентрированной серной кислоты на твердые нитраты металлов. При этом менее летучая серная кислота вытесняет более летучую азотную.
Например , концентрированная серная кислота вытесняет азотную из кристаллического нитрата калия:
2. В промышленности азотную кислоту получают из аммиака . Процесс осуществляется постадийно.
1 стадия. Каталитическое окисление аммиака.
2 стадия. Окисление оксида азота (II) до оксида азота (IV) кислородом воздуха.
3 стадия. Поглощение оксида азота (IV) водой в присутствии избытка кислорода.
Химические свойства
Азотная кислота – это сильная кислота . За счет азота со степенью окисления +5 азотная кислота проявляет сильные окислительные свойства .
1. Азотная кислота практически полностью диссоциирует в водном растворе.
2. Азотная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , азотная кислота взаимодействует с оксидом меди (II):
Еще пример : азотная кислота реагирует с гидроксидом натрия:
3. Азотная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов, сульфитов).
Например , азотная кислота взаимодействует с карбонатом натрия:
4. Азотная кислота частично разлагается при кипении или под действием света:
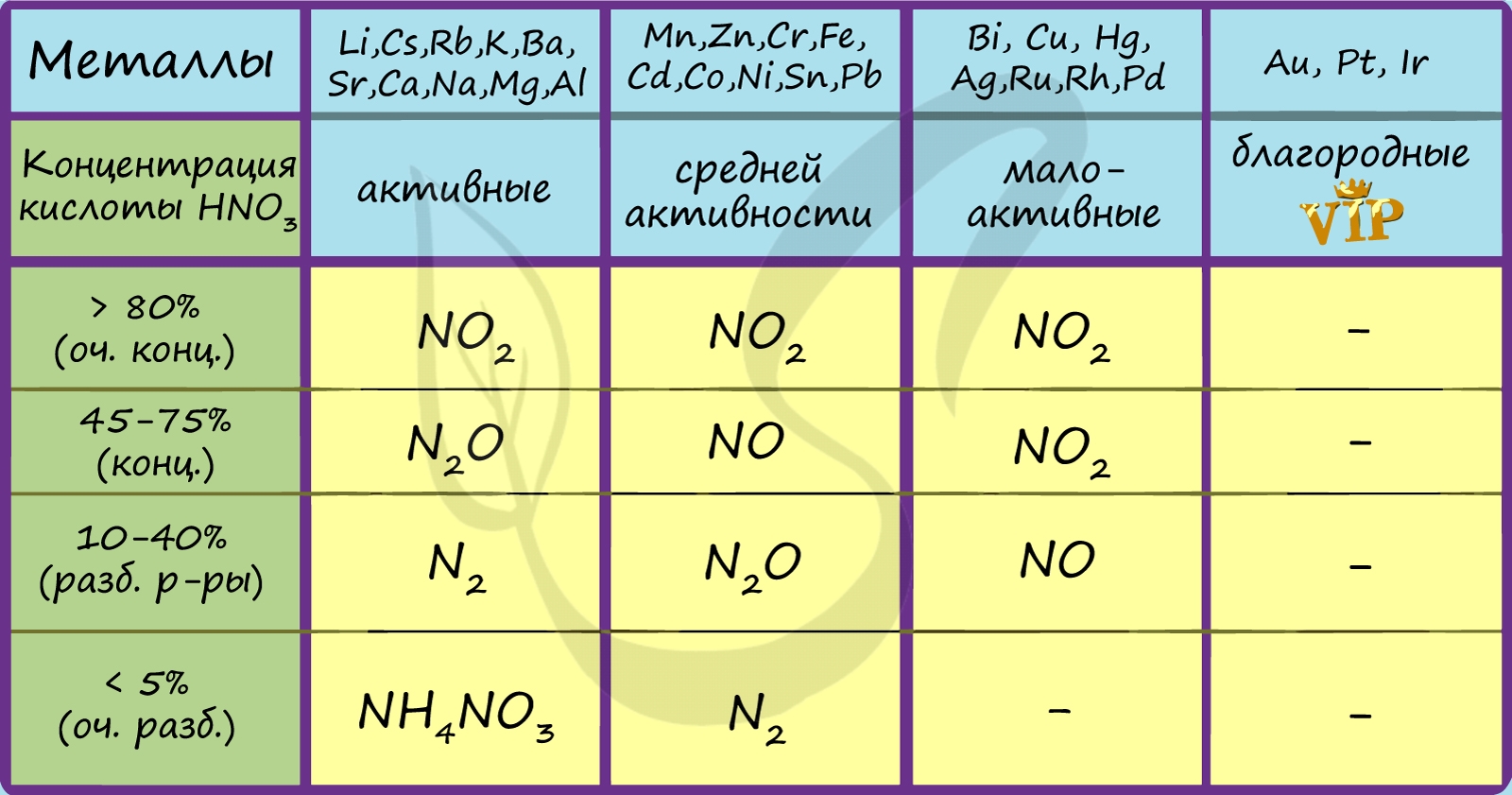
5. Азотная кислота активно взаимодействует с металлами. При этом никогда не выделяется водород! При взаимодействии азотной кислоты с металлами окислителем всегда выступает азот +5. Азот в степени окисления +5 может восстанавливаться до степеней окисления -3, 0, +1, +2 или +4 в зависимости от концентрации кислоты и активности металла.
металл + HNO3 → нитрат металла + вода + газ (или соль аммония)
С алюминием, хромом и железом на холоду концентрированная HNO3 не реагирует – кислота «пассивирует» металлы, т.к. на их поверхности образуется пленка оксидов, непроницаемая для концентрированной азотной кислоты. При нагревании реакция идет. При этом азот восстанавливается до степени окисления +4:
Золото и платина не реагируют с азотной кислотой, но растворяются в «царской водке» – смеси концентрированных азотной и соляной кислот в соотношении 1 : 3 (по объему):
HNO3 + 3HCl + Au → AuCl3 + NO + 2H2O
Концентрированная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (IV), азот восстанавливается минимально:
С активными металлами (щелочными и щелочноземельными) концентрированная азотная кислота реагирует с образованием оксида азота (I):
Разбавленная азотная кислота взаимодействует с неактивными металлами и металлами средней активности (в ряду электрохимической активности после алюминия). При этом образуется оксид азота (II).
С активными металлами (щелочными и щелочноземельными), а также оловом и железом разбавленная азотная кислота реагирует с образованием молекулярного азота:
При взаимодействии кальция и магния с азотной кислотой любой концентрации (кроме очень разбавленной) образуется оксид азота (I):
Очень разбавленная азотная кислота реагирует с металлами с образованием нитрата аммония:
Таблица . Взаимодействие азотной кислоты с металлами.
| Азотная кислота | ||||
| Концентрированная | Разбавленная | |||
| с Fe, Al, Cr | с неактивными металлами и металлами средней активности (после Al) | с щелочными и щелочноземельными металлами | с неактивными металлами и металлами средней активности (после Al) | с металлами до Al в ряду активности, Sn, Fe |
| пассивация при низкой Т | образуется NO2 | образуется N2O | образуется NO | образуется N2 |
6. Азотная кислота окисляет и неметаллы (кроме кислорода, водорода, хлора, фтора и некоторых других). При взаимодействии с неметаллами HNO3 обычно восстанавливается до NO или NO2, неметаллы окисляются до соответствующих кислот, либо оксидов (если кислота неустойчива).
Например , азотная кислота окисляет серу, фосфор, углерод, йод:
Безводная азотная кислота – сильный окислитель. Поэтому она легко взаимодействует с красным и белым фосфором . Реакция с белым фосфором протекает очень бурно. Иногда она сопровождается взрывом.
Видеоопыт взаимодействия фосфора с безводной азотной кислотой можно посмотреть здесь.
Видеоопыт взаимодействия угля с безводной азотной кислотой можно посмотреть здесь.
7. Концентрированная а зотная кислота окисляет сложные вещества (в которых есть элементы в отрицательной, либо промежуточной степени окисления): сульфиды металлов, сероводород, фосфиды, йодиды, соединения железа (II) и др. При этом азот восстанавливается до NO2, неметаллы окисляются до соответствующих кислот (или оксидов), а металлы окисляются до устойчивых степеней окисления.
Например , азотная кислота окисляет оксид серы (IV):
Еще пример : азотная кислота окисляет иодоводород:
Сера в степени окисления -2 окисляется без нагревания до простого вещества, при нагревании до серной кислоты.
Например , сероводород окисляется азотной кислотой без нагревания до молекулярной серы:
При нагревании до серной кислоты:
Соединения железа (II) азотная кислота окисляет до соединений железа (III):
8. Азотная кислота окрашивает белки в оранжево-желтый цвет («ксантопротеиновая реакция«).
Ксантопротеиновую реакцию проводят для обнаружения белков, содержащих в своем составе ароматические аминокислоты. К раствору белка прибавляем концентрированную азотную кислоту. Белок свертывается. При нагревании белок желтеет. При добавлении избытка аммиака окраска переходит в оранжевую.
Видеоопыт обнаружения белков с помощью азотной кислоты можно посмотреть здесь.
Источник
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.
В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.
При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
Реакции с неметаллами
Азотная кислота способна окислить все неметаллы, при этом, если кислота концентрированная, азот обычно восстанавливается до NO2, если разбавленная — до NO.
В любой концентрации азотная кислота проявляет свойства окислителя, при этом азот восстанавливается до степени окисления от +5 до -3. На какой именно степени окисления остановится азот, зависит от активности металла и концентрации азотной кислоты.
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.
Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Соли азотной кислоты — нитраты NO3 —
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.
Нитрат аммония получают реакция аммиака с азотной кислотой.
Обратите внимание на следующую закономерность: концентрированная азотная кислота, как правило, окисляет железо и хром до +3. Разбавленная кислота — до +2.
- Реакции с металлами, основаниями и кислотами
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
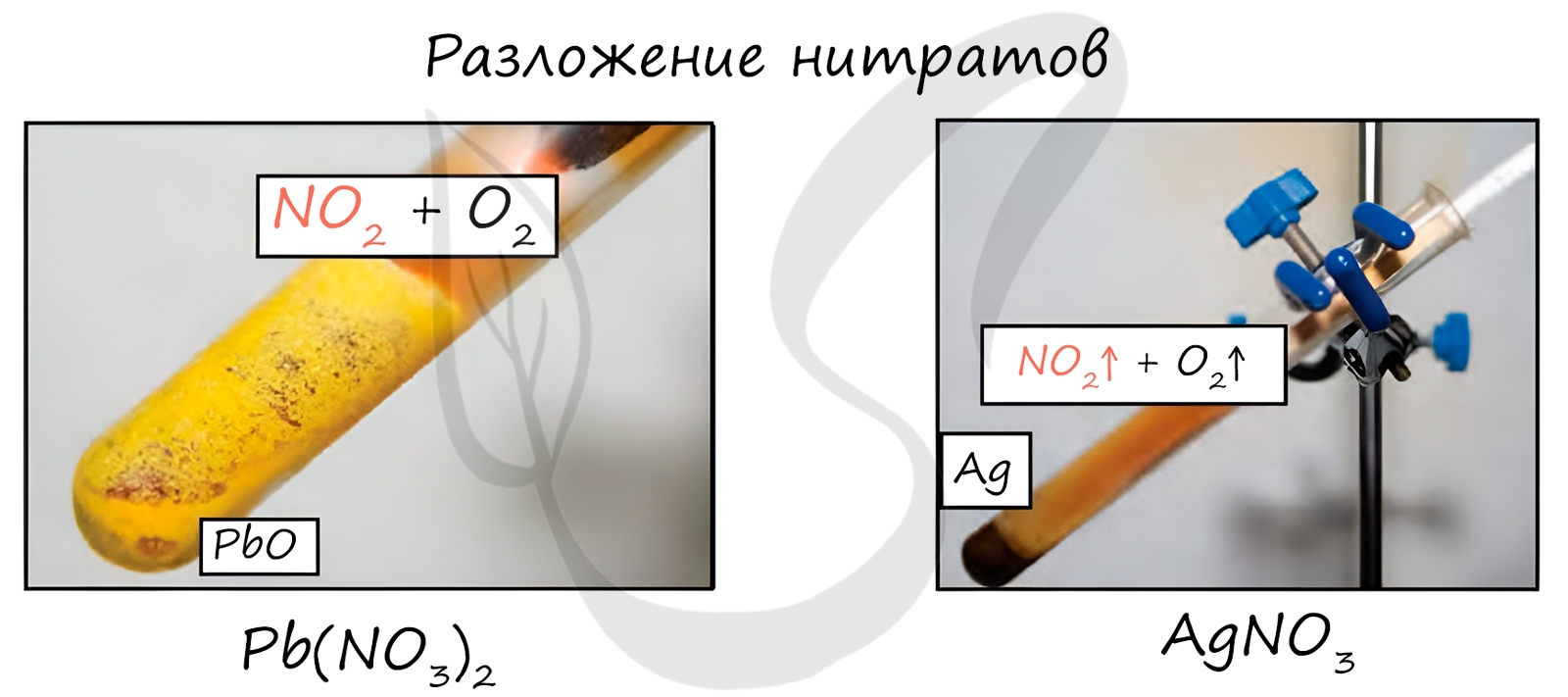
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
Основные свойства и описание способов получения азотной кислоты
Одно из значимых кислородных соединений азота — азотная кислота, получение которой имеет большое промышленное значение. Она используется при производстве химических удобрений, красителей, пластмасс, синтетических волокон, и даже взрывчатки. Это сильный окислитель, поэтому при работе с этим веществом важно соблюдать все меры предосторожности.
Описание основных характеристик
При нормальных условиях азотная кислота (формула HNO3) — жидкость без окраски с характерным запахом (резкий, удушливый). При длительном хранении цвет соединения меняется на желтый. Физические свойства:
- Плотность — 1г/см3.
- Температура кипения 86 °C.
- Температура затвердевания -41,15°C.
С водой она смешивается в любых пропорциях. Растворенный в воде диоксид азота придает смеси желтоватый цвет. Безводная HNO3 «дымит» на воздухе. Кипение сопровождается частичным распадом: 4HNO3 → 2H2O + 4NO2 + O2.
Справка: цвет «дыма» зависит от концентрации кислоты. Он белый, если содержание HNO3 в смеси составляет 86−95%, и становится красным, если насыщенность 95% и выше.
На практике обычно используют не дымящую (концентрация 98−100%) азотную кислоту, а ее 63% раствор (считается насыщенным), плотность которого 1,44 г/см3.
В небольших количествах это соединение образуется во время грозы: при разрядах молний, а также в дождевой воде.
Химические признаки
В водных растворах азотная кислота диссоциирует (делится на несколько молекулярных элементов) полностью, поэтому она относится к сильным кислотам. Благодаря своим высоким окислительным свойствам она может взаимодействовать с целым рядом неметаллов:
- P + HNO3 → HPO3 + 5NO2 + 2H2O.
- S + 6HNO3 → H2SO4 + 6NO2 + 2H2O.
При этом неметаллы окисляются до своей высшей степени.
Реакции окисления с металлами значительно отличаются от тех, что происходят при воздействии на них серной или соляной кислотами: при взаимодействии с HNO3 не выделяется водород (H2):
- Zn + 4HNO3 → Zn (NO3)2 + 2NO2 + H2O.
- 3Zn + 8HNO3 → 3Zn (NO3)2 + 2NO + 4H2O.
Особенностью реакций с металлами (Me) является и то, что при их взаимодействии только часть кислоты затрачивается на получение соответствующей соли (нитрата), а ее остаток ведет себя как окислитель, восстанавливаясь в зависимости от природы Me и концентрации HNO3, до диоксида азота, монооксида, и даже аммиака.
Не подвергаются действию кислоты только золото (Au), платина (Pt), родий (Rh), рутений (Ru), иридий (Ir) и тантал (Ta). Концентрированная HNO3 переводит в неактивное состояние алюминий (Al), железо (Fe) и хром (Cr). При этом образуются нерастворимые оксидные пленки: 2Al + 6HNO3 → Al2O3 + 6NO2 + 3H2O.
Перевозят и хранят эту кислоту в стальных емкостях.
Если взять один объем концентрированной (63%) азотной кислоты и 3 объема соляной кислоты (конц.), можно получить «царскую водку». В ней растворяются золото (Au) и платина (Pt):
- Au + HNO3 + 4HCl → H (AuCL4) + NO + 2H2O.
- 3Pt + 4HNO3 + 18HCl → 3H2 (PtCl6) + 4NO + 8H2O.
Воздействие царской водки заключается в том, что HNO3 окисляет HCL (соляная кислота — водный раствор хлороводорода), выделяя при этом свободный хлор и нитрозилхлорид: HNO3 + 3HCl → NOCl + Cl2 + 2H2O.
Нитрозилхлорид — неустойчивое соединение, которое распадается на монооксид азота и атомарный хлор: NOCl → NO + Cl.
Атомарный хлор обладает высокой реакционной способностью. При взаимодействии с ним металлы образую комплексные хлориды.
Варианты получения HNO3
Впервые соединение было получено еще алхимиками: «жгучее» вещество образовалось при нагревании гептагидрата и калийной селитры («домашний» способ): 4KNO3 + 2FeSO4•7H2O → Fe2O3 + 2K2SO4 + 2HNO3 + 2NO2 + 6H2O, где:
- FeSO4•7H2O — гептагидрат, или «железный купорос».
- Fe2O3 — оксид железа, или «железный сурик».
- K2SO4 — сульфат калия — ценное бесхлорное удобрение.
- NO2 — диоксид азота (газ) — «лисий хвост».
Сейчас ее получают в лабораториях путем воздействия на безводные нитраты концентрированной H2SO4 (серная кислота): NaNO3 + H2SO4 → HNO3 + NaHSO4.
Еще одна лабораторная схема получения — растворение в воде диоксида азота: NO2 + H2O → HNO3 + HNO2.
Примечание: такой способ используется и для получения азотистой кислоты (формула HNO2). Это слабое соединение, имеющее светло-голубую окраску, которое существует только в водных растворах или газовых смесях.
Обладает высокой токсичностью. Применяется в промышленности для получения искусственных красителей, и некоторых других областях.
Промышленный синтез HNO3 может проводиться тремя вариантами.
Речь идет о таких способах:
- Вытеснение HNO3 из ее солей серной кислотой.
- Аммиачный способ.
- Дуговой способ.
Последний метод, хотя и предоставляет возможность получить азотную кислоту нужной концентрации довольно легко, все же используется крайне редко. Причина — большой расход электроэнергии, что делает его экономически невыгодным.
Вытеснение из солей
Схема процесса описывается уравнением реакции: NaNO3 + H2SO4 → NaHSO4 + HNO3. До того, как стали разрабатывать аммиак синтетическим путем, этот способ получения HNO3 был единственным.
Сейчас в промышленности его стали использовать редко. А вот в лабораториях он продолжает находить свое применение — для получения дымящей HNO3. При этом количество H2SO4 берется с таким расчетом, чтобы образовывался гидросульфат натрия (NaHSO4).
Это позволяет провести реакции при более низкой температуре и уменьшить потери синтезируемого вещества, выделяющиеся пары которого отводят в охлаждаемый сосуд, где они конденсируются (переходят из газообразного состояния в жидкое).
Дуговой способ
В этом случае HNO3 образуется при продувании воздуха через электрическую дугу, дающую температуру 3000−3500°C. Схема процесса включает реакции:
- N2 + O2 → 2NO.
- 2NO + O2 → 2NO2.
- 4NO2 + O2 + 2H2O → 4HNO3.
Некоторая доля азота, находящегося в воздухе, взаимодействует с кислородом. В результате процесса образуется монооксид (NO), который после остывания смеси окисляется до диоксида (NO2) — при повышенной температуре реакция протекать не будет, так как монооксид с кислородом не взаимодействует.
Полученный диоксид (NO2) разводят водой. В результате на выходе образуется азотная кислота и окись азота. Если провести эту же реакцию, но в присутствии избытка O2, почти весь диоксид «преобразуется» в HNO3.
Аммиачный метод
Процесс заключается в окислении аммиака на Pt-катализаторе.
По итогу реакции образуется монооксид азота. Полученные нитрозные газы остужают, а выделенную в процессе синтеза двуокись (NO2) поглощают водой. Этот метод позволяет получить только 60−62% раствор HNO3.
Чтобы синтезировать более концентрированный продукт (дымящую HNO3), полученные растворы упаривают в присутствии серной кислоты (если ее не использовать, результатом перегонки так и останется 60% HNO3) или растворяют в них при повышенном давлении жидкий NO2. Для этой цели в качестве исходного сырья можно использовать и димер азота: 2N2O4 + O2 + 2H2O → 4HNO3.
Реакция протекает только в условиях повышенного давления.
Меры безопасности
Этот реактив относится к 3 классу опасности, поэтому при работе нужно соблюдать определенные правила. Все сотрудники, занятые на производстве, должны находиться в специальной одежде, которая не будет легко воспламеняться, но станет препятствовать попаданию на тело брызг вещества (например, в защитных комбинезонах). Кроме того, необходимо иметь:
- Кислотозащитные рукавицы.
- Особую обувь, не поддающуюся воздействию кислот.
- Нитриловые перчатки (нитрил — материал, являющийся заменителем природного каучука).
- Респираторы.
- Очки.
В лабораториях опыты с концентрированной HNO3 разрешается проводить только в защитной одежде: как минимум должен быть халат, обязательно из хлопка — синтетику нельзя категорически. Почему выбирают хлопковые вещи: они не вспыхивают при попадании на них различных химических реактивов, а только тлеют. В то же время материал, в случае возникновения форс-мажорной ситуации, можно легко сорвать с человека, чтобы он мог избежать ожогов.
Попадание на кожу растворов соединения приведет к сильным ожогам. А вдыхание его паров — к отравлениям, и даже отеку легких.
Источник