Получение соляной кислоты сульфатным методом
Сульфатный метод – это самый старый метод получения соляной кислоты. Его используют, когда есть потребность в 
Сульфатный метод протекает по следующим реакциям:
Сырьем для получения хлористого водорода и сульфата натрия служат поваренная соль (обычно измельченная каменная соль – бузун) и купоросное масло – 92 % – 93 % – я серная кислота. Менее концентрированную серную кислоту не применяют, так как в этом случае хлористый водород был бы чрезмерно разбавлен парами воды, что затруднило бы получение концентрированной соляной кислоты. Применение крупнозернистой выварочной соли предпочтительнее вследствие ее пористости – она легко пропитывается кислотой с образованием однородной массы. Однако выварочная соль содержит переменное количество влаги, что затрудняет дозировку сырья и регулирование температурного режима печей. Каменная соль характеризуется постоянной влажностью, но она более загрязнена примесями.
Реакция между хлористым натрием и серной кислотой – эндотермическая.
Взаимодействие хлористого натрия с серной кислотой начинается даже при 0 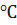
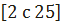
Реакция между поваренной солью и серной кислотой осуществляется в механических или во вращающихся печах.
На рисунке 1 показана механическая сульфатная печь. Она предназначена для получения хлороводорода, представляет собой муфель, под (чаша) 12 и свод 11 которого сложены из фасонных огнеупорных и кислотостойких шамотных плит. Под муфелем и над ним расположены дымоходы. Толщина плит пода 120 мм; свод муфеля для облегчения передачи тепла к реакционной массе делают более тонким – 30 мм. Внутреннюю кладку печи и топки выполняют из шамотного, а наружную – из простого кирпича. Под печью расположен привод мешалки. Поваренная соль через загрузочную воронку непрерывно поступает в центр муфеля с помощью шнекового питателя 8. Туда же по трубе подается купоросное масло. Оно поступает в укрепленный на головке вала и вращающийся вместе с ним распределитель 13 кислоты, имеющий форму чайника, через носик которого сливается в муфель.
1 – шахтная топка; 2 – загрузочная коробка для топлива; 3 – колосниковая решетка; 4 – зольник; 5 – топочный порог; 6 – канал для вторичного воздуха; 7 – загрузочная воронка для соли; 8 – загрузочный шнек для соли; 9 – солевая труба; 10 – кислотная труба; 11 – свод муфеля; 12 – под муфеля; 13 – питатель – распределитель кислоты; 14 – головка мешалки; 15 – вал мешалки; 16 – коронная шестерня привода мешалки; 17 – люк для выхода сульфата натрия; 18 – холодильно – размольный барабан для сульфата; 19 – труба для отвода хлористого водорода.
Рисунок 1 – Механическая сульфатная печь (вертикальный разрез)
Перемешивание поваренной соли и кислоты и передвижение реакционной массы по поду муфеля от центра к периферии производится укрепленной на чугунном валу 15 мешалкой с четырьмя плечами, расположенными крестообразно, на каждом из которых имеется по два (всего восемь) термосилидовых или чугунных гребков с керамическими или корборундовыми наконечниками. Вращение вала (0,75 – 1,25 об/мин) производится через зубчатую передачу электромотором мощностью 4,5 квт при диаметре муфеля 4,25 м и 6,8 квт при диаметре муфеля 5,5 м.
Обогрев муфеля, температуру в котором поддерживают в пределах 500 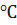
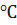
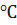
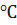

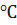
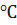
Полученный хлористый водород отправляется на абсорбцию. В соответствии с этим абсорбционные установки сооружены таким образом, чтобы обеспечить наиболее полный отвод тепла гидратации HCl. Обычно газ вначале охлаждают в длинных газопроводах и керамических холодильниках. Охлаждение совмещают с осушкой газа, что дает возможность получать более концентрированную соляную кислоту до 37 % 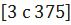
Источник
ПОЛУЧЕНИЕ ХЛОРИСТОГО ВОДОРОДА
Сырьем для получения хлористого водорода и сульфата натрия служат поваренная соль (обычно измельченная каменная соль — бузун) и купоросное масло — 92—93%-ная серная кислота. Менее концентрированную серную кислоту не применяют, так как в этом случае хлористый водород был бы чрезмерно разбавлен парами воды, что затруднило бы получение концентрированной соляной кислоты. Применение крупнозернистой выварочной соли предпочтительнее вследствие ее пористости — она легко пропитывается кислотой с образованием однородной массы. Однако выварочная соль содержит переменное количество влаги, что затрудняет дозировку сырья и регулирование температурного режима печей. Каменная соль характеризуется постоянной влажностью, но она более загрязнена примесями CaS04, Fe203 и другими (см. гл. III), переходящими в сульфат натрия. Помимо этого, применение каменной соли связано с необходимостью ее измельчения и более интенсивного перемешивания с серной кислотой34.
Физико-химические основы взаимодействия хлористого натрия с серной кислотой
Реакция между хлористым натрием и серной кислотой 2NaCl + H2S04 = Na2SO., + 2НС1
— эндотермическая. При применении серной кислоты концентрацией меньше 100% расход тепла на реакцию увеличивается за счет дегидратации серной кислоты. В табл. 31 приведены значения теплового эффекта АН и изменения изоба^ ого потенциала AZ для Некоторых реакций взаимодействия NaCl С серной кислотой и кислыми сульфатами натрия при различных температурах85.
Значения ДИ и SZ Реакций взаимодействия хлористого натрия с серной кислотой и кислыми сульфатами натрия
2NaCI + H2S04 (ж., 100%) «= Na8S04 + 2НС] (г.)
2NaCl + H2S04 (ж., 03%) =
NaCl + H2S04 (ж., 100%) =
NaCl + H2S04 (ж., 93%) = NaHS04 +
NaCl+2NaHS04 = Na3H(S04)2 + HCl (г.)
NaCl + Na3H(S04)s = 2Na2S04 + HCl (г.)
Взаимодействие хлористого натрия с серной кислотой начинается даже при 0° с выделением в газовую фазу почти безводного НС1, но быстро прекращается; жидкая фаза представляет собой раствор образовавшегося сульфата натрия в серной кислоте. При нагревании реакция возобновляется — одновременно с хлористым водородом удаляется водяной пар вследствие дегидратации серной кислоты. Обезвоживание жидкой фазы облегчается тем, что растворение образующегося сульфата натрия в серной кислоте повышает равновесное давление водяного пара.
В системе Na2S04—H2S04—Н20 при 25° существуют следующие твердые фазы: Na2S04 • 10Н20, Na2S04 • 4,5Н20, Na2S04, NasH(S04)2, NaHS04-H20, NaHS04 и NaH3(S04)2 • H20. При 0й существуют эти же фазы и H2S04-H20; NaH3(S04)2 • Н20 находится в метастабильном состоянии, имеется метастабильная фаза Na2S04 • 5,5Н20 36. Однако поскольку реакцию с хлористым натрием ведут при высокой температуре и используют концентрированную серную кислоту, содержащую очень мало воды, вскоре удаляющейся в газовую фазу, практически процессы идут в без
водной системе. В зависимости от температуры реакционной массы образующийся сульфат натрия может полностью оставаться в жидкой фазе или частично кристаллизоваться из нее в виде кислых солей: 2Na2S04-9H2S04, Na2S04 • 2H2S04, Na2S04-H2S04 (бисульфат или гидросульфат натрия NaHS04) и 3Na2S04 • H2S04 [тринатрийгидросульфат Na3H(S04)2]. Нейтральный сульфат кристаллизуется только в заключительной стадии процесса37.
На рис. 114 дана диаграмма растворимости в двойной системе H2S04—Na2S0437. Молярные проценты Na2S04 (верхняя шкала) численно равны степени превращения NaCl в Na2S04. Растворимость сульфата натрия в серной кислоте сильно возрастает, начиная от 4% (вес.) при 0° до 59% при 186°. При повышении температуры до 270° растворимость увеличивается до 67%.
Во избежание преждевременного затвердевания реакционной массы необходимо, чтобы температура на каждой стадии процесса была не ниже той, при которой исчезает жидкая фаза. Реакция в сульфатных печах протекает с высокой интенсивностью, если температурные условия не допускают значительной кристаллизации промежуточных кислых сульфатов натрия. Так, если успела прореагировать третья часть хлористого натрия, а температура при этом еще не достигла 109°, вся масса затвердевает в смесь кристаллов NaCl и Na2S04-2H2S04. Когда в некоторой зоне печи, где температура ниже 186°, NaCl прореагировал на 50%, там будут находиться в твердом состоянии хлористый натрий и бисульфат натрия— жидкая фаза будет отсутствовать. Если NaCl прореагировал на 75% и температура будет ниже 270°, реакционная масса полностью затвердевает, образуя конгломерат, состоящий из остатка NaCl и Na3H(S04)2. Последний особенно часто образуется в сульфатных печах. Выше 270° тринатрийгидросульфат инконгруэнтно плавится, и освобождающаяся серная кислота реагирует с оставшимся хлористым натрием — появляется кристаллический нейтральный сульфат натрия.
Примерное содержание NaCl И Na2S04 В реакционной массе при различной степени разложения NaCl
NaCl, вес. К Na2S04, вас. К разложения NaCl,
Источник
Получение хлороводорода сульфатным способом
Хлороводород, полученный при действии избытка серной кислоты на навеску хлорида натрия массой 11,7 г, пропустили через 100 г 14%-го раствора гидроксида калия. Полученный раствор выпарили. Определите массу твёрдого остатка и его состав (в массовых долях).
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите необходимые вычисления с указанием единиц измерения искомых физических величин.
1) Написаны уравнения всех реакций:
(принимается также )
2) Проведён расчёт по первому уравнению реакции:
3) Проведён расчёт по второму уравнению реакции:
4) Определена масса твёрдого остатка и рассчитан его состав:
| Критерии оценивания выполнения задания | Баллы |
|---|---|
| Ответ правильный и полный: − в ответе правильно записаны уравнения реакций, соответствующих условию задания; − правильно произведены вычисления, в которых используются необходимые физические величины, заданные в условии задания; − продемонстрирована логически обоснованная взаимосвязь физических величин, на основании которых проводятся расчёты; − в соответствии с условием задания определена искомая физическая величина | 4 |
| Допущена ошибка только в одном из перечисленных выше элементов ответа | 3 |
| Допущены ошибки в двух из перечисленных выше элементах ответа | 2 |
| Допущены ошибки в трёх из перечисленных выше элементах ответа | 1 |
| Все элементы ответа записаны неверно. | 0 |
| Максимальный балл | 4 |
Примечание. В случае, когда в ответе содержится ошибка в вычислениях в одном из трёх элементов (втором, третьем или четвёртом), которая привела к неверному ответу, оценка за выполнение задания снижается только на 1 балл.
Источник








