РОСПОТРЕБНАДЗОР по РТ
РОСПОТРЕБНАДЗОР по РТ
Основные меры профилактики инфекций в общественных местах — RSS
Основные меры профилактики инфекций в общественных местах
Основные меры профилактики инфекций в общественных местах
Снижение иммунитета, плохая экология, активный ритм жизни, некачественное питание и недостаток витаминов способствуют проникновению вирусов и бактерий через естественные защитные механизмы организма человека и вследствие этого вызывают инфекционные заболевания.
Для инфекционных заболеваний характерно наличие инкубационного периода, длительность которого зависит от совокупности различных факторов, начиная от способа попадания вируса в организм и заканчивая типом патогенных микроорганизмов.
Использование эффективных мер профилактики позволяют снизить скорость передачи инфекции и сократить количество заболевших.
Механизмы и пути передачи инфекции
Для того чтобы предпринимать адекватные меры при профилактике инфекционного заболевания, необходимо знать, каким именно образом оно попадает в организм человека.
В настоящее время выделяют следующие основные механизмы и пути передачи инфекционных заболеваний:
· аэрозольный, реализуемый воздушно-капельным и воздушно-пылевым путем передачи. Передаются от человека к человеку при вдыхании воздуха, пыли, наполненного вирусами и бактериями, которые выделяются больным при кашле и чихании. К данному виду заболеваний относятся все типы вирусных инфекций: грипп, аденовирусная инфекция, корь, ветряная оспа, краснуха, а также туберкулез, дифтерия, коклюш, менингококковая инфекция.
· фекально-оральныймеханизм передачи инфекции, когда микроорганизмы передаются через зараженные пищевые продукты, грязные руки, воду, Передача данным путем характерна для дизентерии, сальмонеллеза, холеры, различных видов вирусных кишечных инфекций, полиомиелита, гепатита А, брюшного тифа.
· контактно-бытовой механизм передачи при непосредственном контакте с возбудителем инфекции, либо через зараженные предметы обихода.
Такими заболеваниями могут являться половые инфекции, в т. ч. ВИЧ-инфекция, сифилис, герпес, чесотка, бешенство, столбняк.
· трансмиссивнымпутем через укусы насекомых могут передаваться сыпной тиф, малярия, чума, клещевой энцефалит.
Помимо профилактики инфекционных заболеваний с помощью создания специфического иммунитета вакцинами, медицинскими препаратами, стимулирующими общий и местный иммунитет, повышающих резистентность организма к инфекционным заболеваниям существуют простые правила неспецифической профилактики и личной гигиены, выполнение которых поможет предотвратить инфекционное заболевание.
Меры профилактики воздушно-капельных инфекционных заболеваний
· закаливание организма с использованием различных водных процедур;
· выполнение регулярных физических упражнений;
· ежедневное проведение влажной уборки с использованием дезинфицирующих средств, а также частое проветривание помещений;
· промывание слизистых носа и ротоглотки антисептическими растворами;
· соблюдение основных правил личной гигиены (тщательное мытье рук, использование собственного полотенца);
· ограничение контактов в период распространения инфекции, ограничение посещения мест скопления людей.
Меры профилактики фекально-оральных инфекционных заболеваний
· всегда мойте руки с мылом после прихода с улицы и посещения туалета, а также перед едой;
· тщательно следите за сроками годности, указанными на упаковках приобретаемых продуктов;
· не допускайте прямого контакта готовых к употреблению и сырых продуктов (особенно мясных изделий и рыбы);
· при приготовлении пищи подвергайте сырые продукты тщательной термической обработке;
· не оставляйте приготовленные блюда надолго на столе;
· пейте только кипяченую или бутилированную воду;
· избегайте принимать пищу в местах несанкционированной торговли;
· при купании в открытых водоемах избегайте заглатывания воды.
Меры профилактики контактно-бытовых инфекционных заболеваний
· необходимо тщательно обрабатывать предметы и вещи, используемые большим количеством людей одновременно (к примеру, игрушки в детском саду);
· требуется соблюдать гигиену и регулярно мыть руки, при посещении мест общего пользования (бань, саун) иметь при себе предметы личной гигиены;
· желательно отказаться от случайных половых контактов и всегда использовать в качестве способа предохранения презерватив.
Меры профилактики трансмиссивных инфекционных заболеваний
· использовать одежду, максимально защищающую открытые участки тела, проводить осмотр кожных покровов каждые 2-3 часа во время отдыха на природе, использовать реппеленты;
· при выезде в экваториальные страны сделать все необходимые прививки и соблюдать повышенные меры безопасности;
В окружающем нас мире находится огромное количество патогенных микроорганизмов, провоцирующих развитие инфекционных заболеваний, поэтому очень важно своевременно применять необходимые меры профилактики для снижения риска распространения инфекции.
Будьте здоровы и старайтесь предотвратить инфекционные заболевания путем профилактики.
Источник
Профилактика инфекционно-воспалительных осложнений после перкутанной нефролитотрипсии с использованием препарата пиобактериофага
Перепанова Т.С., Меринов Д.С., Казаченко А.В., Толордава Э.Л., Малова Ю.А.
Развитие инфекционно-воспалительных осложнений (ИВО) после урологических операций чаще всего связано с госпитальной инфекцией, однако после перкутанной нефролитотрипсии (ПНЛТ) развитие ИВО имеет свои особенности. Наличие биопленок снаружи и внутри камня, особенно коралловидного, способствует высвобождению эндотоксина и других факторов патогенности возбудителей во время дробления камня. Развитие синдрома системной воспалительной реакции (ССВР) после ПНЛТ часто расценивается как «атака пиелонефрита» и пациентов лечат соответственно этому диагнозу.
Конечно, у части пациентов состояние может осложниться развитием тяжелых инфекционных осложнений – бактериемии, уросепсиса, пиелонефрита и т.д. M.S. Michel с соавт. отмечали развитие лихорадки у 21,0-32,1% больных, тогда как такие тяжелые осложнения, как септицемия встречались в 0,3-4,7% [1]. Лихорадка, развившаяся в послеоперационном периоде после ПНЛТ была отмечена у 10,5% больных в исследовании CROES study. Однако, как отмечают авторы, не всегда она ассоциировалась с развитием инфекционного процесса [2].
В исследовании M. Rivera пациенты получали обширную антибактериальную терапию при наличии положительного культурального анализа мочи или камня, всем остальным проводили антимикробную терапию в течение 7 дней до и 7 дней после ПНЛТ. Авторы пытались идентифицировать пре- и послеоперационные предикторы инфекционных осложнений. Из 227 пациентов, подвергшихся ПНЛТ инфекционные осложнения отмечены у 37 (16%), из них: у 11 (5%) ИМП/пиелонефрит; у 21 (9%) – ССВР и у 2-х пациентов (0.9%) развился сепсис.
Не отмечено значительных различий в группах пациентов с инфекционными осложнениями и без них в отношении возраста, пола, размера камня, наличия сахарного диабета или длительности операции. По результатам проведенного однофакторного анализа выявлено, что наличие струвитного состава камня, положительной культуры камня во время операции, коралловидного камня и множественных камней, ассоциировалось с риском послеоперационных инфекционных осложнений.
Однако при проведении мультивариантного анализа выявлено, что только коралловидные камни ассоциировались с развитием лихорадки/ССВР/сепсиса (OR 3.14; p=0,02) и общими инфекционными осложнениями (OR 2,53; p=0,02) [(3]. К независимым факторам риска развития ИВО после ПНЛТ также относят наличие сахарного диабета (OR=4,511, p=0,001), длительность операции (OR=2,588, p=0,043, длительную ирригацию (OR=2,353, p=0,036) и инфекционный генез камней (OR=5,862, p=0,001)[4].
Также наличие положительной культуры камня и антеградный стент, как факторы риска развития послеоперационных ИВО, подтверждают и S. Bolomytis и соавт. [5], тогда как наличие резидуальных камней и множественных доступов во время ПНЛТ не являлись факторами риска. В руководстве Европейской урологической Ассоциации (ЕУА) 2018 г. опубликовано всего 10 строчек об эффективности разных режимов антибактериальной профилактики перед нефролитотрипсией [6].
Сравнив частоту развития ССВР после ПНЛТ при применении комбинации сульбактама/ампициллина или цефуроксима не выявлено различий в показателях ССВР или уросепсиса [7]. E. Tuzel и соавт. сравнивали однократное введение цефтриаксона и комбинацию цефтриаксона и цефалоспорина 3-го поколения до удаления нефростомы (в среднем, через 1-3 дня) у 73 пациентов. Они не обнаружили различий в частоте инфекционных осложнений между двумя режимами [8].
Таким образом, Руководство ЕУА рекомендует однократно вводить профилактическую дозу антибиотика для снижения риска симптоматических ИМП после перкутанной нефролитотрипсии, причем степень рекомендации – сильная [6]. Развитию инфекционных осложнений также способствует установка уретральных катетеров, стентов, нефростом после ПНЛТ с развитием т.н. «катетер-ассоциированной инфекции мочевых путей». С первых часов установки катетеров и дренажей начинается контаминация их микроорганизмами с формированием различных биопленок на их поверхностях.
В условиях антибиотикорезистентности, а также с учетом специфики возникновения развития мочевой инфекции после перкутанной нефролитотрипсии, актуален поиск альтернативных методов, направленных на улучшение результатов лечения пациентов с камнями почек инфекционного генеза, уменьшение числа рецидивов камней после перкутанной нефролитотрипсии.
Одной из таких альтернатив может стать применение препаратов бактериофагов до и после перкутанной нефролитотрипсии. Наши исследования, проведенные совместно с НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалеи показали возможность проникновения бактериофагов в биопленки.
МАТЕРИАЛЫ И МЕТОДЫ
Наблюдательное исследование проведено на базе 1-го урологического отделения НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиала НМИЦ радиологии Минздрава России в 2018 г.
Цель исследования: изучение эффективности применения Пиобактериофага поливалентного очищенного для лечения и профилактики развития инфекционных осложнений после перкутанной нефролитотрипсии.
Исследование проведено у 60 пациентов с большими и коралловидными камнями почек, которым выполняли ПНЛТ. Больным проводили антимикробную периоперационную профилактику: за 2 часа до операции назначали либо антибиотик, либо препарат пиобактериофаг. Также помещали на 30 минут до операции уретральные катетеры и дренажи в препарат пиобактериофага. Временные отрезки выбраны на основании результатов предварительно проведенных научных исследований в НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалеи (2016-2018гг). Эти исследования показали, что предварительная обработка катетеров фаговыми препаратами несколько уменьшает количество микроорганизмов, прикрепленных к поверхности катетеров (рис. 1).
При этом, увеличение времени экспозиции катетера в фаговом растворе никакого существенного значения не имело. В то же время при исследовании влияния препаратов бактериофагов на уже сформированные биопленки клиническими изолятами микроорганизмов было показано, что препарат бактериофага способен разрушать «свежие» (сформированные в течение 2-6 часов) бактериальные биопленки (рис. 2). Исследования «in vitro» показали, что оптимальным временем инкубации «зрелой» (суточной) биопленки в фаговом препарате является 18 часов. При таком времени инкубации зрелая биопленка практически полностью гибнет.
Таким образом, проведенные исследования препарата «Пиобактериофаг поливалентный очищенный» в НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалеи показали следующее:
- обработка катетеров фаговым препаратом замедляет процесс обсеменения катетеров микроорганизмами;
- оптимальное время экспозиции фагового препарата на поверхности катетеров/нефростом 30 мин;
- «Пиобактериофаг поливалентный очищенный» разрушает свежую бактериальную биопленку. Более длительная инкубация фагового препарата (в течение 18 часов) способна разрушать даже зрелые (суточные) бактериальные пленки.
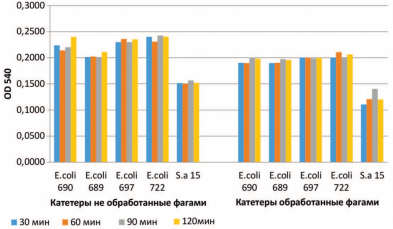
Рис. 1. Сравнительный анализ микробного обсеменения нативных катетеров и катетеров, обработанных фаговыми препаратами в динамике. OD 540 – оптическая плотность при длине волны 540 нм
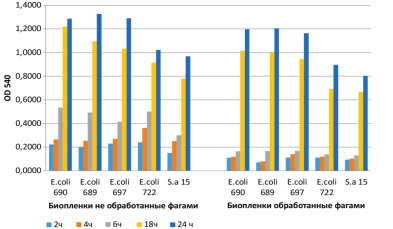
Рис. 2. Влияние фагового препарата «Пиобактериофаг поливалентный очищенный» на сформированные биопленки клинических изолятов. OD 540 – оптическая плотность при длине волны 540 нм
Исследуемый препарат: Пиобактериофаг поливалентный очищенный, производства АО «НПО «Микроген». Препарат содержит смесь очищенных фильтратов фаголизатов бактерий Staphylococcus spp, Streptococcus spp, Proteus spp, Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli.
Клиническая часть исследования Для профилактики инфекционно-воспалительных осложнений препарат Пиобактериофаг поливалентый очищенный назначали перорально в дозе 40 мл однократно внутрь за 2 часа до операции и в послеоперационном периоде по 40 мл 3 раза в день в течение 3-5 дней или проводили периоперационную антибактериальную профилактику (ципрофлоксацин 1г внутривенно капельно в течение всей операции) и антибактериальную терапию в послеоперационном периоде от 3 до 5 дней, в зависимости от результатов чувствительности выделенных микроорганизмов или продолжали ципрофлоксацин.
Катетеры и нефростомические дренажи перед их установкой погружали в раствор пиобактериофага поливалентного очищенного, время экспозиции 30 минут.
Пациенты, в зависимости от результатов бактериологического анализа мочи до операции были разделенына 4 группы (табл. 1).
Катетеры и дренажи исследовали на микрофлору (посев) во всех 4-х группах пациентов в следующие сроки:
- на 1 сутки после операции – уретральный катетер;
- на 3-4 сутки – нефростомический дренаж.
Была разработана карта наблюдения пациента, как в бумажномварианте, так и в электронном виде. Данные на пациентов заносили в таблицу EXСEL, в которых регистрировали ФИО, номер группыпо нашему исследованию, анамнестические данные, диагноз, размер и форма камня, наличие сопутствующих заболеваний (сахарный диабет, хроническая почечная недостаточность, гидронефроз).
Отмечали длительность заболевания, перенесенные операции, наличие бактериурии до операции, вид операции («перк или мини-перк»), количество доступов и установленных нефростом после ПНЛТ, наличие резидуальных (оставленных) камней. Бактериологическое исследование мочи, уретральных катетеров и нефростом выполняли в следующие сроки:
- моча до операции, на 3 и 7 сутки;
- моча из лоханки, взятой во время ее пункции при ПНЛТ;
- уретральный катетер;
- нефростома.
В таблицу также вносили данные о наличии биопленок на катетерах по результатам исследования их в лаборатории биопленок института микробиологии им. Н.Ф. Гамалеи. Обязательно регистрировали все случаи присоединения инфекционных осложнений после операции и в течение всего периода пребывания пациента в отделении.
Вносились данные: развитие ССВР и септических осложнений, уровень прокальцитонина, необходимость в дополнительном назначении антибиотиков у пациентов, леченных препаратом пиобактериофага и, наконец, результаты долгосрочного наблюдения – через 30 дней после операции: их состояние и результаты анализов мочи (по телефонному опросу, так как большинство пациентов были иногородние).
Оценку результатов исследования проводили на основании статистического анализа и экспертной оценки. Статистический анализ результатов осуществляли с помощью программ Statistica v.10, использовали непараметрические критерии статистического анализа. Сравнительный анализ между группами проведен с помощью критерия Манна-Уитни и Хи-критерия Пирсона.
Таблица 1. Распределение больных по группам и методам лечения
| Группа I профилактическая, контрольная (n-15) | Группа II основная, контрольная (n=15) | Группа III профилактическая (n=15) | Группа IV основная (n=15) |
| Пациенты с камнями почек с неинфицированной мочой (роста нет по результатам бактериологических анализов мочи) | Пациенты с камнями почек, с бактериурией по результатам бактериологических анализов мочи | Пациенты с камнями почек с неинфицированной мочой (роста нет по результатам бактериологических анализов мочи) | Пациенты с камнями почек, с бактериурией |
| Антибактериальная профилактика антибиотиком – ципрофлоксацином 1000 мг в\в капельно в течение 60 минут во время ПНЛТ. Установка катетеров, дренажей, стентов (необработанных бактериофагами). В послеоперационном периоде – антибактериальная терапия (3-5 дней) | Антибактериальная профилактика – ципрофлоксацин 1000 мг в\в капельно в течение 60 минут во время ПНЛТ. Установка катетеров, дренажей, стентов, (необработанных бактериофагами. В послеоперационном периоде – антибактериальная терапия, согласно чувствительности к антибиотикам выделенного уропатогена (3-5 дней) | Препарат пиобактериофаг применяли однократно за 2 часа до операции 40 мл перорально. Установка катетеров, дренажей, стентов, обработанных препаратом пиобактериофагом. Назначали терапию пиобактериофагом (по 40 мл 3 р. в день) после операции (3-5 дней), при наличии показаний добавляли антибиотики | Препарат пиобактериофаг применяли за 2 часа до операции 40 мл перорально. Установка катетеров, дренажей, стентов, обработанных пиобактериофагом. В послеоперационном периоде в течение 3-5 дней назначался препарат пиобактериофаг по 40 мл 3 р. в день |
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Перед тем, как начать клиническую часть исследования было проведено определение резистентности выделенных микроорганизмов у урологических пациентов нашего стационара к препаратам бактериофагов (рис. 3).
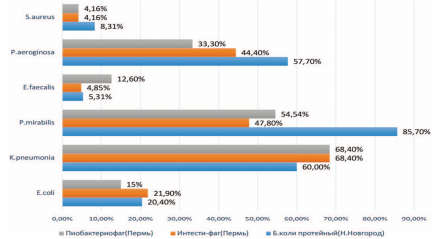
Рис. 3. Резистентность микроорганизмов к препаратм бактериофагов
Как видно из рисунка 3, наиболее устойчивыми к препаратам бактериофагов были P. aeruginosa (от 33% до 57%), P. mirabilis(от 47,8% до 85,7%), K. pneumonia (от 60% до 68%). Устойчивость E. Coli колебалась от 15 до 21%, в зависимости от препарата и производителя.
В таблице 2 перечислены микроорганизмы, которые были выделены из мочи пациентов II и IV групп до операции.
Таблица 2. Выделенные микроорганизмы из мочи пациентов до оперативного вмешательства
| Микроорганизм | Группа пациентов, получавших антибиотики (группа II) | Группа пациентов, получавших бактериофаги (группа IV) | ||
| Количество | % | Количество | % | |
| E.coli* | 11 | 73,3 | 12 | 80 |
| Klebsiella pneumoniae * | 3 | 20,0 | 1 | 6,7 |
| Streptococcus anginosus* | 1 | 6,7 | — | — |
| Providencia stuartii | — | — | 1 | 6,7 |
| Enterococcus faecalis* | — | — | 1 | 6,7 |
Во II группе, E.coli выделили у 11 пациентов, из них у 3 – совместно с Enterococcus faecalis; у одного пациента E. coli гемолитическая в титре 105 КОЕ/мл. Klebsiella pneumoniae обнаружена у трех пациентов, из них у двух – совместно с Enterococcus faecalis. Streptococcus anginosus вместе с Corynebacterium spp. 103 КОЕ/мл. выделили у 1 пациента. В IV группе пациентов с бактериурией E. coli выделили у 12 пациентов, из них у 1 – совместно с Enterococcus faecalis. В этой группе пациентов у всех выделенных возбудителей (E.coli, Klebsiella pneumoniae, Streptococcus anginosus) была выявлена чувствительность к препарату Пиобактериофагу поливалентному очищенному.
У пациентов I и III групп, которым также проводили периоперационную профилактику антибиотиками и фагами, в посеве мочи роста не выявлено.
До начала нашего исследования мы выделили 100 штаммов кишечной палочки из мочи урологических пациентов и отправили их в г. Пермь на фаговое производство НПО «Микроген» (являющегося единственным производителем препаратов бактериофагов в России). До подбора препаратов бактериофагов к нашим штаммам кишечной палочки антибактериальная активность пиобактериофага поливалентного была 72%. После подбора фагов из сточных вод из 12 городов (которые были получены с января по март 2017 г.) антибактериальная активность бактериофагов по Аппельману в разведении 10-4 и выше увеличилась до 92%.
При сравнительном анализе результатов посевов мочи на флору и чувствительность к антимикробным препаратам, взятых из лоханки почки во время ПНЛТ и мочи до операции, были получены результаты, представленные в таблице 3.
Таблица 3. Микроорганизмы, выделенные из лоханки почки во время ПНЛТ у пациентов различных групп
| Микроорганизм | Количество пациентов | % |
| Группа I | ||
| Роста микрофлоры не выявлено | 14 | 93,3 |
| Klebsiella pneumoniae | 1 | 6,7 |
| Группа II | ||
| Роста микрофлоры не выявлено | 5 | 33,3 |
| Enterococcus faecalis | 2 | 13,3 |
| E.coli* | 6 | 40,0 |
| Klebsiella pneumoniae* | 2 | 13,3 |
| E.coli выделилась у 6 пациентов, из них у 1 пациента вместе с Enterococcus faecalis, у 1 пациента вместе с Klebsiella pneumonia Klebsiella pneumoniae у 2 пациентов, из них у 1 пациента вместе Enterococcus faecalis | ||
| Группа III | ||
| Роста микрофлоры не выявлено | 10 | 66,7 |
| E.coli* | 4 | 26,6 |
| Morganella morganii | 1 | 6,7 |
| *Всего E.coli выделилась у 4 пациентов, из них у 1 пациента вместе с Enterococcus faecalis, у 1 пациента — вместе с Streptococcus anginosus, у 1 — вместе с Proteus mirabilis | ||
| Группа IV | ||
| Роста микрофлоры не выявлено | 7 | 46,7 |
| E.coli* | 7 | 46,7 |
| Pseudomonas aeruginosa* | 1 | 6,7 |
| *Всего E.coli выделили у 7 пациентов, из них у 2 пациентов вместе с Enterococcus faecalis, у 1 пациента — совместно со Streptococcus anginosus, у 1 — совместно с Proteus mirabilis. Pseudomonas aeroginosa выделили у 1 пациента совместно с Providencia struartii, Enterococcus faecalis | ||
Таблица 4. Сравнительный анализ данных воспалительной реакции между группами пациентов по Хи-критерию Пирсона
Источник




