- ГБУЗ РХ «РЦПБ СПИД»
- Профилактика перинатального пути передачи ВИЧ-инфекций
- Врожденная ВИЧ-инфекция: клиника, диагностика, лечение
- Профилактика вертикальной передачи ВИЧ от матери ребенку
- Профилактика передачи ВИЧ от матери ребенку в антенатальном периоде
- Профилактика передачи ВИЧ от матери ребенку в интранатальном периоде
- Профилактика ВИЧ-инфекции у новорожденного
ГБУЗ РХ «РЦПБ СПИД»
Профилактика перинатального пути передачи ВИЧ-инфекций
Какова вероятность передачи ВИЧ от матери ребенку?
Ежегодно 15-20 женщин в Республике Хакасия узнают о ВИЧ-статусе в женской консультации. Средний детородный возраст сейчас составляет 30-35 лет. Стоит отметить, что каждая семейная пара, в которой один или оба партнёра живут с ВИЧ, должны максимально ответственно и серьезно подойти к вопросу профилактики передачи ВИЧ ребёнку. Лучше всего проконсультироваться со специалистом ещё на этапе планирования беременности.
Если женщина выполняет все рекомендации врача, риск передачи снижается до 1-2%. Грудное вскармливание повышает риск: по разным данным, от 30 до 80%.
Огромное значение во время беременности имеет функциональная система мать-плацента-плод. Плацента имеет множество функций: дыхательную, выделительную, питательную, гормональную и барьерную. Барьерная функция защищает плод от попадания вируса: здоровая плацента для вируса непроницаема. Но физиологическое истощение, патологии и воспаления могут привести к проникновению вируса от матери плоду.
Во время родов, при прохождении по родовым путям матери, ребенок контактирует с кровью и влагалищным секретом. Кроме того, имеют значение мелкие кровоизлияния в плаценту в активной фазе родов.
При кормлении грудью также повышается риск инфицирования: в молоке содержатся свободные вирусные частицы и провирусы. Также ребёнок может контактировать с кровью матери при травматизации соска.
Как снизить риск перинатальной передачи ВИЧ?
Согласно приказу 572 МЗ РФ, все беременные женщины обследуются на ВИЧ дважды: при постановке на учет и в 28-32 неделе беременности. Дополнительное обследование на ВИЧ ( более 2-х раз) беременной назначается в случаях:
- употреблявшим в течение беременности психоактивные вещества внутривенно;
- имевшим незащищенные половые контакты с ВИЧ-инфицированным партнером;
- если половой партнер беременной не обследован на ВИЧ.
Половой партнер беременной обследуется как минимум однократно при постановке на учет женщины в женской консультации.
Диспансерное наблюдение ВИЧ-позитивной беременной женщины должно осуществляться совместно: при взаимодействии медицинских работников женских консультаций (врачей акушеров-гинекологов, уполномоченного врача по диспансерному наблюдению и лечению больных ВИЧ-инфекцией) со специалистами ГБУЗ РХ «РЦПБ СПИД» в целях контроля лечения и эффективности химиопрофилактики передачи ВИЧ-инфекции от матери ребенку.
Кроме того, для успешной профилактики вертикальной передачи необходимо соблюдение всех трех этапов химиопрофилактики: во время беременности (лучше – при планировании), в родах и профилактики для ребенка.
Все ВИЧ-инфицированные женщины детородного возраста при выявлении у них ВИЧ-инфекции должны получать АРВТ. Если женщина ранее не принимала терапию, то ей необходимо ее начать не позднее 12 недели беременности. В случае если такая женщина становится на учёт после 12-14- й недели, терапию назначают сразу при обращении.
Снижение риска напрямую зависит от АРВ-терапии и приверженности к ней, от скорости снижения вирусной нагрузки и от способности препаратов проникать через плаценту к плоду.
Самая главная задача будущей матери и инфекциониста – успеть подавить до неопредляемого уровня вирусную нагрузку к моменту родов. Это значительно снижает риски перинатальной передачи ВИЧ-инфекции. Уровень вирусной нагрузки на 34-36 неделе беременности является единственным критерием качества перинатальной профилактики. Если нет неопределяемой вирусной нагрузки у женщины в этот срок – нет качественной профилактики.
Профилактика в родах и новорожденному:
- Если женщина поступает в роды в родильном отделении продолжается прием АРТ, также рекомендуется проведение химиопрофилактики во время родов по назначению специалиста..
- Если нагрузка более 1000 копий/мл, то решается вопрос о плановом кесаревом сечении, продолжается схема АРТ и проводится химиопрофилактика во время родов.
Сразу после родов новорожденному назначается химопрофилактика передачи ВИЧ от матери к ребенку. Длительность химиопрофилактики составляет 4 недели.
Ребенок от ВИЧ-позитивной мамы, должен находиться на искусственном вскармливании.
Чтобы уточнить, произошло ли инфицирование ребенка во время беременности или родов, необходимо сделать ПЦР-исследование сразу после рождения, далее на 14-21 день жизни (при высоком риске инфицирования), затем в через 2-4 недели после отмены химиопрофилактики младенца ( в 2-2,5 месяца) затем в возрасте в возрасте в возрасте 4-6 месяцев.
У ребенка исследование на антитела к ВИЧ (метод ИФА) проводится в срок 12 месяцев и 18 месяцев. В случае отрицательного результата ИФА к 18-му месяцу жизни ребёнка решается вопрос о том, чтобы снять его с учёта. В принятии решения участвуют инфекционист и педиатр. В дальнейшем рекомендуется обследование ребенка в возрасте 3-х лет.
Источник
Врожденная ВИЧ-инфекция: клиника, диагностика, лечение
В настоящее время ВИЧ-инфекция у детей является одной из актуальнейших проблем во всем мире.
В настоящее время ВИЧ-инфекция у детей является одной из актуальнейших проблем во всем мире. Первоначально в нашей стране она была обусловлена внутрибольничной заболеваемостью, а в последние годы — рождением детей ВИЧ-инфицированными женщинами. Более 90% детской ВИЧ-инфекции является результатом именно перинатальной трансмиссии вируса.
Больные ВИЧ-инфекцией дети и их близкие нуждаются в профессиональной лечебно-реабилитационной поддержке их социального функционирования и оптимального качества жизни. Эта работа должна быть прежде всего направлена на «обновление взглядов» как на больных детей, так и их родителей. Очень важно не оставлять их в социальной изоляции, ведь порой вторичные проблемы негативно действуют на больного и его родственников не меньше, чем само заболевание.
По данным Федерального научно-методического центра по профилактике и борьбе со СПИДом, в России на 31 декабря 2006 г. зарегистрировано 2093 ребенка с подтвержденным диагнозом «ВИЧ-инфекция», из них 169 детей — в Москве [4].
По данным МГЦ СПИД за последние 10 лет произошло уменьшение числа детей с врожденной ВИЧ-инфекцией. Так, если в 2001 году, когда химиопрофилактика вертикальной трансмиссии ВИЧ-инфекции только начинала проводиться, число ВИЧ-инфицированных детей составляло 8%, то в 2006 году — всего 1,5%. Таких результатов удалось добиться благодаря введению в практику схемы профилактики согласно протоколу от 1996 г. PACTG 076 (Pediatric AIDS Clinical Trial Group), который основан на назначении беременной женщине Азидотимидина — антиретровирусного препарата из группы нуклеозидных ингибиторов обратной транскриптазы.
Однако даже своевременное проведение химиопрофилактики не исключает полностью возможность перинатальной передачи ВИЧ-инфекции от матери плоду.
К факторам, повышающим риск передачи ВИЧ от матери к ребенку, относятся:
При отсутствии профилактики перинатальной передачи ВИЧ, риск заражения составляет 30–40% [3].
Причинами отсутствия химиопрофилактики во время беременности и родов могут быть: диагностика ВИЧ-инфекции только во время родов, употребление наркотических веществ во время беременности, добровольный отказ от профилактики, в т. ч. по религиозным убеждениям, беременность до внедрения в практику профилактики вертикальной передачи ВИЧ и домашние роды.
Особенности клинических проявлений ВИЧ-инфекции у детей определяются стадией онтогенеза, на которой произошло инфицирование плода ВИЧ в организм (внутриутробно или интранатально) и от возраста ребенка в случае постнатального заражения.
При заражении плода в позднем перинатальном периоде или ребенка после рождения течение ВИЧ-инфекции почти не отличается от взрослых.
Целью данной работы является оценка эффективности общей и высокоактивной антиретровирусной терапии (ВААРТ) у детей с врожденной ВИЧ-инфекцией.
Задачи
Нами проанализированы 60 случаев врожденной ВИЧ-инфекции у детей в возрасте от 1 месяца до 7 лет, в т. ч.: 30 амбулаторных карт детей, состоящих на диспансерном учете в московском городском центре СПИД (МГЦ СПИД); 30 историй болезни детей, находящихся на стационарном лечении в МГЦ СПИД.
По результатам анализа амбулаторных карт и историй болезни нами были выявлены следующие наиболее часто встречающиеся клинические проявления врожденной ВИЧ-инфекции у детей: поражение ЦНС, лимфаденопатия, гепатолиенальный синдром, интерстициальные изменения в легких, анемия, гипотрофия, недоношенность.
Поражение ЦНС в нашем исследовании наблюдалось у 75% детей. Установлено, что ВИЧ является не только иммунотропным, но и нейротропным вирусом и проникает через гематоэнцефалический барьер на ранних этапах инфекционного процесса в организме, поражая олигодендроциты и астроциты, нейроциты, микроглию, макрофаги, клетки эндотелия кровеносных сосудов, фибробластоподобные клетки мозга. Указанные клетки имеют рецептор CD4 и считаются прямыми клетками-мишенями для ВИЧ. Патоморфологические изменения головного мозга при ВИЧ-инфекции могут быть охарактеризованы как альтернативно-дистрофические, с периваскулярным отеком, дистрофией нейронов, очаговой демиелинизацией и циркуляторными нарушениями.
У обследованных нами ВИЧ-инфицированных детей наблюдался полиморфизм клинических неврологических проявлений.
В начале заболевания отмечались астеноневротический и цереброастенический синдромы. Для этой стадии СПИДа характерной была ВИЧ-энцефалопатия. Также было установлено, что тяжесть поражения нервной системы более выражена у детей первого года жизни.
ВИЧ-энцефалопатия — тяжелое заболевание, затрагивающее все функции ЦНС. При подострой прогрессирующей энцефалопатии утрачиваются ранее приобретенные умения и навыки. Вялотекущая прогрессирующая энцефалопатия замедляет или прекращает формирование новых навыков, не затрагивая при этом старых. Обе формы прогрессирующей энцефалопатии резко замедляют психомоторное развитие. Дети с непрогрессирующей энцефалопатией продолжают приобретать новые навыки, но медленнее, чем здоровые сверстники.
Одновременно поражение ЦНС проявлялось грубой задержкой психомоторного развития, синдромом гипервозбудимости и гидроцефальным синдромом.
Клиническая манифестация ВИЧ-инфекции у детей разнообразна и зачастую неспецифична. Нами установлено, что лимфаденопатия, ассоциированная с гепатоспленомегалией, является одним из наиболее ранних признаков врожденной ВИЧ-инфекции. Так, персистирующая генерализованная лимфаденопатия выявлена в 64% случаев, а гепатолиенальный синдром — в 38% случаев. Сочетание обоих синдромов наблюдалось у 36% детей.
Интерстициальные изменения в легких были у 25% детей, они развивались в результате многократно перенесенных ранее пневмоний различной этиологии.
Из гематологических проявлений чаще всего отмечалась анемия (24% больных), что было связано с приемом антиретровирусного препарата из группы нуклеозидных ингибиторов обратной транскриптазы ВИЧ — «Зидовудина».
Гипотрофия (от I до III степени) была выявлена у 18% больных, недоношенность отмечалась в 14% случаев.
Из сопутствующих заболеваний чаще встречались хронический вирусный гепатит С и туберкулез, а из оппортунистических заболеваний — грибковые поражения кожи и слизистых, пневмоцистная пневмония, герпетическая инфекция, цитомегаловирусная инфекция.
Грибковые поражения кожи и слизистых отмечались у 38% детей.
Наиболее частая этиология — грибы рода Candida.
Чаще всего наблюдался оральный кандидоз, которому сопутствовал ангулярный хейлит, когда в углах рта возникали мацерации, эрозии, трещины. По краям трещин иногда отмечался гиперкератоз. Для детей, больных ВИЧ/СПИДом, характерно рецидивирующее течение орофарингеального кандидоза. В зависимости от степени иммунодефицита (определяется по количеству CD4-лимфоциов), было отмечено возникновение рецидивов через несколько месяцев, недель, а иногда и дней после отмены антимикотической терапии. Продолжительность периодов ремиссии была индивидуальна у каждого больного.
Наиболее опасная оппортунистическая инфекция, пневмоцистная пневмония, наблюдалась у 26% детей. Пневмоцистная пневмония может развиться в любом возрасте, но у наблюдавшихся нами больных почти в половине случаев приходилась на первые 6 месяцев жизни.
Обычно она развивалась остро, проявляясь одышкой и кашлем. Однако в некоторых случаях сначала появлялся кашель, и в течение нескольких дней к нему присоединялось постепенно нарастающее тахипноэ. Вначале появлялось навязчивое покашливание, затем кашель становился коклюшеподобным, особенно в ночное время. У ребенка отмечалась прогрессирующая слабость, снижение аппетита, бледность кожного покрова, цианоз носогубного треугольника. Температура тела в начале заболевания была нормальной или субфебрильной [1, 5].
При физикальном исследовании выявлялись тахипноэ, одышка, влажные и сухие хрипы. При прогрессировании пневмонии, возможно, возникала легочно-сердечная недостаточность.
Рентгенологические изменения, характерные для пневмоцистной пневмонии в виде снижения прозрачности легких, появления симметричных теней в виде крыльев бабочки, «ватных легких», определялись менее чем у половины больных.
Диагноз пневмоцистной пневмонии был основан на обнаружении возбудителя в мокроте, в материале, полученном при бронхоальвеолярном лаваже или биопсии легкого. У большинства детей пневмоцистная пневмония сочеталась с другими оппортунистическими заболеваниями.
Для лечения применялся Бисептол (сульфаметоксазол + триметоприм), который назначался при первом подозрении на пневмоцистную пневмонию до получения результатов микробиологического исследования. Профилактика пневмоцистной пневмонии проводилась тем же препаратом всем детям, рожденным ВИЧ-инфицированными женщинами в возрасте от 6 недель до 4 месяцев до исключения диагноза «ВИЧ-инфекция». ВИЧ-инфицированным детям первичная профилактика пневмоцистной пневмонии проводилась в течение первого года жизни. Дальнейшее проведение профилактики рекомендуется детям при уровне CD4-лимфоцитов 5 лет, независимо от клинических симптомов и уровня вирусной нагрузки;
Антиретровирусную терапию можно временно не назначать детям, у которых нет клинических проявлений ВИЧ-инфекции или они слабо выражены, при уровне CD4-лимфоцитов ≥ 25% у детей от 1 года до 5 лет или уровне CD4-лимфоцитов ≥ 350 клеток/мм3 у детей > 5 лет и уровне вирусной нагрузки
Н. О. Голохвастова, студентка 6 курса МГМСУ, Москва
Источник
Профилактика вертикальной передачи ВИЧ от матери ребенку
По данным ВОЗ, число лиц, живущих с ВИЧ-инфекцией, во всем мире составляет более 40 млн. Ежегодно выявляется более 2 млн новых случаев ВИЧ-инфекции [23]. Актуальность проблемы ВИЧ-инфекции в России не вызывает сомнений.
По данным ВОЗ, число лиц, живущих с ВИЧ-инфекцией, во всем мире составляет более 40 млн. Ежегодно выявляется более 2 млн новых случаев ВИЧ-инфекции [23].
Актуальность проблемы ВИЧ-инфекции в России не вызывает сомнений. Огромный рост количества ВИЧ-инфицированных обусловлен по большей части неосведомленностью потребителей наркотиков о риске совместного использования инъекционного оборудования; второй ведущей причиной развития эпидемии в последнее время стал половой путь передачи ВИЧ-инфекции — через «незащищенные» сексуальные контакты.
На январь 2005 г. в России за все годы наблюдения, начиная с 1987 г., было выявлено 309 410 случаев ВИЧ-инфекции, из которых 13 291 — у детей.
По состоянию на 7 сентября 2005 г. зарегистрировано 328 978 случаев ВИЧ-инфекции, что подтверждает неконтролируемый характер эпидемии ВИЧ/СПИДа. По оценкам многих экспертов, включая Федеральный научно-методический центр МЗиСР РФ по профилактике и борьбе со СПИДом (ФНМЦ ПБ СПИД) и ВОЗ, реальное число людей, живущих с ВИЧ/СПИДом (ЛЖВС), может превышать официальные показатели в 3–5 раз, что позволяет предположить, что на сегодняшний день в РФ насчитывается более 1 млн ВИЧ-инфицированных. По прогнозам академика РАМН В. В. Покровского, прирост может составить 10–15% — по сравнению с 2004 г. [13]. ВИЧ-инфекция угрожает молодому, работоспособному населению страны, а значит, ее будущему.
Повсеместная, доступная, постоянная информация о ВИЧ/СПИДе нужна: чтобы не заразиться этой инфекцией; чтобы научиться жить в новой ситуации, когда среди знакомых, соседей, коллег по работе становится все больше ВИЧ-позитивных; чтобы не стать изгоем, если заражение по какой-либо причине произошло.
Прошло уже более 20 лет с тех пор, как была установлена этиологическая роль ВИЧ в развитии СПИДа. ВИЧ относится к группе РНК-содержащих ретровирусов. Мишенью вируса являются все клетки человека, несущие на своей поверхности рецептор СД4 – в основном это СД4 — положительные Т-лимфоциты (хелперы), а также все клетки моноцитарно-макрофагальной системы, например Купферовские клетки печени, олигодендроциты головного мозга и т. п. (именно с этим связано то, что клинические проявления при ВИЧ-инфекции объясняются не только иммунодефицитом, но также и прямым действием вируса на различные ткани).
Одним из важных свойств вируса, с которым связана невозможность элиминации ВИЧ из организма, является способность вирусной ДНК (построенной на матрице РНК с помощью обратной транскриптазы) становиться частью генетического материала клетки хозяина. Это значит, что инфицированные клетки остаются такими до конца своего существования.
Выделено два типа вируса с различными структурой генома, серологическими характеристиками и патогенностью — ВИЧ-1 и ВИЧ-2. ВИЧ-1, обладающий большей вирулентностью, распространен в Европе, Восточной и Южной Африке, Азии, а ВИЧ-2 встречается преимущественно в Западной Африке. ВИЧ передается от человека человеку на всех стадиях заболевания. Зараженный человек остается источником инфекции пожизненно [2, 17].
На цепочке вирусной РНК с помощью фермента ревертазы (обратной транскриптазы) синтезируется ДНК, которая встраивается в генетический аппарат клетки человека, где может сохраняться в виде провируса пожизненно. При активизации провируса в зараженной клетке происходит интенсивное накопление новых вирусных частиц, что ведет к разрушению клеток и поражению новых. Содержащие вирус Т4-клетки не могут выполнять хелперную функцию. Происходит постепенная деструкция иммунной системы [1, 2, 17].
ВИЧ присутствует в крови, спинномозговой жидкости, сперме и вагинальных выделениях инфицированных людей; передаваться другим людям может только в результате попадания этих жидкостей в их организмы [7, 10]. Таким образом, основными путями передачи ВИЧ являются половой, парентеральный и вертикальный.
Половой путь — незащищенный (т. е. без презерватива) оральный, вагинальный и анальный сексуальные контакты. ВИЧ не может проникнуть через презервативы высокого качества (изготовленные из латекса и полиуретана), однако передача вируса возможна в случае неправильного использования презерватива или при его разрыве во время сексуального контакта. ВИЧ обнаруживают как в жидкой части спермы, так и в присутствующих в ней лимфоцитах и моноцитах (повышение их числа наблюдается при уретритах и эпидидимите). Риск инфицирования при анальных половых сношениях крайне высок, поскольку вирус легко проникает из спермы сквозь тонкую слизистую прямой кишки и поражает клетки-мишени, находящиеся в толще слизистой или подслизистом слое. Кроме того, анальные половые сношения сопряжены с высоким риском травмирования слизистой прямой кишки. Таким образом, ВИЧ проникает в кровь (если слизистая прямой кишки повреждена), либо сначала заражает клетки-мишени, такие, как клетки Лангерганса.
Хотя слизистая влагалища, покрытая многослойным эпителием, толще слизистой кишечника и менее подвержена травмированию при половом акте, гетеросексуальный контакт может привести к заражению как женщины, так и мужчины (длительный контакт эндометрия со спермой, инфекции половых органов, герпес, цервициты повышают риск инфицирования).
При оральных половых сношениях риск инфицирования значительно ниже, чем при анальных, в связи с чем бытует мнение, что они безопасны. Однако такая точка зрения ошибочна: описаны достоверные случаи инфицирования орального партнера [17].
Парентеральный путь чаще всего реализуется при многоразовом использовании инструментов для инъекций наркотиков, при переливании инфицированной крови или ее компонентов (эритроцитарная, тромбоцитарная или лейкоцитарная массы, свежезамороженная плазма). Введение иммуноглобулинов (в том числе против гепатита В) в этом отношении безопасно, поскольку эти препараты прогревают для инактивации вируса или удаляют из них вирус другим способом.
До введения обязательной проверки на ВИЧ доноров спермы, а также доноров органов и тканей регистрировались случаи заражения женщин при искусственном оплодотворении и инфицирования больных, перенесших трансплантацию.
За более чем пятнадцатилетнюю историю изучения ВИЧ-инфекции не зарегистрирована передача ВИЧ-инфекции контактно-бытовым путем, при поцелуях, рукопожатиях, коллективных занятиях спортом, пользовании общей посудой, столовыми приборами, полотенцами, а также при укусах насекомых. В слюне, слезной жидкости и моче концентрация вируса невысока, поэтому заражение через эти биологические жидкости маловероятно [7, 8, 21, 22, 17].
Вертикальный путь — передача ВИЧ от инфицированной матери ее новорожденному ребенку — является основным в развитии детской ВИЧ-инфекции.
В последние годы наблюдается постоянное увеличение доли женщин среди зарегистрированных с ВИЧ-инфекцией. Подавляющее большинство ВИЧ-позитивных женщин находятся в фертильном возрасте [13].
С увеличением числа женщин, живущих с ВИЧ/ СПИДом, возрастает количество рожденных ими детей.
По оценкам ЮНЭЙДС (Объединенная программа ООН по ВИЧ/СПИДу), по состоянию на конец 2004 г. в мире с ВИЧ/СПИДом живет 2,2 млн детей. В Российской Федерации от ВИЧ-инфицированных матерей родились 11422 детей, что составляет 3,7% от общего количества заболевших [21, 22]. Перинатальная передача ВИЧ от матери ребенку возможна во время беременности, родов или кормления грудью. Источником при ВИЧ-инфекции новорожденных являются, как правило, инфицированные матери.
Риск вертикальной трансмиссии (рис.) без профилактических мероприятий колеблется от 10 до 40%, причем из них 15–30% приходятся на трансплацентарный путь передачи вируса (т. е. внутриутробное заражение), 50–75% случаев заражения имеют место во время родов и 10–20% — при грудном вскармливании [1, 6, 11, 16].
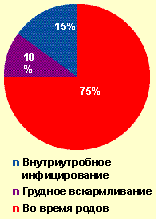 |
| Рисунок. Структура вертикальной передачи ВИЧ |
При многоплодной беременности близнец, родившийся первым, имеет более высокий риск заражения от ВИЧ-инфицированной матери, чем ребенок, появившийся на свет вторым. Риск инфицирования плода повышен также при затяжных родах, длительном безводном периоде и контакте плода с большим количеством материнской крови (эпизиотомии, разрывах влагалища и шейки матки, наложении электродов на головку плода). Четко установлена возможность заражения детей при кормлении грудью. Вирус обнаружен как в молозиве, так и в грудном молоке ВИЧ-инфицированной матери.
Риск заражения от ВИЧ-инфицированной матери при кесаревом сечении ниже, чем при родоразрешении через естественные родовые пути [1, 4].
Вероятность рождения инфицированного ребенка от ВИЧ-позитивной матери колеблется в зависимости от страны, культуры, экономических условий. В экономически развитых странах и странах со средним достатком благодаря превентивным мероприятиям (профилактика в период беременности, в период родов и новорожденному) удалось снизить процент вертикальной трансмиссии ВИЧ до 2% и менее [8, 18].
В первые годы после выявления эпидемии СПИДа лечение ВИЧ-инфицированных людей осуществляла лишь небольшая группа врачей в нескольких клиниках, в основном расположенных в крупных городах. Сегодня уже не вызывает сомнений тот факт, что каждый врач должен уметь распознавать ВИЧ-инфекцию, иметь представление о принципах обследования и ведения таких больных. Семейным врачам, терапевтам, акушерам, гинекологам, педиатрам, хирургам и врачам других специальностей все чаще приходиться сталкиваться с ВИЧ-позитивными пациентами, которые нуждаются в лечении заболеваний, как связанных, так и не связанных с ВИЧ-инфекцией.
Для предотвращения инфицирования ребенка при грудном вскармливании рекомендуется детей, родившихся от ВИЧ-инфицированной женщины, не прикладывать к груди и не кормить материнским молоком.
Применение антиретровирусных препаратов для профилактики передачи ВИЧ от инфицированной женщины ее ребенку во время беременности и родов (при отказе от последующего грудного вскармливания молоком инфицированной женщины) значительно снижает риск заражения ребенка (с 30–40% до 0,5–3%). Столь высокая эффективность при достаточной безопасности для матери и плода доказана лишь для схем с применением азидотимидина, которые приводятся в общепринятых рекомендациях [15, 16].
Mayaux M. И. и соавторы, Cao U. и соавторы отмечают, что основное внимание при назначении антиретровирусной терапии (АРТ) беременной женщине должно уделяться степени репликативной активности ВИЧ; при обсуждении вопроса о кесаревом сечении следует учитывать уровень «вирусной нагрузки» [15, 16, 18, 19].
Профилактика перинатального заражения ВИЧ включает применение антиретровирусных препаратов в период беременности, родов, а также у новорожденного.
Наиболее успешные результаты получаются при проведении всего комплекса терапевтических мероприятий (три ступени), однако если какой-либо из этапов осуществить не удается (например, вследствие позднего выявления ВИЧ-инфекции у женщины), это не является основанием для отказа от следующего.
Перед назначением АРТ врач проводит беседу с женщиной (консультирование), в ходе которой информирует беременную о целях применения АРТ, разъясняет вероятность рождения ВИЧ-инфицированного ребенка при проведении профилактики или отказе от нее, дает информацию о возможных побочных эффектах от применяемых препаратов. Пациентке предлагается дать письменное информированное согласие на проведение химиопрофилактики [9, 12, 14].
Профилактика передачи ВИЧ от матери ребенку в антенатальном периоде
Если при обследовании женщины во время беременности установлено наличие ВИЧ-инфекции, ведение беременной проводят специалисты территориального центра профилактики и борьбы со СПИДом и акушер-гинеколог по месту жительства в женской консультации.
Рекомендуется избегать при наблюдении во время беременности проведения любых инвазивных процедур, в ходе которых нарушается целостность кожных покровов, слизистых и возможен контакт плода с кровью матери (амниоцентез и др.).
Если в период беременности ВИЧ-инфицированная женщина находится на диспансерном наблюдении по беременности, химиопрофилактику ей назначает врач-инфекционист центра профилактики и борьбы со СПИДом или врач-инфекционист ЛПУ (в зависимости от условий), которые дают рекомендации по проведению химиопрофилактики во время родов (ее проводит врач акушер-гинеколог, ведущий роды) и новорожденному (ее назначает врач неонатолог или педиатр) [3]. Если ВИЧ-инфицирование выявлено в период родов, химиопрофилактику роженице назначает и проводит врач акушер-гинеколог, ведущий роды, а новорожденному ребенку — врач-неонатолог или педиатр.
Профилактическое лечение (профилактика) назначается не ранее 14 нед беременности после консультирования женщины и при наличии информированного письменного согласия. На более поздних сроках беременности — с момента диагностики ВИЧ-инфицирования.
В соответствии с протоколом ACTG 076 (MMWR, 1994, 43, RR-1:1-20), для профилактики передачи ВИЧ противовирусная терапия назначается до родов: перорально азидотимидин (азидотимидин, ретровир) 300 мг 2 раза или начиная с 28-й недели беременности на протяжении всего периода, продолжая вплоть до родов.
Согласно приказу № 606 МЗ РФ рекомендуемые схемы химиопрофилактики в период с 14-й до 28-й недели следующие:
- азидотимидин (азидотимидин, тимазид, ретровир) перорально по 0,2 г 3 раза в сутки (суточная доза 0,6 г) в течение всей беременности;
- фосфазид (никавир) перорально по 0,2 г 3 раза в сутки (суточная доза 0,6 г) в течение всей беременности.
ВОЗ [15] рекомендует химиопрофилактику передачи ВИЧ-инфекции от матери ребенку по разным клиническим сценариям в зависимости от того, нуждается женщина в лечении ВИЧ-инфекции или нет. Схема химиопрофилактики в случаях, когда женщина не нуждается в лечении ВИЧ-инфекции, приведена в таблице.
Назначение зидовудина матери во время беременности и родов и ребенку после рождения снижает вероятность передачи ВИЧ на 67% (при условии искусственного вскармливания). В исследовании NIVNET 012 была доказана эффективность однократного применения невирапина, назначаемого матери во время родов и ее новорожденному ребенку при условии грудного вскармливания. Частота передачи ВИЧ составила 11,8 и 20% в контрольной группе, получавшей зидовудин, и 15,7 и 25,8% в группе, однократно получавшей невирапин (в сроки 6 и 18 мес после родов соответственно) [8].
Простота, дешевизна и эффективность этой схемы послужили стимулом для внедрения перинатальной профилактики в странах с ограниченными ресурсами [8]. Однако свидетельства развития лекарственной устойчивости ВИЧ после однократного приема невирапина положили начало дискуссии об эффективности данной стратегии, поскольку лекарственная устойчивость к невирапину осложняет последующее воздействие на мать и/или ребенка препаратов высокоактивной антиретровирусной терапии (ВААРТ) схем первого ряда (невирапин — основной (и недорогой) препарат в стандартной схеме ВААРТ первого ряда).
В случае, когда женщина нуждается в лечении ВИЧ-инфекции и тройная АРТ недоступна, используются те же рекомендации, что и при первом сценарии. Профилактическое лечение необходимо начинать как можно раньше. Плановое кесарево сечение следует проводить с 38-й недели при вирусной нагрузке более 1000 копий/мл.
В тех же случаях, когда женщина нуждается в лечении ВИЧ-инфекции и тройная АРТ доступна, применяется следующая схема. Для матери: зидовудин 300 мг внутрь (при непереносимости или анемии — ставудин) + ламивудин 150 мг + невирапин 200 мг (при уровне CD4 менее 250 мкл увеличивается риск гепатотоксичности невирапина в 12 раз. Рекомендуется строго следить за показателями функции печени в течение первых 18 нед лечения); после родов продолжать терапию по той же схеме. Для ребенка: сироп зидовудина 4 мг/кг каждые 12 ч в течение 7 дней и/или невирапин 2 мг/кг однократно и/или оба препарата.
Химиопрофилактику следует начинать со II триместра, если речь не идет о тяжелобольных. Плановое кесарево сечение необходимо проводить с 38-й нед при вирусной нагрузке более 1000 копий/мл.
К вопросам о профилактическом лечении матери необходимо подходить в зависимости от схемы обычной АРТ, которую женщина получает, и от стандартных схем профилактического лечения. Например, для женщин, получающих обычную АРТ по схеме с невирапином, лишняя доза препарата во время родов, скорее всего, не принесет никакого вреда. В этом случае проще и безопаснее следовать стандартным схемам профилактики, подразумевающим однократное применение невирапина, независимо от того, получала беременная обычную АРТ или нет. Однако женщинам, у которых проводится обычная АРТ по схеме без невирапина (схема может содержать абакавир или нелфинавир), профилактику в виде однократного назначения невирапина проводить не рекомендуется [8]. В этом случае риск возникновения лекарственной устойчивости ВИЧ после одной дозы невирапина превышает возможную пользу от данного вмешательства.
Профилактика передачи ВИЧ от матери ребенку в интранатальном периоде
Основная доля случаев передачи инфекции приходится на период родов, случаи инфицирования в раннем периоде беременности встречаются реже [4]. Следовательно, ведение родов у ВИЧ-инфицированной женщины имеет свои особенности. Тактика родоразрешения для ВИЧ-инфицированных [1]:
- следует избегать длительного безводного периода, поскольку передача ВИЧ от матери ребенку возрастает при безводном периоде более 4 ч;
- не следует проводить амниотомии, если роды протекают без осложнений;
- не проводить эпизиотомию или перинеотомию как рутинную методику;
- избегать наложения акушерских щипцов, вакуум-экстракторов;
- нежелательно проводить родовозбуждение и родостимуляцию;
- необходимо проводить санацию родовых путей на протяжении всего родового акта (2% раствором хлоргексидина каждые 2 ч);
- новорожденного желательно вымыть в дезинфицирующем или мыльном растворе, избегать повреждений кожи и слизистых;
- кесарево сечение выполнять по акушерским показаниям или в плановом порядке, взвешивая риски и преимущества для матери и плода.
Как новый метод родоразрешения предложена техника гемостатического кесарева сечения М. Песареси и соавторов (2000 г.) [6]. Во время операции благодаря сохранению целостности плодного пузыря и бескровному рассечению матки удается полностью изолировать новорожденного от организма матери, тем самым избежав контаминации кожных покровов и слизистых оболочек новорожденного инфицированной кровью матери [4].
Согласно рекомендациям ВОЗ [15], плановое кесарево сечение проводят в сроке беременности 38 и более недель, однако по возможности необходимо определять вирусную нагрузку. При показателе вирусной нагрузки менее чем 1000 копий/мл роды можно вести консервативно (оценить риск оперативного вмешательства). Операцию рекомендуется выполнить до начала родовой деятельности и разрыва плодных оболочек.
По протоколу ACTG 076 (MMWR, 1994, 43, RR-1:1-20) в период родов назначается азидотимидин (азидотимидин, ретровир) внутривенно в дозе 2 мг/кг веса в первый час, инфузия продолжается в дозе 1 мг/кг веса тела в час вплоть до конца родов.
Рекомендации МЗ РФ (приказ № 606 от 19.12.2003 г.) в основном совпадают с рекомендациями ВОЗ.
Если ВИЧ-инфицирование установлено до или во время беременности, при поступлении женщины в родильный дом профилактическое лечение с применением азидотимидина, начатое во время беременности, продолжается по прежней схеме с добавлением невирапина (вирамуна) — 1 таблетка (0,2 г) перорально с началом родовой деятельности.
Если ВИЧ-инфицирование выявлено во время родов, химиопрофилактику роженице назначает и проводит акушер-гинеколог по основным схемам:
- азидотимидин (ретровир) внутривенно струйно 0,002 г (0,2 мл)/кг массы тела в течение первого часа родов, затем до момента пересечения пуповины 0,001 г (0,1 мл)/кг/ч;
- невирапин (вирамун) 1 таблетка (0,2 г) перорально однократно с началом родовой деятельности, в случае затяжных родов — повторить через 12 ч.
С целью исключения возможного развития лактоацидоза и летального исхода не рекомендуется использовать комбинацию ставудина с диданозином.
Если женщина не получала дозу невирапина или приняла его менее чем за 2 ч до рождения ребенка, новорожденному назначают две дозы невирапина: первую сразу после рождения, вторую — через 72 ч.
Роды при таком клиническом сценарии рекомендовано проводить через естественные родовые пути, избегая проведения инвазивных процедур (взятие крови из плода, эпизиотомии и др.) [15].
В случае, если беременная женщина больна туберкулезом и получала АРТ, необходимо следовать рекомендациям по лечению ВИЧ-инфекции у больных туберкулезом. Плановое кесарево сечение нужно проводить с 38-й недели при вирусной нагрузке более 1000 копий/мл [15].
Профилактика ВИЧ-инфекции у новорожденного
Профилактика у новорожденного, родившегося от ВИЧ-инфицированной матери, проводится независимо от того, получала ли мать во время беременности и родов профилактическое лечение. Антиретровирусные препараты новорожденному назначает врач-неонатолог или педиатр с 8-го часа жизни, но не позднее 72 ч жизни. Эффективность профилактического действия препарата существенно снижается в случае более позднего назначения (после 72 ч жизни), так как вирус внедряется в ДНК клеток организма ребенка.
Рекомендуемые схемы химиопрофилактики новорожденному:
- по протоколу ACTG 076 (MMWR, 1994,43,RR-1:1-20): азидотимидин (ретровир) перорально в сиропе 2 мг/кг массы каждые 6 ч в течение первых 6 нед жизни (можно сократить до 7–28 дней, начиная с 8–12 ч после рождения). Если ребенок не может принимать препарат орально, то азидотимидин вводится внутривенно в дозе 1,5 мг/кг массы тела каждые 6 ч;
- согласно приказу № 606 МЗ РФ: азидотимидин (сироп) перорально 0,002 г (0,2 мл)/кг каждые 6 ч в течение 6 нед или невирапин (суспензия) перорально по 0,002 г (0,2 мл)/кг 1 раз в сутки;
- по рекомендациям ВОЗ:
– невирапин 2 мг/кг однократно после рождения и/или зидовудин (сироп) 4 мг/кг каждые 12 ч в течение 7 дней;
– альтернативный режим: зидовудин (сироп) 4 мг/кг + ламивудин (сироп) 2 мг/кг каждые 12 ч в течение 7 дней.
В заключение хотелось бы отметить, что при невозможности проведения обследования профилактика женщине и новорожденному назначается по эпидемиологическим показаниям. Каждый родильный дом должен быть обеспечен экспресс-тестами на ВИЧ и противовирусными препаратами для проведения профилактического лечения.
Применение данных схем лечения и разумное назначение антиретровирусных препаратов во время беременности могут принести существенную пользу матери и снизить риск вертикальной трансмиссии ВИЧ-инфекции до 2% и менее. В то же время проведение АРТ во время беременности сопряжено со многими специфическими проблемами, среди которых необходимость согласованной работы женских консультаций, родильных домов и центров по профилактике и борьбе со СПИДом.
Многие женщины, желая иметь здоровых детей, обращаются в медицинские учреждения для дородового наблюдения. Внедрение именно в этом первичном звене (в континууме оказания помощи беременным женщинам) добровольного консультирования и тестирования на ВИЧ-инфекцию позволило многим женщинам узнать свой ВИЧ-статус, а программы профилактики передачи ВИЧ-инфекции от матери ребенку открыли им доступ к лечению, снижающему риск инфицирования плода. Кроме того, выявление ВИЧ-инфекции именно на этом этапе ведения беременных женщин даст возможность медицинским работникам назначить терапию самой ВИЧ-позитивной пациентке.
Увеличение доступа к дородовой и послеродовой помощи ВИЧ-позитивным женщинам является ключевым элементом в обеспечении профилактики передачи ВИЧ-инфекции от матери ребенку.
В то же время проведение трехэтапной, трехкомпонентной химиопрофилактики сопряжено со многими сложностями. Нехватка препаратов для химиопрофилактики, пробелы в организации закупок и распределении препаратов, в том числе и недостаточное финансирование, приводят к низкому охвату женщин перинатальной химиопрофилактикой и недостаточному обеспечению заменителями грудного молока.
Все сотрудники служб родовспоможения должны быть информированы о методах профилактики профессионального заражения ВИЧ ввиду возможного контакта с кровью и другими биологическими жидкостями организма. Наряду с этим медицинским работникам следует руководствоваться общепринятыми мерами предосторожности (нормативные акты МЗ РФ), направленными на снижение риска передачи ВИЧ и других инфекций не только при контакте с лицами, у которых выявлена положительная реакция на ВИЧ.
Сегодня не вызывает сомнений тот факт, что для улучшения качества социально-психологического сопровождения и патронажа беременной женщины, матери, ребенка и, как следствие, реализации механизмов профилактики вертикальной трансмиссии ВИЧ на всех трех этапах (до, во время и после родов) необходимо слаженное взаимодействие некоммерческих, негосударственных СПИД-сервисных организаций и государственных лечебно-профилактических учреждений родовспоможения.
Литература
- Рахманова А. Г., Виноградова В. В., Воронин Е. Е. и др. Химиопрофилактика передачи ВИЧ от матери к ребенку: метод. пособие для медицинской и социально-психологической службы. СПб., 2005. С. 8–9.
- Покровский В. В., Ермак Т. Н., Беляева В. В. и др. ВИЧ-инфекция: клиника, диагностика и лечение. М.: ГЭОТАР-МЕД, 2003. 488 с.
- Кулаков В. И., Баранов И. И. ВИЧ: профилактика передачи от матери ребенку. М., 2003.
- Ястребова Е. Б. Характеристика летальных исходов у детей, рожденных ВИЧ-инфицированными женщинами//СПИД. СЕКС. ЗДОРОВЬЕ. 2005. № 2.
- Воронин Е. Е. ВИЧ-инфекция у детей. Клинико-организационные аспекты: автореф. дис. . д-ра мед. наук. СПб., 2001.
- Ежегодные бюллетени ФНМЦ ПБ СПИД.
- Рюмина И. И. Профилактика передачи ВИЧ-инфекции от матери ребенку: лекция. М., 2004.
- Клиническое руководство Колумбийского университета. М., 2004.
- Основы законодательства Российской Федерации об охране здоровья граждан от 22 июля 1993 г. № 5487-1 (с изменениями).
- Покровский В. В. и др. Профилактика передачи ВИЧ от матери к ребенку во время беременности, родов и в период новорожденности: инструкция для медицинских работников центров по профилактике и борьбе со СПИДом и инфекционными заболеваниями, службы детства и родовспоможения. Ижевск, 2003.
- Покровский В. В. Материалы конференции по паллиативной помощи при ВИЧ-инфекции. М., 2005.
- Покровский В. В., Юрин О. Г., Беляева В. В. и др. Рекомендации по профилактике вертикальной передачи ВИЧ от матери к ребенку: учеб. пособие. М., 2003.
- Приказ МЗ РФ № 170 от 16.08.1994 г. «О мерах по совершенствованию профилактики и лечения ВИЧ-инфекции в Российской Федерации».
- Приказ МЗ РФ № 606 от 19 декабря 2003 г. «Об утверждении инструкции по профилактике передачи ВИЧ-инфекции от матери ребенку и образца информированного согласия на проведение химиопрофилактики ВИЧ».
- Протоколы ВОЗ для стран СНГ (клинические сценарии ППМР). М., 2004.
- Рахманова А. Г., Воронин Е. Е., Фомин Ю. А. ВИЧ-инфекция у детей. СПб., 2003.
- Фаучи Э., Лейн К. ВИЧ-инфекция и СПИД. М., 2004. Гл. 38.
- Guay L. A., Musoke P., Fleming T. et al. Intrapartum and neonatal single dose nevirapine compared with zidovudine for prevention of mother-to-child transmission of HIV-1 in Kampala. Uganda: HIVNET 012 randomised trial// Lancet. 1999; 354 (9181): 795–802.
- Mayaux M. J., Burgard M., Teglas J. P. et al. Neonatal characteristics in rapidly progressive perinatally acquired HIV-1 diseases//The French Pediatric HIV Infection Study Group. JAMA. 1996; 257 (8): 606–610.
- Pregnancy and HIV Infection: a European Consensus on Management. AIDS, 2002.
- UNAIDS, AIDS epidemic update, 2004.
- UNICEF and WHO. Young People and HIV/AIDS: Opportunity in Crisis, United National Children’s Fund, UNAIDS, and World Health Organization. 2002.
- WHO HIV/AIDS Treatment and Care Protocols for Countries of the Commonwealth of Independent States. March 2004.
Т. Х. Мирзоев, кандидат медицинских наук
«СПИД Фонд Восток–Запад», Москва
Источник





