Перинатальный способ передачи инфекции это
Перинатальные инфекции: бактериемия и пневмония. В первые дни жизни новорождённого существует лишь несколько характерных клинических симптомов, указывающих на бактериемию: увеличение количества нейтрофилов (этот показатель не всегда диагностически значим), уменьшение содержания тромбоцитов, брадикардия, повышение концентрации С-реактивного белка.
Развитие менингита не считают характерным признаком инфекции. Для установления окончательного диагноза для анализа отбирают кровь, мочу и спинномозговую жидкость, но лечение необходимо начать до получения результатов. Основное направление медикаментозной терапии — эрадикация Escherichia coli и стрептококка группы В (бензилпенициллин в сочетании с гентамицином или цефотаксимом).
В некоторых странах исследование на стрептококк группы В проводят ещё во время беременности и иногда назначают профилактический интранатальный курс антибиотикотерапии пенициллином. В других регионах обследуют только женщин из группы риска.
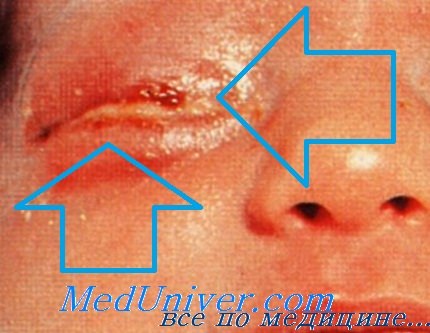
Перинатальные инфекции: гонококковая бленнорея новорождённых. Во время родов может произойти заражение Neisseria gonorrhoeae, вызывающей бленнорею новорождённых (гнойный конъюнктивит). Диагноз устанавливают после микроскопии мазков, окрашенных по Граму. Для лечения системной инфекции применяют пенициллин или цефотаксим (при возникновении устойчивости).
Перинатальные инфекции: хламидиоз. Хламидийная бленнорея новорождённых — тяжелейший конъюнктивит, возникающий в течение первых четырёх дней жизни. На исходе 6-й нед обычно развивается пневмония, характеризующаяся учащением дыхания и кашлем. Для лечения конъюнктивита применяют местные лекарственные средства, содержащие тетрациклин. При хламидийной пневмонии препаратом выбора считают эритромицин.
Перинатальные инфекции: буллёзное импетиго (синдром Лайелла). При заражении Staphylococcus aureus эксфолиативный токсин, вырабатываемый возбудителем, вызывает возникновение поверхностных волдырей или булл, вскрывающихся с образованием обширных зон токсического эпидермального некролиза («синдром ошпаренной кожи»).
Для лечения применяют флуклоксациллин. Мать и ребёнка помещают в отдельный бокс.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Перинатальный способ передачи инфекции это
Инфекции, передающиеся половым путем (ИППП), вносят ощутимый вклад в проблему инфекционной заболеваемости беременных и новорожденных.
В последние годы прослеживается тенденция к возрастанию заболеваемости ИППП, особенно хламидийной и микоплазменной этиологии, во время беременности, что увеличивает удельный вес данной патологии среди поражений плода и новорожденного.
По данным литературы, у беременных наиболее часто выявляются такие ИППП, как бактериальный вагиноз, герпетическая и хламидийная инфекция, реже – трихомониаз, гонорея, вирусный гепатит В (ВГВ), сифилис и ВИЧ-инфекция. Однако частота перинатальной инфекции, связанной с отдельными ИППП, определяется не только их распространенностью в популяции, но и частотой передачи. Риск перинатального инфицирования составляет около 30 % для гонококковой, 20–50 % для микоплазменной, 20–40 % для хламидийной, 5–50 % для герпетической инфекции и около 50 % для сифилиса. Наиболее высок риск перинатального заражения новорожденного при острой первичной инфекции.
Сроки перинатального заражения ИППП варьируются в зависимости от нозологической формы. Например, сифилис передается трансплацентарно и заражает ребенка в утробе матери. Гонорея, хламидиоз, ВГВ и генитальный герпес передаются интранатально при прохождении ребенка через родовые пути. Инфицирование ВИЧ может происходить и трансплацентарно, и в родах, и постнатально при грудном вскармливании.
Инфицирование плода на ранних стадиях беременности сопровождается наиболее высоким риском ее преждевременного прерывания или возникновения тяжелых, не совместимых с жизнью пороков развития. Поражение плода в более поздние сроки может приводить к развитию органной патологии. При антенатальном инфицировании клинические проявления инфекции у новорожденного выявляются, как правило, в первые часы или сутки после рождения, тогда как при интранатальном и постнатальном заражении манифестация инфекции может произойти значительно позже, особенно если ребенку была назначена антибактериальная или противовирусная терапия по другим показаниям.
Поскольку заражение ИППП может наступить как до возникновения беременности, так и на любых ее сроках, в качестве профилактики перинатального инфицирования важно обследование женщин на этапе планирования беременности, а также последующее наблюдение с проведением повторных обследований, в т. ч. в предродовом периоде.
Общие принципы профилактики перинатального заражения ИППП включают:
• выявление и лечение ИППП у женщины и ее полового партнера на этапе планирования беременности, когда инфекция еще не успела оказать негативное воздействие на течение беременности, а спектр допустимых к использованию препаратов неограничен (наиболее эффективная стратегия);
• практика безопасных с точки зрения заражения ИППП сексуальных контактов женщины и ее партнера до и во время беременности;
• обследование женщины во время беременности для выявления ранее не диагностированного или недавнего заражения ИППП;
• адекватная терапия (с одновременным лечением полового партнера) при выявлении ИППП в период беременности (в большинстве случаев позволяет предотвратить заражение новорожденного);
• обследование и оказание необходимой медицинской помощи новорожденному в послеродовом периоде (антибиотикотерапия, вакцинация и др.).
Далее рассматриваются ИППП, роль которых в развитии перинатальной патологии наиболее значима.
Гонорея
Гонорея относится к числу наиболее распространенных ИППП. По оценке экспертов ВОЗ, ежегодно в мире выявляется около 200 млн новых случаев гонококковой инфекции (ГИ), однако истинные масштабы распространения ГИ оценить сложно.
Хотя передача ГИ от матери к ребенку происходит преимущественно интранатально, у женщин с нелеченой гонореей отмечено повышение частоты преждевременных родов (15–22 %). При интранатальном инфицировании новорожденных Neisseria gonorrhoeae наиболее часто (30–50 %) вызывает поражения глаз – гонококковую офтальмию новорожденных, которая может осложняться изъязвлением роговицы с перфорацией, приводящим к слепоте. Отмечаются также локализованные поражения слизистых оболочек гортани и мочеполовых путей . У недоношенных новорожденных может развиться диссеминированная инфекция с клиникой артрита, менингита и сепсиса.
Хламидиоз
С начала регистрации заболеваемости хламидиозом в нашей стране в 1993 г. отмечается неуклонный рост частоты выявления новых случаев инфекции, что, однако, может быть связано с совершенствованием методов диагностики. Частота инфицирования хламидиями беременных колеблется от 3 до 40 %, достигая 70 % при хронических воспалительных заболеваниях урогенитального тракта (УГТ) и отягощенном акушерско–гинекологическом анамнезе
Беременность у женщин с урогенитальным хламидиозом нередко протекает с осложнениями, такими как многоводие, поражение плаценты и ее оболочек, преждевременные роды, угроза прерывания или спонтанное прерывание беременности и мертворождение. В ходе проспективного исследования, проведенного в США, показано, что инфицирование Chlamydia trachomatis во время беременности приводит к задержке внутриутробного развития ребенка, а также повышает риск преждевременных родов.
Заражение плода может происходить антенатально и интранатально в результате аспирации инфицированных околоплодных вод. Вероятность антенатального инфицирования составляет, по данным различных источников, от 60 до 70 % даже при бессимптомном течении инфекции у матери, интранатально поражаются 6–7 % новорожденных . Перинатальная смертность при хламидиозе достигает 15,5 %, причем доля новорожденных, погибших в постнатальном периоде, составляет более 50 % всех перинатальных потерь.
ХИ новорожденных может протекать бессимптомно или проявляться конъюнктивитом, поражениями верхних и нижних дыхательных путей, гениталий, центральной нервной системы и др. По данным зарубежных авторов, риск развития конъюнктивита у новорожденных, инфицированных хламидиями, колеблется от 20 до 50 %, пневмонии – от 5 до 20 %. У недоношенных новорожденных могут развиваться респираторный дистресс–синдром и сепсис.
Скрининг беременных – наиболее эффективная стратегия профилактики перинатального заражения ХИ. В США проводится рутинный скрининг на C. trachomatis всех сексуально активных женщин и подростков, а также беременных во время первого антенатального визита. Женщины из групп повышенного риска обследуются повторно в III триместре беременности. Хотя скрининговое обследование на ХИ не входит в перечень обязательных тестов при беременности и выполняется в нашей стране эпизодически, целесообразность его проведения не вызывает сомнений, особенно у женщин с отягощенным акушерско–гинекологическим анамнезом.
Поскольку доксициклин (и другие тетрациклины) противопоказаны при беременности и лактации, терапия ХИ у беременных проводится преимущественно макролидами.
Всем новорожденным с симптоматикой конъюнктивита рекомендуется проводить лечение препаратами, активными в отношении как хламидий, так и гонококков, вследствие высокой вероятности микст–инфекции.
Микоплазмоз/уреаплазмоз
Истинные масштабы инфицирования населения микоплазмами/уреаплазмами неизвестны, однако, согласно оценкам, частота колонизации этими микроорганизмами достигает 50 %. Хотя вопрос об этиологической роли микоплазм и уреаплазм в инфекционной патологии УГТ обсуждается, в последние годы наметилась тенденция к рассмотрению их в качестве факультативных патогенов, способных в определенных условиях (например, при беременности) вызывать инфекционно–воспалительные процессы в УГТ преимущественно в ассоциации с другими патогенными и условно–патогенными микроорганизмами.
Частота выявления Ureaplasma urealyticum у беременных составляет 50–75 %, Mycoplasma hominis– 20–25 %. Отметим, что беременность способствует повышению колонизации УГТ данными патогенами в полтора–два раза, что объясняется изменениями иммунного и гормонального статуса женщины.
Практически у всех женщин, инфицированных урогенитальными микоплазмами, беременность протекает с осложнениями, наиболее частые из которых – преждевременное прерывание на разных сроках, многоводие, поражение плаценты и плодных оболочек, преждевременное излитие околоплодных вод, послеродовый эндометрит и другие формы инфекции. Частота перинатального заражения новорожденных достигает 45 % при уреаплазмозе и 3–20 % – при микоплазмозе.
При антенатальном инфицировании плода может развиваться генерализованный патологический процесс с поражением органов дыхания и зрения, печени, почек, ЦНС, кожных покровов. При интранатальном заражении входными воротами инфекции наиболее часто являются слизистые оболочки глаз, ротовой полости, половых органов и дыхательных путей. Риск интранатального инфицирования недоношенных новорожденных превышает таковой для доношенных в три раза.
Проведение рутинного скрининга на микоплазменную инфекцию у беременных считается нецелесообразным. Однако в случае патологического течения или невынашивания предыдущей беременности обследование и при его положительном результате лечение необходимы.
Лечение урогенитального микоплазмоза у беременных рекомендуется проводить эритромицином в дозе 500 мг внутрь четыре раза в сутки в течение 7–10 дней начиная со II триместра.
Трихомониаз
По данным ВОЗ, около 180 млн женщин в мире инфицированы Trichomonas vaginalis, при этом частота инфицирования клинически здоровых женщин детородного возраста колеблется от 2–10 % в США до 15–40 % в тропических странах. Трихомонадная инфекция (ТИ) нередко сочетается с другими ИППП, особенно с ГИ и бактериальным вагинозом (БВ). В ряде зарубежных исследований показано, что инфицирование T. vaginalis повышает риск преждевременного отхождения околоплодных вод, преждевременных родов и рождения ребенка с низкой массой тела .
Рутинный скрининг на ТИ у беременных при отсутствии клинической симптоматики не рекомендуется.
Лечение трихомониаза у беременных (не ранее II триместра) и детей проводится препаратами группы нитроимидазолов. Возможность использования метронидазола в период беременности остается спорной из–за его потенциального мутагенного и канцерогенного эффекта. В то же время повышенный риск развития дефектов плода и тератогенности не подтвержден, поэтому в ряде стран (США, Канада) терапию ТИ метронидазолом проводят в максимально ранние сроки, в т. ч. в I триместре беременности. Более безопасной альтернативой пероральному приему признаны интравагинальные формы метронидазола или клотримазола, хотя микробиологическая эффективность местной терапии является более низкой. Лечение ТИ показано детям с признаками трихомониаза или урогенитальной колонизацией, сохраняющейся после четвертого месяца жизни.
Бактериальный вагиноз
БВ характеризуется изменениями экосистемы влагалища в виде замещения доминирующих в микрофлоре лактобацилл ассоциацией Gardnerella vaginalis и анаэробных бактерий.
По данным российских авторов, распространенность БВ варьируется в различных возрастных и социальных группах: 17–19 % – в группах планирования семьи, 24–37 % – среди лиц, находящихся на лечении по поводу венерических заболеваний, и 15–37 % – у беременных. Беременность может провоцировать развитие БВ, поскольку сопровождается выраженными изменениями гормонального статуса.
Результаты многоцентрового исследования по изучению факторов риска преждевременных родов (2929 беременных) показали значимую связь между наличием у женщины БВ и преждевременными родами до 32 недель гестации. Развитие БВ также является фактором риска спонтанного прерывания беременности, преждевременного излития околоплодных вод и преждевременных родов. Риск неблагоприятного исхода беременности у женщин с БВ отчетливо повышается при сопутствующей ТИ.
Эксперты ВОЗ рекомендуют проводить скрининг беременных на ТИ и БВ при наличии в анамнезе эпизодов спонтанного прерывания беременности или преждевременных родов. Тотальный скрининг беременных на данные инфекции в отсутствие клинической симптоматики не оправдан.
С учетом локального характера поражений при БВ при беременности оптимально проведение местной терапии. Хороший клинический эффект показан для нитроимидазолов, назначаемых интравагинально в форме таблеток, тампонов или свечей. При неэффективности местных средств эксперты ВОЗ рекомендуют использовать системную терапию по одной из следующих схем:
• метронидазол 200–250 мг внутрь три раза в сутки, 7 дней (не ранее II–III триместра беременности);
• метронидазол 2 г внутрь однократно (в экстренных случаях провести лечение в I триместре, а также во II–III триместре);
• клиндамицин 300 мг внутрь два раза в сутки, 7 дней.
Урогенитальный кандидоз
В последние годы отмечается выраженный рост заболеваемости кандидозной инфекцией, в т. ч. урогенитальной локализации. По данным ВОЗ, доля урогенитального кандидоза (УГК) среди инфекционных поражений вульвы и влагалища составляет 30–40 %. Частота встречаемости вагинального кандидоза возрастает как в период беременности, так и с увеличением срока гестации.
Основным путем инфицирования новорожденных считается постнатальный. У здоровых доношенных детей кандидозный процесс, как правило, ограничивается кожным покровом и/или слизистыми оболочками и хорошо отвечает на местную антимикотическую терапию. У недоношенных, новорожденных с низкой массой тела при рождении, а также при нарушении целостности кожных покровов возможно развитие инвазивного кандидоза с гематогенной диссеминацией вплоть до генерализованной инфекции.
Лечение УГК у беременных рекомендуется проводить исключительно местными препаратами азолового ряда, наиболее эффективными из которых эксперты ВОЗ считают миконазол, клотримазол, бутоконазол и терконазол. Системные азолы при беременности противопоказаны.
У относительно здоровых новорожденных с нормальной массой тела при рождении можно ограничиться местным лечением. У детей с высоким риском острой гематогенной или висцеральной диссеминации рекомендуется проводить системную терапию. В качестве препарата выбора можно использовать амфотерицин В (в дозе 0,5–1 мг/кг/сут, общая доза – 10–25 мг/кг), в качестве альтернативы – флуконазола.
Папилломавирусная инфекция
Папилломавирусная инфекция (ПВИ) широко распространена, особенно у женщин детородного возраста. Согласно результатам скрининговых обследований, ПВИ выявляется у 40–50 % молодых женщин, однако длительная персистенция вируса в области шейки матки, реже – вульвы и влагалища, наблюдается только у 5–15 % женщин. Беременность предрасполагает к рецидивированию папилломатозных образований, их разрыхлению и увеличению в размерах.
Путь перинатального инфицирования до конца не ясен, а его частота варьируется, по разным данным, от 4 до 87 %. Наиболее частым проявлением ПВИ у новорожденных является ювенильный папилломатоз гортани. Описаны случаи папилломатоза гортани у детей, рожденных путем операции кесарева сечения.
Поскольку лечение ПВИ сводится исключительно к удалению экзофитных очагов, а пути заражения новорожденного до конца не определены, скрининг беременных для профилактики перинатального инфицирования нецелесообразен.
При наличии экзофитных высыпаний лечение беременных проводят с осторожностью, по возможности на ранних сроках, с использованием физических методов деструкции (криодеструкция, лазеротерапия, диатермокоагуляция, электрохирургическое иссечение). Аналогично проводится лечение детей. Использование химических методов в период беременности и у новорожденных противопоказано.
Хотя, по данным ряда источников, кесарево сечение в несколько раз снижает риск развития респираторного папилломатоза, наличие кондилом на половых органах или субклинические формы инфекции не являются показанием для проведения этой операции ввиду возможности анте– и постнатального инфицирования . Оперативное родоразрешение может быть необходимо при больших размерах кондилом с угрозой обтурации родовых путей и кровотечения.
Вирусный гепатит В
ВГВ сегодня остается самым распространенным из всех вирусных гепатитов. Им инфицированы около 2 млрд человек в мире, причем более чем у 350 млн инфекция носит хронический характер. Общее число больных хроническим ВГВ и “вирусоносителей” в РФ составляет от 3 млн до 5 млн человек и имеет тенденцию к росту.
Беременность у женщин с хроническим ВГВ в большинстве случаев не сопровождается осложнениями. Случаи антенатального инфицирования редки, однако оно может произойти при повышении проницаемости плаценты, например при угрозе прерывания беременности . Заражение ребенка происходит преимущественно при прохождении через родовые пути. При ко–инфекции матери вирусным гепатитом D он также может передаваться перинатально. Риск перинатального инфицирования в значительной степени зависит от состояния инфекционного процесса у беременной и составляет 85–90 % при положительном результате обследования на HBeAg и 32 % – при отрицательном.
Особую угрозу представляет появление мутантных штаммов вируса, не продуцирующих HBeAg. Инфицированные ими дети подвергаются высокому риску развития вирусного гепатита с фульминантным течением в первые 2-4 месяца после рождения. Поэтому иммунопрофилактику следует проводить всем детям, рожденным HBsA гамма–положительными матерями независимо от результатов обследования на HBeAg.
Обследование на выявление инфицирования ВГВ (определение HBsAg) входит в программу скрининга беременных, рекомендуется к выполнению при первичном обращении и является обязательным в III триместре.
Основной стратегией профилактики перинатального инфицирования ВГВ в настоящее время является проведение пассивно–активной иммунизации (введение гипериммунного глобулина к ВГВ и вакцинация) всем новорожденным, матери которых HBsA гамма–положительны. По данным зарубежных авторов, адекватная иммунизация позволяет предотвращать заражение в 90 % случаев .
Предварительные результаты контролируемого исследования у беременных с высокой степенью виремии (концентрация ДНК в крови > 1000 мэкв/мл) показали, что проведение короткого курса терапии ламивудином позволяет снизить риск перинатального инфицирования, однако возможность использования данного подхода в повседневной клинической практике пока остается на стадии обсуждения.
Острый ВГВ, перенесенный во время беременности, не сопровождается повышением смертности или тератогенным эффектом и не является показанием к прерыванию беременности. Поскольку снижение риска заражения ВГВ при родоразрешении путем кесарева сечения не доказано, выполнение данной операции с целью профилактики перинатального инфицирования в настоящее время также не рекомендуется.
Заключение
Несмотря на совершенствование методов диагностики и появление новых препаратов, ИППП продолжают оставаться актуальной проблемой медицины в целом и акушерства и перинатологии в частности. Повышение осведомленности практических врачей по данному вопросу, широкое внедрение современных стратегий обследования женщин как на этапе планирования, так и во время беременности и их своевременное лечение, несомненно, позволят снизить частоту перинатальной инфекционной патологии.
Источник




