Фотометрический метод анализа
Отчет о лабораторной работе
по курсу “Физико-химических методов анализа”
ЯГТУ 240100.62-001 ЛР
студентка гр. ХТБВ-33
Фотометрический метод анализа основан на измерении интенсивности светового потока, прошедшего через анализируемый раствор. Основным законом фотометрии является закон Ламберта-Бугера-Бера (1.1):


где 
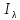



Смысл закона Ламберта-Бугера-Бера можно выразить следующим образом. Одинаковые слои одного и того же вещества поглощают свет в одинаковой степени в независимости от интенсивности падающего на них светового потока.
Если прологарифмировать уравнение (1.1) и изменить знаки на обратные, то уравнение принимает вид (1.2):

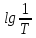

где Т – светопропускание раствора, отн. ед.
Величина 

Из уравнения (1.3) вытекает, что абсорбция раствора прямо пропорциональна концентрации анализируемого вещества и толщине слоя раствора.
Существует два метода фотометрического анализа:
Прямой фотометрический анализ.
Метод основан на определении концентрации анализируемого вещества по закону Ламберта-Бугера-Бера (1.3). Аналитическим сигналом в этом методе является либо абсорбция, либо светопропускание растворов.
Если вещество окрашено (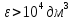

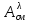
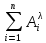
где 

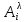
Если вещество не окрашено (
Абсорбция (светопропускание) анализируемых растворов измеряется на фотометрах или колориметрах. При измерении абсорбции используется относительный метод, который позволяет исключить поглощение света растворителем и учесть спектральные характеристики источников приемников излучения. В качестве раствора сравнения используют либо чистый растворитель (метод «обычной», или «прямой» фотометрии), либо раствор анализируемого вещества с точно известной концентрацией (метод «дифференциальной» фотометрии). Метод обычной фотометрии используется для анализа растворов с абсорбцией до 0,8 отн. ед. абсорбции. В методе дифференциальной фотометрии измеряется относительная абсорбция 

Косвенный метод – фотометрическое титрование.
Фотометрическое титрование – это титриметрический метод анализа, в котором точка эквивалентности (Т.Э.) определяется по резкому изменению абсорбции в ходе титрования. С помощью этого метода можно изучить реакции, протекающие с изменением окраски растворов в ходе титрования. По результатам титрования вычерчивают кривую в координатах «абсорбция – объем титранта», аналитическим сигналом в этом методе является объем титранта в точке эквивалентности.
В фотометрическом титровании используются реакции нейтрализации, осаждения, окислительно-восстановительные и комплексообразования. Метод позволяет проводить титрование по собственному поглощению и с помощью реагентов, в качестве последних могут использоваться индикаторы. Для фотометрического титрования необходимо, чтобы титруемые растворы или продукты реакции имели собственную характерную полосу поглощения в видимой области спектра.
Если ни анализируемое вещество, ни титрант, ни продукты реакции не поглощают излучение в видимой области спектра, то применяют цветовой индикатор. На практике титрование осуществляют либо в кювете с мешалкой при непрерывном добавлении титранта из бюретки к анализируемому раствору, либо титрант добавляется порциями в мерные колбы с одинаковой аликвотой анализируемого раствора, объем колб доводят растворителем до метки, перемешивают, а затем фотометрируют растворы. В первом случае удобно проводить титрование на монохроматоре, установив аналитическую длину волны в максимуме полосы поглощения окрашенного компонента или индикатора, во втором – на фотоколориметре.
Фотометрический метод анализа используется для широкого диапазона определяемых концентраций от 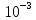


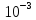

Источник
Фотометрические методы анализа (стр. 2 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 |
Характерными полосами поглощения обладают соединения, содержащие хромофорные группы (см. раздел 1.3.2). Спектральные исследования в этой области часто дают полезную качественную информацию о наличии или отсутствии некоторых функциональных групп, таких как карбонил, ароматическое кольцо, нитрогруппа или сопряженная двойная связь. Следует иметь в виду, что идентификация надежна, если хромофоры в молекуле изолированы. В присутствии ауксохромов и цепей сопряжения идентификация затрудняется.
1.5.2. Количественный анализ методами фотометрии
В фотометрическом анализе количество вещества определяется по интенсивности окраски или светопоглощению окрашенных соединений. Раствор или предмет кажутся окрашенными, если он по-разному пропускает или поглощает видимый свет различных длин волн. В видимой области цвет раствора обусловлен длиной волны излучения, не поглощенного этим раствором. Например, раствор, поглощающий излучение в синей части спектра (»475 нм), окрашен в желтый цвет, т. е. синий цвет является дополнительным к окраске раствора. В таблице 1.3 приводятся такие данные для всей области видимого излучения.
Абсорбционная спектроскопия, особенно в видимой и УФ-областях – один из наиболее распространенных методов количественного анализа. Фотометрические методы используют для определения веществ с собственным поглощением (органические вещества с хромофорными группами,
переходные металлы), а также для определения непоглощающих веществ.
При определении неорганических компонентов для получения окрашенных соединений чаще всего используют реакции образования (иногда – разрушения) комплексных соединений; значительно реже применяются реакции окисления-восстановления. Для фотометрического определения
Таблица 1.3. Цвета видимого излучения
Область максимального поглощения, нм
органических компонентов чаще всего используют реакции синтеза окрашенных соединений. Такие реакции называют фотометрическими.
Основные требования к реакциям сводятся к следующему: избирательное действие реагента, высокая скорость реакции, большое значение константы равновесия, постоянство состава и устойчивость окрашенных соединений во время проведения анализа. Важное значение в связи с этим имеют рН среды, время реакции, концентрации реагентов, температура.
1.5.3. Основные этапы анализа в фотометрии
Прежде чем приступить к выполнению фотометрического определения необходимо выбрать условия анализа. Можно рекомендовать следующую схему.
– перевод анализируемого образца в раствор и отделение, в случае необходимости, мешающих компонентов;
– выбор фотометрической формы вещества и проведение химических реакций для получения окрашенного соединения (если определяемое вещество не обладает интенсивным собственным поглощением)
– установление области концентраций, в которой выполняется основной закон светопоглощения:
– измерение оптической плотности исследуемого раствора;
– расчет содержания вещества в анализируемой пробе и его метрологическая оценка.
1.5.4. Метрологические характеристики метода
Чувствительность характеризуется углом наклона градуировочного графика. Тангенс угла наклона равен молярному коэффициенту поглощения. Если принять минимальное значение оптической плотности, измеренное с необходимой точностью, Аmin = 0,01, можно рассчитать минимально определяемую концентрацию:
При величинах e » 105 чувствительность определения может составлять 10–7–10–6 М.
Воспроизводимость. Для получения воспроизводимых результатов необходимо учитывать погрешности при измерении оптической плотности. Измерительное устройство фотометрического прибора обычно имеет постоянную по всей шкале погрешность измерения в величине пропускания Т, погрешность измерения величины А не будет одинакова, так как А = – lgТ. Относительная погрешность определения концентрации DС/C имеет минимальное значение при Т = 0,37 или оптической плотности А = 0,435. Для измерения концентрации с погрешностью, не превышающей удвоенной минимальной, нужно проводить измерение А в интервале 0,1–1,0. Для снижения случайной погрешности измерения в области больших и малых значений А существуют специальные приемы, один из них – дифференциальный метод анализа.
Правильность. Систематические погрешности в фотометрии могут возникнуть в связи с отклонениями от закона Бера, в связи с немонохроматичностью светового потока и химическими взаимодействиями в измеряемой системе, а также при наличии примесей, которые поглощают свет в данной области спектра. Для снижения систематической ошибки существуют специальные приемы, как, например, приготовление раствора сравнения, содержащего все компоненты, кроме определяемого.
Точность фотометрических методов зависит от индивидуальных особенностей фотометрической реакции, характеристик применяемого прибора и других факторов. Обычная относительная погрешность фотометрических методов составляет 1–2%.
1.5.5. Анализ однокомпонентных систем фотометрическим методом
Метод сравнения оптических плотностей стандартного и исследуемого соединений. Для анализа вещества этим способом готовят раствор исследуемого вещества и два-три стандартных раствора, затем измеряют оптические плотности этих растворов в одинаковых условиях (длина волны, толщина поглощающего слоя). Погрешность определения будет меньше, если оптические плотности исследуемого и стандартного растворов будут иметь близкие значения. Для этого вначале фотометрируют исследуемый раствор, а затем подбирают нужную концентрацию стандартного раствора. Согласно закону Бера, оптические плотности исследуемого и стандартного растворов равны:
Разделив уравнение (1.9) на (1.10) и учитывая, что оптические плотности измеряют в одних и тех же условиях (l = const, l = const) и в растворе одни и те же светопоглощающие частицы (el = const), получим:
Метод сравнения используется для единичных анализов и требует обязательного соблюдения закона Бера.
Метод молярного коэффициента поглощения. При работе по этому методу определяют оптическую плотность нескольких стандартных растворов Аст, для каждого стандартного раствора рассчитывают молярный коэффициент поглощения:
и полученное значение e усредняют. Поскольку молярный коэффициент светопоглощения не зависит от толщины поглощающего слоя, измерения можно проводить в кюветах разной длины. Затем измеряют оптическую плотность исследуемого раствора Ах и рассчитывают концентрацию Сх:
Метод требует обязательного соблюдения закона Бера хотя бы в области исследуемых концентраций; используется довольно редко.
Метод градуировочного графика. В соответствии с законом Бугера – Ламберта – Бера график зависимости оптической плотности от концентрации должен быть линейным и проходить через начало координат.
Готовят серию стандартных растворов различной концентрации и измеряют оптическую плотность в одинаковых условиях. Для повышения точности определения число точек на графике должно быть не меньше трех-четырех. Затем определяют оптическую плотность исследуемого раствора Ах и по графику находят соответствующее ей значение концентрации Сх (рис.1.7).
Интервал концентраций стандартных растворов подбирают таким образом, чтобы концентрация исследуемого раствора соответствовала примерно середине этого интервала.
Метод является наиболее распространенным в фотометрии. Основные ограничения метода связаны с трудоемким процессом приготовления эталонных растворов и необходимостью учитывать влияние посторонних компонентов в исследуемом растворе. Чаще всего метод применяется для проведения серийных анализов.
 |
Рис.1.7. Градуировочный график зависимости оптической
плотности от концентрации
Метод добавок. Этот метод применяют для анализа сложных растворов, так как он позволяет автоматически учитывать влияние посторонних компонентов анализируемого образца. Сначала измеряют оптическую плотность исследуемого раствора с неизвестной концентрацией
затем в анализируемый раствор добавляют известное количество стандартного раствора определяемого компонента (Сст) и измеряют оптическую плотность А х+ст:
Для повышения точности добавку стандартного раствора определяемого компонента делают дважды и полученный результат усредняют.
 |
Концентрацию анализируемого вещества в методе добавок можно найти графичеcким путем (рис.1.8).
Рис.1.8. Градуировочный график для определения
концентрации вещества по методу добавок
Уравнение (1.16) показывает, что если строить график Ах+ст как функции Сст, то получится прямая, экстраполяция которой до пересечения с осью абсцисс дает отрезок, равный –Сх. Действительно, при Ах+ст = 0 из уравнения (1.16) следует, что –Сст = Сх.
Метод дифференциальной фотометрии. В этом методе оптические плотности исследуемого и стандартных растворов измеряют не по отношению к растворителю или раствору сравнения с нулевым поглощением, а, в отличие от прямых спектрофотометрических методов, по отношению к раствору с известной концентрацией определяемого вещества Со.
В зависимости от способов измерения относительной оптической плотности различают несколько вариантов метода.
1.Метод высокого поглощения – концентрация раствора сравнения меньше концентрации исследуемого раствора (Со Сх). В этом случае применяют обратный порядок измерения: анализируемый и стандартные растворы условно принимают за растворы сравнения и по отношению к ним измеряют оптическую плотность изначального раствора сравнения. При обратном порядке измерения относительная оптическая плотность А¢ равна разности оптических плотностей исследуемого раствора (стандартного) и раствора сравнения:
Концентрацию Сх рассчитывают по формуле:
Источник


















